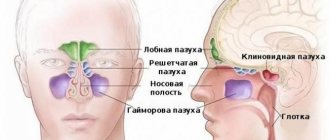
Синдром кошачьего крика, который еще называют синдром Лежена – это достаточно редко встречающееся хромосомное заболевание, которое характеризуется дефектом строения пятой хромосомы. При этом хромосомном дефекте отмечаются различные тяжелые пороки развития внутренних органов и тканей. Дети с синдромом кошачьего крика очень часто страдают от осложнений, которые возникают при дефекте пятой хромосомы.
По статистическим данным, синдром кошачьего крика является не очень распространенной хромосомной патологией. Так, данное заболевание встречается у 1 ребенка на 30-60 тысяч новорожденных. При этом, возникновение синдрома Лежена не зависит от региона или климатических условий. Однако отмечено, что женский пол является фактором риска.
По сравнению, с большинством других наследственных патологий синдром кошачьего крика имеет относительно благоприятный прогноз. При этой патологии дети могут дожить до зрелого возраста при соответствующем медицинском уходе и недопущении развития серьезных осложнений. Однако, у людей с этим недугом невозможна нормальная жизнь без физических и умственных отклонений.
Интересная информация о синдроме:
- Синдром кошачьего крика первоначально обнаружил и описал в середине двадцатого века генетик Джером Лежен, именем которого и был назван этот синдром.
- Это патологическое состояние имеет специфические симптомы, по которым его можно диагностировать у только родившихся деток.
- Данный синдром отличается специфическим криком ребенка (пронзительный и очень громкий), что напоминает мяуканье кошки. При этом недуге наблюдается дефект развития гортанных хрящей.
- При синдроме Лежена у больных отмечается нормальное количество хромосомного материала, что отличает его от других генетических патологий. Наблюдается только небольшой недостаток пятой хромосомы, что и является причиной заболевания.
Причины синдрома кошачьего крика
Синдром Лежена является хромосомной патологией. Ведущая причина синдрома кошачьего крика заключается в изменении структуры хромосом в генной информации ребенка. Геном содержит всю информацию о каком-либо организме. В состав генома входит 23 пары хромосом. Хромосомные заболевания возникают по причине нарушения целостности какой-либо из хромосом.
Синдром кошачьего крика характеризуется тем, что в геноме каждая пятая хромосома будет иметь дефект в любой клетке, независимо от ее функции. При данной патологии пятая хромосома не имеет короткого плеча, на котором локализуется большое количество генов. Такое патологическое состояние в генетике носит название делеции (отсутствие определенного участка ДНК).
Существует несколько вариантов мутаций, которые являются факторами развития синдрома:
- Абсолютное отсутствие короткого плеча на пятой хромосоме. Данный вариант характерен для очень тяжелого течения болезни.
- Уменьшение короткого плеча характеризуется потерей определенной генной информации. При этой форме отмечается потеря генной информации, что приводит к появлению данного синдрома.
- Мозаичный вариант синдрома Лежена является относительно легким течением заболевания (менее выраженные физические и психические отклонения). При данной форме заболевания изначально геном меняет свою структуру во время роста зародыша. Во время деления пятой хромосомы короткое плечо было утеряно, что явилось причиной заболевания.
Синдром кошачьего крика, мутация которого находится в пятой хромосоме, наблюдается при всех вышеперечисленных вариантах отклонений. При этом отмечаются специфические симптомы, которые являются результатом деления клеток, имеющих дефектный ген. Деление таких клеток характеризуется меньшей интенсивностью, так как у них отсутствуют нужные химические компоненты. За счет этого дети с синдромом кошачьего крика зачастую имеют низкую массу тела.
Как правило, дефект в пятой хромосоме наследуется от одного из родителей. Основная причина синдрома кошачьего крика не ясна, так как развитие этой патологии обусловлено множеством факторов, которые воздействуют из окружающей среды. Данные факторы приводят к нарушению процесса деления зиготы в самом начале беременности или повреждению половых клеток одного из родителей.
Факторы, которые провоцируют развитие патологии пятой хромосомы:
- Возраст женщины, которая является матерью ребенка. Вероятность наследственных заболеваний увеличивается с возрастом матери. Для синдрома эта зависимость является довольно слабой. При данной патологии риск развития заболевания увеличивается после 45 лет у матери. При этом возраст отца не влияет на риск развития синдрома Лежена;
- Курение. Курение особенно опасно в молодом возрасте, когда происходит активное формирование репродуктивной системы. Это является частой причиной хромосомной патологии;
- Алкоголь действует таким же образом, как и курение (наблюдается нарушение биохимических процессов, что существенно повышает риск хромосомных аномалий);Некоторые лекарственные средства негативно влияют на репродуктивные органы, в том числе и на мутацию хромосом. Особенно это касается приема препаратов в первом триместре беременности. Это способствует развитию риска мозаичной формы синдрома Лежена. При этом наркотические вещества являются наиболее тератогенными;
- Синдром кошачьего крика, мутация при котором может наблюдаться при наличии внутриутробных инфекций;
- Радиоактивное излучение, направленное на половые органы, часто проявляется хромосомными мутациями;
- Неблагоприятные экологические условия. Ученые отмечают, что в регионах, где добывают токсические полезные ископаемые, часто наблюдается рождение детей с хромосомными болезнями.
Причина синдрома кошачьего крика часто кроется в одном из этих факторов, но встречаются случаи, когда у родителей, на которых не воздействовали вышеперечисленные факторы, рождаются дети с синдромом кошачьего крика.
Этиопатогенетические факторы
Синдром кошачьего крика развивается у лиц, имеющих структурную деформацию пятой хромосомы. Данное генетическая патология обусловлена утратой части или целой половины короткого плеча. У хромосомы может полностью отсутствовать плечо – небольшой фрагмент с множеством генов. Особенности клинической картины синдрома связаны не с размером ее потерянного участка, а с определенным фрагментом. Клетки с поврежденными хромосомами не могут полноценно синтезировать химические соединения. Они производят дефектные белки, что и приводит к появлению характерных симптомов болезни.
Возможна транслокация части плеча 5 хромосомы на иную, негомологичную хромосому. Подобные хромосомные аберрации обычно вызваны спонтанной мутацией генов и лишь в 10% случаев они наследуются от родителей.
СКК может развиться при любом из этих вариантов мутационных изменений:
- Полное отсутствие короткого плеча — самый распространенный вариант патологии, приводящий к тяжелым врожденным дефектам внутренних органов.
- Потеря части плеча хромосомы сопровождается развитием меньшего числа аномалий.
- Кольцевая хромосома – замкнутая двухцепочечная молекула ДНК, у которой оба конца укорочены и сцеплены друг с другом. В результате подобной трансформации теряется небольшой конечный участок хромосомы. Если делеция затрагивает ключевые гены, развивается синдром Лежена.
- Мозаицизм – легкий вариант мутации, встречающийся крайне редко. Ребенок получает от родителей нормальные хромосомы. Их структурные изменения происходят после образования зиготы. При этом большинство клеток имеет нормальный геном, а их меньшая часть – набор генов, характерный для СКК. У больных детей имеется меньше врожденных аномалий: их физическое развитие остается нормальным, внутренние органы функционируют полноценно, но имеется выраженное снижение интеллекта.
Причины образования структурного дефекта пятой хромосомы в настоящее время до конца не определены. Считается, что их огромное количество, и ни одна из них не является главной. На развитие патологии оказывает влияние совокупность факторов внешней среды, которые повреждают яйцеклетки и сперматозоиды или нарушают процесс деления зиготы.
Факторы, провоцирующие развитие синдрома:
- возраст матери,
- вредные привычки,
- наркотики,
- влияние медикаментов,
- инфекционные заболевания беременных — цитомегаловирусы, герпес-вирусы,
- ионизирующее излучение,
- неблагоприятные условия среды,
- воздействие химикатов и иных токсинов,
- оперативные вмешательства при беременности.
Имеет место генетический фактор, когда патологии кариотипа наблюдаются у родителей. Если в семье имеется ребенок с СКК, то вероятность повторного рождения малыша с аналогичной аномалией повышается.
Внешность новорожденных с синдромом кошачьего крика
Ученые определили комплекс симптомов и синдромов, которые в совокупности характерны для синдрома кошачьего крика. Данные симптомокомплексы можно увидеть сразу после рождения ребенка. Типичные симптомы заболевания, которые наблюдаются сразу после рождения малыша:
- Специфический плач новорожденного малыша.
- Аномалии развития костей черепа.
- Определенная форма глазных щелей.
- Атипичная форма ушных хрящей.
- Агенезия нижней челюсти.
- Низкая масса тела при рождении.
- Аномалии развития костного аппарата кисти.
- Косолапость.
Синдром кошачьего крика постоянно проявляется специфическим плачем ребенка. Дефект пятой хромосомы клинически проявляется в первые минуты после рождения ребенка характерным криком в виде мяуканья кошки. Этот крик по тональности отличается от крика нормальных детей. Причиной этого является:
- Уменьшение размеров хряща надгортанника;
- Уменьшение просвета дыхательных путей в проекции надгортанника;
- Аномальное увеличение эластичности хрящевой ткани;
- Образование складок на слизистой оболочке, которая выстилает хрящи гортани.
Так как эти изменения происходят в области голосовых связок, то у детей изменяется тональность голоса.
Аномалии развития головы
Дети с синдромом кошачьего крика в более, чем в 80 % случаев, имеют аномалии развития формы черепной коробки. Чаще всего наблюдается микроцефалия, которая сопровождается уменьшением размеров черепа. Поэтому у новорожденных голова имеет продолговатую форму и пропорционально она меньше размеров туловища. Для того, что подтвердить диагноз микроцефалии, необходимо сделать краниометрию. Микроцефалия всегда сопровождается энцефалопатией различной степени тяжести.
Специфическая форма глазных щелей
Данный симптом характерен для многих хромосомных заболеваний, в том числе и для синдрома Лежена. В основном эта аномалия обусловлена патологической формой костей черепа. Дети с синдромом кошачьего крика имеют нарушения развития глаз, которые можно отличить по четырем признакам:
- Антимонголоидный глазной разрез отличается тем, что медиальный угол глаза располагается всегда выше наружного;
- Косоглазие характеризуется асимметричным расположением роговиц по отношению к векам;
- Гипертелоризм глаз отличается широкой посадкой глазных яблок;
- Эпикантус представляет собой складку у внутреннего угла глаза.
Нарушение формы наружного уха
Для новорожденных детей с синдромом кошачьего крика характерно наличие изменения в строении и локализации ушных раковин. Наиболее частой патологией является птоз ушных раковин. Это является следствием недоразвития хрящей уха, что визуально представлено уменьшением размеров ушей. Также около ушных раковин на коже могут наблюдаться своеобразные уплотненные кожные узелки.
Агенезия нижней челюсти
Недоразвитие нижней челюсти проявляется микрогнатией или микрогенией. Во время беременности из-за хромосомных аномалий кость, которая формирует нижнюю челюсть, может не достигнуть нужных размеров. Все это приводит к втягиванию подбородка по отношению к верхнечелюстной кости. Частые формы микрогнатии – двухсторонняя или односторонняя. В целом нарушение развития нижней челюсти у таких детей приводит к затруднению при питании (ребенок не может полностью сомкнуть губы около соска, что приводит к нарушению сосательного рефлекса).
Патологически сниженный вес ребенка
Новорожденные дети с синдромом кошачьего крика часто имеют аномально низкий вес при рождении. Это является следствием тяжелых нарушений развития внутренних органов.
Патология развития костей костного аппарата
Синдром кошачьего крика часто проявляется развитием синдактилии. Этот синдром характеризуется сращением пальцев на руках и ногах ребенка. При этом возможно соединение пальцев только тонкой кожной перепонкой, что легко исправить при помощи хирургического вмешательства. В случае сращения пальцев костной тканью исправить данную патологию намного сложнее.
Также может наблюдаться клиндактилия, которая характеризуется нарушением формы пальцев в суставах кисти и стопы.
Косолапость
Данный признак проявляется при наличии аномалий развития костного аппарата нижней конечности. Косолапость – это нарушение расположения стопы по отношению к оси голени. В будущем у таких деток могут проблемы с ходьбой. Совокупность этих симптомов можно диагностировать на пренатальном этапе.
Симптоматика
Новорожденные с СКК появляются на свет с пренатальной гипотрофией – недостаточной массой тела. Их внутренние органы и системы не до конца сформированы. При этом рождаются такие дети чаще всего в положенный срок. Беременность протекает хорошо, патологических процессов при ней не наблюдается.
внешние признаки синдрома кошачьего крика
Клиника синдрома кошачьего крика:
- Характерный плач ребенка обусловлен дефектом гортани, который формируется внутриутробно. Специфический крик на высоких тонах напоминает кошачье мяуканье. У больных детей размеры надгортанника намного меньше, чем у здоровых, дыхательные пути сужены, хрящевая ткань более мягкая, имеются складки на слизистой оболочке гортани. Изменение тембра голоса — основной симптом патологии, который присущ каждому больному. Это патономоничный признак, который исчезает к концу первого или второго года жизни.
- У 85% новорожденных наблюдается микроцефалия. Маленькая голова новорожденных вытягивается в продольном направлении. Краниометрия подтверждает наличие данной аномалии. У больных с микроцефалией в будущем прогрессирует умственная отсталость.
- У некоторых новорожденных встречается антимонголоидный разрез глаз. Узкие глазные щели имеют опущенные внешние и приподнятые внутренние уголки. Больные с СКК страдают страбизмом, астигматизмом, снижением остроты зрения, катарактой, близорукостью. Для новорожденных с СКК характерно наличие гипертелоризма, депигментированной сетчатки и эпикантуса.
- Дефекты слухового анализатора проявляются низким расположением ушных раковин, патологически мягкой хрящевой тканью, образованием небольших плотных узелков вокруг ушей. У больных орган слуха имеет маленький размер и суженный слуховой проход.
- Микрогения или микрогнатия – гипоплазия костей нижней челюсти с втянутостью подбородка. При двусторонней микрогнатии уменьшенная нижняя челюсть остается симметричной, а между зубами образуются широкие промежутки. При односторонней микрогнатии недоразвита только одна из ветвей нижней челюсти, что делает лицо несимметричным. Данный признак нарушает нормальный процесс грудного вскармливания. Сосательный рефлекс быстро угасает.
- Низкая масса тела характерная практически для всех новорожденных с СКК. В среднем их вес при рождении не превышает 2500 грамм.
- Синдактилия — неполное или полное сращение двух или более пальцев кисти или стопы. Обычно они соединены кожной перепонкой, которую легко рассекают во время операции. Если сращена костная ткань, исправить ситуацию намного сложнее. Клинодактилия – искривление пальцев или искажение их положения относительно оси конечности, не позволяющее полностью согнуть или разогнуть кисть.
- Косолапость – порок развития костно-суставного аппарата, при котором стопа сильно отклоняется внутрь по отношению к голени. Дети, имеющие такой дефект, поздно начинают ходить. Поражение костно-мышечной системы проявляется вывихом бедра, развитием сколиоза, плоскостопия, паховыми или пупочными грыжами.
- Патология дыхательной системы у больных детей проявляется частыми простудными заболеваниями, высоким риском развития пневмоний, которые нередко заканчиваются летальным исходом.
- Врожденные пороки сердца и сосудов – открытый артериальный поток, ДМПП, ДМПЖ, тетрада Фалло, количественное и структурное изменение сосудов, приводящее к дисциркуляторным нарушениям и развитию сердечной недостаточности. У детей синеет кожа, возникает слабость, одышка, усиливается сердцебиение, колеблется давление, возможны обмороки. Врожденные пороки сердца — основная причина летального исхода при СКК.
- Аномалии почек – гидронефроз, атрофия почечной ткани, подковообразная форма почек.
- Гипоспадия – патологическое развитие полового члена, когда внешнее отверстие уретры открывается не на головке полового органа, а на его стволе. Больные дети испытывают трудности при мочеиспускании, которое становится болезненным или полностью невозможным.
- Врожденные дефекты пищеварительного тракта — сужение или полное закрытие просвета пищеварительной трубки на всем ее протяжении. У больных нарушается процесс глотания и переваривания пищи, возникает задержка кала, рвота, пропадает аппетит, больные резко худеют. Нарушение нервной регуляции кишечника проявляется запорами.
- К прочим признакам синдрома относятся: готическое небо, нарушение глотания, гиперсаливация, расщепление язычка, плоская спинка носа, расщелина неба, шумное дыхание, цианоз, аномальный прикус.
Дети с СКК отстают в умственном и физическом развитии от своих сверстников. У них чаще развиваются офтальмологические патологии, снижается тонус мышц, нарушается координация движений, часто возникают перепады настроения: плач беспричинно сменяется истеричным хохотом. В коллективе дети агрессивны и чрезмерно активны. У больных развивается имбецильность или олигофрения. У них появляются проблемы с речью, снижается способность к обучению. Больные дети не могут освоить обычную школьную программу, учатся на дому или в спецшколах.
У больных лицевые кости намного шире черепных, что придает лицу характерную форму — лунообразную. Нарушение осанки и короткая шея также являются типичными признаками синдрома. Дискоординация движений, неустойчивая походка, частые падения обусловлены гипоплазией мозжечка.
Дети с синдромом кошачьего крика рано погибают от врожденных пороков внутренних органов. Лишь 10% больных умирает в возрасте 12-15 лет, и только единицы переживают 50-летний рубеж. У лиц с СКК репродуктивная функция полностью сохраняется, несмотря на развитие у женщин двурогой матки, а у мужчин – гипотрофии или атрофии яичек.
Особенности детей с синдромом кошачьего крика
Выживаемость детей с данным синдромом достаточно высока, поэтому многие из них достигают подросткового возраста. Дети с синдромом кошачьего крика имеют такие фенотипические особенности внешнего вида:
- Умственная отсталость;
- Снижение мышечного тонуса;
- Сниженная координация движений;
- Запоры;
- Лунообразное лицо;
- Укороченная шея;
- Лабильная нервная система;
- Ухудшение зрения.
Умственная отсталость
Часто данный симптом становится заметным в первые годы жизни ребенка и является одним из важных диагностических признаков данного заболевания на фоне полного здоровья.
Сниженный мышечный тонус
Этот симптом развивается при патологии нервной системы или неполноценном развитии определенных мышц. Клинически это заметно в виде повышенной усталости детей во время ходьбы.
Сниженная координация движений
Данное проявление синдрома кошачьего крика развивается при недоразвитии мозжечка, так как у таких деток наблюдается микроцефалия.
Запоры
Этот симптом отмечается вследствие патологически суженного желудочно-кишечного тракта, а также из-за нарушения нейрогуморальной регуляции кишечника.
Лицо лунообразной формы
Данный симптом возникает в результате нарушения развития костей черепа и долихоцефалии. При этом кости лицевой части черепа больше, чем мозговой.
Укороченная шея
При данном симптоме детям трудно повернуть голову в разные стороны. Это возникает в результате недоразвития шейных позвонков и хрящей между ними.
Лабильность нервной системы
У таких деток часто без обоснованной причины меняется настроение. Это является следствием недоразвития нервной системы. Часто такие дети проявляют повышенную агрессивность и активность в детских коллективах.
Ухудшение зрения
Данная симптоматика возникает из-за нарушения развития органа зрения.
Распространенность аутизма и умственной отсталости варьирует в пределах от 1 до 1,5 % и от 3 до 4 %, соответственно [1-6], позволяя рассматривать их в качестве одних из наиболее часто встречающихся состояний, ассоциированных с нарушением психического развития у детей. Комплексные психологические и генетические исследования умственной отсталости и аутизма начались сравнительно недавно [1, 3]. Данные нарушения развития впервые начали оцениваться с помощью психологических методов в начале XX века с использованием психометрических методов исследования. Первая генетическая причина синдромальной умственной отсталости (трисомия хромосомы 21 для синдрома Дауна) выявлена только в 50-х годах XX века. Было показано, что на долю генетических факторов, вносящих вклад в этиологию умственной отсталости и аутизма, приходится не менее 40-50 % случаев [6, 8, 40, 41]. На протяжении последних десятилетий изучение поведенческих фенотипов становится все более значимым для клинической психологии и генетики. Под поведенческими фенотипами понимают характерные особенности поведения, личности, когнитивного и коммуникативного развития, которые ассоциированы со специфическим биологическим нарушением [32]. Понимание поведенческих особенностей заболевания имеет большое значение и позволяет оптимизировать условия проведения диагностики и коррекции. Определение устойчивых особенностей поведения и функционирования индивидуума может быть столь же важным для диагностики, как наличие аномалий развития. На данный момент в некоторых исследованиях рекомендуется оценивать, как минимум, пять различных сфер, включая интеллектуальное развитие, речь, внимание, социальное взаимодействие и поведение [33].
Прогресс в изучении генетических механизмов умственной отсталости и аутизма был во многом обеспечен появлением новых молекулярных технологий. С помощью современных методов стало доступно обнаружение сравнительно небольших изменений генома (микроперестройки, CNV, SNP), которые часто ассоциируют с тяжелыми формами идиопатической умственной отсталости и аутизма [4, 7, 22, 23, 25, 40, 41]. Расстройства аутистического спектра и умственная отсталость представляют собой группы состояний, и наблюдаются при многих генетических заболеваниях. На данный момент причины многих форм несиндромальных умственной отсталости и аутизма остаются неизвестными. Современные цитогенетические и молекулярно-цитогенетические методы, направленные на изучение хромосомных аномалий среди индивидуумов с нарушениями психики, позволяют выявить причинно-следственную связь между заболеванием и аномалиями генома, картировать гены психических заболеваний и определить взаимодействия между белками, кодируемыми данными генами, вследствие чего применение подобных методов является необходимым в контексте мультидисциплинарного подхода к диагностике и оказанию помощи пациентам. Известно, что абилитационные и коррекционные занятия с детьми с расстройствами аутистического спектра и умственной отсталостью проводятся, как правило, в психологических центрах, при этом геномные заболевания практически не исследованы с психологической точки зрения. Одной из причин отсутствия подобных работ является сравнительная новизна высокоразрешающих генетических методов. Технологии, разработанные в последнее время (например, молекулярное кариотипирование с использованием серийной сравнительной геномной гибридизации, array CGH) способны определить геномную перестройку размером 5-10 пн, тогда как другие методы, например классический цитогенетический метод анализа, обладают значительно более низким разрешением (3-5 млн пн и выше) [5, 41].
Необходимо также обратить внимание на степень выраженности умственной отсталости и/или аутизма при нарушениях генома. Генетические исследования нередко проводятся для индивидуумов с отсутствием экспрессивной речи и понимания обращенной речи; гиперактивностью, нарушением тонкой и крупной моторики, различными нарушениями, входящими в структуру сложного дефекта, тяжелой степенью умственной отсталости и расстройствами аутистического спектра. С другой стороны, психологическая диагностика таких пациентов значительно затруднена в связи с отсутствием корректных методов исследования. Следует также отметить, что дети с тяжелой и глубокой умственной отсталостью до 1993 г. не были включены в систему образования в нашей стране, так как считались «необучаемыми» [3]. Поскольку такой практики не было в системе образования, то и не стояло задачи изучения данной категории детей. Для оказания квалифицированной помощи основной акцент диагностики должен быть сделан на решении коррекционно-развивающих задач, которое не представляется возможным без знания сохранных способностей детей и их возможностей. Необходимость диагностики и терапии как умственной отсталости, так и расстройств аутистического спектра в раннем возрасте признается в настоящее время многими исследователями [15, 38]. Было отмечено, что раннее вмешательство может способствовать улучшению результатов стандартизированных тестов интеллекта и измерения уровня развития речи у детей с аутизмом [20]. Обзор исследований по ранней интервенции позволил сделать вывод о том, что наиболее эффективным является вмешательство в возрасте от 24 до 48 месяцев [35].
В целом, при исследовании умственной отсталости и аутизма используются разнообразные психологические тесты, однако, как правило, в большинстве случаев исследователи оценивают уровень интеллекта, степень аутистических проявлений, адаптивное поведение, память, мышление, внимание, речь. В случае обследования детей с генетическими синдромами принцип проведения исследования не меняется, однако подбор тестов в данном случае зависит от особенностей синдрома и характерных для заболевания нарушений развития той или иной психической функции, что представлено в табл. 1.
Таблица 1
Психологические тесты, используемые для оценки различных сфер у детей с наиболее распространенными генетическими синдромами, ассоциированными с аутизмом и умственной отсталостью
| Генетический синдром | Название теста | Оцениваемые сферы | Ссылки |
| Синдром Ретта | Поведенческий опросник для синдрома Ретта (The Rett Syndrome Behavior Questionnaire) | Поведение, эмоциональные реакции | [31] |
| Шкала адаптивного поведения Вайнленд (Vineland Adaptive Scales) | Адаптивное поведение (коммуникация, навыки самообслуживания и др.) | [34] | |
| Шкала интеллекта Кеттела для детей (Cattell Infant Intelligence Scale) | Когнитивные навыки | [34] | |
| Синдром Дауна | Тест Струпа (Stroop Type Task – Day/NightVersion), Лондонская башня (Tower of London), Тест сортировки карточек (Modi?ed Card Sorting Test) | Исполнительные функции (торможение, планирование, поддержание внимания, переключение) | [26] |
| Синдром умственной отсталости, сцепленный с ломкой хромосомой Х | Тест ежедневного внимания для детей, адаптированное задание на пространственную интерференцию (Test of Everyday Attention for Children, adapted Simon spatial interference task) | Исполнительные функции | [42] |
| Синдром Вильямса | Прогрессивные матрицы Равена, тест Векслера | Интеллект, зрительно – пространственные способности | [9] |
| Международная шкала действия Лейтер (Leiter International Performance Scale) | Интеллект | [29] | |
| Синдром Прадера-Вилли | Аутистическое диагностическое интервью, шкала наблюдения для диагностики аутизма (Autism Diagnostic Interview – Revised; the Autism Diagnostic Observation Schedule – Generic) | Выраженность аутистических проявлений | [27] |
Исследования, проведенные в группах пациентов с умственной отсталостью определенной генетической этиологии (например, синдромы Дауна и Вильямса, синдром умственной отсталости, сцепленной ломкой хромосомы Х) показывают, что индивидуумы с умственной отсталостью при определенном генетическом заболевании часто демонстрируют одинаковые поведенческие и когнитивные особенности и проявления, соответствующий характер развития. Следовательно, при наличии генетической причины, лежащей в основе синдромальной патологии, можно говорить не только о подобных паттернах нарушений взаимодействия между генами, анатомических и физиологических характеристик, но и о характерных особенностях поведения, а также интеллектуальных, когнитивных, личностных особенностях функционирования детей [30]. Отличительные черты синдромов, выявленные в сравнительных исследованиях, описаны далее.
Синдром Дауна (трисомия хромосомы 21)
Основными признаками при данном синдроме являются нарушение речи и моторных способностей, тогда как зрительно-пространственные способности остаются относительно сохранными [17]. У детей с синдромом Дауна по сравнению с другими детьми с тяжелой умственной отсталостью в большей степени нарушена моторика, для них характерна моторная неловкость, повышенная гибкость суставов. У детей нарушено стереоскопическое распознавание объекта, что объясняют недоразвитием тонких моторных навыков пальцев рук. При синдроме Дауна описано значительное расхождение между активным и пассивным словарем [16].
Синдром Ретта
При классическом синдроме Ретта, связанным с мутациями в гене МЕСР2 (Xq28), нарушения развития впервые проявляются у детей в возрасте от 6 до 18 месяцев. Для заболевания характерна стадийность течения. После замедления психического развития, нарушения игровой деятельности и остановки приобретения новых навыков на первой стадии, наблюдается потеря ранее приобретенных речевых и двигательных навыков, утрачиваются целенаправленные движения рук. На третьей стадии улучшается взаимодействие с окружающими людьми, восстанавливается глазной контакт, хотя любая деятельность непродолжительна по времени. На четвертой стадии происходит увеличение количества двигательных нарушений, происходит полная утрата экспрессивной речи [24, 31, 34, 39].
Синдром умственной отсталости, сцепленной с ломкой хромосомой Х (FRAXA) (увеличение количество CGG повторов в гене FMR1)
Среди особенностей поведения детей этим синдромом отмечается периодическое активное стремление ребенка к полноценному общению, аутистические черты более неустойчивы по сравнению с классическим аутизмом. В периоды спадов активности обостряются моторные и речевые стереотипии, ребенок перестает отвечать на обращенную речь. С возрастом у индивидуумов с синдромом умственной отсталости, сцепленной с ломкой хромосомы Х, увеличивается количество моторных стереотипий в виде потирания ладоней рук, потряхивания кистями рук, в речи отмечаются эхолалии [1].
Синдром Вильямса (делеция в участке 7q11.23)
Основными проявлениями синдрома являются хрипловатый голос, отсутствие чувства дистанции при общении. У пациентов с синдромом Вильямса наблюдается слабая зрительно-моторная интеграция, в результате чего вместо целостной картинки они видят ее отдельные составные части. Многие из них могут играть на музыкальных инструментах, общительны, не имеют задержек в речевом развитии [11].
Синдром Ангельмана (делеция или унипарентальная дисомия в участке 15q11.2-q13 материнской хромосомы)
Основной значимой характеристикой синдрома Ангельмана является чрезмерно положительное настроение, постоянная улыбка и смех. Наблюдаются фокальные стереотипии, однако у пациентов не наблюдается специфичных, часто повторяющихся стереотипных паттернов. Дети заинтересованы в социальных взаимодействиях, многие пациенты стремятся к коммуникации, несмотря на выраженные нарушения речи. Пациенты испытывают трудности во взаимодействии по причине слабого понимания социальных и эмоциональных сигналов [33].
Синдром Прадера-Вилли (делеция или унипарентальная дисомия в участке 15q11.2-q13 отцовской хромосомы)
Нарушения поведения при данном синдроме проявляются в резких перепадах настроения, упорстве, манипулятивном поведении, обсессивно-компульсивных характеристиках, а также сложностью в отвлечении от ежедневно повторяемых рутинных событий. Синдром Прадера-Вилли также ассоциирован с повышенным риском психиатрических нарушений. Пациенты с унипарентальной дисомией более подвержены психозу, чем с делецией [18].
Синдром делеции 1p36
При данном синдроме наблюдается задержка моторного развития; некоторые исследователи [10] отмечают, что 25 % пациентов могут ходить самостоятельно, широкой походкой, примерно к 2-7 годам. Экспрессивная речь отсутствует в 75 % случаев, понимание обращенной речи ограничено определенными ситуациями. Стремление к коммуникации в ранние годы проявляется слабо, но улучшается со временем, с расширением репертуара используемых жестов.
Синдром Клайнфельтера (наличие дополнительной хромосомы X при мужском кариотипе)
Характерным для детей с этим синдромом является слабость эмоционально-волевой сферы, которая приближается к психическому инфантилизму. Отмечается чрезмерная внушаемость, подражательность, подчиняемость, несамостоятельность, чрезмерная привязанность к близким, нередко с элементом назойливости. Настроение обычно повышенное, с эйфорическим оттенком, имеет тенденцию к беспричинным колебаниям, иногда отмечается склонность к аффективным вспышкам [36].
Синдром Шерешевского-Тернера (потеря хромосомы Х у девочек)
Для данного синдрома, как правило, не характерна умственная отсталость, за исключением случаев с кольцевой хромосомой Х, однако специалисты в качестве характерных особенностей выделяют трудности в обучении, пространственных отношениях, нарушения моторного контроля. В различных исследованиях также отмечаются нарушение зрительно-пространственной координации, исполнительных функций (беглость речи, навыки планирования и др.), памяти и внимания. Описан также инфантилизм [12].
Синдром Смит-Маженис (делеция в участке 17p11.2)
У восьмидесяти процентов пациентов проявляется самоповреждающее поведение (аутоагрессия), включая онихотилломанию, кусание запястий, качание головой, а также повышенная толерантность к боли, нарушение сна. Аутизм был описан у не менее 4 пациентов с делецией в участке делеции Смит-Маженис. Навыки импрессивной речи, как правило, выше, чем экспрессивной. Хриплый голос может являться диагностическим маркером синдрома. Использование языка жестов значительно способствует улучшению коммуникативных способностей ребенка [37].
Синдром крика кошки (cri du chat, делеция в участке 5p15.2)
Наибольшее отставание в развитии наблюдается для навыков, которые требуют мобильности, ловкости и вербальной коммуникации. По сравнению с мелкой моторикой, крупная моторика рук относительно сохранна и дети способны махать рукой или поймать катящийся мяч. Отсутствие речи компенсируется у примерно 2/3 детей при помощи невербальных методов коммуникации, примерно 50 % детей способны использовать язык жестов для сообщения основных потребностей [14].
Основные характерные особенности, свойственные распространенным генетическим синдромам, представлены в табл. 2.
Таблица 2
Характеристика наиболее часто встречающихся генетических синдромов
| Синдром | Основная генетическая причина | Частота | Умственная отсталость | Аутизм | Характерные нарушения, области выявляемых нарушений |
| Синдром Дауна | Трисомия хромосомы 21 | 1:650-850 | От умеренной до тяжелой степени (IQ=25–55) | В некоторых случаях обнаруживаются аутистические проявления | Речь, моторика, рабочая память, исполнительные функции [1, 13, 26] |
| Синдром Ретта | Мутации, делеция в гене MECP2 | 1:10000 (у девочек) | Тяжелая степень | Аутистические проявления | Мелкая моторика, речь, стереотипные «моющие» движения [24, 31, 34] |
| Синдром умственной отсталости, сцепленной с ломкой хромосомой Х | Увеличение количества CGG повторов в гене FMR1 | 1:3600 – 1:4000 у мальчиков и 1:4000 – 1:6000 у девочек | От пограничного уровня (около IQ = 70) до тяжелой степени. Чаще легкая или умеренная степень. | Аутистические проявления | Характерная речь, исполнительная функция, кратковременная память, зрительно – пространственная память, СДВГ(синдром дефицита внимания и гиперактивности) [19] |
| Синдром Вильямса | Делеция 7q11.23 | 1 : 7500 до 1 : 20000 | Cредний IQ 58-69 | Нет | Моторные, речевые навыки, высокая тревожность, СДВГ [9, 28, 29] |
| Синдром Ангельмана | Делеция 15q11.2 на материнской хромосоме | 1:12000 | Тяжелая степень | Аутистические проявления | Речь, нарушения походки, координации, гиперактивность, концентрации внимания и импульсивность [33] |
| Синдром Прадера – Вилли | Делеция 15q11.2 на отцовской хромосоме | 1:15000 | Умеренная умственная отсталость (средний IQ – 60) | Расстройство аутистического спектра | Дизлексия, ритуальное поведение, компульсивные симптомы [18] |
| Синдром делеции 1p36 | Делеция 1p36 | 1:5000 – 1:10000 | Тяжелая умственная отсталость | Не отмечено | Речь, взаимодействие, резкие перемены настроения, самоповреждающее поведение, стереотипии [10] |
| Синдром Клайнфельтера | Дополнительная хромосома Х при мужском кариотипе | 1:500 – 1:1000 | Легкая степень или нормальный интеллект | Нет | Исполнительные функции, внимание, нарушения восприятия, памяти и абстрактного мышления, дизлексия [36] |
| Синдром Шерешевского – Тернера | Отсутствие одной хромосомы Х при женском кариотипе | 1:2000 – 1:5000 | Легкая степень или нормальный интеллект | Нет | СДВГ, зрительно-пространственные и исполнительные функции [21] |
| Синдром Смит – Маженис Синдром | Делеция 17p11.2 | 1:25000 | От умеренной до тяжелой степени | Варьирует | Нарушения поведения, агрессия, резкие смены настроения, недостаток внимания [37] |
| Кошачьего крика | Делеция 5p12 | 1:50000 | От умеренной до тяжелой степени | Аутистические черты | Нарушения поведения, повторяющиеся движения, сверхчувствительность к стимулам [14] |
Заключение
Анализ литературных данных о различных аспектах поведенческих фенотипов и функционировании детей с синдромальными формами генетических заболеваний свидетельствует о достаточном количестве публикаций, освещающих психологические особенности детей с данными нарушениями развития. Несмотря на наличие работ в данной области, необходимо отметить, что такое утверждение справедливо лишь для наиболее частых синдромов, тогда как менее распространенные генетические заболевания остаются мало описанными с психологической точки зрения. Генетические заболевания являются актуальным объектом психологических исследований, так как при генетических синдромах, как правило, наблюдаются множественные когнитивные, моторные и поведенческие нарушения, а также нарушения социального взаимодействия и общения. Если для наиболее частых синдромов могут быть использованы стандартные тесты, то для более редких нарушений психологические методы исследования еще не разработаны, и часто сложно применить существующий арсенал методик к анализу этих детей. При проведении психологического тестирования и разработке специального метода оценки необходимо принимать во внимание особенности детей, типичные для всех индивидуумов с данным нарушением. Следовательно, в настоящее время имеется острая необходимость в создании подходов к психологическим исследованиям детей с генетическими заболеваниями известной этиологии, которые будут способствовать полноценному описанию различных областей функционирования ребенка и позволят разработать целенаправленные опросники для обследования этих детей.
Библиографическая ссылка
Зеленова М.А., Юров Ю.Б., Ворсанова С.Г., Юров И.Ю. ПСИХОЛОГИЧЕСКИЕ АСПЕКТЫ ГЕНЕТИЧЕСКИХ СИНДРОМОВ, АССОЦИИРОВАННЫХ С АУТИЗМОМ И УМСТВЕННОЙ ОТСТАЛОСТЬЮ // Международный журнал прикладных и фундаментальных исследований. – 2015. – № 12-10. – С. 1870-1876; URL: https://applied-research.ru/ru/article/view?id=8400 (дата обращения: 10.07.2020).
Диагностика синдрома кошачьего крика
Диагностика любой хромосомной аномалии проводится в два этапа. Первый этап заключается в выявлении женщин, у которых повышен риск развития детей с хромосомной патологией. Второй этап проводят для подтверждения определенного заболевания. Таким образом, всем беременным женщинам необходима пренатальная диагностика, которая является комплексом диагностических исследований на дородовом этапе. Благодаря данным мероприятиям на ранних сроках выявляются генетические аномалии, среди которых встречается и синдром кошачьего крика.
Синдром кошачьего крика включает следующие диагностические методы:
- Анамнестические данные;
- Кариотипирование обоих родителей;
- Ультразвуковое исследование;
- Исследование крови на выявление плазменных маркеров;
- Инвазивные методы исследования;
- Исследование на послеродовом этапе.
Детальный сбор анамнеза
Подробный опрос родителей педиатром или генетиком.
Кариотипирование родителей
При повышенном риске развития хромосомной аномалии доктор назначает данное исследование, которое позволяет полноценно изучить структуру клетки и ее ядро.
Как диагностируется синдром кри-дю-чата?
Болезнь кошачьего крика — это генетическое заболевание, связанное с аномалией хромосом пациента. Поэтому для подтверждения этого синдрома у ребенка необходимо провести тест на молекулярный кариотип, который позволяет анализировать все хромосомы с разрешением, недостижимым другими методами (так называемый метод микроматрицы — aCGH).
Тест на молекулярный кариотип
Современная медицина также позволяет выявлять этот вид дефектов еще на стадии внутриутробного развития. После 10-й недели беременности в крови матери появляется свободная ДНК плода, на основании которой с вероятностью> 99% можно оценить риск развития хромосомных дефектов, например синдром кошачьего крика. Пренатальные тесты, которые делают это возможным, абсолютно безопасны и неинвазивны. Они включают:
- Тест Sanco;
- Тест Sanco Plus;
- Тест Nifty Pro.
Тесты анализа кариотипа плода выявляют трисомии (например, Дауна, Эдвардса, Патау), а также оценивают возникновение редких генетических дефектов, так называемых синдромов микроделеции и микродупликации. Каждый из этих тестов также определяет пол плода и дефекты, возникающие в результате анеуплоидии половых хромосом (синдромы Тернера, Клайнфельтера, XXX, XXYY, XYY).
Пренатальные тесты, такие как Sanco или Nifty Pro, также рекомендуются в случае неверных результатов первоначальных тестов на беременность, таких как УЗИ или двойной тест. Они также являются хорошей альтернативой инвазивным тестам, таким как амниоцентез, фетоскопия в ситуации, когда есть противопоказания для их выполнения, например, повышенный риск выкидыша или вирусной инфекции (например, ВИЧ, ВГВ).
ЗАПИСЬ НА ПРИЕМ
[contact-form-7 id=»296" title=»Без названия»]
Клиника абортов и контрацепции в Санкт-Петербурге — отделение медицинского гинекологического объединения «Диана»
Запишитесь на прием, анализы или УЗИ через контактную форму или по т. +8 (812) 62-962-77. Мы работаем без выходных с 09:00 до 21:00.
Мы находимся в Красногвардейском районе, рядом со станциями метро «Новочеркасская», «Площадь Александра Невского» и «Ладожская».
Стоимость медикаментозного аборта в нашей клинике 3300 руб. В стоимость входят все таблетки, осмотр гинеколога и УЗИ для определения сроков беременности.
УЗИ
Частые неспецифические признаки синдрома кошачьего крика на ультразвуковом исследовании:
- Увеличение воротникового пространства;
- Повышенное или сниженное количество околоплодных вод;
- Аномалии развития сердца;
- Брахицефалия или долихоцефалия;
- Непроходимость кишечника;
- Короткие трубчатые кости.
Анализ крови на плазменные маркеры включает такие исследования:
- Определение ХГЧ;
- Выявление уровня протеина А;
- Определение концентрации эстриола;
- Определение альфа-фетопротеина.
Диагностика
Чтобы правильно диагностировать любое заболевание, в том числе хромосомное, необходимо тщательно обследовать больного. Специалисты собирают семейный или наследственный анамнез, проводят кариотипирование супругов, пренатальный скрининг и инвазивные процедуры.
В центрах пренатальной диагностики выявляют женщин с высоким риском появления на свет детей с врожденными аномалиями. С помощью целого ряда диагностических мероприятий, проводимых на дородовом этапе, можно выявить различные хромосомные аномалии плода в самом начале беременности.
Методы пренатальной диагностики:
- Кариотипирование родителей – выделение клеток, изучение их ядра, окрашивание материала и микроскопическое изучение хромосом. Нормальный женский кариотип — 46 ХХ, мужской — 46 ХУ. При наличии каких-либо отклонений у родителей шансы родить больного ребенка возрастают во много раз.
- УЗИ-признаки генетических патологий плода – увеличение воротниковой зоны, недостаток или избыток околоплодных вод, ВПС, короткоголовость, непроходимость кишечника. При наличии данных признаков плод с СКК погибает до рождения.
- В крови у беременных определяют количество хорионического гонадотропина, протеина А, эстриола, альфа-фетопротеина.
делеция небольшого участка хромосомы у ребенка
Кордоцентез — исследование пупочной крови плода, позволяющее на 100% подтвердить или исключить заболевания, при которых изменяется количество или структура хромосом.- Исследование околоплодных вод на хромосомные и генетические заболевания плода начинается с пункции амниотической оболочки, забора материала и его последующего исследования.
- Хорионбиопсия — метод пренатальной диагностики, заключающийся в получении ворсин хориона и исследовании биоматериала. Проводят этот пренатальный тест с 10 по 12 неделю беременности.
Все инвазивные методики проводят специальными тонкими иглами под контролем УЗИ. Данные анализы показаны женщинам в возрасте старше 30 лет или имеющим в семейном анамнезе хромосомные заболевания.
Послеродовая диагностика:
- Всех новорожденных с признаками СКК сразу после рождения обследуют неонатологи и врачи-педиатры.
- Данные кардиограммы и эхокардиографического исследования позволяют выявить врожденные пороки сердца.
- Рентгенографическое или ультразвуковое исследование необходимо для обнаружения патологий ЖКТ, почек.
- Чтобы диагностировать заболевание, у новорожденного берут мочу и кровь на анализы.
- Проводят цитогенетическое исследование хромосомного набора пациента.
- Новорожденным показана консультация специалистов в области детской кардиологии, офтальмологии, урологии, ортопедии и других узких областях медицины.