Тромбоэмболия легочной артерии (ТЭЛА) — симптомы и лечение
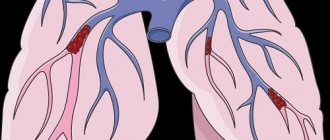
Тромбоэмболия лёгочной артерии (ТЭЛА) — это закупорка лёгочных артерий тромбами различной природы, чаще всего образующихся в крупных венах нижних конечностей или малого таза.
Факторами риска тромбоэмболии лёгочной артерии являются патологические состояния, при которых имеется нарушенный возврат венозной крови, повреждение эндотелия или эндотелиальная дисфункция и гиперкоагуляционные нарушения.
В результате тромбоэмболии лёгочных артерий прекращается кровоснабжение лёгочной ткани, развивается некроз (отмирание тканей), возникает инфаркт-пневмония, дыхательная недостаточность. Увеличивается нагрузка на правые отделы сердца, развивается правожелудочковая недостаточность кровообращения: цианоз (посинение кожи), отёки на нижних конечностях, асцит (скопление жидкости в брюшной полости). Заболевание может развиваться остро или постепенно, в течение нескольких часов или дней. В тяжёлых случаях развитие ТЭЛА происходит стремительно и может привести к резкому ухудшению состояния и гибели больного.
Каждый год от ТЭЛА умирает 0,1% населения земного шара. По частоте смертельных исходов заболевание уступает только ИБС (ишемической болезни сердца) и инсульту. Больных ТЭЛА умирает больше, чем больных СПИДом, раком молочной, предстательной желез и пострадавших в дорожно-траспортных проишествиях вместе взятых. Большинству больным (90%), умершим от ТЭЛА, вовремя не был установлен правильный диагноз, и не было проведено необходимое лечение. ТЭЛА часто возникает там, где её не ожидают — у больных некардиологическими заболеваниями (травмы, роды), осложняя их течение. Смертность при ТЭЛА достигает 30%. При своевременном оптимальном лечении смертность может быть снижена до 2-8%.[2]
Симптомы ТЭЛА зависят от величины тромбов, внезапности или постепенного появления симптомов, длительности заболевания. Течение может быть очень разным — от бессимптомного до быстро прогрессирующего, вплоть до внезапной смерти.
ТЭЛА — болезнь-призрак, которая носит маски других заболеваний сердца или лёгких. Клиника может быть инфарктоподобная, напоминать бронхиальную астму, острую пневмонию. Иногда первым проявлением болезни является правожелудочковая недостаточность кровообращения. Главное отличие — внезапное начало при отсутствии других видимых причин нарастания одышки.
Этиология
ТЭЛА развивается, как правило, в результате тромбоза глубоких вен, который развивается обычно за 3-5 дней до начала заболевания, особенно при отсутствии антикоагулянтной терапии.
Факторы риска тромбоэмболии лёгочной артерии
При диагностике учитывают наличие факторов риска тромбоэмболии. Наиболее значимые из них: перелом шейки бедра или конечности, протезирование бедренного или коленного сустава, большая операция, травма или поражение мозга.
К опасным (но не столь сильно) факторам относят: артроскопию коленного сустава, центральный венозный катетер, химиотерапию, хроническую сердечную недостаточность, гормонзаместительную терапию, злокачественные опухоли, пероральные контрацептивы, инсульт, беременность, роды, послеродовой период, тромбофилию. При злокачественных новообразованиях частота венозной тромбоэмболии составляет 15% и является второй по значимости причиной смерти этой группы больных. Химиотерапевтическое лечение увеличивает риск венозной тромбоэмболии на 47%. Ничем не спровоцированная венозная тромбоэмболия может быть ранним проявлением злокачественного новообразования, которое диагностируется в течение года у 10% пациентов эпизода ТЭЛА.[2]
К наиболее безопасным, но всё же имеющим риск, факторам относят все состояния, сопряжённые с длительной иммобилизацией (неподвижностью) — длительный (более трёх суток) постельный режим, авиаперелёты, пожилой возраст, варикозное расширение вен, лапароскопические вмешательства.[3]
Некоторые факторы риска — общие с тромбозами артериального русла. Это те же факторы риска осложнений атеросклероза и гипертонической болезни: курение, ожирение, малоподвижный образ жизни, а также сахарный диабет, гиперхолестеринемия, психологический стресс, низкий уровень употребления овощей, фруктов, рыбы, низкий уровень физической активности.
Чем больше возраст больного, тем более вероятно развитие заболевания.
Наконец, сегодня доказано существование генетической предрасположенности к ТЭЛА. Гетерозиготная форма полиморфизма V фактора увеличивает риск исходных венозных тромбоэмболий в три раза, а гомозиготная форма — в 15-20 раз.
К наиболее значимым факторам риска, способствующим развитию агрессивной тромбофилии, относятся антифосфолипидный синдром с повышением антикардиолипиновых антител и дефицит естественных антикоагулянтов: протеина С, протеина S и антитромбина III.
Статистика заболеваемости и смертности ТЭЛА
Статистические данные говорят о том, что ежегодно от тромбоэмболии легочной артерии умирает около 0,1% населения планеты. По частоте летальных исходов эта патология уступает лишь ишемической болезни сердца, инсультам и некоторым онкологическим заболеваниям.
Основная причина смертности при тромбоэмболии легочной артерии – поздняя постановка диагноза. Около 90% больных не получают необходимого лечения на ранних стадиях этого острого состояния.
Трудность диагностики тромбоэмболии заключается в том, что это состояние может маскироваться под большое количество заболеваний сердца и легких. Многие пациенты начинают получать терапию от инфаркта или бронхиальной астмы. В результате теряется драгоценное время.
Еще одна опасность тромбоэмболии легочной артерии – это внезапность. Она поражает не только пациентов с сердечно-сосудистыми заболеваниями, но и женщин во время родов, практически здоровых людей после травм. Чаще всего после установления диагноза ТЭЛА удается спасти лишь 70% пациентов. Но если патология была своевременно диагностирована и начато оптимальное лечение, то этот показатель может увеличиться до 98% процентов.
Установление клинического класса и верификация диагноза
Легочные функциональные тесты позволяют выявить обструктивные или рестриктивные изменения с целью дифференциальной диагностики ЛГ и уточнения тяжести поражения легких. Для больных характерно уменьшение диффузионной способности легких в отношении монооксида углерода (40-80% от нормы), небольшое или умеренное снижение легочных объемов, нормальное или незначительно сниженное PaO2 и обычно сниженное из-за альвеолярной гипервентиляции PaСO2.
Вентиляционно-перфузионная сцинтиграфия легких является методом скрининга для исключения хронической тромбоэмболии как причины легочной гипертензии. У больных после тромбоэмболии обнаруживаются дефекты перфузии в долевых и сегментарных зонах при отсутствии нарушений вентиляции. Перфузионная сцинтиграфия исторически стала одним из первых методов обнаружения дефектов перфузии легочной паренхимы при ТЭЛА. Изображения, получаемые при острой ТЭЛА и ХТЭЛГ, существенно различаются. Дефекты перфузии при острой ТЭЛА более четко очерчены и резко контрастируют с нормально функционирующей тканью. При ХТЭЛГ дефекты перфузии очерчены не четко и часто не соответствуют зоне кровоснабжения крупной легочной артерии.
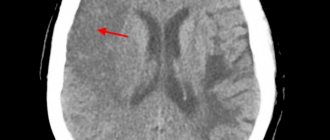
Компьютерная томография и КТ-ангиопульмонография
КТ- картина хронической тромбоэмболии может быть представлена окклюзиями и стенозами легочных артерий, эксцентрическими дефектами наполнения вследствие наличия тромбов, в том числе реканализованных.КТ-ангиопульмонография проводится на спиральных компьютерных томографах в фазу прохождения контрастного вещества через легочное артериальное русло. Из методологических особенностей следует отметить, что исследование должно быть проведено с использованием не менее чем 8- спирального томографа, с минимальным шагом (не более 3 мм) и толщиной среза (не более 1мм). Тщательное сканирование должно охватить оба легких полностью – от верхушек до диафрагмальных синусов. Контрастное усиление правых отделов сердца и легочных артерий должно соответствовать или превышать степень контрастирования левых камер сердца и аорты. Выполнение второй, артериальной фазы сканирования рекомендуется всем больным старше 40 лет, особенно при наличии данных за артериальные тромбозы и ИБС в анамнезе. Современное программное обеспечение позволяет провести реконструкции изображений легочных артерий в любых плоскостях, построить проекции максимальной интенсивности и трехмерные изображения. В большинстве случаев для уточнения характера поражения достаточно проанализировать поперечные срезы с использованием программы просмотра изображений, что позволяет определить наличие изменений не только в долевых и в сегментарных ветвях, но и в ряде субсегментарных артерий. Патологические изменения помимо наличия «старого» тромботического материала могут включать локальные утолщения стенки сосуда, сужения в устье сосудов и на их протяжении, окклюзии, внутрисосудистые структуры в виде мембран и перемычек. При выявлении изменений в нескольких ветвях легочных артерий можно сделать вывод о высокой вероятности тромбоэмболического характера ЛГ. Важно отметить, что разрешающая способность современных КТ-сканеров ограничена и не позволяет определять очень тонкие мембранные и тяжистые структуры в просвете ЛА, особенно если размеры объекта не превышают 2-3 мм. В ряде случаев развивается кальцификация «старого» тромботического материала, и КТ может оказать неоценимую помощь в определении локализации кальциноза. КТ позволяет выявить не только стенотические изменения сосудов легких, но и нарушения перфузии легочной ткани по характеру контрастирования паренхимы. В некоторых случаях контрастирование паренхимы настолько неравномерно, что на сканах определяется мозаичное контрастирование. Четко выраженная мозаичность сегментов обычно свидетельствует о хорошем прогнозе оперативного лечения. Контрастирование исключительно прикорневых зон не является истинной мозаичностью и нередко наблюдается при микрососудистых формах ЛГ. Обеспечивая детальное изображение легочной паренхимы, КТ позволяет диагностировать и другие заболевания легких. Помимо состояния артериального русла, КТ может дать исчерпывающую информацию обо всех внутригрудных структурах, что важно для подтверждения диагноза и построения плана оперативного лечения. Перед выполнением операции следует учитывать состояние легочной паренхимы, бронхиального дерева, легочных вен.
Ангиографическая диагностика
Основными задачами ангиографической диагностики являются определение степени тяжести легочной гипертензии, уточнение характера поражения легочного русла посредством ангиопульмонографии, выявление/исключение коронарной болезни. Проведение катетеризации в изолированном виде без качественной ангиопульмонографии у больного с четкими признаками ХТЭЛГ нецелесообразно. Это исследование должно дать четкую информацию врачам для решения вопроса об операбельности больного и тяжести его состояния. Гемодинамическими критериями постэмболической легочной гипертензии, выявляемыми при катетеризации правых отделов сердца, являются: среднее давление в легочной артерии (ДЛА) выше 25 мм рт. ст., давление заклинивания легочной артерии (ДЗЛА) ≤ 15 мм рт. ст., ЛСС > 2 ЕД. по Вуду (160 дин. сек см-5) при наличии множественных стенозирующих и/или окклюзирующих поражений ветвей легочной артерии различного калибра.
Неинвазивная диагностика
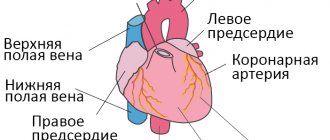
Электрокардиография(ЭКГ) выявляет признаки гипертрофии и перегрузки правого желудочка, дилатации и гипертрофии правого предсердия (p-pulmonale), отклонение электрической оси сердца вправо.
Рентгенография органов грудной клетки позволяет уточнить этиологию ЛГ: выявить интерстициальные заболевания легких, приобретенные и врожденные пороки сердца, а также судить о тяжести ЛГ. Основными рентгенологическими признаками ЛГ являются выбухание ствола и левой ветви легочной артерии, которые формируют в прямой проекции II дугу по левому контуру сердца, расширение корней легких, увеличение правых отделов сердца. У больных постэмболической легочной гипертензией можно выявить признаки, указывающие на наличие тромбов в крупных ветвях легочной артерии (ЛА)- расширение ствола и главных ветвей ЛА, симптом деформации и укорочения корня. Специфическим признаком является обеднение легочного рисунка в зоне нарушенного кровоснабжения.
Эхокардиография (ЭхоКГ) — УЗИ сердца считается наиболее ценным неинвазивным методом диагностики ЛГ, так как не только позволяет оценить уровень давления в легочной артерии, но и дает важную информацию о причине и осложнениях ЛГ. С помощью этого метода можно исключить поражения митрального, аортального клапанов, болезни миокарда, врожденные пороки сердца с шунтированием крови, приводящие к развитию ЛГ. К сожалению, метод не позволяет дифференцировать постэмболической легочной гипертензии от других форм прекапиллярной ЛГ. Исключение составляют редкие случаи наличия массивных тромбов в стволе и основных ветвях ЛА в непосредственной близости от бифуркации.
Функциональная классификация легочной гипертензии
| Класс I | отсутствует ограничение физической активности. Обычная физическая активность не вызывает появление одышки, слабости, боли в грудной клетке, головокружения |
| Класс II | некоторое снижение физической активности. Обычная физическая активность сопровождается появлением одышки, слабости, боли в грудной клетке, головокружения |
| Класс III | выраженное ограничение физической активности. Небольшая физическая активность вызывает появление одышки, слабости, боли в грудной клетке, головокружения |
| Класс IV | неспособность выполнять любую физическую нагрузку без вышеперечисленных клинических симптомов. Одышка или слабость могут присутствовать даже в покое, дискомфорт возрастает при минимальной нагрузке |