Хронический гастрит — это группа рецидивирующих, длительно протекающих заболеваний, которые характеризуются воспалительными и дистрофическими изменениями слизистой оболочки желудка.
Классификация хронических гастритов по функциональному признаку:
- Гастрит с нормальной секрецией.
- Гастрит с повышенной секрецией (гиперацидный).
- Гастрит с недостаточностью секреции (гипоацидный).
- Гастрит с отсутствием секреции (анацидный).
Гастрит, характерной особенностью которого является пониженная кислотность, в медицине называется гипоацидным.
При данном виде гастрита воспаление слизистой оболочки желудка приводит к снижению секреторной и моторной функций. Гипоацидный гастрит проявляется нарушением функций клеток, которые вырабатывают соляную кислоту, что и ведет к снижению уровня кислотности.
Причины гипоацидного гастрита
Причины, вследствие которых появляется это заболевание, могут быть внешние и внутренние.
К внешним относят:
- злоупотребление табачными изделиями и алкогольными напитками;
- неправильный режим питания, острая, жаренная, жирная, копченая еда;
- злоупотребление медикаментозными препаратами с побочными эффектами для слизистой желудка;
- вредное влияние химических и радиоактивных веществ;
К внутренним относят:
- патологии ЖКТ и нарушения в иммунной системе;
- нарушенные метаболизм, работа печени, поджелудочной и щитовидной желез;
- различные генетические отклонения в развитии слизистой оболочки.
Гипоацидным гастритом чаще болеют взрослые и представители мужской половины. Дети и женщины подвержены этому заболеванию в меньшей степени.
Стадии развития болезни
Заболевание протекает в четыре этапа:
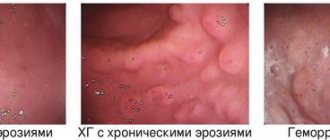
- Гиперемический. Слизистая оболочка желудка приобретает красноватый цвет и становится отечной.
- Гипертрофический. Происходит утолщение слизистой с одновременным снижением выработки соляной кислоты. Возможны изменения в тканях и клетках (дисплазия) и скопление в стенке органа лейкоцитов (метаплазия).
- Атрофический. При длительном воспалении слизистая желудка истончается, регенерация ухудшается, эпителиальные клетки отмирают, их замещает рубцовая ткань.
- Эрозивный и/или язвенный. На внутренней поверхности органа ввиду истончения слизистой оболочки образуются очаги поражения разной глубины.
Симптомы и признаки заболевания
Симптомы такого гастрита связаны со степенью тяжести болезни. В самом начале они вообще могут быть незаметны. Но позже жалобы при гипоацидном гастрите заключаются в следующем:
- болевые ощущения в верхней части живота (иногда с отдачей под ребра с левой стороны);
- ощущение дискомфорта (чувство тяжести, вздутия желудка);
- отрыжка «тухлыми яйцами», привкус металла во рту, язык с серым налетом;
- плохой аппетит;
- частая диарея или запор;
- тошнота, чрезмерное слюноотделение;
- хроническая усталость, головные боли, низкая работоспособность;
- потеря веса, изменения в режиме сна.
Во время сильного обострения могут добавиться и другие признаки: учащенное сердцебиение, обморочное состояние.
Как диагностировать гипоацидный гастрит
Заметив похожие симптомы, за диагностикой следует обратиться к специалисту в области гастроэнтерологии. Чтобы определить клиническую картину и поставить правильный и точный диагноз врач обычно проводит осмотр, узнает жалобы и назначает анализы и исследования, в результате чего определяется разновидность патологии и то, насколько поражена слизистая желудка. Чтобы определить хронический гипоацидный гастрит используют:
- визуальный осмотр желудка с помощью гастроскопа (гастроскопия);
- эндоскопическую биопсию (взятие материала на биопсию);
- РН-метрию кислотности выделяемого желудочного сока;
- анализы крови и копрограмму.
Собрав полную картину в результате инструментального и лабораторного исследований, врач переходит к составлению программы лечения.
Диагностика.
Диагностика хронического гастрита основывается на выявлении жалоб, сбора анамнеза, объективного осмотра и проведении лабораторно-инструментальных методов обследования.
Больному рекомендуется сдать клинический анализ крови, биохимический анализ крови — АЛТ, АСТ, общий билирубин, амилаза, глюкоза. Золотым стандартом диагностики является проведение ФГДС, для диагностики хеликобактерной инфекции применяется дыхательный уреазный тест, или анализ кала на Нр Аг.
Дополнительные методы:
- УЗИ органов брюшной полости;
- при атрофии слизистой желудка — определение в крови: пепсиноген 1, пенсиноген 2, гастрин 17;
- определение антител в крови к париетальным клеткам желудка, внутреннему фактору Касла;
- определение уровня витамина В12 в крови.
Гипоацидный гастрит: лечение
В основе лечения такого гастрита лежит комплексный подход с использованием различных методов и медикаментов, действующих в разных направлениях.
- Для возвращения в норму работы системы пищеварения применяют заместительную терапию (препараты натурального желудочного сока, соляной кислоты, ферменты).
- Для устранения боли используют спазмолитики.
- Если по результатам исследований в организме был обнаружен хеликобактер пилори (Helicobacter pylori), то выписываются антибиотики.
- Нарушенный обмен веществ при гастрите приводит к нехватке полезных веществ, поэтому назначается прием витаминных комплексов с содержанием витаминов группы В и фолиевой кислоты.
- Для восстановления кишечной флоры используются пробиотики.
Препараты при гипоацидном гастрите должны применяться строго по предписанию врача, поскольку отклонение от схемы может нарушить ход лечения. Немаловажным фактором во время лечения является соблюдение диеты. При этом пациенту назначается стол No2, где из рациона исключается грубая и трудноперевариваемая пища, сильно горячие и холодные блюда. Кроме того, при снижении секреции соляной кислоты следует уменьшить потребление молока, заменив его кисломолочными продуктами. Порции должны быть небольшими, но 6 раз в день. Как вспомогательное лечение возможны средства народной медицины, которые также лучше согласовать с лечащим специалистом. Чаще всего используются отвары шиповника, ягод черники, смеси алое с медом.
Пищеварительная недостаточность и ее коррекция с позиции врача-гастроэнтеролога в г. Королеве
О.И. Костюкевич
Пищеварение – совокупность процессов, обеспечивающих обработку и превращение пищевых продуктов в простые химические соединения, способные усваиваться клетками организма. Этот процесс обеспечивает пополнение энергетических и пластических ресурсов, а следовательно, необходим для жизнедеятельности организма. Пищеварение – сложный многоэтапный процесс: 1 этап: ротовое 2 этап: желудочное 3 этап: в двенадцатиперстной кишке 4 этап: в тонкой кишке 5 этап: в толстом кишечнике Любые его нарушения могут привести к серьезным последствиям для организма. В ротовой полости происходит первичный гидролиз углеводов под действием амилазы и мальтазы слюны. Нарушения синтеза ферментов слюны не будет иметь столь выраженных последствий, как при панкреатической недостаточности. Однако недостаток панкреатической амилазы в какой–то степени может быть скомпенсирован амилазой слюны. Это объясняет такой клинический симптом у больных хроническим панкреатитом, как гиперсаливация. В желудке происходит механическая и химическая обработка пищи. Механическая обеспечивается моторной деятельностью желудка, химическая осуществляется за счет ферментов желудочного сока. В желудке происходит начальный гидролиз белков. Размельченные и химически обработанные пищевые массы в смеси с желудочным соком образуют жидкий или полужидкий химус. Пищеварение в тонкой кишке. В тонкой кишке происходят основные процессы переваривания и всасывания нутриентов. Особенно велика роль ее начального отдела – 12–перстной кишки. В процессе пищеварения здесь участвуют панкреатический, кишечный соки и желчь. С помощью ферментов, входящих в состав панкреатического и кишечного соков, происходит гидролиз белков, жиров и углеводов. Внешнесекреторная деятельность поджелудочной железы заключается в образовании и выделении в двенадцатиперстную кишку 1,5–2,0 л панкреатического сока. Панкреатический сок представлен протеолитическими, липолитическими и амилолитическими ферментами. Альфа–амилаза, липаза и нуклеаза секретируются в активном состоянии; протеазы – в виде проэнзимов. Альфа–амилаза поджелудочной железы расщепляет полисахариды до олиго–, ди– и моносахаридов. Панкреатическая липаза, активная в присутствии солей желчных кислот, действует на липиды, расщепляя их до моноглицеридов и жирных кислот. Кишечный сок представляет собой секрет желез, расположенных в слизистой оболочке тонкой кишки. У взрослого человека за сутки выделяется 2–3 л кишечного сока. В кишечном соке находится более 20 ферментов, обеспечивающих конечные стадии переваривания всех пищевых веществ. Разделяют 2 основных этапа пищеварения:
- Полостное;
- Пристеночное (мембранное).
Полостное пищеварение происходит с помощью ферментов, поступающих в полость тонкой кишки (поджелудочный сок, желчь, кишечный сок). В результате полостного пищеварения крупномолекулярные вещества (полимеры) гидролизуются до олигомеров. Дальнейший их гидролиз идет в зоне, прилегающей к слизистой оболочке и непосредственно на ней. Пристеночное пищеварение в широком смысле происходит в зоне гликокаликса и на поверхности микроворсинок. Гликокаликс адсорбирует из полости тонкой кишки ферменты пищеварительных соков. Продукты гидролиза поступают на апикальные мембраны энтероцитов, в которые встроены кишечные ферменты, осуществляющие собственное мембранное пищеварение, в результате которого образуются мономеры, способные всасываться. Пищеварение в толстой кишке. Роль толстой кишки в процессе переваривания пищи небольшая, так как пища почти полностью переваривается и всасывается в тонкой кишке, за исключением растительной клетчатки. В толстой кишке происходят концентрирование химуса путем всасывания воды, формирование каловых масс и удаление их из кишечника. Здесь также происходит всасывание электролитов, водорастворимых витаминов, жирных кислот, углеводов. На каждом из этих этапов могут произойти изменения, повлекшие за собой нарушения переваривания (мальдигестия) и/или всасывания пищи (мальабсорбция), что будет иметь неизбежные клинические последствия. Пищеварительная недостаточность – несоответствие возможностей пищеварительной системы по перевариванию и всасыванию нутриентов объему и/или составу поступающей пищи. Пищеварительная недостаточность сопровождает широкий спектр заболеваний желудочно–кишечного тракта, а также может встречаться и у здорового человека вследствие несбалансированной диеты или слишком большого количества съеденной пищи, а потому очень часто встречается в повседневной практике гастроэнтеролога. Клинические проявления недостаточности пищеварения обнаруживают у 25–41% населения [1]. Для обозначения многочисленных симптомов, связанных с нарушением пищеварения, употребляется термин «диспепсия». К проявлениям диспепсического синдрома традиционно относят [2]:
- Изжогу
- Тошноту и рвоту
- Отрыжку
- Неприятные ощущения (дискомфорт или боль) в эпигастральной области
- Метеоризм
- Нарушения стула.
Симптомы диспепсии могут наблюдаться как вместе, так и по отдельности и сопровождать практически любое заболевание желудочно–кишечного тракта. В то же время каждый из них имеет различное происхождение и различные механизмы возникновения, а также требует совершенно различных подходов к лечению, что делает нецелесообразным столь широкое объединение всех симптомов единым термином. В настоящее время основные патофизиологические механизмы пищеварительной недостаточности можно классифицировать следующим образом: 1. Недостаточность полостного пищеварения, причинами которой являются:
- Заболевания поджелудочной железы, как наследственные, так и приобретенные (хронический панкреатит, состояние после панкреатэктомии, рак поджелудочной железы, муковисцидоз).
- Секреторная недостаточность желудка (атрофический гастрит, постгастрэктомический синдром).
- Дефицит желчных кислот или асинхронизм поступления желчи в тонкую кишку при билиарной обструкции, гепатитах, циррозах, ЖКБ, после холецистэктомии.
- Инактивация пищеварительных ферментов при гастродуодените, язвенной болезни 12–перстной кишки, дисбактериозе тонкой кишки.
- Нарушения транзита кишечного содержимого и нарушения смешивания ферментов с пищевым химусом при дуодено– и гастростазе, интестинальной псевдообструкции, синдроме раздраженного кишечника.
2. Вторая группа связана с нарушением функции ферментов пристеночного пищеварения, например, лактазная недостаточность. Как в первом, так и во втором случаях в полости кишечника остается большое количество недопереваренных нутриентов, что приводит к нарушению состава внутренней среды кишечника, в т.ч. изменению рН, осмотического давления, химического состава. Указанные сдвиги приводят, с одной стороны, к вторичному повреждению слизистой оболочки кишечника и еще большему нарушению процессов пищеварения, и, с другой стороны – к изменению состава микрофлоры кишечника, который усугубляет имеющиеся нарушения. Нарушения пристеночного пищеварения развиваются вследствие:
- дисахаридазной недостаточности (врожденная и приобретенная лактазная недостаточность);
- дистрофических изменений или гибели энтероцитов (глютеновая энтеропатия, саркоидоз, болезнь Крона, избыточный бактериальный рост).
Гастрогенная пищеварительная недостаточность развивается при гипоацидных состояниях, после резекции желудка. В результате снижается секреция желудочного сока, а также из–за недостаточной секретиновой стимуляции поджелудочной железы снижается и панкреатическая секреция. Важно, что низкая желудочная секреция также приводит к микробной контаминации тонкой кишки, которая, в свою очередь, способствует инактивации пищеварительных ферментов. Гастрогенная пищеварительная недостаточность может проявляться чувством тяжести в эпигастральной области, тошнотой, отрыжкой, рвотой. Панкреатическая недостаточность. Несмотря на многообразие причин, вызывающих нарушение пищеварения, наиболее выраженные расстройства связаны с заболеваниями поджелудочной железы (ПЖ), поскольку она является наиболее мощным источников пищеварительных ферментов. Внешнесекреторную недостаточность поджелудочной железы делят на первичную и вторичную [3]:
- первичная панкреатическая недостаточность обусловлена заболеваниями самой поджелудочной железы, в результате чего снижается синтез ферментов;
- при вторичной панкреатической недостаточности количество пищеварительных ферментов достаточное, но их действие не реализуется в полной мере по тем или иным причинам. Вторичную панкреатическую недостаточность делят на гепатогенную (холегенную), гастрогенную, энтерогенную и сосудистую [4].
При гепатогенной недостаточности нарушена активация липазы в просвете кишки из–за сниженного количества желчных кислот или асинхронизма поступления желчи, панкреатических ферментов и химуса в двенадцатиперстную кишку. Гастрогенная панкреатическая недостаточность развивается из–за недостаточной секретиновой стимуляции ПЖ. Кроме того, сниженная секреция желудка в течение некоторого времени компенсируется функциональным напряжением ПЖ, что постепенно приводит к ее истощению. Энтерогенная панкреатическая недостаточность в основном связана с бактериальной контаминацией. Важно, что в развитии этой недостаточности имеет значение не только повреждение слизистой тонкой кишки патогенной и условно–патогенной флорой, но и эндотоксинами, выделяемыми этой флорой. Сосудистая панкреатическая недостаточность развивается при нарушениях микроциркуляции в стенке кишки. Панкреатическая недостаточность клинически проявляется усилением моторики кишечника, учащением стула, полифекалией, стеатореей, метеоризмом, изменениями аппетита. Клинические проявления липазной недостаточности развиваются раньше снижения амилазной и протеазной активности. Это связано с более ранним по сравнению с другими ферментами развитием нарушений продукции липазы поджелудочной железой и с более быстрой инактивацией липазы в кишечнике.
Коррекция пищеварительной недостаточности
Основным направлением в лечении больных с синдромами нарушенного пищеварения и всасывания, особенно при невозможности устранения причин их развития, является заместительная терапия ферментными препаратами. Около 150 лет назад голландский врач Д. Флеш применил при лечении стеатореи у больного с сахарным диабетом водный экстракт из поджелудочной железы телят, однако до сих пор многие аспекты использования ферментных препаратов остаются спорными. Учитывая разнообразие нозологических форм и патогенетических механизмов, протекающих с нарушением пищеварения, спектр показаний к назначению ферментных препаратов довольно широк. Эти показания делятся на несколько групп [5,9]. I. Заболевания поджелудочной железы: хронический панкреатит с болевым и диспепсическим синдромами, с внешне– и внутрисекреторной недостаточностью; состояния после резекции ПЖ; большие кисты, опухоли поджелудочной железы; сахарный диабет; врожденная гипоплазия (синдромы Швахмана, Иогансона–Близзарда) или ее атрофия (синдром Кларка–Хэдвилда) и др. II. Заболевания желудка: хронический гастрит с пониженной желудочной секрецией или ахилией; состояния после резекции желудка. III. Заболевания тонкой и толстой кишок: хронический энтерит; избыточный бактериальный рост. IV. Заболевания печени и желчных путей: холестатические болезни печени; состояния после холецистэктомии; хронический холецистит с гипомоторной дисфункцией желчного пузыря. V. Нарушения моторики пищеварительного тракта функционального или другого происхождения: функциональная диспепсия, гастро– и дуоденостаз другого генеза; дисфункция желчного пузыря и/или сфинктера Одди. VI. Другие показания: состояния после облучения; ферментная недостаточность у пожилых людей («стареющие» органы пищеварения); переедание; однообразное питание; длительный постельный режим; малоподвижный образ жизни; подготовка к УЗИ и др. Причем выбор ферментного препарата при каждой нозологической группе будет различен. В настоящее время ферментные препараты, используемые в клинической практике, должны отвечать определенным требованиям [6]:
- хорошая переносимость;
- отсутствие существенных побочных реакций;
- оптимум действия в интервале рН 5–7;
- устойчивость к действию соляной кислоты, пепсинов и других протеаз;
- содержание достаточного количества активных пищеварительных ферментов;
- иметь длительный срок хранения.
Ферментные средства по форме выпуска классифицируют на безоболочечные и оболочечные. По составу ферментные средства классифируются следующим образом [6]:
- Экстракты слизистой оболочки желудка, основным действующим веществом которых является пепсин.
- Панкреатические энзимы, представленные амилазой, липазой и трипсином (например, Панзинорм форте-Н).
- Комбинированные ферменты, содержащие панкреатин в комбинации с компонентами желчи, гемицеллюлозы и прочими дополнительными компонентами.
Эти ферментные препараты отнюдь не являются взаимозаменяемыми. Различные группы имеют четкие и строгие показания и противопоказания к применению, пренебрежение которыми может привести не только к отсутствию ожидаемого результата, но и вызвать различные побочные эффекты.
- Первая группа ферментов в основном направлена на коррекцию секреторной дисфункции желудка. Эти препараты используются преимущественно при гипоацидном атрофическом гастрите как правило, в комбинации с прокинетиками.
- Препараты, включающие только панкреатические энзимы, используются преимущественно для заместительной терапии при наличии внешнесекреторной недостаточности поджелудочной железы, а также для создания «функционального покоя» органу при наличии обострения заболевания, особенно сопровождающегося внутрипротоковой гипертензией. С этой целью используют препараты, содержащие основные ферменты поджелудочной железы – липазу, трипсин, химотрипсин и амилазу (например, Панзинорм форте–Н). Препараты отличаются друг от друга прежде всего количеством ферментов, а также формой выпуска. Входящая в комплекс амилаза разлагает крахмал и пектины до простых сахаров – сахарозы и мальтозы. Протеазы (химотрипсин, трипсин), соответственно, участвуют в гидролизе белков. Кроме того, они снижают панкреатическую секрецию по механизму обратной связи и регулируют моторику кишечника. Липаза участвует в гидролизе нейтрального жира. Препараты панкреатина не оказывают влияния на функцию желудка, печени, моторику билиарной системы и кишечника, но снижают секрецию панкреатического сока.
- В состав комбинированных препаратов, помимо панкреатических ферментов, входят также желчные кислоты, пепсин, гемицеллюлаза. Введение в препарат желчных кислот существенно изменяет его действие на моторику желудочно–кишечного тракта, функцию желудка и желчевыводящих путей. Эти препараты стимулируют панкреатическую секрецию и холерез, усиливают моторику кишечника и желчного пузыря. Наличие в ферментном препарате гемицеллюлазы обеспечивает расщепление растительных полисахаридов.
Однако следует учитывать, что комбинированные препараты следует избегать при патологии печени, поскольку желчные кислоты вступают в энтерогепатическую циркуляцию и метаболизируются в печени, что увеличивает ее функциональную нагрузку. Учитывая стимулирующее воздействие на панкреатическую секрецию, препараты не стоит принимать при внутрипротоковой гипертензии и при обострении панкреатита. При наличии синдрома избыточного бактериального роста перед назначением желчных кислот необходимо провести селективную деконтаминацию тонкой кишки с тем, чтобы избежать деконъюгации желчных кислот микрофлорой. Деконъюгированные желчные кислоты повреждают слизистую оболочку желудочно–кишечного тракта с последующим развитием осмотической и секреторной диареи. Таким образом, каждая группа ферментных препаратов имеет свои, строго ограниченные показания для использования. Применение и назначение препаратов по показаниям в пределах этих рамок способствуют нормализации процессов пищеварения и улучшению состояния больного. Неправильное использование различных групп ферментов приводит к дискредитации этих препаратов, отсутствию положительного эффекта или к ухудшению состояния пациента. Даже в рамках одной группы препараты отличаются по количественному составу их компонентов, способу производства и форме. Различие структуры панкреатических ферментов обосновывает разнообразие их клинического применения.
Клинические особенности применения ферментных препаратов
В настоящее время сложилась концепция применения высоких доз ферментов для заместительной терапии при первичной внешнесекреторной недостаточности поджелудочной железы и низких – для коррекции функциональных изменений и вторичной панкреатической недостаточности [7]. 1. Назначение ферментных препаратов при заболеваниях поджелудочной железы. А. Для компенсации внешнесекреторной недостаточности поджелудочной железы как правило, применяют высокоактивные ферментные препараты, содержащие большие дозы энзимов. Заместительная терапия необходима при заболеваниях, сопровождающихся атрофией более чем 90% паренхимы органа [8]. Доза ферментов зависит от степени внешнесекреторной недостаточности, а также от способности пациента соблюдать диету. При внешнесекреторной недостаточности поджелудочной железы однократная доза ферментов составляет от 20 до 40 тыс. ед. липазы. Препараты принимают вместе с едой 3 р/д. Эффективность терапии оценивается клинически и лабораторно (копрологическое исследование, экскреция жира с калом, эластазный тест). Препараты хорошо переносятся, однако в исключительных случаях, при при длительном применении более 50000 ед липолитической активности возможно развитие фиброзирующей колопатии, мочекаменной болезни. Поэтому доза ферментов не должна превышать необходимую. Б. Еще одно показание к применению препаратов панкреатина – создание «функционального покоя» поджелудочной железы при обострении хронического панкреатина, внутрипротоковой гипертензии для купирования болевого синдрома. Лечение панкреатита с болевым синдромом требует строгой диеты в сочетании с гипосекреторными препаратами, спазмолитиками и препаратами чистого панкреатина. Последние по механизму обратной связи угнетают собственную панкреатическую секрецию, снижая внутрипротоковую гипертензию и приводя к купированию болевого синдрома. Для создания функционального покоя железе ферменты назначают в несколько ином режиме: за 15–20 мин до еды 3 р/сут. 2. При гипосекреторных заболеваниях желудка, снижении моторики желудка целесообразно применение как препаратов панкреатина, так и комбинированных ферментных препаратов, действие которых направлено на компенсацию нарушений деятельности слизистой оболочки желудка. Препараты, содержащие пепсин, принимают из расчета 0,2–0,5 г пепсина на прием пищи 2–3 раза в сутки перед или во время приема пищи. Эти препараты не следует назначать при заболеваниях, связанных с повышенным кислотообразованием, а также при болевых формах хронического панкреатита. Поскольку гипоацидные состояния в большинстве случаев сопровождаются вторичной панкреатической недостаточностью, препаратами выбора можно считать комбинированные ферментные препараты. 3. Для лечения гипомоторной дискинезии желчевыводящих путей применяют ферментные препараты, содержащие желчные кислоты, которые стимулируют сократительную активность желчного пузыря, нормализуют биохимические свойства желчи. 4. Для лечения пациентов с нарушением двигательной функции и тонуса толстой кишки, помимо спазмолитиков, слабительных препаратов, применяются пищеварительные ферменты, в состав которых входят компоненты желчи, вызывающие усиление моторики кишечника и способствующие разрешению запоров. 5. При функциональной диспепсии, у пожилых пациентов, при малоподвижном образе жизни, а также для купирования симптомов переедания целесообразен эпизодический прием небольших доз ферментов, содержащих компоненты желчи, что создает оптимальные условия для переваривания и всасывания нутриентов в тонкой кишке. Одним из ферментных препаратов, отвечающим всем современным требованиям к данной группе лекарственных веществ, является Панзинорм форте–Н. Панзинорм форте–Н содержит в каждой таблетке свиной панкреатин с энзимной активностью: липазы 20000 ЕД Ph.Eur., амилазы 12000 ЕД Ph. Eur.. протеазы 900 ЕД Ph. Eur. Показаниями к применению препарата являются:
- Недостаточность внешнесекреторной функции поджелудочной железы (хронический панкреатит, муковисцидоз и др.)
- Хронические воспалительно–дистрофические заболевания желудка, кишечника, печени, желчного пузыря; состояния после резекции или облучения этих органов, сопровождающиеся нарушениями переваривания пищи, метеоризмом, диареей (в составе комбинированной терапии).
- Для улучшения переваривания пищи у пациентов с нормальной функцией желудочно–кишечного тракта в случае погрешностей в питании.
Подготовка к рентгенологическому и ультразвуковому исследованию органов брюшной полости. Доза определяется индивидуально в зависимости от степени нарушения пищеварения. Продолжительность лечения может варьировать от однократного приема или нескольких дней (при нарушении процесса пищеварения вследствие погрешностей в диете) до нескольких месяцев или лет (при необходимости постоянной заместительной терапии). Важно помнить, что каждая группа ферментных препаратов имеет свои показания. Назначение препаратов строго по этим показаниям способствует эффективной нормализации процессов пищеварения, позволяет избежать побочных эффектов и приводит к улучшению клинического состояния пациентов. Неправильное использование ферментных препаратов приводит не только к отсутствию желаемого положительного эффекта, но даже к ухудшению состояния пациента, что способствует дискредитации этих препаратов. Нормализация такого сложного процесса, как пищеварение – трудоемкий процесс, требующий значительных усилий как со стороны врача, так и со стороны пациента. Терапия должна быть комплексной и основываться на патогенетических механизмах развития пищеварительной недостаточности у данного конкретного больного.
Литература
- Ивашкин В.Т., Шептулин А.А. и др. Краткое руководство по гастроэнтерологии.– М.: Издат. Дом М–Вести, 2001.
- Григорьев П.Я., Яковенко А.В. Клиническая гастроэнтерология. М.: МИА, 2001. с. 693.
- Губергриц Н. Б., Христич Т. Н. Клиническая панкреатология. — Донецк: Лебедь, 2000.
- Петухов В. А., Туркин П. Ю. Внешнесекреторная недостаточность поджелудочной железы при желчно–каменной болезни: этиопатогенез, диагностика и принципы лечения // Рус. мед. журн. — 2002. — Т. 10. — № 4. — С. 167–171.
- Губергриц Н. Б., Лукашевич Г. М. Ферментные препараты: от теории к практике. — Донецк: Лебедь, 2002.
- Щербаков панкреатическая недостаточность и ее лечение. Фармацевтический вестник №28 (227), 2001.
- Григорьев П.Я., Яковенко Э.П. Рекомендации к назначению ферментных препаратов при синдроме нарушенного пищеварения и всасывания. Леч. врач, № 5–6, 2001, С. 48–50, 52.
- Sarles H., Pastor J., Pauli A.M., Barthelemy M. Determination of pancreatic function. A statistical analysis conducted in normal subjects and in patients with proven chronic pancreatitis (duodenal intubation, glucose tolerance test, determination of fat content in the stools, sweat test) // Gastroenterol. 1963. Vol. 99. P. 279–300.
- Пчелинцев М.В. Препараты панкреатических ферментов, критерии выбора врачом общей практики. Новые СПб врач. ведомости, № 1, 2001, С. 63–66.
Пищеварительная недостаточность и ее коррекция с позиции врача–гастроэнтеролога. Костюкевич О.И. Русский Медицинский Журнал. Болезни органов пищеварения. 2008. Том 10, № 1, с. 10-14.
Популярные вопросы про гипоацидный гастрит
Как определить низкую кислотность желудка?
Точное определение кислотности может дать только РН-метрия. Но заподозрить ее низкий уровень можно в том случае, если вы спокойно можете есть кислый лимон.
Как отличить гастрит с повышенной и пониженной кислотностью?
Есть определенные признаки, характеризующие разные виды кислотности. Если это изжога или кислая отрыжка, то, скорее всего это говорит о повышенной кислотности. Для пониженной — характерна отрыжка с запахом тухлых яиц, что свидетельствует о плохо переваренной пище.
Что нельзя есть при гастрите с пониженной кислотностью?
Если обнаружен такой гастрит, лучше забыть о копченых, жирных, острых блюдах, ферментированных сырах, шоколаде, кофе и газированных напитках.
Кислотность — в чем смысл?
Как отмечает специалист, кислотность желудка — это характеристика концентрации соляной кислоты в желудочном соке, которая измеряется в единицах рН. Соляную кислоту вырабатывают клетки фундальных желез, их называют париетальными.
В гастроэнтерологии есть несколько типов pH-среды:
- повышенная (максимальный показатель 0,86 рН);
- пониженная (минимальный показатель 8,3 рН);
- нейтральная или нормальная (1,5-2,0 рН.).
«Здоровым считается только последний тип. При нормальной pH-среде ЖКТ быстро и хорошо переваривает поступающую пищу, нейтрализует попадающие вместе с ней токсины и инфекции. Если же кислотный показатель отклоняется в какую-либо сторону, человек начинает испытывать неприятные симптомы», — отмечает терапевт.
Заглянуть в желудок. Зачем делать гастроскопию через нос Подробнее