Форма выпуска, состав и упаковка
Мазь для наружного применения белого или почти белого цвета, с характерным запахом.
| 1 г | |
| сульфадиазин серебра | 10 мг |
Вспомогательные вещества: масло вазелиновое — 230 мг, пропиленгликоль — 100 мг, цетостеариловый спирт — 60 мг, глицерил моностеарат 40-55 — 30 мг, полисорбат 80 — 20 мг, метилпарагидроксибензоат — 0.8 мг, пропилпарагидроксибензоат — 0.2 мг, вода очищенная — до 1 г.
50 г — тубы алюминиевые (1) — пачки картонные.
Способ применения и дозы
Наружно, как открытым способом, так и в виде окклюзионных повязок.
После очищения и хирургической обработки на рану с соблюдением условий стерильности наносят препарат толщиной 2–3 мм 2–3 раза в сутки. Во время лечения вся рана должна быть покрыта кремом. Если часть раны откроется, необходимо дополнительно нанести крем. Наложение окклюзионной повязки возможно, но не является обязательным.
Крем наносится до полного заживления раны или до момента пересадки кожи. В случае применения препарата на инфицированные раны может появиться экссудат. Перед применением крема необходимо промыть рану антисептиком.
Максимальная суточная доза — 25 г. Максимальная продолжительность лечения — 60 дней.
Фармакологическое действие
Противомикробное средство широкого спектра действия, сульфаниламид. Оказывает бактерицидное действие.
Препарат активен в отношении грамположительных и грамотрицательных бактерий (Escherichia coli, Proteus spp., Staphylococcus spp., Klebsiella spp.).
Бактерицидные свойства мази Сульфаргин® обусловлены активностью ионов серебра, которые высвобождаются в ране в результате диссоциации серебряной соли сульфадиазина; высвобождение ионов серебра происходит постепенно (умеренная диссоциация), обеспечивая постоянство противомикробного действия. Бактерицидная активность ионов серебра дополняется бактериостатическим эффектом сульфадиазина (также высвобождающегося в процессе диссоциации серебряной соли сульфадиазина).
Сульфаргин® характеризуется умеренной осмотической активностью и не обладает некролитическими свойствами.
Трофические язвы чаще всего осложняют течение основного заболевания – варикозной или посттромбофлебетической болезни, синдрома диабетической стопы [3]. С точки зрения современной базисной теории, трофические нарушения при хронической венозной недостаточности (ХВН) являются следствием клапанной недостаточности различных отделов венозного русла нижних конечностей, в результате которой формируется и нарастает флебогипертензия. Последняя не вызывает прямой деструкции тканей, а действует через каскад патологических изменений на молекулярном, клеточном, микроциркуляторном и тканевом уровнях. Основными доказанными патогенетическими механизмами нарушений трофики при ХВН являются [4]: – лейкоцитарный захват (trapping) – значительное возрастание количества лейкоцитов в венах и венулах пораженной конечности; – окклюзия сосудов микроциркуляторного русла вследствие сладжирования и образования микротромбов; – активация лейкоцитов и их пенетрация в окружающие ткани; – экстравазальная полимеризация фибриногена в виде фибриновой «манжетки» вокруг венозного и артериального колен капилляров; – отек мягких тканей, следствием которого является увеличение расстояния между капиллярами и ухудшение метаболических процессов. В конечном итоге развивается повреждение тканей с возникновением первичного аффекта. Диабетические трофические язвы являются следствием диабетической макро-микроангиопатии и полинейропатии. Основной причиной заболеваемости, госпитализации и смертности больных сахарным диабетом является инфекционное поражение нижних конечностей. Инфекция – обычное осложнение формирующихся язв или ран на стопе [8]. В условиях нарушенного кровотока инфекция существенно ухудшает прогноз вероятности сохранения конечности или даже самой жизни [2]. Инфекционный процесс способствует тромбозу уже измененных вследствие атеросклероза артерий, что приводит к прогрессированию ишемии и развитию гангрены [6]. В настоящее время общепризнан полимикробный характер гнойного очага с ассоциацией аэробов и анаэробов на стопах у больных сахарным диабетом [5, 7]. Арсенал средств, используемых для местного лечения ран, в настоящее время значительно расширился, но его результаты остаются не вполне удовлетворительными в связи с высокой стоимостью и малой доступностью ряда препаратов. Стационарное лечение в течение нескольких месяцев является экономически нецелесообразным [1]. Одним из альтернативных методов местного лечения трофических язв нижних конечностей различной этиологии является назначение препарата Аргосульфан, представляющего собой 2% крем сульфатиазола серебряной соли. Установлено, что соединение серебра с сульфаниламидами оказывают антибактериальное действие, в несколько десятков раз более мощное, чем одни сульфаниламиды. Аргосульфан оказывает местное антимикробное действие, проявляя широкий спектр действия по отношению к грамотрицательным и грамположительным бактериям. Антибактериальное действие сульфатиазола усиливается влиянием серебра, которое обладает олигодинамическим эффектом и одновременно ослабляет сенсибилизирующие свойства сульфаниламидов. Ионы серебра тормозят рост и деление бактерий путем связывания с ДНК. Сульфатиазол тормозит размножение бактерий. Кроме того серебро способствует ускорению регенераторных процессов в ране. Слабая растворяемость серебряной соли сульфатиазола позволяет поддерживать постоянную концентрацию лекарства в ране, а также обеспечивает нетоксичность, обусловленную минимальной резорбцией. Гидрофильная основа и соответствующий уровень рН крема Аргосульфана, обеспечивают его болеутоляющее действие и хорошую переносимость. Следует подчеркнуть, что препарат характеризуется стабильностью, не разлагается под влиянием света. Материалы и методы исследования Исследование проводилось на базе отделения гнойно-септической хирургии ГКБ № 81. Был проведен анализ результатов лечения 72 пациентов с трофическими дефектами мягких тканей различной локализации и генеза, у которых в качестве местного лечения применяли Аргосульфан. Из их числа 44 больных находились в стационаре по поводу осложненных форм диабетической стопы (раны после лечения диабетических флегмон и гангрены стоп), 26 – с трофическими язвами голеней на фоне хронической венозной недостаточности с продолжительностью существования от 3 до 5 лет. Возраст пациентов составлял от 36 до 76 лет. Мужчин было 31 (43,1%), женщин 41 (56,9%). Характеристика больных по возрастному и половому составу представлена в таблице 1. Средняя длительность сахарного диабета у 44 больных превышала 15лет, что несомненно влияло на тяжесть течения раневого процесса в связи с нейро-вегетативными нарушениями и выраженными изменениями микроциркуляции. Отсутствие в отечественной хирургической практике рабочей классификации синдрома диабетической стопы позволяет нам предложить обобщенную классификацию, разработанную в нашей клинике, с учетом имеющих место морфо-анатомических изменений стопы, отражением состояния регионарного кровотока и сенсомоторных нарушений [1]. Классификация осложненных форм синдрома диабетической стопы А. По форме: 1. Нейропатическая стопа; 2. Ишемическая стопа; 3. Нейроишемическая стопа.
Б. По распространенности поражения (Wagner): 0 степень – отсутствуют изменения на кожных покровах и костные деформации; 1 степень – поверхностная язва без проникновения в глубокие слои; 2 степень – поверхностная язва с поражением сухожилия, кости, суставных связок; 3 степень – воспаление сухожильного влагалища, остеомиелиты или глубокие абсцессы; 4 степень – гангрена пальцев или всей стопы; 5 степень – гангрена всей ноги.
В. По локализации и характеру поражения: Правая, левая стопа, поражение обеих стоп. Поверхность – тыльная, подошвенная и одновременно та и другая. Область стопы – пальцы, плюсна, предплюсна, суставы, стопа в целом.
1. Пальцы (панариции: кожный, ногтевой (паронихия, подногтевой панариций), подкожный, сухожильный (гнойный тендовагинит, подошвенный и тыльный гнойный тендобурсит), костный, суставной, костно-суставной) 1.1. Язва: поверхностная, перфорирующая 1.2. Акральный некроз пальца 1.3. Пандактилит: гангрена – сухая, влажная.
2. Стопа 2.1. Абсцессы 2.1.1. Кожный 2.1.2. Мозольный
2.2. Флегмоны: 2.2.1. Эпифасциальная подошвенной и тыльной поверхности 2.2.2. Межпальцевая 2.2.3. Субапоневротическая подошвенной поверхности и тыла стопы 2.2.4. Латерального подошвенного пространства 2.2.5. Медиального подошвенного пространства 2.2.6. Срединного подошвенного пространства
2.3. Язва стопы 2.3.1. Поверхностная 2.3.2. Перфорирующая
2.4. Гангрена стопы 2.4.1. Сухая 2.4.2.Влажная
2.5. Панфлегмона.
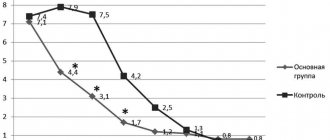
На основании предложенной классификации, у 26 больных (59,1%) диагностирована нейропатическая форма поражения стопы, у 18 (40,9%) – нейроишемическая. Нейроишемическая форма поражения стопы протекала с преобладанием нейропатии – у 65% и доминированием ишемии – у 35%. В группе наблюдаемых больных представлены пациенты с I и II типом сахарного диабета. В табл. 2 представлено распределение больных в зависимости от типа диабета, тяжести его течения и инсулинозависимости. Все изучаемые нами больные с осложненным синдромом диабетической стопы имели трофические нарушения в тканях стопы с формированием язв, абсцессов, флегмоны, остеомиелита, некроза, гангрены. У всех пациентов были выполнены различные органосохраняющие оперативные вмешательства на стопе (вскрытие и дренирование флегмон, экзартикуляция пальцев, резекции стоп, некрэктомии). В контрольную группу вошли 88 пациентов с трофическими язвам и ранами на нижних конечностях. Из них – 56 с осложненным синдромом стопы диабетика и 32 – с трофическими язвами на фоне венозной недостаточности, получавших в качестве местного лечения раневого процесса терапию стандартными препаратами (диоксидин, хлоргексидин, мазевые повязки с Левосином, Левомеколем). Для оценки эффективности проводимой антибактериальной терапии использовали данные цитологических исследований содержимого из ран и микробной обсемененности тканей гнойного очага. Результаты и обсуждение Применение Аргосульфана в местном лечении раневого процесса позволило добиться улучшения течения раневого процесса у всех больных. Это выражалось, в первую очередь, в уменьшении или исчезновении болевых ощущений при перевязках и вне их, в очищении раневого дефекта от некротических тканей с появлением зрелых грануляций и краевой эпителизации в области язвы к 10 суткам лечения у 24 из 26 больных с ХВН нижних конечностей, а также отсутствие или резкое снижение (до 102) роста микрофлоры. Наиболее часто высеваевыми возбудителями у этой группы пациентов явились Staphylococcus aureus – 78%, Pseudomonas aeruginosa – 13%, Proteus vulgaris – 9%. Использование Аргосульфана у пациентов этой группы приводило к быстрому рубцеванию язв (в среднем в течение 20–22 дней в зависимости от глубины и обширности дефекта), у 18 больных и у 8 позволило подготовить трофическую язву к пластическому закрытию, в отличие от пациентов контрольной группы, где данная динамика со стороны раневого процесса была отмечена только к 30–32 дню. У больных с осложненным синдромом диабетической стопы положительная динамика в местном лечении ран также получена у подавляющего числа пациентов. Локально: у 26 больных с нейропатической формой поражения стопы отмечали уменьшение или исчезновение отека на стопе, уменьшение или купирование явлений бактериального целлюлита, ограничение некрозов, тенденцию к очищению послеоперационных ран. Наиболее часто высеваемые возбудители у больных с осложненным синдромом стопы диабетика представлены в табл. 3. При нейроишемической форме поражения стопы у всех пациентов отмечали ограничение гнойно-некротического процесса на стопе с тенденцией к его очищению с купированием явлений перифокального воспаления. Следует отметить, что предотвращение генерализации инфекции на стопе у этой категории больных позволило провести комплекс консервативной терапии или выполнить реконструктивную операцию, направленную на купирование явлений критической ишемии на пораженной стопе. Данный момент считаем важным в патогенетическом лечении нейроишемической формы поражения стопы, так как ранние радикальные хирургические вмешательства на стопе без восстановления кровотока приводят в условиях ишемии к генерализации инфекции с развитием гангрены, что завершается высокой ампутацией конечности. У 4 пациентов на фоне местного применения Аргосульфана и комплексной консервативной терапии успешно выполнены реконструктивные хирургические вмешательства на артериях нижних конечностей и у 8-внебрюшинная поясничная симпатэктомия, направленная на улучшения регионарного кровотока на пораженной конечности. Таким образом, клиническая эффективность местного лечения раневого процесса Аргосульфаном составила 100%. Продолжительность местного лечения Аргосульфаном у больных с осложненным синдромом диабетической стопы осуществляли в среднем 14–20 дней, до появления отчетливого клинического эффекта и снижения уровня микробной контаминации в ране до 103 микробных тел в 1 г ткани, что позволило добиться заживление раны или подготовки ее к пластическому закрытию. Для оценки эффективности проводимого лечения использовали данные исследований цитологических отпечатков из ран и микробной обсемененности тканей гнойного очага. Цитологическое исследование отпечатков ран позволяет судить о характере и фазах течения раневого процесса, эффективности проводимого комплексного лечения, а также в свою очередь определить показания или противопоказания к различным консервативным и хирургическим мероприятиям. Цитологическое исследование основывалось на определении количественного и качественного состава нейтрофилов, лимфоцитов, макрофагов, фибробластов, наличия микрофлоры. Для более точного представления о динамике клеточного состава его выражали в процентах при подсчете 100 клеток в различных участках препарата, в зависимости от однородности клеточного состава раневых отпечатков у больных с различными формами осложненного синдрома стопы диабетика (нейропатическая, нейроишемическая). Анализ полученных данных свидетельствует, что при поступлении в стационар у 23% пациентов цитология раневого процесса носила дегенеративно-воспалительный характер. Клеточный состав раны при этом виде цитограммы характеризовался присутствием нейтрофилов, находящихся в состоянии различной степени разрушения, а также большим количеством микроорганизмов. У 39% больных отмечен гнойно-некротический тип цитограммы. Об этом свидетельствовало большое количество нейтрофилов, находящихся в состоянии дегенерации и деструкции. У всех пациентов в цитограммах среди разрушенных нейтрофилов отмечалось присутствие микроогранизмов. У 38% больных цитология раневого процесса соответствовала гнойно-воспалительному типу. У этой группы пациентов клеточный состав характеризовался преобладанием нейтрофилов, большая часть которых находилась в стадии распада. Другие клеточные элементы в раневом отпечатке имели дистрофические изменения. Цитологическую динамику раневого процесса оценивали с момента поступления больного, на 3, 5, 10, 15 сутки лечения. На 10–14 сутки проведения антибактериальной терапии левофлоксацином цитологическая характеристика раневого процесса менялась – у 42% с переходом на воспалительный тип, у 38% на воспалительно-регенераторный, который характеризовался преобладанием нейтрофильной реакции, в сочетании с высоким уровнем лимфоцитов и макрофагов, а также присутствием в мазках-отпечатках единичных фибробластов. Продолжение курса антибактериальной терапии у больных с воспалительным типом цитограммы в течение 10–14 дней позволило изменить его у 79% больных на регенераторный. В те же сроки удавалось достигнуть снижения уровня микробной контаминации в гнойном очаге до 103–104 микробных тел у 97% больных, в отличие от контрольной группы, где данная степень микробной контаминации была достигнута только у 78%. Комплекс клинических, микробиологических и цитологических исследований позволяли решить вопрос об отмене антибактериальных препаратов. Дальнейшее лечение открытой раны проводили только под повязками с Аргосульфаном, обеспечивающим высокий антимикробный эффект непосредственно в ране. В контрольной группе у 36% пациентов продолжали применять антибактериальную терапию широкого спектра действия. Выводы 1. Аргосульфан хорошо смешивается с прираневым секретом и предупреждает прилипание марлевой повязки к прираневой поверхности. 2. Во время лечения препаратом наблюдается активизация процессов грануляции и эпителизации в прираневой поверхности. 3. Аргосульфан хорошо переносится больными, во время лечения не выявлено ни одного случая местных или общих аллергических реакций. 4. Аргосульфан 2% крем эффективно предупреждает возникновение реинфекции прираневой поверхности благодаря широкому спектру антимикробной активности.
РЕФЕРАТ Аргосульфан в лечении трофических и диабетических язв нижних конечностей В статье представлены результаты собственного исследования эффективности Аргосульфана в лечении трофических и диабетических язв нижних конечностей. В ходе исследования клиническая эффективность местного лечения раневого процесса Аргосульфаном составила 100%. Наблюдалось ускорение грануляции и эпителизации раневой поверхности и уменьшение микробной обсемененности. Препарат удобен в применении, не вызывает побочных реакций и может быть рекомендован в качестве местного антибактериального и ранозаживляющего средства для широкого применения в клинической практике у больных с трофическими язвами нижних конечностей.
ЛИТЕРАТУРА 1. Брискин Б.С., Прошин А.В., Кузнецов Е.В. и соавт. Основные направления в комплексной терапии больных с осложненными формами стопы диабетика //Международный медицинский журнал. 2001. № 8. С. 49-52. 2. Дибиров М.Д., Брискин Б.С. Хирургическое лечение осложнений диабетической ангиопатии // Москва. 2001. 327с. 3. Кириенко В.Ю., Богачев В.Ю., Богданец Л.И. Лечение трофических язв венозной этиологии // Consilium medicum. 2000. С. 22-26. 4. Савельев В.С., Кириенко А.И., Богачев В.Ю. Венозные трофические язвы // Флеболимфология. 2000. № 11. С. 5-10. 5. Светухин А.М., Земляной А.Б. Гнойно-некротические формы синдрома диабетической стопы // Consilium medicum. 2002. Т. 4. № 10. С. 537-544. 6. Boyko E.J., Lipsky B.A. Infection and diabetes. In: Harris (ed) Diabetes in America, 2nd Ed. Bethesda, Md., National Institutes of Health Publication 1995:95 – 1468. 7. Gerding D.N. Foot infections in diabetic patients: the role of anaerobes. Clin. Infect. Dis 1995;20(Suppl. 2):283- 8. Lipsky E.A. Infections problems of the foot in diabetic patients. Levin and O’Neal’s The Diabetic Foot. Eds. Bowker J.H., Pfeifer M.A. St. Louis, CV Mosby, 6th Ed. 2001. 467-80.
Поликлиника № 2 2006 (14-19)
Режим дозирования
Применяют наружно.
После хирургической обработки раны и удаления некротических тканей мазь наносят на поврежденную поверхность тонким слоем 2-4 мм (под повязку или открытым способом) 1-2 раза/сут. Максимальная разовая доза — 300 г. Длительность лечения устанавливается индивидуально, зависит от характера заболевания и эффективности применяемого лечения и, как правило, составляет до 3 недель.
Если применение препарата было пропущено, следует как можно быстрее нанести мазь и продолжать применение в обычное время, не удваивая дозу.
Если пациент чувствует, что действие препарата слишком сильное или слабое, следует сообщить об этом врачу или провизору.
Противопоказания
Гиперчувствительность (в т.ч. к другим сульфаниламидам), врожденный дефицит глюкозо−6-фосфатдегидрогеназы, ранний детский возраст (новорожденные и младенцы до 2 мес, недоношенные дети) в связи с риском развития ядерной желтухи.
Не рекомендуется применять во время беременности. В период кормления грудью препарат можно назначать только в случае, если поверхность ожога не превышает 20% поверхности тела, и лечебная польза для матери больше, чем возможный риск для ребенка.
Побочное действие
Местные реакции: жжение и зуд в месте нанесения, нарушение пигментации кожи, кожные аллергические реакции, некроз кожи.
Системные реакции: многоформная эритема, интерстициальный нефрит, лейкопения, которая характеризуется в основном снижением числа нейтрофилов. Максимальное снижение числа лейкоцитов наблюдается на 2-4 сут после начала лечения; нормализация числа лейкоцитов наблюдается на 2-4 сут, при этом продолжение лечения препаратом не оказывает влияния на процесс восстановления числа лейкоцитов.
При длительном применении на больших раневых поверхностях: системные побочные эффекты, характерные для сульфаниламидов, в т.ч. нарушение кроветворения (агранулоцитоз, апластическая и гемолитическая анемия, тромбоцитопения, лейкопения), кожные и аллергические реакции, в т.ч. синдром Стивенса-Джонсона и эксфолиативный дерматит; диспепсия, гепатит, гепатоцеллюлярный некроз, нарушение функции ЦНС и токсический нефроз.
Степень абсорбции препарата зависит от размера ожоговой поверхности и степени повреждения тканей.
Фармакокинетика
Содержащаяся в препарате серебряная соль сульфатиазола обладает небольшой растворимостью, в результате чего после местного применения концентрация лекарства в ране длительно поддерживается на одинаковом уровне. Благодаря минимальной резорбции препарата он не оказывает токсического действия. Только незначительное количество серебряной соли сульфатиазола оказывается в кровотоке, после чего подвергается в печени ацетилированию.
В моче находится в виде неактивных метаболитов и частично в неизмененном виде. Абсорбция сульфатиазола увеличивается после применения лекарства на обширных раневых поверхностях.
Противопоказания к применению
— беременность;
— период лактации;
— выраженный дефицит глюкозо-6-фосфатдегидрогеназы;
— детский возраст до 1 года;
— повышенная чувствительность к сульфаниламидам.
Препарат не следует применять для лечения глубоких гнойных ран и ожоговых поверхностей с обильной экссудацией.
С осторожностью: почечная/печеночная недостаточность, дефицит глюкозо-6-фосфатдегидрогеназы (риск развития гемолиза).
Перед применением лекарства рекомендуем проконсультироваться с врачом онлайн
Показания препарата Аргосульфан®
Ожоги различной степени, любой природы (термические, солнечные, химические, электрическим током, лучевые и т.д.), обморожения.
Пролежни, трофические язвы голени различного генеза (в т.ч. при хронической венозной недостаточности, облитерирующем эндартериите, нарушениях кровоснабжения при сахарном диабете, роже и т.д.).
Гнойные раны, мелкие бытовые травмы (порезы, ссадины).
Инфицированные дерматиты, простой контактный дерматит, осложненный импетиго, микробная экзема, стрептостафилодермия.
Особые указания
При лечении пациентов с печеночной и/или почечной недостаточностью необходимо регулярно проводить контроль концентрации сульфаниламидов в плазме.
Соли серебра, вступая в реакции с кислородом воздуха, металлами и другими химическими компонентами, особенно при катализирующем тепловом воздействии, темнеют, поэтому препарат следует хранить в закрытой таре и вдали от источников тепла.
Части тела, обработанные препаратом, рекомендуется предохранять от действия прямых солнечных лучей.
Влияние на способность к управлению транспортными средствами и механизмами
Препарат не влияет на способность управлять транспортными средствами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.