Химические свойства
Дроспиренон — что это такое? Данное вещество относится к группе пероральных контрацептивных средств. Чаще всего его применяют в комбинации с другими гормонами. Лекарство способно оказывать терапевтическое действие на андрогензависимые болезни.
Дроспиренон — что это за гормон? Дроспиренон – это синтетический гормон, по своим свойствам близок к натуральному прогестерону, производное спиронолактона. Молекулярная масса химического соединения = 366,5 грамм на моль. Плотность вещества = 1,26 грамм на см3, температура плавления составляет примерно 200 градусов Цельсия.
Дроспиренон в Википедии упоминается в статьях о гормональной контрацепции и влиянии лекарственных средств на половую функцию человека.
Фармакодинамика и фармакокинетика
Благодаря тому, что данное вещество обладает ярко выраженными антиандрогенными свойствами, оно благоприятно влияет на течение андрогензависимых заболеваний, таких как акне, алопеция и себорея. Дроспиренон стимулирует выведение ионов натрия и прочих жидкостей из организма, вследствие чего нормализуется артериальное давление, спадает отечность и болезненность в молочных железах, снижается масса тела.
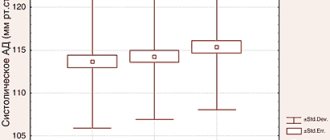
Клинические исследования показали, что уже после 4 месяцев применения лекарства систолическое давление снижается в среднем на 2-4 мм ртутного столба, а диастолическое — на 1-3 мм рт. ст., вес снижается на 1-2 кг. У женщин во время менопаузы значительно снижается вероятность возникновения рака толстой кишки, гиперплазии и рака эндометрия.
Синтетический гормон не обладает эстрогенной, андрогенной и глюкокортикостероидной активностью, не изменяет инсулинорезистентность и реакцию организма на глюкозу. В процессе лечения препаратом у пациента снижается уровень холестерина в крови и ЛПНП, незначительно повышается концентрация триглицеридов.
После приема таблеток, содержащих Дроспиренон, активное вещество быстро и практически полностью усваивается организмом. Биологическая доступность вещества составляет порядка 75-85%. Параллельный прием пищи не оказывает влияния на фармакокинетику препарата. Концентрация лекарства в плазме крови снижается двухфазно, период полувыведения составляет 35-40 часов. При систематическом, ежедневном приеме равновесная концентрация средства наблюдается через 10 суток.
У средства большая степень связывания с белками плазмы (сывороточный альбумин) – порядка 95-97%. Основные метаболиты гормона образуются, не затрагивая систему цитохрома Р450. Выводится препарат в форме метаболитов с калом и мочой, незначительная часть экскретируется в неизмененном виде.
Опыт применения дроспиренон–содержащего гормонального контрацептива
Геворкян М.А., Манухин И.Б., Тихомиров А.Л., Кузнецова Е.М.
Планирование семьи в течение многих десятилетий является важной медико–социальной проблемой. В России этот вопрос стоит наиболее остро, поскольку количество абортов продолжает оставаться высоким. Каждый второй аборт (даже без осложнений) впоследствии приводит к бесплодию, что значительно снижает репродуктивный потенциал нации. Особенно это касается подросткового возраста, когда еще не сформировалась функция репродуктивной системы. Известно, что период полового созревания является критическим в жизни женщины и влияние различных факторов (в частности, прерывание беременности) способствует нарушениям овариальной функции, эндокринному бесплодию.
Из всех методов предохранения от нежеланной беременности наиболее надежным является использование оральных контрацептивов (ОК). Применение внутриматочных контрацептивов, особенно у нерожавших молодых женщин, нежелательно из–за риска развития воспалительных заболеваний органов малого таза и трубного бесплодия. В последние годы в России все больше женщин отдают предпочтение ОК. В крупных городах число пользователей ОК составляет до 15 %. И это, несомненно, связано с совершенствованием препаратов, которые оказывают минимальные побочные эффекты. Основной причиной как нежелания принимать ОК, так и прекращения их дальнейшего использования является прибавка веса. Кроме того, поводом к прекращению приема ОК становятся боли в молочных железах (масталгия), изменение настроения, головные боли. Все эти побочные эффекты в основном обусловлены эстрогенами и усугубляются прогестагенным компонентом, поэтому десятилетиями продолжался поиск прогестагена, который по свойствам был бы максимально приближен к эндогенному прогестерону.
Дроспиренон – новый прогестаген, входящий в состав монофазного ОК Мидиана (). Дроспиренон является аналогом спиролактона и обладает антиминералокортикоидным эффектом, благодаря чему он предотвращает симптомы эстрогенов, связанные с задержкой натрия, что клинически проявляется прибавкой веса, отеками и масталгией. Это очень важное преимущество Мидианы, позволяющее использовать его при ПМС (предменструальный синдром), симптомы которого можно наблюдать более чем у 50 % женщин репродуктивного возраста.
Кроме того, являясь производным спиролактона (который давно известен, как блокатор периферических рецепторов к андрогенам), дроспиренон эффективен в лечении дерматологических проявлений гиперандрогении, особенно угревой сыпи. Известно, что все эстроген–содержащие ОК обладают антиандрогенным действием, которое основано на увеличении концентрации в крови глобулинов, связывающих половые стероиды (ГСПС), в результате чего снижается свободная (биологически активная) фракция андрогенов. Однако большинство прогестагенов предыдущего поколения нивелировали эти эффекты. Дроспиренон не влияет на вызванное эстрогенами повышение в крови содержания ГСПС. Эти антиандрогенные эффекты дроспиренона предоставляют женщинам дополнительные неконтрацептивные преимущества.
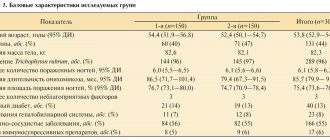
Для определения эффективности и побочного действия нового ОК Мидиана в наше исследование было включено 54 женщины в возрасте 16–40 лет (средний возраст 26±1,6)), из них 34 – «переключившиеся» с других ОК и 20 – впервые начинающие использовать ОК. Препарат применяли в течение 6 циклов (всего 324 цикла). Учитывая наш большой опыт, для уменьшения частоты ациклических кровянистых выделений у впервые использующих ОК рекомендовали применять препарат с 5 по 25–й день цикла с дополнительной барьерной контрацепцией в 1 цикле.
В процессе наблюдения оценивали контрацептивную надежность, которая составила 100%, что, возможно, связано с небольшой длительностью наблюдения (6 циклов). Кроме того, оценивали характер побочных эффектов, частота которых была выше у начинающих пользователей.
Ациклические кровянистые выделения не отмечались в 96% циклов. В 3,7 % циклов отмечались мажущие кровянистые выделения в 1–2 цикле, частота циклов с прорывными кровотечениями составила всего 0,3%. Только одна женщина (из начинающих) в связи с этими побочными эффектами отказалась от дальнейшего приема ОК.
Прибавка веса (незначительная, на 1–2 кг) отмечалась у 5 женщин (9,3%), в основном это начинающие пользователи ОК, что можно объяснить, скорее всего, эстрогенным компонентом ОК. Однако это не послужило поводом для прекращения приема препарата. Этих женщин устраивали дополнительные преимущества Мидианы, в частности, регресс угревой сыпи. Интерес представляют 28% женщин (все из «переключившихся» с других ОК), которые отмечали снижение веса на фоне Мидианы, что связано с антиминералокортикоидным действием дроспиренона.
Болезненность молочных желез (масталгия) отмечали 3 женщины (5,6%) – все они впервые начали прием ОК. Эти эффекты также больше связаны с эстрогенным компонентом и прекратились на 4–м цикле, т.е. оптимальное время привыкания к ОК.
Головные боли отмечали 11% женщин в первые 2 цикла, из них в основном начинающие пользователи ОК. Симптоматические средства купировали эти эффекты, и женщины продолжали принимать ОК.
Изменение настроения, тошнота также отмечались у небольшого числа женщин (1,9 и 3,7% соответственно) в группе начинающих пользователей. Следует отметить, что у женщин, жаловавшихся на тошноту, в анамнезе были нарушения функции желудочно–кишечного тракта или дисбактериоз кишечника после применения антибактериальных препаратов. Эти побочные эффекты отмечались в течение 1–3 циклов и не явились причиной отказа от дальнейшего использования ОК Мидиана.
Следует отметить, что имелось сочетание нескольких побочных эффектов у одной женщины, поэтому общее число женщин, предъявляющих различные жалобы, значительно меньше.
Таким образом, небольшая частота побочных эффектов (11%) на фоне приема нового ОК Мидиана свидетельствует о его хорошей переностимости и высокой контрацептивной эффективности, что обусловлено прогестагеном (дроспиренон), по структуре максимально приближенному к эндогенному прогестерону. Этот вывод подтверждается также тем, что только одна женщина (1,9%) в связи с продолжающимися прорывными кровотечениями отказалась от использования ОК. Более того, ациклические кровянистые выделения наблюдаются на фоне любых ОК.
Как было отмечено, ОК XXI века имеют дополнительные преимущества, в частности, положительное влияние на состояние кожи и симптомы ПМС, которые оказывают отрицательное действие на психоэмоциальную сферу, снижая качество жизни. Поэтому, исходя из свойств дроспиренона интерес представляет влияние ОК Мидиана на состояние кожи (угревую сыпь) и симптомы ПМС.
Влияние ОК Мидианы на состояние кожи. Из 54 женщин, включенных в исследование, 29 принимали ОК не только с целью контрацепции, но и для лечения угревой сыпи. В основном это молодые девушки 16–23 лет, не рожавшие. Выбор ОК у этого контингента женщин требует особой осторожности, поскольку длительный прием ОК может привести к синдрому гиперторможения гонадотропной функции гипофиза. Прогестагены, приближенные к эндогенному прогестерону (дроспиренон) в составе ОК, оказывают наименее выраженное антигонадотропное действие, что подтверждено нашими данными УЗ мониторинга фолликулогенеза, который выявил нормальный рост фолликулов у 25% женщин. Контрацептивный эффект препарата основан на уровне подавления овуляторного пика гонадотропинов, и в большей степени – атрофических процессах в эндометрии. С целью лечения угревой сыпи длительное время успешно применялся ОК Диане–35. Однако у женщин с избыточной массой тела он способствовал прибавке веса. 9 переключившихся на Мидиану женщин не только отметили улучшение состояния кожи, но и снижение массы тела на 2–3 кг.
Эффективность лечения симптомов ПМС. Из 54 обследованных женщин симптомы ПМС выявлены у 19. Возраст этих женщин составил в среднем 34,5 лет, т.е. более старший. В этом возрасте повышается частота метаболического синдрома и других экстрагенитальных заболеваний, что требует выбора наиболее безопасного ОК, к которым относится Мидиана. Более того, в гетерогенной клинике ПМС всегда имеются симптомы, связанные с задержкой жидкости (отеки, мастодиния), что ограничивало использование ОК предыдущего поколения. Антиминералокортикоидное действие дроспиренона открывает новые возможности в лечении ПМС, наблюдаемого у большинства овулирующих женщин репродуктивного возраста. По результатам настоящего исследования, уже через 3 цикла отмечена положительная динамика в регрессе симптомов ПМС, а через 6 циклов все женщины отметили значительное улучшение и были согласны на продолжение приема Мидианы.
Таким образом, на основании результатов проведенного исследования, имеющихся работ зарубежных авторов можно заключить, что новый ОК Мидиана является высокоэффективным контрацептивом; содержит новый прогестаген дроспиренон, максимально приближенный к эндогенному прогестерону, обладающий антиминералокортикоидным и антиандрогенным действием. Именно дроспиренон способствует стабильному весу, хорошей переносимости с минимальными побочными эффектами. Дополнительные преимущества – уменьшение симптомов ПМС и угревой сыпи делают ОК Мидиана на сегодня препаратом первого выбора.
Литература
1. Руководство по контрацепции. Под редакцией В.Н. Прилепской. М. 2006.
2. Манухин И.Б., Тумилович Л.Г., Геворкян М.А. Клинические лекции по гинекологической эндокринологии. М. Геотармедиа. 2009.
3. J.Verchaeghe. Hormonal contraception in women with metabolic syndrome. Contraception Reproductive Health Care. 2010. 5 (5); 305–314.
4. A. Motivala, B. Pitt. Drospirenone fore Oral Contraception and Hormone Replacement Therapy. Drugs. 2007; 7 (5): 47–655.
5. U. Halbreich, T. Backstrom et all. Clinical diagnostic criteria for premenstrual syndrome and guidelines for research studies. Genecolodical Endocrinjlogy. 2007; 23 (3); 123–130.
6. G. Paul, C. Bell et al. The real deal: A feasibility study of peer–led sex education for early school leavers. Contraception Reproductive Health Care. 2010. 5 (5); 343–357.
Показания к применению
Средство назначают:
- в составе комплексной терапии для профилактики постменопаузного остеопороза;
- при необходимости проведения гормональной контрацепции у женщин с дефицитом фолатов или задержкой жидкости в организме;
- в качестве заместительного гормонального лечения при климактерических расстройствах для устранения приливов, потливости и прочих вазомоторных симптомов;
- при инволюционных изменениях мочеполового тракта у женщин с неудаленной маткой;
- в сочетании с прочими синтетическими гормонами для контрацепции;
- для контрацепции при тяжелом ПМС;
- при тяжелой и умеренной форме угрей для контрацепции.
Противопоказания
Лекарство противопоказано:
- пациентам с аллергией на Дроспиренон;
- при порфирии;
- лицам со склонностью к образованию тромбов;
- при тяжелой печеночной недостаточности;
- во время лактации;
- при тромбоэмболии или тромбофлебите в тяжелой форме;
- если у пациентки наблюдаются вагинальные кровотечения неизвестного происхождения;
- при раке молочной железы или других половых органов;
- беременным женщинам.
Побочные действия
Во время лечения препаратом могут развиться:
- аллергические реакции различной степени тяжести, головокружение;
- тромбоэмболия легочной артерии или сосудов головного мозга;
- тромбофлебит, тромбы в венах сетчатки;
- артериальная гипертензия, отечность, головные боли;
- калькулезный холецистит;
- сонливость, апатия, депрессивные состояния;
- снижение остроты зрения, рвота, рост или снижение веса;
- галакторея, тошнота, гирсутизм;
- алопеция, болезненные ощущения и набухание молочных желез;
- кровянистые или необычной консистенции вагинальные выделения;
- снижение сексуального влечения, хлоазма;
- бессонница, снижение судорожного порога, варикоз.
Взаимодействие
При длительном лечении препаратами, который индуцируют ферменты печени (барбитуратами, карбамазепином, оскарбазепином, производными гидантоина, примидоном, рифампицином, топираматом, гризеофульвином, фелбаматом) повышает клиренс данного вещества и снижает их эффективность. Как правило этот эффект проявляется через 2-3 недели, после начала проведения терапии и сохраняется в течение месяца после прекращения приема препаратов.
Лекарство снижает эффективность препаратов, стимулирующих гладкую мускулатуру матки и анаболических стероидов.
Видора таб п/об пленочной 3мг+0.03мг 28 шт (21+7)
Внутрь, целиком, не разжевывая, с небольшим количеством воды, по 1 таблетке в день, по порядку, обозначенному на блистере, начиная с активных таблеток (21 таблетка желтого цвета) и заканчивая таблетками плацебо (7 таблеток белого цвета) желательно в одно и то же время суток, непрерывно в течение 28 дней. Во время приёма неактивных таблеток (плацебо, таблетки белого цвета) наблюдается менструальноподобное кровотечение. Оно обычно начинается на 2-3 день после приема последней активной таблетки и может не закончиться до начала приема таблеток из новой упаковки. Прием препарата из каждой последующей упаковки начинается без перерыва на следующий день, как только заканчиваются таблетки в предыдущей упаковке. При отсутствии приема каких-либо гормональных контрацептивных препаратов в предыдущем месяце приём препарата Видора® следует начинать в первый день менструального цикла (в первый день менструального кровотечения). Допускается начало приёма на 2-5 день менструального цикла, но в этом случае рекомендуется дополнительно использовать барьерный метод контрацепции в течение первых 7 дней приёма таблеток из первой упаковки Переход с другого комбинированного гормонального контрацептива (КОК, вагинального кольца или трансдермального пластыря) Предпочтительно начинать приём препарата на следующий день после приёма последней активной таблетки/драже, но не позднее следующего дня после обычного 7-дневного перерыва в приёме (для препаратов, содержащих 21 таблетку/драже) или после приёма последней неактивной таблетки/драже (для препаратов, содержащих 28 таблеток/драже в упаковке). Прием таблеток препарата Видора® следует начинать в день удаления вагинального кольца или пластыря, но не позднее дня, когда должно быть введено новое кольцо или наклеен новый пластырь
Переход с гормональных контрацептивов, содержащих только гестагены («мини-пили», инъекционных форм, подкожных имплантатов и внутриматочных систем с контролируемым высвобождением гестагена) При переходе с «мини-пили» можно начинать приём препарата в любой день (без перерыва), с имплантата или внутриматочной системы с гестагеном — в день удаления имплантата или внутриматочной системы, с инъекционной формы — со дня, когда должна была быть сделана следующая инъекция. Во всех случаях необходимо дополнительно использовать барьерный метод контрацепции в течение первых 7 дней приёма таблеток Видора®.
После аборта в I триместре беременности
Можно начинать приём препарата немедленно. При соблюдении этого условия нет необходимости в дополнительной контрацептивной защите.
После родов или аборта во II триместре беременности
Рекомендуется начинать приём препарата на 21-28 день после родов, при отсутствии грудного вскармливания, или аборта. Если приём начат позднее, необходимо использовать дополнительно барьерный метод контрацепции в течение первых 7 дней приёма таблеток препарата Видора®. В случае наличия полового контакта до начала приема препарата должна быть исключена беременность или необходимо дождаться первой менструации.
Приём пропущенных неактивных таблеток (плацебо) Если пропущен прием таблеток плацебо (белых таблеток из последнего ряда блистерной упаковки), никаких мер принимать не требуется. Непринятые таблетки необходимо выбросить, чтобы избежать непреднамеренного увеличения продолжительности периода приема таблеток плацебо.
Приём пропущенных активных таблеток
Если пропущен прием активных (желтых) таблеток и опоздание в приёме очередной таблетки составило менее 12 ч, контрацептивная защита не снижается. Пропущенную таблетку следует принять как можно скорее. Далее таблетки следует принимать в обычном режиме. Если опоздание в приёме очередной таблетки составило более 12 ч (интервал с момента приёма последней таблетки больше 36 ч), контрацептивная защита может быть снижена. Чем больше таблеток пропущено подряд, и чем ближе этот пропуск к 7 дневному перерыву в приёме препарата, тем выше вероятность наступления беременности, поскольку 7 дней непрерывного приема препарата требуются для достижения адекватного подавления гипоталамо-гипофизарно- яичниковой системы. Для таких ситуаций могут быть даны следующие рекомендации:
На 1 неделе приёма препарата
Пропущенную таблетку следует принять как можно скорее (как только женщина вспомнит), даже если это означает приём двух таблеток одновременно. Далее таблетки следует принимать в обычном режиме. Дополнительно должен быть использован барьерный метод контрацепции в течение последующих 7 дней. Если половой контакт имел место в течение недели перед пропуском в приёме очередной таблетки, необходимо учитывать вероятность наступления беременности.
На 2 неделе приёма препарата
Пропущенную таблетку следует принять как можно скорее (как только женщина вспомнит), даже если это означает приём двух таблеток одновременно. Далее таблетки следует принимать в обычном режиме. Если в течение 7 дней, предшествующих первому пропуску в приёме, все таблетки принимались правильно, нет необходимости использовать дополнительные меры контрацепции. В противном случае, а также в случае пропуска двух и более таблеток, необходимо использовать дополнительный барьерный метод контрацепции в течение последующих 7 дней.
На 3 неделе приёма препарата
В случае пропуска на 3 неделе приема препарата, необходимо принять последнюю пропущенную таблетку как можно скорее (даже если это означает прием 2 таблеток одновременно). В случае пропуска таблеток не следует принимать более двух активных таблеток в один день. Далее таблетки следует принимать в обычном режиме, пока не закончатся активные таблетки в упаковке. Неактивные таблетки следует выбросить и незамедлительно начать прием таблеток из следующей упаковки, т.е. без перерыва. Дополнительно должен быть использован барьерный метод контрацепции в течение следующих 7 дней. Вероятнее всего, кровотечения «отмены» не будет до конца второй упаковки, но могут наблюдаться «мажущие» кровянистые выделения или маточное кровотечение «отмены» в дни приема препарата из второй упаковки. Если женщина пропускала прием активных таблеток, и во время приема неактивных таблеток кровотечения «отмены» не наступило, необходимо исключить беременность
Рекомендации при желудочно-кишечных расстройствах
При тяжелых желудочно-кишечных расстройствах всасывание может быть неполным, поэтому следует принять дополнительные меры контрацепции. Если в течение 4 ч после приема активной (желтой) таблетки произошла рвота или была диарея, следует ориентироваться на рекомендации при пропуске таблеток. Если женщина не хочет менять обычную схему приема и переносить начало менструальноподобного кровотечения на другой день недели, дополнительную активную таблетку следует принять из другой упаковки.
Изменение дня начала менструальноподобного кровотечения
Чтобы отсрочить наступление менструальноподобного кровотечения, женщине следует продолжить прием таблеток из следующей упаковки препарата Видора®, пропустив неактивные таблетки из текущей упаковки. Таким образом, цикл приема препарата может быть продлен, по желанию, на любой срок, пока не закончатся активные таблетки из второй упаковки. На фоне приема препарата из второй упаковки у женщины могут о выделения или «прорывные» маточные кровотечения. Регулярный прием препарата Видора® возобновляется после окончания приема неактивных таблеток. Чтобы перенести начало менструальноподобного кровотечения на другой день недели, женщине следует сократить длительность приема неактивных таблеток на желаемое количество дней. Чем короче интервал, тем выше риск, что у нее не будет кровотечения «отмены», и в дальнейшем будут «мажущие» выделения и «прорывные» кровотечения во время приема таблеток из второй упаковки
Дополнительная информация о применении в особых клинических группах
Применение у детей. Препарат Видора® показан только после наступления менархе. Имеющиеся данные не предполагают коррекции дозы у данной группы пациенток.
Применение в пожилом возрасте. Препарат Видора® не показан после наступленияменопаузы.
Применение при нарушении функции печени. Препарат Видора® противопоказан женщинам с тяжелыми заболеваниями печени до тех пор, пока показатели функциональных проб печени не придут в норму.
Применение при нарушении функции почек. Препарат Видора® противопоказан женщинам с тяжелой почечной недостаточностью.
Особые указания
При проведении ряда неконтролируемых рандомизированных исследований был выявлен повышенный риск развития венозной тромбоэмболии во время лечения средством. Необходимо с особой осторожностью назначать препарат женщинам, у которых имеется предрасположенность к возникновению венозной тромбоэмболии (наследственность, ожирение, возраст). Необходимо внимательно соотнести показатели “риск – польза”.
Редко на фоне лечения возникали доброкачественные, и еще реже — злокачественные опухоли печени. Если у пациента имеются какие-либо признаки данного заболевания, боли в области под ребрами, увеличение органа и внутрибрюшное кровотечение, то лечение необходимо прервать.
У пациенток с умеренной и легкой степенью почечной недостаточности прием данного синтетического гормона может повлиять на концентрацию ионов калия в сыворотке крови. Имеется небольшой риск развития гиперкалиемии, особенно, если пациент дополнительно принимает калийсберегающие лекарства.
Перед началом лечения средством рекомендуется пройти гинекологическое и общемедицинское обследование, особое внимание рекомендуется уделить цитологическому исследованию церквиальной слизи и молочных желез, систему свертывания крови, исключить беременность. Во время проведения терапии периодически эти исследования следует повторять.
Дроспиренон (Drospirenone)
Фармакокинетика
После приема внутрь дроспиренон всасывается быстро и почти полностью. Cmax действующего вещества в сыворотке крови составляет 38 нг/мл и достигается через 1-2 ч после однократного приема. Биодоступность составляет 76-85%. Одновременный прием пищи не влияет на биодоступность дроспиренона.
Дроспиренон связывается с альбумином сыворотки крови и не связывается с глобулином, связывающим половые гормоны (ГСПГ) или с глобулином, связывающим кортикоиды (ГСК). Всего 3-5% общей сывороточной концентрации дроспиренона существует в виде свободных стероидов. Индуцированное этинилэстрадиолом увеличение ГСПГ не влияет на связывание дроспиренона с сывороточными белками. Средний кажущийся Vd дроспиренона составляет 3.7±1.2 л/кг.
Во время одного цикла лечения Cssmax дроспиренона в плазме крови составляет около 70 нг/мл, достигается после 8 дней лечения. Концентрации дроспиренона в сыворотке крови увеличиваются приблизительно в 3 раза вследствие соотношения конечного T1/2 и интервала дозирования.
После приема внутрь дроспиренон подвергается интенсивному метаболизму. Основные метаболиты в плазме крови — кислотная форма дроспиренона, образовавшиеся при раскрытии лактонного кольца, и 4,5-дигидро-дроспиренон-3-сульфат, оба образуются без участия системы Р450. Дроспиренон в малой степени метаболизируется CYP3А4 и способен ингибировать этот фермент, а также CYP1А1, CYP2С9 и CYP2С19 in vitro.
Т1/2 дроспиренона с соответствующим снижением его концентрации в сыворотке крови после приема внутрь составляет 31 ч. Почечный клиренс метаболитов дроспиренона в сыворотке крови составляет 1.5±0.2 мл/мин/кг. Дроспиренон экскретируется только в следовых количествах в неизмененном виде. Метаболиты дроспиренона выводятся через кишечник и почками в соотношении около 1.2:1.4. T1/2 метаболитов почками и через кишечник составляет около 40 ч.
Css дроспиренона в плазме крови у женщин с почечной недостаточностью легкой степени тяжести (КК 50-80 мл/мин) была сравнима с соответствующими показателями у женщин с нормальной функцией почек. У женщин с почечной недостаточностью средней степени тяжести (КК 30-50 мл/мин) концентрация дроспиренона в плазме крови была в среднем на 37% выше, чем у женщин с нормальной функцией почек. Терапия дроспиреноном хорошо переносилась женщинами с почечной недостаточностью как легкой, так и средней степени. Прием дроспиренона не оказывал клинически значимого влияния на содержание калия в сыворотке крови.
В исследовании однократного применения клиренс при пероральном приеме у добровольцев с печеночной недостаточностью средней степени тяжести был снижен примерно на 50% по сравнению с лицами с нормальной функцией печени. Отмеченное снижение клиренса дроспиренона у добровольцев с печеночной недостаточностью средней степени тяжести не приводит к каким-либо значимым различиям в отношении содержания калия в сыворотке крови. Даже при сахарном диабете и сопутствующем применении спиронолактона (два фактора, которые могут спровоцировать гиперкалиемию у пациента) не отмечалось увеличения содержания калия в сыворотке крови выше ВГН. Можно сделать вывод о том, что дроспиренон хорошо переносится пациентами с печеночной недостаточностью легкой и средней степени тяжести (класс В шкале по Чайлд-Пью).
Препараты, в которых содержится (Аналоги)
Совпадения по коду АТХ 4-го уровня:
Трисеквенс
Cилует
Анжелик
Дивина
Клайра
Гормон Дроспиренон в контрацептивах: Анжелик, Анжелик Микро (с эстрадиолом); Ярина, Даилла, Мидиана, Димиа, Джес, Видора, Модэлль Про, Симициа, Модэлль Тренд (+ этинилэстрадиол); Ярина Плюс, Джес Плюс (+ этинилэстрадиол + кальция левомефолинат).
Гестоден или Дроспиренон, что лучше?
Оба синтетических гормона относятся к препаратам последнего поколения. Они достаточно эффективны и обладают минимальным количеством побочных эффектов. Лекарственные средства, содержащие Гестоден, чаще назначают при дисменорее и для установки регулярного менструального цикла. Дроспиренон же целесообразно использовать для контрацепции, чтобы снизить выраженность ПМС, избавиться от акне, вывести лишнюю жидкость из организма. Необходимо помнить о повышенном риске развития тромбоэмболии и гиперкалиемии во время лечения Дроспиреноном.
Дезогестрел или Дроспиренон, что лучше?
Дезогестрел, как и Дроспиренон относится к гормональным контрацептивами последнего поколения. По аналогии с Гестоденом, вещество применяют для устранения дисменореи. Также следует отметить, что в ходе клинических исследований было установлено, что риск набора веса выше во время лечения Дроспиреноном. В любом случае, решение о том, какое из перечисленных выше веществ следует выбрать, должен принимать лечащий врач.
Сегодня гормональная контрацепция – это не только средство профилактики незапланированной беременности, но и эффективный метод лечения гинекологических заболеваний. Это стало возможным благодаря тому, что в современных комбинированных препаратах значительно уменьшена доза гормональных компонентов, осуществлен синтез прогестагенов с высокой селективностью к рецепторам прогестерона, разработаны новые пути введения гормонов, изменена продолжительность и кратность схем применения и т. д., что дает реальную возможность для индивидуализации лечения. Применение современных контрацептивных средств, особенно гормональных, женщинами, не нуждающимися в них, является сегодня не только новой главой в истории контрацепции, но и новым направлением в гинекологии (David Serfaty, 2011).
Интенсивные исследования и разработки в области гормональной контрацепции в течение последних лет, казалось бы, сделали невозможным дальнейшее улучшение гормональных контрацептивов. Следует подчеркнуть, что контрацептивное действие гормональных препаратов обусловлено в основном действием прогестагенов, эстрогены лишь потенцируют тормозящий эффект прогестагенов на овуляцию на уровне гипоталамо-гипофизарно-яичниковой системы.
Таким образом, сосредоточив внимание в первую очередь на дополнительных неконтрацептивных эффектах гестагенов, ученые в 1980 г. разработали прогестаген диеногест, не содержащий этинильной группы в положении 17α, который сочетает преимущества производных прогестерона и 19-норстероидов, а в 2000 г. – совершенно новый прогестаген, являющийся производным спиронолактона, – дроспиренон [1].
В настоящее время синтезирована масса разнообразных прогестагенов, что открывает широкие возможности для индивидуального выбора гормонального препарата. Прогестагены относятся к стероидным гормонам. По химической классификации их подразделяют на производные прогестерона (хлорамдинона ацетат, медроксипрогестерона ацетат, ципротерона ацетат), производные 19-нортестостерона, подразделяющиеся на эстраны (норэтинодрел, норэтинодрон, этинодиола диацетат) и гонаны (левоноргестрел, дезогестрел, норгестимат, гестоден), а также диеногест, объединяющий преимущества производных прогестерона и 19-норстероидов, и производные спиронолактона (дроспиренон) [2]. Производные прогестерона не обладают контрацептивным действием при приеме внутрь.
Механизм действия прогестагенов связан с воздействием на стероидные рецепторы. Существует пять типов стероидных рецепторов: для глюкокортикоидов, минералокортикоидов, эстрогенов, гестагенов и андрогенов. Прогестерон и прогестагены специфически связываются с гестагенными рецепторами, но могут в той или иной мере связываться и с другими типами стероидных рецепторов, что определя- ет особенности их действия. Так, прогестерон помимо гестагенных рецепторов связывается с минералокортикоидными рецепторами, что обусловливает его антиминералокортикоидное действие, медроксипрогестерона ацетат – с глюкокортикоидными рецепторами, поэтому он обладает небольшой глюкокортикоидной активностью, ряд гестагенов (ципротерона ацетат, хлорамдинон, диеногест) связываются с андрогенными рецепторами [1].
Таким образом, спектр фармакологической активности любого прогестагена определяется выраженностью гестагенного эффекта, наличием или отсутствием антиандрогенной, антиэстрогенной, антиминералокортикоидной активности, зависящих от его химической структуры.
Дроспиренон – первый синтетический прогестин, используемый в комбинированных гормональных препаратах, который не является производным половых стероидов, а синтезируется на основе 17α-спиронолактона и химически похож на мочегонный и антигипертензивный препарат – спиронолактон. В отличие от других прогестинов он обладает антиминералокортикоидной и антиандрогенной активностью. А его фармакологический профиль к эндогенному прогестерону ближе, чем у любого другого синтетического прогестина, используемого сегодня. Дроспиренон ингибирует овуляцию путем супрессии синтеза лютеинизирующего гормона. Он также предотвращает оплодотворение путем замедления транспорта сперматозоидов через изменения в шейке матки и цервикальной слизи, препятствует имплантации, т. к. вызывает атрофию эндометрия.
Дроспиренон препятствует овуляции в зависимости от дозы. Результаты ряда рандомизированных исследований, проведенных с участием здоровых менструирующих женщин, показывают, что оптимальная доза дроспиренона для приема внутрь составляет 3,0 мг. В этих исследованиях применение комбинации 3,0 мг дроспиренона и 30 мкг этинилэстрадиола полностью подавляло овуляцию. Как и эндогенный прогестерон, дроспиренон оказывает антиминералокортикоидное действие на ренин-ангиотензин-альдостероновую систему. Антиминералокортикоидная активность 3,0 мг дроспиренона сравнима с таковой 25 мг спиронолактона, таким образом, антиминералокортикоидная активность дроспиренона в 8 раз выше, чем у спиронолактона.
Дроспиренон и ципротерона ацетат проявляют свою антиандрогенную активность в терапевтических дозах. Как и 2,0 мг ципротерона ацетата/35 мкг этинилэстрадиола, комбинация дроспиренон/этинилэстрадиол уменьшает выработку андрогенов яичниками и себореи у женщин с мягкой и умеренной выраженностью акне в двойном слепом рандомизированном исследовании [3]. Антиандрогенная активность дроспиренона составляет около 30 % активности ципротерона ацетата. Доклинические исследования показали, что дроспиренон не имеет эстрогенной, андрогенной, глюкокортикоидной или антиглюкокортикоидной активности. Особые свойства молекулы дроспиренона, связанные с отсутствием этинильного радикала, а именно более эффективное воздействие на прогестероновые рецепторы, отсутствие угнетающего действия на печеночные ферменты системы цитохромов (Р450), определяют его дополнительные преимущества.
Ярким примером может служить применение дроспиренон-содержащих препаратов пациентками с синдромом поликистозных яичников (СПКЯ) – патологией структуры и функции яичников, основными критериями которого являются овуляторная дисфункция и гиперандрогения. Синдром поликистозных яичников встречается от 4 до 8 % в женской популяции фертильного возраста и является одной из наиболее распространенных эндокринопатий [4]. Синдром является ведущей причиной ановуляторного бесплодия, кожных проявлений гиперандрогении (гирсутизма, акне), а также связан с высоким риском развития сахарного диабета 2 типа и сердечно-сосудистой патологии [5]. Вместе с тем до настоящего времени его этиология неизвестна, терапия носит симптоматический характер. Диагностика СПКЯ требует дифференциального подхода и исключения сходной нозологии. Детальное обследование и выявление основных симптомов СПКЯ, а также исключение сходных по клинике заболеваний необходимы для постановки диагноза.
Многочисленные нарушения обмена веществ при СПКЯ могут приводить к ряду заболеваний, в т. ч. и раку эндометрия. Длительное влияние эстрогена на эндометрий при дефиците прогестерона является частой причиной гиперплазии эндометрия, что в отсутствие лечения может прогрессировать до карциномы эндометрия даже у молодых женщин. Стратегия сокращения риска рака при СПКЯ включает использование комбинированных оральных контрацептивов (КОК), адекватное консультирование по поводу диеты, снижение массы тела, физические нагрузки. Лечение СПКЯ вне планирования беременности заключается в коррекции кожных проявлений гиперандрогении (гирсутизма, акне, алопеции), регуляции менструального цикла, профилактике смертности от сердечно-сосудистых заболеваний (лечение метаболических расстройств). При СПКЯ у женщин, не планирующих беременность, микродозированные КОК, содержащие дроспиренон, являются препаратом первой линии, т. к. дроспиренон является метаболически нейтральным прогестином, не вмешивающимся в углеводный и жировой обмен.
Многочисленные исследования показали, что дроспиренон-содержащие контрацептивы можно рассматривать как средства, характеризующиеся хорошей переносимостью и высокой контрацептивной эффективностью (индекс Перля 0,7) [6, 7]. В одном известном крупном многоцентровом исследовании с участием 11 тыс. женщин, проведенном в 2004 г. в 15 странах Европы, было показано достоверное улучшение общего самочувствия женщин, что проявлялось уменьшением симптомов задержки жидкости и изменений настроения, связанных с циклом, а также улучшением состояния кожи [8]. В другом исследовании было показано значимое уменьшение задержки жидкости и булимии в период, предшествующий менструации, а также улучшение настроения у женщин к 6-му циклу приема дроспиренон-содержащего КОК [6].
Таким образом, обобщая вышеприведенные данные, можно выделить следующие основные преимущества дроспиренона: • антиминералокортикоидный эффект (уменьшает задержку натрия и воды, в результате не оказывает влияния на массу тела, не вызывает масталгии и оказывает лечебный эффект при предменструальном синдроме); • гестагенный эффект (надежная блокада овуляции и контроль цикла); • антиандрогенный эффект (лечение акне и себореи) [9].
На сегодняшний день в России только три препарата содержат в качестве гестагенного компонента дроспиренон: Ярина (дроспиренон 3 мг, этинилэстрадиол 30 мкг), Джес (дроспиренон 3 мг, этинилэстрадиол 20 мкг) и не так давно зарегистрированный Мидиана (дроспиренон 3 мг, этинилэ- страдиол 30 мкг).
Хотелось бы привести результаты применения Мидианы, полученные нашими коллегами и нами в НЦ АГиП МЗСР РФ. В исследование И.Б. Манухина и соавт. были включены 54 женщины в возрасте 16–40 лет (средний возраст – 26,0 ± 1,6 года), из них 34 до этого принимали другие оральные контрацептивы (ОК) и 20 – впервые начали использовать ОК. Препарат применяли в течение 6 циклов (всего 324 цикла). Для уменьшения частоты ациклических кровянистых выделений у пациенток, впервые использовавших ОК, авторы рекомендовали применять препарат с 5-го по 25-й день цикла с дополнительной барьерной контрацепцией в 1-м цикле. Контрацептивная надежность составила 100 %. Кроме того, оценивали характер побочных эффектов, частота которых была выше у пациенток, впервые принявших гормональную контрацепцию. Ациклические кровянистые выделения отмечены лишь в 4 % случаев. Частота циклов с прорывными кровотечениями составила всего 0,3 %. Прибавка массы тела (на 1–2 кг) отмечена у 5 (9,3 %) женщин, в основном это были начинающие пользователи ОК. А у 28 % женщин (все из “переключившихся” с других ОК), было отмечено снижение массы тела на фоне приема Мидианы. Авторы отметили и другие побочные эффекты, такие как масталгия, головная боль, изменение настроения, тошнота, но они возникали крайне редко. Все побочные эффекты купировались в первые несколько месяцев приема препарата, не оказав существенного влияния на переносимость и приверженность лечению. Только 1 (1,9 %) женщина в связи с продолжавшимися прорывными кровотечениями отказалась от использования препарата. Таким образом, небольшая частота побочных эффектов (11 %) на фоне приема нового препарата Мидиана свидетельствует о его хорошей переносимости и высокой контрацептивной эффективности [10].
Наши предварительные данные, основанные на применении Мидианы 32 женщинами репродуктивного возраста, свидетельствуют о хорошей переносимости препарата, надежном контроле цикла и отсутствии случаев отказа от его применения. Длительность применения препарата составила 6 месяцев.
Таким образом, увеличение арсенала дроспиренон-содержащих соединений с внедрением препарата Мидиана позволяет надеяться на дальнейшее расширение возможностей их применения в практике врача акушера- гинеколога.