С конца 2022 года и до сегодняшнего дня внимание всего здравоохранения и мировой общественности в целом приковано к одной большой проблеме – распространению новой коронавирусной инфекции, которую ВОЗ охарактеризовала как чрезвычайную ситуацию международного значения. Один из самых важных вопросов, который возник перед врачами, – как лечить covid-19 у взрослых и детей. Мы поговорили об этом с заведующей кафедрой детских инфекционных болезней Красноярского государственного медицинского университета, главным специалистом по инфекционным заболеваниям у детей МЗ РФ по Сибирскому федеральному округу и Красноярскому краю доктором медицинских наук, профессором Галиной Петровной Мартыновой.
-Галина Петровна, расскажите, с какими сложностями столкнулись практикующие врачи во время пандемии.
-Коронавирусы – это большое семейство вирусов, способных поражать человека и некоторых животных, они известны нам с 60-х годов прошлого столетия. До 2002 года коронавирусы рассматривались в качестве агентов, вызывающих нетяжелые заболевания верхних дыхательных путей. Однако в 2002 году был открыт высокопатогенный штамм SARS-CoV, вызвавший эпидемию атипичной пневмонии, а через 10 лет – MERS-CoV. Поэтому появление еще одного представителя альфакоронавирусов SARS-CoV-2 в декабре 2022 года в городе Ухани (КНР) поначалу не вызвало особых опасений. Но сегодня уже совершенно ясно, что COVID-19 – это совершенно новая инфекция, охватившая весь мир и поставившая перед медицинскими работниками целый ряд задач диагностического и лечебного плана.
Особенно большие трудности при оказании медицинской помощи пациентам имели место в начале пандемии, когда масштабы распространения новой коронавирусной инфекции СOVID-19 стали очевидны. Терапия назначалась, по сути, of -label ввиду отсутствия достоверных доказательств эффективности и безопасности тех или иных лекарственных препаратов, назначаемых пациентам. Но уже сегодня накоплено достаточное количество сведений об эпидемиологии, клинических особенностях, профилактике и лечении этого заболевания, проведен ряд клинических исследований, подтвердивших эффективность и безопасность целого ряда препаратов, которые могут быть использованы при лечении COVID-19 у взрослых и детей.
-Есть мнение, что дети практически не болеют COVID-19. Насколько они подвержены инфекции?
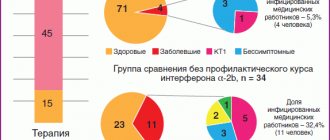
-Дети восприимчивы к SARS-CoV-2: согласно статистике, они составляют от 5 до 7% в структуре заболевших новой коронавирусной инфекцией. Однако по сравнению со взрослыми у детей COVID-19 протекает в более легкой форме. Лишь 10% инфицированных детей нуждаются в госпитализации, и только у 1% развиваются тяжелые формы заболевания.
В большинстве случаев новая коронавирусная инфекция COVID-19 у детей протекает как легкая форма острой респираторной инфекции, но в то же время, несмотря на отсутствие выраженных симптомов интоксикации, физикальных и аускультативных изменений в легких, у 20–50% детей развивается пневмония (по данным компьютерной томографии органов грудной клетки).
Примечательно, что наряду с новой коронавирусной инфекцией сегодня регистрируется традиционное сезонное повышение заболеваемости, вызванной другими респираторными вирусами: риновирусами, респираторно-синцитиальным вирусом, аденовирусом, вирусом гриппа и парагриппа. Но сезонный подъем ОРВИ в современных условиях, конечно, необычен: он протекает на фоне продолжающейся пандемии, когда ввиду большого сходства клинических проявлений определить, какой вирус (или вирусы) явился причиной заболевания, очень сложно, особенно в амбулаторных условиях. Вот почему рациональный подход к терапии новой коронавирусной инфекции у детей, по мнению специалистов, проводится согласно основным принципам лечения острых респираторных вирусных инфекций.
При этом следует учитывать, что респираторные вирусы, в том числе и коронавирус, способны мутировать, изменять свою антигенную структуру, вырабатывать резистентность к ряду препаратов прямого противовирусного действия. Возьмем в качестве примера вирус гриппа, в отношении которого были созданы мощные противовирусные препараты, имеющие убедительную доказательную базу. В то же время на сегодняшний день более 40% штаммов вирусов гриппа нечувствительны к «Римантадину» и другим препаратам амантадина. Имеются данные о появлении штаммов вируса гриппа, резистентных к препаратам первой линии – ингибиторам нейраминидазы, в частности «Осельтамивиру». И это касается только гриппа. Но ведь нельзя исключить возможность сочетанного поражения респираторного тракта, когда причиной заболевания являются сразу несколько вирусов, что, конечно, в значительной степени затрудняет выбор противовирусной терапии.
В связи с этим при лечении респираторных вирусных инфекций возникла необходимость применения препаратов, действующих не на конкретные белки вируса, а на иммунные механизмы противовирусной защиты. В этой ситуации препаратами выбора при лечении ОРВИ различной этиологии, в том числе новой коронавирусной инфекции COVID-19, являются препараты рекомбинантного интерферона.
-Некоторые специалисты считают, что организму достаточно эндогенного интерферона. Насколько это мнение обоснованно?
-К сожалению, это не совсем так. Конечно, вирусы являются мощными стимуляторами выработки эндогенного интерферона, которая не зависит от таксономических свойств возбудителя и будет продолжаться весь период его репликации. С момента контакта возбудителя с эпителием слизистых оболочек респираторного тракта начинается активная индукция эндогенного (внутреннего) интерферона. Однако это не значит, что его концентрация достаточна для надежной защиты от инфекции, в том числе и новой коронавирусной инфекции. У детей раннего возраста, особенно у новорожденных, при инфекционно-воспалительных заболеваниях снижается способность организма к продукции интерферона альфа и гамма, что снижает эффективность защитных сил организма, в том числе и местного иммунитета.
Более того, результаты экспериментальных и клинических исследований наших европейских коллег свидетельствуют, что SARS-CoV-2, в отличие от других респираторных вирусов, подавляет синтез собственного интерферона в организме. При ослаблении иммунитета вирусы ускользают от иммунных механизмов, болезнь затягивается, развиваются осложнения, которые могут стать причиной даже неблагоприятного исхода. В связи с вышесказанным логичным в данной ситуации является использование в педиатрической практике препаратов рекомбинантного интерферона, противовирусная, иммуномодулирующая и антиоксидантная активность которых продемонстрирована в многочисленных клинических исследованиях. Препараты рекомбинантного интерферона-α-2b проявляют эффект при инфекциях различной этиологии (вирусной и бактериальной) и локализации (заболевания респираторного и желудочно-кишечного тракта, нервной и мочевыделительной системы, врожденные инфекции). Немаловажно, что препараты интерферона могут применяться у пациентов совершенно разных возрастных категорий: у детей, в том числе новорожденных, подростков, взрослых, включая беременных женщин и пожилых людей. Поэтому спектр показаний к применению препаратов рекомбинантного интерферона очень велик, без всякого преувеличения.
Лидером среди препаратов рекомбинантного интерферона-α-2b, конечно, является ВИФЕРОН®, лечебная и профилактическая эффективность которого доказана в многочисленных исследованиях у пациентов разных возрастных групп с различным состоянием здоровья. Наша клиника также приняла участие в изучении эффективности и безопасности препаратов рекомбинантного интерферона при лечении детей с новой коронавирусной инфекцией СOVID-19.
-А почему объектом исследований стал именно ВИФЕРОН®?
-Прежде всего потому, что ВИФЕРОН® имеет удобные для детской практики формы выпуска – свечи (действуют системно, то есть на весь организм в целом), а также гель и мазь (действуют местно, в очаге поражения). При местном применении интерферон препятствует фиксации и размножению вирусов в месте их внедрения, таким образом создает препятствие для них: вирус не может проникнуть в клетку, ему негде размножаться. Поэтому местные гелевые или мазевые формы могут с успехом использоваться не только с целью лечения, но и для эффективной профилактики.
Назначение рекомбинантного интерферона-α-2b с момента появления самых первых симптомов заболевания подавляет репликацию вирусов. Неудивительно, что не только в России, но и в Европе в настоящее время идет активное изучение применения препаратов рекомбинантного интерферона при лечении и профилактике новой коронавирусной инфекции COVID-19.
-Расскажите подробнее об исследовании, в котором Вы участвовали.
-Исследование проводилось в трех научно-исследовательских центрах, в которых были развернуты госпитали для лечения детей с COVID-19: в Москве, Красноярске и Казани. Целью исследования явилось изучение эффективности интерферона-α-2b в высоких дозах. Ведь SARS-CoV-2 блокирует выработку эндогенного интерферона, и поэтому целесообразно вводить именно высокие дозы рекомбинантного интерферона-α-2b.
В исследовании участвовали 140 детей в возрасте от 1 года до 17 лет, которые были разделены на две возрастные группы. Первая – дети с 1 года до 7 лет, получавшие в качестве этиотропной противовирусной терапии рекомбинантный интерферон-α-2b (ВИФЕРОН®) в форме ректальных суппозиториев в дозировке 1 000 000 МЕ 2 раза в сутки в комбинации с ВИФЕРОН® Гель 5–6 раз в сутки местно (на слизистую оболочку носа).
Вторая группа – дети от 8 до 17 лет, получали ректальные суппозитории ВИФЕРОН® 3 000 000 МЕ 2 раза в день в комбинации с ВИФЕРОН® Гель местно 5–6 раз в день.
Контрольную группу составили 70 детей, получавших в качестве противовирусной терапии препарат с прямым противовирусным действием «Умифеновир» в терапевтической дозировке в соответствии с возрастом ребенка.
Клиническая эффективность оценивалась по уменьшению выраженности клинических симптомов заболевания: купированию лихорадки, кашля, заложенности носа, ринореи, боли в животе, восстановлению слизистых оболочек глаз, нормализации обоняния, вкуса. В ходе исследования изучались динамика выделения коронавируса, уровень антител класса IgM и IgG к SARS-CoV-2 в сыворотке крови, позволяющие оценить скорость формирования иммунного ответа.
-Мы можем уже говорить о результатах работы?
-Да, исследование практически закончено, и его результаты показали положительную динамику на фоне терапии у пациентов основной и контрольной групп. В то же время необходимо отметить, что у пациентов основной группы, получающих комбинированную терапию препаратами рекомбинантного интерферона-α-2b (ВИФЕРОН® Суппозитории ректальные и Гель), купирование клинических симптомов заболевания происходило достоверно быстрее по сравнению с детьми группы сравнения.
У детей основной группы достоверно быстрее в сыворотке крови появлялись антитела к SARSCoV-2 (сначала – IgM, а затем – IgG) по сравнению с участниками контрольной группы. Это подтверждает факт, что иммунный ответ к новому коронавирусу на фоне применения рекомбинантного интерферона в высоких дозах в комбинированной схеме формировался быстрее по сравнению с терапией препаратом прямого противовирусного действия. Безусловно, это отражалось и на продолжительности клинических проявлений заболевания, сокращало сроки пребывания детей в стационаре.
Хочу отметить, что среди пациентов контрольной группы были дети (как правило, подростки с поражением нижних дыхательных путей, пневмонией), у которых на 8–9-й день с момента назначения противовирусной терапии «Умифеновиром» сохранялись клинические проявления болезни, в контрольных мазках из носоглотки продолжалось выделение SARS-CoV-2. Назначение больным второго курса противовирусной терапии препаратами рекомбинантного интерферона-α-2b (ректальные суппозитории и гель) приводило не только к купированию клинических симптомов COVID-19, но и к санации организма от вируса, уже на 5–7-й день вирус в мазках из носоглотки не определялся.
-То есть на фоне применения препаратов интерферона сокращается период выделения вируса?
-Да, при применении препарата ВИФЕРОН® быстрее происходила санация организма: в мазках из носоглотки более чем у половины детей уже на 5–7-й день вирус не определялся (методом ПЦР) в отличие от детей контрольной группы. Более того, его использование позволяло сократить период выделения вируса из кала, хотя, согласно литературным данным, выделение вируса с калом происходит более длительное время по сравнению с выделением его со слизистых оболочек носоглотки.
Мы проанализировали результаты исследования ПЦР кала на SARS-CoV-2 у детей с новой коронавирусной инфекцией, разделив их на три группы. Первая группа пациентов в качестве противовирусной терапии получала «Умифеновир» вторая – ВИФЕРОН® в стандартных невысоких дозировках и третья – ВИФЕРОН® в высоких дозировках (это были дети, участвовавшие в нашем исследовании). Во время терапии у пациентов трех групп проводилось исследование кала на SARS-CoV-2 методом ПЦР в начале терапии и по ее окончании – на 11–13-й день. Результаты показали, что на фоне применения препарата ВИФЕРОН® достоверно быстрее прекращается выделение вируса с фекалиями по сравнению с детьми, получающими «Умифеновир». Более того, была выявлена зависимость между дозой интерферона и сроком выделения вируса: в группе детей, получающих высокие дозировки препарата ВИФЕРОН®, этот период был меньше, чем у детей на стандартных дозировках.
Таким образом, мы говорим не только о клинической эффективности рекомбинантного интерферона-α-2b с антиоксидантами в виде ректальных суппозиториев и геля для наружного применения при лечении новой коронавирусной инфекции, но и в значительной степени о сокращении времени репликации вируса и продолжающегося вирусовыделения. Это очень важно, поскольку выделение вируса в окружающую среду – причина распространения инфекции. Пациент, у которого уже нет клинических симптомов заболевания, может считать себя здоровым, но на самом деле может продолжать выделять вирус в окружающую среду, оставаясь потенциальным источником инфекции.
-А можно ли использовать интерфероны для лечения взрослых пациентов?
-Да, мы изучали и этот вопрос. В стационаре со многими детьми находятся мамы, которые, как правило, тоже больны коронавирусной инфекцией. Чаще всего в качестве противовирусной терапии им назначался «Умифеновир», однако в ряде случаев, несмотря на проводимую терапию, женщины продолжали выделять вирус в мазках из носоглотки. В таких ситуациях был рекомендован ВИФЕРОН®, который продемонстрировал положительный результат.
Данные исследований, клинический опыт подтверждают, что рекомбинантные интерфероны, в частности ВИФЕРОН®, в системной (суппозитории) и местной (гель или мазь) формах целесообразно использовать для лечения острых респираторных инфекций, в том числе коронавирусной инфекции как у детей, так и у взрослых.
Оригинальная публикация: https://viferon.su/vestnikferona_sp_2020_2/
Автор: Марина Изварина
Заинтересовала статья? Узнать еще больше Вы можете в разделе Мнения экспертов
Состав
Действующие вещества: Альфа-глутамил-триптофан натрий [Тимоген натрий] (в пересчете на альфа-глутамил-триптофан) 0,15 мг Аскорбиновая кислота 12 мг Бендазола гидрохлорид (дибазол) 1,25 мг Вспомогательные вещества: Сахароза 800,0 мг Вода очищенная до 1 мл
Описание:
Сироп от бесцветного до жёлтого цвета.
Фармакотерапевтическая группа:
Иммуностимулирующее средство.
Код АТХ: L03AХ
Фармакологическое действие:
Фармакодинамика:
препарат является средством этиотропной и иммуностимулирующей терапии, обладает опосредованным противовирусным действием в отношении возбудителей гриппа А и В, а также других вирусов, вызывающих острые респираторные заболевания. Снижает выраженность основных клинических симптомов гриппа и ОРВИ, а также сокращает продолжительность заболевания и способствует его неосложненному течению. В исследованиях in vitro препарат специфически подавляет (ингибирует) размножение (репликацию) вируса SARS-CoV-2, который является возбудителем новой коронавирусной инфекции (COVID-19). Увеличивает содержание секреторного иммуноглобулина А (slgA) в слизистой носоглотки – входных воротах инфекции, повышая местную иммунорезистентность организма к респираторным инфекциям вирусной и бактериальной природы. При профилактическом действии препарат повышает потенциальную метаболическую активность клеток врожденного иммунитета (нейтрофильных гранулоцитов и моноцитов), что, в случае развития инфекции, увеличивает их способность к поглощению и разрушению бактериальных и вирусных агентов за счет усиления ферментативной (окислительной) активности, синтеза катионных белков и увеличения числа фагоцитирующих клеток. При этом исходное состояние метаболической активности клеток врожденного иммунитета, в отсутствии инфекционных агентов, не изменяется, находясь в пределах нормальных значений. Бендазол индуцирует в организме выработку эндогенного интерферона, обладает иммуномодулирующим действием (нормализует иммунный ответ организма). Ферменты, выработка которых индуцируется интерфероном в клетках различных органов, ингибируют репликацию вирусов. Альфа-глутамил-триптофан (тимоген) является синергистом иммуномодулирующего действия бендазола, нормализуя Т-клеточное звено иммунитета. Аскорбиновая кислота активирует гуморальное звено иммунитета, нормализует проницаемость капилляров, уменьшая тем самым воспаление, и проявляет антиоксидантные свойства, нейтрализуя кислородные радикалы, сопровождающие воспалительный процесс, повышает устойчивость организма к инфекции.
Фармакокинетика:
при приеме внутрь препарат полностью всасывается из желудочно-кишечного тракта. Биодоступность бендазола – около 80 %, альфа-глутамил-триптофана – не более 15 %, аскорбиновой кислоты – до 70 %. Аскорбиновая кислота абсорбируется в ЖКТ (преимущественно в тощей кишке). Связь с белками плазмы – 25%. TCmax после приема внутрь – 4 ч. Легко проникает в лейкоциты, тромбоциты, а затем во все ткани, проникает через плаценту. Заболевания ЖКТ (язвенная болезнь желудка и 12-перстной кишки, нарушения моторики кишечника, глистная инвазия, лямблиоз), употребление овощных и фруктовых соков, щелочного питья уменьшают связывание аскорбиновой кислоты в кишечнике. Метаболизируется аскорбиновая кислота преимущественно в печени в дезоксиаскорбиновую, далее в щавелевоуксусную и дикетогулоновую кислоты. Выводится почками, через кишечник, с потом, грудным молоком в неизмененном виде и в виде метаболитов. Продуктами биотрансформации бендазола в крови являются два конъюгата, образующиеся вследствие метилирования и карбоэтоксилирования иминогруппы имидазольного кольца бендазола: 1-метил-2-бензилбензимидазол и 1-карбоэтокси-2-бензилбензимидазол. Метаболиты бендазола выводятся с мочой. Альфаглутамил-триптофан под воздействием петидаз расщепляется на L-глутаминовую кислоту и L-триптофан, которые используются организмом в синтезе белка.
Показания к применению:
Профилактика и комплексная терапия гриппа и острых респираторных вирусных инфекций у детей от одного года.
Противопоказания:
гиперчувствительность к компонентам препарата, сахарный диабет, беременность, детский возраст до 1 года. В случае необходимости, пожалуйста, проконсультируйтесь с врачом перед приемом препарата.
Меры предосторожности при применении.
Проконсультируйтесь с врачом перед приемом препарата, если у Вас артериальная гипотензия.
Применение при беременности и в период грудного вскармливания:
в период беременности прием препарата не рекомендуется в связи с недостаточными клиническими данными. В период грудного вскармливания применение возможно, если предполагаемая польза для матери превышает потенциальный риск для ребёнка. В случае необходимости приема препарата в период грудного вскармливания, пожалуйста, проконсультируйтесь с врачом.
Способ применения и дозы:
Внутрь за 30 мин до еды. Для лечения:
Детям в возрасте от 1 до 3 лет – по 2 мл 3 раза в день; детям в возрасте от 3 до 6 лет – по 4 мл 3 раза в день; детям в возрасте от 6 до 10 лет – по 8 мл 3 раза в день; детям в возрасте старше 10 лет – по 12 мл 3 раза в день. Курс применения – 4 дня. Если через 3 дня лечения улучшения не наступает или симптомы усугубляются, или появляются новые симптомы, необходимо проконсультироваться с врачом.
Для профилактики:
— при непосредственном контакте с больным гриппом и другими ОРВИ: Детям в возрасте от 1 до 3 лет – по 2 мл 3 раза в день; детям в возрасте от 3 до 6 лет – по 4 мл 3 раза в день; детям в возрасте от 6 до 10 лет – по 8 мл 3 раза в день; детям в возрасте старше 10 лет – по 12 мл 3 раза в день. Курс применения – 4 дня. Профилактические курсы, при необходимости, повторяют через 3 недели (до нормализации эпидемической обстановки).
Побочное действие:
возможно кратковременное снижение артериального давления. Возможны аллергические реакции: крапивница. В этих случаях применение препарата прекращают и назначают симптоматическое лечение, антигистаминные средства. Проконсультируйтесь с врачом, если у Вас проявились упомянутые побочные эффекты или другие побочные эффекты, не указанные в инструкции. Если побочные эффекты, указанные в инструкции, усугубляются, сообщите об этом врачу.
Передозировка:
Случаи передозировки не описаны.
Взаимодействие с другими лекарственными средствами:
Взаимодействие альфа-глутамил-триптофана с лекарственными средствами не выявлено. Бендазол препятствует увеличению общего периферического сопротивления сосудов, обусловленному применением неселективных бета-адреноблокаторов. Усиливает гипотензивное (снижение артериального давления) действие гипотензивных и диуретических лекарственных средств. Фентоламин усиливает гипотензивное действие бендазола. Аскорбиновая кислота повышает концентрацию в крови антибактериальных препаратов тетрациклинового ряда и бензилпенициллина. Улучшает всасывание в кишечнике препаратов железа (Fe). Снижает эффективность гепарина и непрямых антикоагулянтов. Ацетилсалициловая кислота (АСК), пероральные контрацептивы, свежие соки и щелочное питье снижают ее всасывание и усвоение. При одновременном применении с АСК повышается выделение с мочой аскорбиновой кислоты и снижается выделение АСК. АСК снижает абсорбцию аскорбиновой кислоты примерно на 30%. Аскорбиновая кислота увеличивает риск развития кристаллурии при применении препаратов, содержащих ацетилсалициловую кислоту (АСК) и сульфаниламидами короткого действия, замедляет выведение почками кислот, увеличивает выведение лекарственных средств имеющих щелочную реакцию (в т.ч. алкалоидов), снижает концентрацию в крови пероральных контрацептивов. При одновременном применении уменьшает хронотропное действие изопреналина. Уменьшает терапевтическое действие антипсихотических лекарственных средств (нейролептиков) – производных фенотиазина, канальцевую реабсорбцию амфетамина и трициклических антидепрессантов. Барбитураты и примидон повышают выведение аскорбиновой кислоты с мочой. Возможно одновременное применение с противовирусными препаратами и средствами симптоматической терапии гриппа и ОРВИ. Проконсультируйтесь с врачом, если Вы принимаете указанные в разделе или другие препараты.
Особые указания:
после повторного курса рекомендован контроль концентрации глюкозы в крови.
Влияние на способность управлять транспортными средствами, механизмами:
препарат не влияет на способность управлять транспортными средствами, работать с движущимися механизмами и заниматься другими потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Форма выпуска:
Сироп [для детей]. По 50 мл во флаконе темного стекла. Флакон укупоривают пластмассовой крышкой с контролем первого вскрытия или пластмассовой крышкой с контролем первого вскрытия и защитой от детей. По одному флакону помещают в пачку из картона. Инструкцию по применению вкладывают в пачку или в виде сложенного листка помещают под открывающуюся часть этикетки. В пачку вкладывают дозирующее устройство: мерный стаканчик или ложку дозировочную, или пипетку дозировочную.
Условия хранения:
Хранить при температуре не выше 25 Сo. Хранить в недоступном для детей месте.
Срок годности:
2 года. Не использовать по истечении срока годности, указанного на упаковке.
Условия отпуска:
отпускают без рецепта.
Производитель / юридическое лицо, на имя которого выдано регистрационное удостоверение/ организация, принимающая рекламации по качеству препарата: Акционерное общество «Медико-биологический научно-производственный комплекс «Цитомед» (АО «МБНПК «Цитомед»). Адрес: Россия, 194356, г. Санкт-Петербург, Орлово-Денисовский проспект, дом 14, строение 1, тел., cytomed.ru Адрес производственной площадки: Россия, г. Санкт-Петербург, г., Орлово-Денисовский проспект, дом 14, строение 1.
Генеральный директор А.Н. Хромов АО «Медико-биологический научно-производственный комплекс «Цитомед»
Лечение острых респираторных заболеваний у детей
Острые респираторные заболевания (ОРЗ) — большая группа инфекций, которые имеют много общего в патогенезе и путях передачи: речь идет в основном о воздушно-капельных инфекциях, хотя и контактный (через грязные руки) путь передачи играет не меньшую роль. Этим термином принято объединять острые неспецифические инфекции вне зависимости от их локализации — от ринита до пневмонии. Однако как клинический диагноз ОРЗ требует расшифровки: должно быть указание либо на органное поражение (отит, бронхит, фарингит и т. д.), для которого известен спектр возбудителей, либо на возможную этиологию заболевания (вирусное, бактериальное ОРЗ). Поскольку до 90% ОРЗ вызваны респираторными вирусами и вирусами гриппа в отсутствие признаков бактериальной инфекции оправдан термин «острая респираторно-вирусная инфекция» (ОРВИ) и назначение противовирусной терапии.
По данным авторов серии работ, выполненных под эгидой ВОЗ, в разных странах — как развитых, так и развивающихся — дети раннего возраста ежегодно переносят 5–8 ОРЗ, причем в сельской местности они болеют реже, чем в городах, где ребенок может переносить 10–12 инфекций в год. Дети, которые в раннем детстве реже контактируют с источниками инфекции и поэтому меньше болеют в этот период, «добирают недостающие инфекции» в начальной школе. Констатация этого факта, конечно, не должна быть причиной развития фатализма в отношении ОРВИ — детей следует закалять и по возможности ограждать от источников заражения, полноценно кормить и лечить заболевания (хронический тонзиллит, аллергию), на фоне которых ОРЗ развивается особенно часто. В то же время необходимо всемерно ограждать заболевших детей от излишних терапевтических вмешательств, поскольку именно ОРЗ являются поводом для необоснованного лечения и наиболее частой причиной побочного действия лекарств.
Противовирусные средства
Строго говоря, противовирусная терапия показана при любом респираторно-вирусном заболевании. К сожалению, противовирусные средства, имеющиеся в нашем распоряжении, часто не дают выраженного эффекта, да и легкость большинства эпизодов ОРВИ, ограничивающихся 1–3 лихорадочными днями и катаральным синдромом в течение 1–2 нед, не оправдывает проведения химиотерапии. Но в более тяжелых случаях, особенно при гриппе, противовирусные средства дают определенный эффект и должны применяться шире, чем это считается целесообразным сегодня.
Основное правило применения противовирусных химиопрепаратов — их назначение в первые 24–36 ч болезни, в более поздние сроки их эффект не виден. Основным противогриппозным средством, действующим также и на ряд других вирусов [1], является римантадин, который подавляет репродукцию всех штаммов гриппа типа А. Римантадин также ингибирует репродукцию респираторно-синцитиальных (РС) и парагриппозных вирусов. Рекомендуется; 5-дневный курс из расчета 1,5 мг/кг/сут в 2 приема детям 3–7 лет; по 50 мг 2 раза детям 7–10 лет — 3 раза в сутки — старше 10 лет [2]. В раннем возрасте римантадин используют в виде альгирема (0,2% сироп): у детей 1–3 лет по 10 мл; 3–7 лет — по 15 мл: 1-й день 3 раза, 2–3-й дни — 2 раза, 4-й — 1 раз в день. Эффективность римантадина увеличивается при его приеме с препаратом но-шпа (дротаверином) перорально, в дозе 0,02–0,04 г — у детей 4–6 лет и 0,04–0,1 г — для пациентов 7–12 лет, особенно при нарушении теплоотдачи (холодные конечности, мраморность кожи) [3].
Сходным противовирусным действием обладает арбидол, ингибирующий слияние липидной оболочки вирусов гриппа с мембраной эпителиальных клеток. Он также является индуктором интерферона. Этот малотоксичный препарат можно назначить и при среднетяжелой ОРВИ с 2-летнего возраста: детям 2–6 лет по 50 мг на прием, 6–12 лет по 100 мг, старше 12 лет — по 200 мг на прием 4 раза в сутки. И римантадин, и арбидол сокращают лихорадочный период в среднем на 1 день как при гриппе А2, смешанных инфекциях, так и при не гриппозных ОРВИ [1].
Рибавирин (рибамидил, виразол) — противовирусный препарат, первоначально использовавшийся (в основном в США) как обладающий активностью в отношении РС-вируса при бронхиолитах у наиболее тяжелых больных с неблагоприятным преморбидным фоном (недоношенные, с бронхолегочной дисплазией). Препарат применяется для этой цели в виде постоянных (до 18 ч в сутки) ингаляций через специальный ингалятор в дозе 20 мг/кг/сут; из-за высокой цены и побочных явлений в Европе практически не применяется. Оказалось также, что этот препарат активен в отношении вирусов гриппа, парагриппа, простого герпеса, аденовирусов, а также коронавируса — возбудителя тяжелого острого респираторного синдрома (ТОРС — SARS). При гриппе у подростков старше 12 лет его применяют внутрь в дозе 10 мг/кг/сут в течение 5–7 дней. При ТОРС рибавирин вводят внутривенно.
Прогресс в отношении лечения гриппа, вызываемого вирусами как типа А, так и типа В, может быть связан с использованием ингибиторов нейраминидазы озельтамивир — тамифлю и занамивир — реленца. Эти препараты при раннем приеме уменьшают длительность лихорадки на 24–36 ч и обладают профилактическим действием, но опыта их применения у детей (с 12 лет) в России мало, да и в справочниках последних лет о них практически не пишут. Реленца применяется в виде ингаляций порошка (в США с 7 лет) — по 2 ингаляции (5 мг каждая) в день с интервалом не менее 2 ч (в 1-й день) и 12 ч (со 2-го по 5-й день лечения). Тамифлю (капсулы по 75 мг и суспензия 12 мг/мл) у взрослых и детей с 12 лет используется по 75 мг 1 раз в день в течение 5 дней (в США дозы для детей 1–12 лет: весом до 15 кг — 30 мг 2 раза в день, 15–23 кг — 45 мг 2 раза в день, 23–40 кг — 60 мг 2 раза в день). Этот препарат — единственный, к которому чувствителен птичий грипп H5N1, и в настоящее время ряд стран производят его накопление на случай эпидемии, что, видимо, ограничивает его применение при относительно небольшом производстве (Хоффман-Ля Рош, Швейцария, выпускает 7 млн доз тамифлю в год).
Используемые местно (в нос, в глаза) препараты флореналь 0,5%, оксолиновая мазь 1–2%, бонафтон, локферон и другие обладают некоторой противовирусной активностью; они показаны, например, при аденовирусной инфекции. Хотя их эффект оценить трудно, низкая токсичность оправдывает применение этих средств.
Протеолитические процессы, происходящие при синтезе вирусных полипептидов, а также слияние вирусов с мембранами клеток способны ингибировать апротинины — контрикал, гордокс и др., а также амбен. Эти препараты могут использоваться при тяжелых формах респираторных инфекций с высокой активностью воспаления, обычно при признаках ДВС-синдрома (как ингибиторы фибринолиза) и расстройствах микроциркуляции. Амбен входит в состав гемостатических губок. Контрикал используют в дозе 500–1000 ЕД/кг/сут. Применяемые у взрослых олифен и эрисод, входящие в состав препаратов этой группы, у детей пока не апробированы.
Интерфероны и их индукторы обладают универсальными противовирусными свойствами, подавляя репликацию как РНК, так и ДНК, стимулируя одновременно иммунологические реакции макроорганизма. Раннее применение интерферонов способно если и не оборвать течение инфекции, то смягчить ее проявления.
Нативный лейкоцитарный интерферон α (1000 МЕ/мл — 4–6 раз в день в нос в общей дозе 2 мл в 1–2-й день болезни) менее эффективен, чем препараты рекомбинантных интерферонов [4] . Из числа последних перспективно использование гриппферона — интерферона α-2β (10 000 МЕ/мл) с загустителями; его вводят в виде капель в нос — 5 дней, детям до года — по 1 капле 5 раз в день (разовая доза 1000 МЕ, суточная доза — 5000 МЕ), детям от 1 до 3 лет по 2 капли 3–4 раза в день (разовая доза 2000 МЕ, суточная — 6000–8000 МЕ), от 3 до 14 лет — по две капли 4–5 раз в день (разовая доза — 2000 МЕ, суточная — 8000–10 000 МЕ). Введение препаратов интерферона парентерально, практикуемое, например, для лечения хронического гепатита, вряд ли оправдано при подавляющем большинстве респираторных инфекций. Однако в ряде работ показана эффективность при гриппе и ОРВИ ректальных свечей виферон — интерферон α-2β + витамины Е и С. Виферон-1 (150 000 МЕ) применяют у детей до 6 лет, виферон-2 (500 000 МЕ) у детей старше 7 лет — их назначают по 2–3 раза в сутки в течение 5 дней. Виферон применяют и профилактически — у часто болеющих детей [3].
Лаферон — порошок интерферона α-2β — используют в виде капель в нос, а у детей старше 12 лет его вводят внутримышечно по 1–3 млн МЕ.
Помимо арбидола, в качестве индукторов интерферона используют ряд препаратов. Наибольшую популярность у детей старше 7 лет завоевал амиксин (тилорон) — его вводят при первых симптомах ОРЗ или гриппа внутрь после еды по 60 мг 1 раз в день на 1-й, 2-й, и 4-й день от начала лечения. Детский анаферон — гомеопатические дозы афинно очищенных антител к интерферону α, его применяют по 1 таблетке каждые 30 мин в течение 2 ч, далее 3 раза в сутки, однако убедительных данных о его эффективности пока собрано мало.
У детей, больных ОРВИ, часто приходится лечить первичную герпесвирусную инфекцию, протекающую как тяжелый фебрильный стоматит. У детей с атопическим дерматитом часто развивается экзема Капоши — герпесвирусная инфекция пораженной кожи, также протекающая тяжело. У старших детей ОРВИ — самая частая причина реактивации герпес-вирусов в виде специфических высыпаний на губах, крыльях носа, реже — на гениталиях. Эта инфекция хорошо поддается лечению ацикловиром — его применяют по 20 мг/кг/сут в 4 приема, в тяжелых случаях — до 80 мг/кг/сут или внутривенно по 30–60 мг/кг/сут. Валацикловир не требует дробного введения, его доза для взрослых и подростков старше 12 лет составляет 500 мг 2 раза в день.
Для лечения ОРВИ на практике применяется значительно большее число средств, в том числе растительного происхождения (адаптогены, БАД, настойки и т. д.). В отношении эффективности подавляющего большинства из них данных не существует, однако с побочными их воздействиями сталкиваться приходится часто.
Антибактериальные средства
Бактериальные ОРЗ у детей, как и у взрослых, относительно немногочисленны, но именно они представляют наибольшую угрозу в плане развития серьезных осложнений. Постановка диагноза бактериального ОРЗ у постели остро заболевшего ребенка представляет большие трудности ввиду сходства многих их проявлений с таковыми при ОРВИ (повышение температуры, насморк, кашель, боли в горле), а экспресс-методы этиологической диагностики практически недоступны. Да и выявление микробного возбудителя в материале дыхательных путей еще не говорит о его этиологической роли, поскольку большинство бактериальных заболеваний вызываются возбудителями, постоянно вегетирующими в дыхательных путях.
В этих условиях, естественно, врач при первом контакте с ребенком склонен переоценивать возможную роль бактериальной флоры и использовать антибиотики чаще, чем это необходимо. Наши данные показывают, что в Москве антибиотики назначают 25% детей с ОРВИ, в некоторых городах России эта цифра достигает 50–60%. Та же тенденция характерна и для других стран: антибиотики при ОРВИ используют у детей в 14–80% случаев [6, 7]. Близкие к нашим данным показатели приводят авторы из Франции (24% [8]) и США (25% [9]). В развивающихся странах антибактериальные препараты при ОРЗ применяются также излишне широко, хотя этот процесс сдерживается более низкой их доступностью. В Китае антибиотики получают 97% детей с ОРЗ, обратившихся за медицинской помощью [10]. Очевидно, что при вирусной этиологии заболевания антибиотики по меньшей мере бесполезны и, скорее всего, даже вредны, поскольку они нарушают биоценоз дыхательных путей и тем самым способствуют заселению их несвойственной, чаще кишечной, флорой [11].
Антибиотики у детей с ОРВИ чаще, чем при бактериальных заболеваниях, вызывают побочные действия — различные сыпи и другие аллергические проявления. При бактериальных процессах в организме происходит мощный выброс ряда медиаторов (например, циклического аденозина монофосфата), препятствующих манифестации аллергических проявлений. При вирусных инфекциях этого не происходит, поэтому аллергические реакции реализуются намного чаще.
Другая опасность избыточного применения антибиотиков — распространение лекарственно-устойчивых штаммов пневмотропных бактерий, отмечающееся во многих странах мира. Очевидно, что неоправданное применение антибиотиков ведет и к излишним расходам на лечение.
Не следует игнорировать и влияние антибиотиков на становление иммунной системы ребенка. Характерное для новорожденного преобладание иммунного Т-хелперного ответа 2-го типа (Тh-2) уступает более зрелому Т-хелперному ответу 1-го типа (Тh-1) в значительной степени под влиянием стимуляции эндотоксинами и другими продуктами бактериального происхождения. Такая стимуляция происходит как во время бактериальной инфекции, так и во время ОРВИ, поскольку и вирусная инфекция сопровождается усиленным (хотя и неинвазивным) размножением пневмотропной флоры [11]. Естественно, применение антибиотиков ослабляет или вообще подавляет эту стимуляцию, что, в свою очередь, способствует сохранению Тh-2-направленности иммунного ответа, повышающей риск аллергических проявлений и снижающей интенсивность противоинфекционной защиты.
Показания к антибактериальному лечению ОРЗ
В рекомендациях профессиональных обществ педиатров большинства стран подчеркивается важность отказа от применения антибактериальных средств у детей с неосложненной респираторно-вирусной инфекцией. В рекомендациях Академии педиатрии США подчеркивается, что антибиотики не используют не только при неосложненной ОРВИ, но и слизисто-гнойный насморк также не является показанием к назначению антибиотиков, если он длится менее 10–14 дней [8]. Французский консенсус допускает применение антибиотиков при ОРВИ лишь у детей с рецидивами отита в анамнезе, у малышей в возрасте до 6 мес, если они посещают ясли и при наличии иммунодефицита [9].
В рекомендациях Союза педиатров России указано, что при неосложненных ОРВИ системные антибиотики в подавляющем большинстве случаев не показаны [4]. В этом документе перечисляются наблюдающиеся в первые 10–14 дней проявления болезни, которые не могут оправдать введения антибиотиков.
Вопрос о назначении антибиотиков у ребенка с ОРВИ возникает, если у него в анамнезе есть рецидивирующий отит, неблагоприятный преморбидный фон (выраженная гипотрофия, врожденные пороки развития) или при наличии клинических признаков иммунодефицита.
Ниже приведены признаки бактериальной инфекции, требующие антибактериального лечения:
- гнойные процессы (синусит с отеком лица или глазницы, лимфаденит с флюктуацией, паратонзиллярный абсцесс, нисходящий ларинготрахеит);
- острый тонзиллит с высевом стрептококка группы А;
- анаэробная ангина — обычно язвенная, с гнилостным запахом;
- острый средний отит, подтвержденный отоскопией или с гноетечением;
- синусит — при сохранении клинических и рентгенологических изменений в пазухах через 10–14 дней от начала ОРВИ;
- респираторные микоплазмоз и хламидиоз;
- пневмония.
Чаще, чем эти явные очаги, педиатр видит лишь косвенные симптомы вероятной бактериальной инфекции, среди которых наиболее часто выявляются стойкая (3 дня и более) фебрильная температура, одышка в отсутствие обструкции (частота дыхания выше 60 в 1 мин у детей 0–2 мес жизни, более 50 в 1 мин в возрасте 3–12 мес и более 40 — у детей 1–3 лет), асимметрия аускультативных данных в легких. Такая симптоматика заставляет назначить антибиотик, который, в случае если диагноз при последующем обследовании не подтвердился, следует тут же отменить.
Для стартовой терапии бактериальных ОРЗ используют небольшой набор антибиотиков. При отите и синусите для подавления основных возбудителей — пневмококка и гемофильной палочки назначают амоксициллин внутрь 45–90 мг/кг/сут. У недавно получавших антибиотики детей используют амоксициллин/клавуланат 45 мг/кг/сут, подавляющий рост вероятно устойчивых у этих больных гемофильной палочки и моракселлы.
Острый тонзиллит требует дифференциальной диагностики между аденовирусной ангиной, инфекционным мононуклеозом и стрептококковым тонзиллитом. Для вирусной ангины характерен кашель, катаральный синдром, для стрептококковой — отсутствие кашля, для мононуклеоза — изменения крови. Антибиотики (пенициллин фау, цефалексин, цефадроксил) показаны при стрептококковом тонзиллите; применение амоксициллина нежелательно, поскольку при мононуклеозе он способен вызывать токсические сыпи. Хотя аденовирусная ангина не требует назначения антибиотика, наличие выраженного лейкоцитоза (15–25х109/л) и повышение уровня С-реактивного белка оправдывают их применение во многих случаях.
Бронхит, как правило, представляет собой вирусное заболевание, не требующее антибактериального лечения. Исключение составляют бронхиты, вызванные микоплазмой, при их выявлении показано использование макролидов (азитромицин, мидекамицин и др.). Клиническими признаками микоплазменного бронхита являются:
- возраст (дошкольный и старше);
- высокая температура без выраженного токсикоза;
- обилие крепитирующих хрипов (как при бронхиолите у грудных детей);
- асимметрия хрипов;
- неяркий «сухой» катар верхних дыхательных путей;
- гиперемия конъюнктив («сухой конъюнктивит»);
- локальное усиление бронхо-сосудистого рисунка на рентгенограмме.
Выбор антибактериальных средств для стартового лечения внебольничной пневмонии также не очень велик, поскольку бoльшая часть «типичных» пневмоний вызывается пневмококком или гемофильной палочкой (исключение — первые месяцы жизни, когда возбудителем могут быть стафилококки и кишечная флора), тогда как «атипичные» формы поддаются лечению макролидами. Выбор стартового антибиотика при пневмонии определяется с учетом вероятного возбудителя заболевания.
При типичной пневмонии (фебрильная, с очагом или гомогенным инфильтратом) применяют:
- 1–6 мес (наиболее вероятные возбудители — E. coli, стафилококк) — амоксициллин/клавуланат внутрь, внутривенно; цефуроксим, цефтриаксон или цефазолин + аминогликозид внутривенно, внутримышечно;
- 6 мес–18 лет: нетяжелая (наиболее вероятные возбудители — пневмококк, H. influenzae) — амоксициллин внутрь; тяжелая (наиболее вероятные возбудители — пневмококк, у детей до 5 лет — H. influenzae типа b) — цефуроксим, цефтриаксон или цефазолин + аминогликозид внутривенно, внутримышечно.
При атипичной (с негомогенным инфильтратом) пневмонии:
- 1–6 мес (наиболее вероятные возбудители — C. trachomatis, U. urealyticum, редко P. carinii) — макролид, азитромицин внутрь, ко-тримоксазол;
- 6 мес–15 лет (наиболее вероятные возбудители — М. pneumoniae, C. pneumoniae) — макролид, азитромицин, доксициклин (> 12 лет) внутрь.
Патогенетические методы лечения
К этим методам можно отнести вмешательства, применяемые при остром ларингите и обструктивных формах бронхита.
Острый ларингит, круп представляют собой состояния, требующие оценки степени стеноза, о чем судят по интенсивности инспираторных втяжений грудной клетки, частоте пульса и дыхания. Круп 3-й степени требует неотложной интубации, круп 1-й и 2-й степени лечится консервативно. Больному с ларингитом антибиотики не вводят, согласно всемирному консенсусу наиболее эффективно введение дексаметазона внутримышечно 0,6 мг/кг, что останавливает прогрессирование стеноза. Дальнейшее лечение продолжают ингаляционными стероидами (дозированными или через небулайзер — пульмикорт) в комплексе со спазмолитиками (сальбутамол, беротек, беродуал в ингаляциях).
Стеноз гортани может быть вызван эпиглоттитом (в его этиологии основная роль принадлежит H. influenzae типа b) — для него характерны высокая температура и усиление стеноза в положении на спине; назначение антибиотика (цефуроксим, цефтриаксон) в данном случае обязательно.
Затруднение дыхания и экспираторная одышка часто наблюдаются при бронхиолите и обструктивном бронхите, а также при приступе астмы на фоне ОРВИ. Поскольку бактериальная инфекция в таких случаях — редкость, назначение антибиотиков не оправдано. Лечение — ингаляции симпатомиметиков (у маленьких детей лучше в комбинации с ипратропия бромидом) и применение стероидов в рефрактерных случаях — дает возможность справиться с обструкцией за 1–3 дня.
Симптоматическая терапия ОРЗ
Как указано выше, ОРЗ — наиболее часто встречающаяся причина применения лекарств, в частности симптоматических средств, которые занимают бoльшую часть аптечных полок. Важно, однако, четко представлять себе, что одно лишь наличие того или иного симптома не должно быть основанием для вмешательства, надо прежде всего оценить, в какой степени этот симптом нарушает жизнедеятельность и не окажется ли лечение опаснее симптома.
Лихорадка сопровождает большинство ОРЗ и является защитной реакцией, так что снижение ее уровня жаропонижающими средствами оправдано лишь в определенных ситуациях. К сожалению, многие родители да и врачи считают лихорадку наиболее опасным проявлением болезни и стремятся нормализовать температуру во что бы то ни стало. Согласно проведенным нами исследованиям [12], жаропонижающие получают 95% детей с ОРВИ, в том числе 92% детей с субфебрильной температурой. Такую тактику нельзя считать рациональной, поскольку лихорадка как компонент воспалительного ответа организма на инфекцию во многом носит защитный характер.
Жаропонижающие не влияют на причину лихорадки и не сокращают ее длительность, они увеличивают период выделения вирусов при ОРЗ [12, 13]. При большинстве инфекций максимум температуры редко превышает 39,5°. Такая температура не таит в себе какой-либо угрозы для ребенка старше 2–3 месяцев; обычно, чтобы наступило улучшение самочувствия, бывает достаточно понизить ее на 1–1,5°. Показания для снижения температуры [4]:
- Ранее здоровым детям в возрасте старше 3 мес — при температуре > 39,0°–39,5°, и/или при дискомфорте, мышечной ломоте и головной боли.
- Детям с фебрильными судорогами в анамнезе, с тяжелыми заболеваниями сердца и легких, а также от 0 до 3 мес жизни — при температуре > 38°–38,5°.
Наиболее безопасным жаропонижающим для детей является парацетамол, его разовая доза составляет 15 мг/кг, суточная — 60 мг/кг. Ибупрофен (5–10 мг/кг на прием) чаще дает побочные эффекты (при сходном жаропонижающем эффекте), его рекомендуют использовать в случаях, когда требуется противовоспалительный эффект (артралгии, мышечные боли и т. д.).
При ОРЗ у детей не применяются ацетилсалициловая кислота (аспирин) — в связи с развитием синдрома Рея, метамизол натрия (анальгин) внутрь (опасность агранулоцитоза и коллаптоидного состояния), амидопирин, антипирин, фенацетин. Нимесулид гепатотоксичен; к сожалению, его детские формы были зарегистрированы в России, хотя они не применяются больше нигде в мире.
Лечение насморка сосудосуживающими каплями улучшает носовое дыхание лишь в первые 1–2 дня болезни, при более длительном применении они могут усиливать насморк, а также вызывать побочные явления. В раннем возрасте из-за болезненности используют только 0,01% и 0,025% растворы. Удобны (после 6 лет) назальные спреи, позволяющие при меньшей дозе равномерно распределить препарат (длянос, виброцил). Но наиболее эффективно очищает нос и носоглотку, особенно при густом экссудате, физиологический раствор (или его аналоги, в том числе приготовленный дома раствор поваренной соли: на 1/2 стакана воды добавить соли на кончике ножа) — по 2–3 пипетки в каждую ноздрю 3–4 раза в день в положении лежа на спине со свешивающейся вниз и назад головой. Орально применяющиеся средства от насморка, содержащие симпатомиметики (фенилэфрин, фенилпропаноламин, псевдоэфедрин) используют после 12 лет, с 6 лет назначают фервекс для детей, не содержащий этих компонентов. Противогистаминные препараты, в том числе второго поколения, эффективные при аллергическом рините, ВОЗ не рекомендует применять при ОРЗ [15].
Показанием для назначения противокашлевых средств (ненаркотические центрального действия — глауцин, бутамират, окселадин) является только сухой кашель, который при бронхитах обычно быстро становится влажным. Отхаркивающие средства (их действие, стимулирующее кашель, аналогично рвотному) имеют сомнительную эффективность и у маленьких детей могут вызывать рвоту, а также аллергические реакции — вплоть до анафилаксии. Их назначение скорее дань традиции, чем необходимость, дорогие средства из этой группы не имеют преимуществ перед обычными галеновыми, ВОЗ вообще рекомендует ограничиться «домашними средствами» [15].
Из числа муколитиков наиболее активен ацетилцистеин, но при острых бронхитах у детей нужды в его применении практически нет; карбоцистеин назначают при бронхите — в расчете на его благоприятное влияние на мукоцилиарный клиренс. Амброксол при густой мокроте применяют как внутрь, так и в ингаляциях. Аэрозольные ингаляции муколитиков используют при хронических бронхитах; аэрозольные ингаляции воды, физраствора и прочее при ОРЗ не показаны.
При длительно сохраняющемся кашле (коклюш, упорный трахеит) показаны противовоспалительные средства: ингаляционные стероиды, фенспирид (эреспал). Смягчающие пастилки и спреи при фарингите обычно содержат антисептики, их применяют с 6 лет; начиная с 30 мес используют антибиотик местного действия фюзафюнжин, выпускаемый в аэрозоле (биопарокс) и применяемый как назально, так и орально.
Все еще популярные в России при бронхитах горчичники, банки, жгучие пластыри у детей применяться не должны; при ОРЗ редко возникают показания для физиотерапии. Удивление вызывает популярность галокамер, пребывание в которых имеет целью «ингаляцию паров поваренной соли», как в соляной шахте. Но в соляной шахте на пациента воздействует не соль (которая к летучим субстанциям никак не относится), а чистый воздух, свободный от пыли и других аллергенов; кроме того, находятся там не по 15 мин. Лечение в галокамере не значится и в консенсусе по астме, тем не менее многие поликлиники тратят огромные деньги на их сооружение.
Указанные в этом разделе средства, за немногими исключениями, нельзя считать обязательными при ОРВИ; более того, мы сплошь и рядом сталкиваемся с побочными явлениями, возникшими в результате такого лечения. Поэтому следует взять за правило минимизацию лекарственных нагрузок в случаях нетяжелых ОРВИ.
Проблема ОРЗ в детском возрасте остается актуальной не только из-за их распространенности, но и в связи с необходимостью пересмотра и оптимизации лечебной тактики. Накопленные данные показывают, что преобладающие в практике педиатров подходы по меньшей мере не способствуют становлению иммунной системы ребенка, поэтому пересмотр тактики должен быть в первую очередь направлен на модификацию терапевтической активности, в частности на снижение случаев неоправданных назначений антибактериальных и жаропонижающих средств.
Литература
- Дриневский В. П. Оценка безвредности и эффективности новых препаратов для этиотропного лечения и специфической профилактики гриппа у детей. М., 1999.
- Дриневский В. П., Осидак Л. В., Нацина В. К. и др. Химиопрепараты в терапии гриппа и других ОРВИ у детей//Антибиотики и химиотерапия. М., 1998. Т. 43. Вып. 9. С. 29–34.
- Минздрав РФ, РАМН, НИИ гриппа. Стандартизированные принципы диагностики, лечения и экстренной профилактики гриппа и других острых респираторных инфекций у детей. СПб, 2004.
- Союз педиатров России, Международный Фонд охраны здоровья матери и ребенка: Научно-практическая программа «Острые респираторные заболевания у детей. Лечение и профилактика». М., 2002.
- Mainous A., Hueston W., Love M. Antibiotics for colds in children: who are the high prescribers? Arch. Pediatr. Adolesc. Med. 1998; 52: 349–352.
- Pennie R. Prospective study of antibiotic prescribing for children. Can. Fam. Physician 1998; 44: 1850–1855.
- Nyquist A., Gonzales R., Steiner G. F., Sande M. A. Antibiotic prescribing for children with colds, upper respiratory infections, and bronchitis. JAMA 1998; 279: 875–879.
- Chalumeneau M., Salannave B., Assathiany R. et al. Connaissance et application par des pediatres de ville de la conference de concensus sur les rhinopharyngites aigues de l’enfant. Arch. Pediatr. 2000; 7 (5), 481–488.
- Jacobs R. F. Judicious use of antibiotics for common pediatric respiratory infections. Pediatr. Infect. Dis. J. 2000; 19 (9): 938–943.
- Li Hui, Xiao–Song Li, Xian–Jia Zeng et al. Pattern and determinants of use of antibiotics for acute respiratory tract infections in children in China. Pediatr. Infect. Dis J. 1997; 16 (6): 560РЗР–564.
- Острые пневмонии у детей/Под ред. В. К. Таточенко. Чебоксары: Изд. Чувашского университета, 1994.
- Шохтобов Х. Оптимизация ведения больных с острыми респираторными инфекциями на педиатрическом участке: Дис. … канд. мед. наук. М., 1990. 130 с.
- Романенко А. И. Течение и исходы острых респираторных заболеваний у детей: Автореф. дис. … канд. мед. наук. М., 1988.
- Stanley E. D., Jackson G. G., Panusarn C. et al. Increased virus shedding with aspirin treatment of rhinovirus infection. JAMA 1975; 231: 1248.
- World Health Organization. Cough and cold remedies for the treatment of acute respiratory infections in young children. WHO/FCH/CAH/01.02. WHO. 2001.
В. К. Таточенко, доктор медицинских наук, профессор НЦЗД РАМН, Москва
Состав и форма выпуска
5 мл (1 ч. ложка) сиропа содержат витамина B1 4 мг (тиамина 5 мг), витамина B2 1 мг (рибофлавина 1,32 мг), витамина B6 (пиридоксина гидрохлорида) 2 мг, витамина B12 5 мкг, ниацина (никотинамида, витамина B3) 8 мг, фолиевой кислоты 150 мкг, витамина C (аскорбиновой кислоты) 10 мг, пантотеновой кислоты 2 мг, кальция глицерофосфата 10 мг, железа 7 мг (железа аммония цитрата 35 мг), цинка (сульфата) 5 мг, марганца 0,25 мг (марганца сульфата 21,99 мг), меди 0,25 мг (меди сульфата 0,91 мг), йода 40 мкг (калия йодида 52,32 мкг), лизина гидрохлорида 40 мг, меда 100 мг, экстракта солода 500 мг; во флаконах темного стекла по 200 мл, в коробке 1 флакон.
Фармакологическое действие
Фармакологическое действие — восполняющее дефицит железа, восполняющее дефицит витаминов и минеральных веществ, нормализующее биосинтез гемоглобина.
Витамины B1, B2, B3, B6, B12, фолиевая и пантотеновая кислоты, цинк необходимы для биосинтеза гемоглобина и др. белков, энергетического обмена, поддержания в нормальном состоянии ЦНС. Железо — основной компонент гемоглобина. Витамин C, медь повышают эффективность всасывания железа. Марганец регулирует обмен углеводов. Йод необходим для образования тироксина, регуляции функций щитовидной железы, особенно у детей и во время беременности. Глицерофосфат кальция и лизин поддерживают нормальное состояние организма в целом.
Инструкция по применению порошка Цитовир-3
Фармакодинамика:
препарат является средством этиотропной и иммуностимулирующей терапии, обладает опосредованным противовирусным действием в отношении возбудителей гриппа А и В, а также других вирусов, вызывающих острые респираторные заболевания.
В исследованиях in vitro препарат специфически подавляет (ингибирует) размножение (репликацию) вируса SARS-CoV-2, который является возбудителем новой коронавирусной инфекции (COVID-19).
Степень ингибирования возбудителя возрастает с увеличением концентрации препарата (показана линейность зависимости доза-эффект).
Снижает выраженность основных клинических симптомов гриппа и ОРВИ, а также сокращает продолжительность заболевания и способствует его неосложненному течению. Увеличивает содержание секреторного иммуноглобулина А (sIgA) в слизистой носоглотки — входных воротах инфекции, повышая местную иммунорезистентность организма к респираторным инфекциям вирусной и бактериальной природы.
При профилактическом действии препарат повышает потенциальную метаболическую активность клеток врожденного иммунитета (нейтрофильных гранулоцитов и моноцитов), что, в случае развития инфекции, увеличивает их способность к поглощению и разрушению бактериальных и вирусных агентов за счет усиления ферментативной (окислительной) активности, синтеза катионных белков и увеличения числа фагоцитирующих клеток. При этом исходное состояние метаболической активности клеток врожденного иммунитета, в отсутствии инфекционных агентов, не изменяется, находясь в пределах нормальных значений.
Бендазол индуцирует в организме выработку эндогенного интерферона, обладает иммуномодулирующим действием (нормализует иммунный ответ организма). Ферменты, выработка которых индуцируется интерфероном в клетках различных органов, ингибируют репликацию вирусов. Альфа–глутамил–триптофан (тимоген) является синергистом иммуномодулирующего действия бендазола, нормализуя Т–клеточное звено иммунитета.
Аскорбиновая кислота активирует гуморальное звено иммунитета, нормализует проницаемость капилляров, уменьшая тем самым воспаление, и проявляет антиоксидантные свойства, нейтрализуя кислородные радикалы, сопровождающие воспалительный процесс, повышает устойчивость организма к инфекции.
Фармакокинетика:
при приеме внутрь препарат полностью всасывается из желудочно-кишечного тракта. Биодоступность бендазола – около 80 %, альфа–глутамил–триптофана не более 15 %, аскорбиновой кислоты – до 70 %. Аскорбиновая кислота абсорбируется в ЖКТ (преимущественно в тощей кишке). Связь с белками плазмы – 25 %. ТСmах после приема внутрь – 4 ч. Легко проникает в лейкоциты, тромбоциты, а затем во все ткани, проникает через плаценту.
Заболевания ЖКТ (язвенная болезнь желудка и 12–перстной кишки, нарушения моторики кишечника, глистная инвазия, лямблиоз), употребление овощных и фруктовых соков, щелочного питья уменьшают связывание аскорбиновой кислоты в кишечнике.
Метаболизируется аскорбиновая кислота преимущественно в печени в дезоксиаскорбиновую, далее в щавелевоуксусную и дикетогулоновую кислоты.
Выводится почками, через кишечник, с потом, грудным молоком в неизмененном виде и в виде метаболитов. Продуктами биотрансформации бендазола в крови являются два конъюгата, образующиеся вследствие метилирования и карбоэтоксилирования иминогруппы имидазольного кольца бендазола: 1–метил–2–бензилбензимидазол и 1–карбоэтокси–2бензилбензимидазол. Метаболиты бендазола выводятся с мочой. Альфаглутамил–триптофан под воздействием пептидаз расщепляется на L–глутаминовую кислоту и L–триптофан, которые используются организмом в синтезе белка.