Фармакодинамика
Пимекролимус является производным макролактама аскомицина и обладает противоспалительным действием. Пимекролимус селективно ингибирует продукцию и высвобождение цитокинов и медиаторов воспаления из Т-лимфоцитов и тучных клеток.
Пимекролимус специфично связывается с цитозольным рецептором макрофилином-12 и ингибирует кальцийзависимую фосфатазу — кальциневрин. Ингибирование кальциневрина приводит к подавлению пролиферации Т-лимфоцитов и предотвращает транскрипцию и выработку в Т-хелперах типов 1 и 2 ранних цитокинов, таких как ИЛ-2, γ-интерферон, ИЛ-4, ИЛ-5, ИЛ-10, фактор некроза опухоли (ФНОα) и гранулоцитарно-макрофагальный колониестимулирующий фактор. Пимекролимус и такролимус в равной степени подавляют вторичный иммунный ответ в изолированных клеточных колониях Т-хелперов кожи, полученных у больных с атопическим дерматитом.
Кроме того, in vitro после взаимодействия с комплексом антиген/IgE пимекролимус предотвращает антиген/IgE-опосредованное высвобождение цитокинов и медиаторов воспаления из тучных клеток. Пимекролимус не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток и, в отличие от кортикостероидов, оказывает селективное действие на клетки иммунной системы и не вызывает нарушений функции, жизнеспособности, процессов дифференциации, созревания клеток Лангерганса мышей и дендритных клеток моноцитарного происхождения у человека. Препарат не оказывает влияния на дифференцировку «наивных» Т-лимфоцитов в Т-эффекторные клетки под действием клеток Лангерганса и дендритных клеток, являющуюся одним из основных механизмов специфического иммунного ответа.
На экспериментальных моделях кожного воспаления была продемонстрирована высокая противовоспалительная активность пимекролимуса после его местного и системного применения. При местном применении на экспериментальных моделях аллергического контактного дерматита (АКД) пимекролимус сопоставим по эффективности с высокоактивными кортикостероидами: клобетазолом-17-пропионатом и флутиказоном, ингибирует воспалительную реакцию в ответ на воздействие кожных раздражителей, не вызывая изменения консистенции и атрофии кожи.
Кроме того, при местном и пероральном применении пимекролимус на экспериментальных моделях АКД эффективно уменьшает кожное воспаление, зуд и выраженность гистопатологических изменений. При местном применении степень проникновения в кожу такролимуса и пимекролимуса одинаково хорошая. Однако способность пимекролимуса проникать через кожу меньше, чем у такролимуса и ГКС. Таким образом, пимекролимус обладает селективным действием на кожу.
Уникальность механизма действия пимекролимуса состоит в сочетании селективного противовоспалительного действия на кожу с незначительным влиянием на системный иммунный ответ.
При применении в течение 6 нед у детей в возрасте от 3 мес до 17 лет пимекролимус эффективно уменьшает зуд и кожное воспаление (эритему, инфильтрацию, экскориацию и лихенизацию). При длительном применении в течение 12 мес пимекролимус эффективно снижает частоту возникновения внезапных обострений АКД, не вызывая атрофии, раздражения и повышения чувствительности кожи, не обладая фототоксическим или фотосенсибилизирующим действием.
Элидел в дерматологической практике
В.И. Кулагин, Д.К. Нажмутдинова, Е.В. Таха
Атопический дерматит (АД) является одной из наиболее актуальных проблем дерматологии, что связано со значительным ростом заболеваемости этим дерматозом, характеризующимся хроническим течением с частыми рецидивами, а также с недостаточной эффективностью существующих методов лечения. Частота АД увеличилась в последние десятилетия. Среди людей, родившихся до 1960 г., от 1,4 до 3% имели один эпизод АД или более, а среди родившихся после 1970 г. этот показатель составил от 8,9 до 20,4%. Частота АД особенно высока у детей.
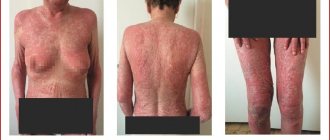
В развитых странах приблизительно 10–15% детей в возрасте менее 5 лет страдают АД , и у 48–75% из них начальные признаки заболевания появились в течение первых 6 мес. жизни. Таким образом, АД стал социально значимой болезнью, особенно учитывая высокую заболеваемость среди детей. Клинические проявления атопического дерматита характеризуются интенсивным зудом, возникновением воспаления, инфильтрации, лихенификации в типичных местах локализации кожного процесса, а также общей повышенной сухостью кожного покрова. Заболевание чаще всего возникает в детском возрасте, рецидивы, как правило, связаны с погрешностями в диете, стрессами. Атопический дерматит – иммунозависимое заболевание, характеризующееся со стороны иммунной системы гиперпродукцией IgE, нарушением цитокиновой регуляции и соотношения Th1/|Th2 лимфоцитов, детерминированным дефицитом Т–лимфоцитов супрессоров, нарушением процессов апоптоза. В патогенезе заболевания существенное значение имеют дисбаланс внутриклеточных регуляторных механизмов (соотношение цАМФ/цГМФ), нарушение мембранной рецепции, активация неиммунных механизмов высвобождения медиаторов аллергии, нарушение нейровегетативной и периферической циркуляции с сосудистой нестабильностью и нарушением рецепции эндотелия; психофизиологические и психосоматические отклонения. В наружной терапии этого дерматоза очень часто применяют кортикостероидные средства, не свободные от побочных эффектов. Однако значительный прогресс и научные достижения в области клинической иммунологии позволили расшифровать многие не известные ранее механизмы иммунопатогенезаэтого заболевания, что послужило стимулом для создания новых препаратов с целенаправленным, селективным действием на аллергические процессы в коже.
Такими средствами стали наружные ингибиторы воспалительных цитокинов , принадлежащие к классу аскомициновых макролактамов. На отечественном рынке лекарственных средств представителем этой группы является 1% пимекролимус (крем «Элидел», , Швейцария). Пимекролимус (Элидел) – это новый нестероидный ингибитор воспалительных цитокинов, разработанный специально как средство местной терапии атопического дерматита. Это вещество обладает избирательным действием в отношении воспалительного процесса в коже и не оказывает влияния на местный и системный иммунный ответ. Пимекролимус является производным макролактама аскомицина. Селективно ингибирует продукцию и высвобождение цитокинов и медиаторов из Т–лимфоцитов и тучных клеток. Обладает противовоспалительными свойствами. Пимекролимус специфично связывается с макрофилином–12 и ингибирует кальцийзависимую фосфатазу кальциневрин. В результате, блокируя транскрипцию ранних цитокинов, пимекролимус подавляет активацию Т–лимфоцитов. В частности, в наномолярных концентрациях пимекролимус ингибирует синтез в человеческих Т–лимфоцитах интерлейкина–2, интерферона–? (Th1 тип), интерлейкина–4 и интерлейкина–10 (Th2 тип). Кроме того, in vitro после взаимодействия с комплексом антиген/IgE пимекролимус предотвращает антиген/IgE–опосредованное высвобождение цитокинов и медиаторов воспаления из тучных клеток. Пимекролимус не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток. На экспериментальных моделях кожного воспаления была продемонстрирована высокая противовоспалительная активность пимекролимуса после его местного и системного применения. При местном применении на моделях аллергического контактного дерматита (АКД) у свиней пимекролимус так же эффективен, как и высокоактивные кортикостероиды клобетазола–17–пропионат и флутиказон.
В отличие от клобетазола–17–пропионата пимекролимус не вызывает атрофию кожи у свиней. В отличие от клобетазола–17–пропионата и флутиказона пимекролимус также не вызывает уплотнения и изменения консистенции кожи у свиней. Как было показано на моделях контактного дерматита у крыс, пимекролимус ингибирует воспалительную реакцию в ответ на воздействие кожных раздражителей. Кроме того, при местном и пероральном применении пимекролимус эффективно уменьшает кожное воспаление и зуд и нормализует гистопатологические изменения у бесшерстных крыс с гипомагниемией, которые являются моделями атопического дерматита острого течения. По сравнению с такролимусом пимекролимус при местном применении одинаково хорошо проникает в кожу, как было показано на экспериментальных моделях. Тем не менее из–за высокой липофильности степень проникновения пимекролимуса через кожу в 10 раз меньше, чем такролимуса. Следовательно, пимекролимус обладает селективным действием на кожу. Пимекролимус эффективнен при кожном воспалении, в то же время его влияние на системный иммунный ответ весьма незначительно. В целом уникальность механизма действия пимекролимуса состоит в сочетании противовоспалительной активности, селективной в отношении кожи, с низкой способностью вызывать системные иммунные ответы. Лечение следует начинать при первых проявлениях заболевания для предотвращения резкого развития его обострения. 1% крем Элидел 2 раза в день наносят тонкимслоем на пораженную поверхность и осторожно втирают до полного впитывания.
Препарат можно наносить на кожу любых частей тела, включая голову, лицо, шею, а также на области опрелостей. Крем следует применять 2 раза в день, до полного исчезновения симптомов. После прекращения лечения, во избежание последующих обострений, при первых признаках рецидива атопического дерматита терапию следует возобновить. Смягчающие средства можно применять сразу после нанесения 1% крема Элидел. Однако после водных процедур смягчающие средства следует применять перед нанесением крема Элидел. Применение 1% крема Элидел может вызывать незначительные преходящие реакции в месте нанесения, такие как чувство тепла и/или жжения. При значительной выраженности этих реакций пациенты должны проконсультироваться у врача. Наиболее часто регистрируемыми побочными эффектами были реакции в месте применения препарата, которые отмечались у 19% пациентов, леченных 1% кремом Элидел, и у 16% пациентов из контрольной группы. Эти реакции в основном возникали на раннем этапе лечения, были незначительными/умеренными и непродолжительными.
Частота побочных эффектов: очень часто ?10%; часто – от ?1% до <10%; иногда – от ?0,1% до <1%; редко – от ?0,01% до <0,1%; очень редко <0,01%. Очень часто: жжение в месте нанесения крема. Часто: местные реакции (раздражение, зуд и покраснение кожи), кожные инфекции (фолликулит). Иногда: нагноение; ухудшение течения заболевания; простой герпес; дерматит, обусловленный вирусом простого герпеса (герпетическая экзема); контагиозный моллюск, местные реакции, такие как сыпь, боль, парестезии, шелушение, сухость, отечность, кожные папилломы, фурункулы. Клинические исследования Элидела (Э) в терапии больных АД продемонстрировали быстрое начало действия препарата, при котором интенсивность зуда уменьшалась уже после 2–3 дня применения крема Элидел , а все симптомы АД регрессировали у большинства больных в течение курса терапии . Благоприятный эффект лечения пимекролимусом наблюдался на протяжении всего исследования (в сроки до 43 дней) у младенцев 3–23 месяцев и у детей 2–17 лет, причем особенно эффективен Э был при локализации процесса на лице и шее, а при последующем клиническом наблюдении отсутствие выраженных симптомов АД сохранялось в сроки до 6 месяцев [ Eichenfield L . et al ., 2002; Ho V . et al ., 2003]. Последующие клинические исследования подтвердили эффективность использования Э в терапии АД у детей и взрослых, установили, что долгосрочное (до 6 месяцев) применение Э способствует контролю над заболеванием и предотвращает развитие выраженных обострений АД, в то же время не приводит к развитию значимых побочных явлений, таких как пиогенная или вирусная суперинфекция . Клинические исследования, проведенные в России (РГМУ, ММА имени И.М. Сеченова, Уральский НИИ дерматовенерологии и иммунопатологии и др.), с участием больных АД различных возрастных групп, в лечении которых использовался новый топический препарат крем Элидел, продемонстрировали эффективность более чем у 95% пациентов .
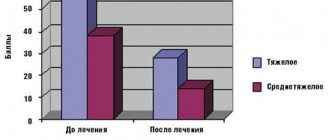
Действие препарата отмечалось уже в первую неделю применения, когда площадь поражения кожи, выраженность симптомов АД уменьшались в 1,4–1,8 раза, а интенсивность зуда и нарушений сна практически в 2 раза. Показатель SCORAD снижался в 2,5–4,6 раза по сравнению с исходным. Крем Элидел был особенно клинически эффективен в терапии больных АД детей до 3–х лет и подростков, что подтверждалось значительным снижениеминдекса SCORAD и его составляющих. У взрослых пациентов было отмечено значительное уменьшение интенсивности зуда после окончания терапии. За время исследования отсутствовали нежелательные явления и осложнения, переносимость крема Элидел была хорошей у большинства пациентов. Таким образом, обобщая результаты исследований и опыт зарубежных и отечественных ученых, можно сделать вывод,что крем Элидел эффективен в терапии больных АД детей, подростков, взрослых и его использование в широкой клинической практике дерматологами позволяет оптимизировать лечение больных АД.
Литература
1. Атопический дерматит у детей. Руководство для врачей. Под ред.Н.Г.Короткого. 2003; 82–90.
2. Атопический дерматит. Руководство для врачей. Под ред. Ю.В.Сергеева. 2002; 8 с.
3. Балаболкин И.И., Гребенюк В.Н. Атопический дерматит у детей, –М.: Медицина, 1999. –238 с.
Кунгуров Н.В., Герасимова Н.М., Кохан М.М. Атопический дерматит (типы течения, принципы терапии) – Екатеринбург: изда–во Урал. ун–та, 2000.–266 с.
4. Кунгуров Н.В., Кохан М.М.Кениксфест Ю.В. и соавт. Опыт примения крема Элидел в терапии топического дерматита у детей и взрослых:РМЖ,т.12,№4,с 171–174. Сергеев Ю.В., Иванов О.Л., Новиков Д.К. Атопический дерматит: современная диагностика и лечение // Иммунопатология, аллергология, инфектология. –2001. –№4. –С. 28–48
5. Скрипкин Ю.К., Самсонов В.А., Селисский Г.Д., Гомберг М.А. Современные проблемы дерматовенерологии // Вестник дерматологии и ве-
нерологии. –1997. –N6. –С.4–8.
6. Смирнова Г.И. Современные технологии местного лечения атопического дерматита у детей // Иммунопатология, аллергология, инфектология. –2003. –№3. –С. 75–82.
7. Феденко Е. С. Атопический дерматит: обоснование поэтапного подхода к терапии // Consilium medicum. –2001. –№3 (4). –С. 176–184.
8. Hultsch T. et al. Ascomycin macrolactam derivative SDZ ASM 981 inhibits the release of granule–associated mediators and of newly synthesized cytokines in RBL 2H3 mast cells in an immunophilin–dependent manner // Arch. Dermatol. Res. – 1998. –Vol.290. –P.501–507.
9. Kapp A. et al. Long–term management of atopic dermatitis in infants with topical pimecrolimus, a nonsteroid anti–inflammatory drug // J. Allergy Clin. Immunol. – 2002. –Vol.110. –P.277–284.
10. Lewis–Jones M.S., Finlay A.Y., Dykes P.J. The Infants’ Dermatitis Quality of Life Index // Br. J. Dermatol. – 2001. –Vol. 144. –P. 104–110.
11. Meurer M. et al. Pimecrolimus cream in the long–term management of atopic dermatitis in adults: A six–month study // Dermatology. – 2002. –Vol. 205. –P.271–277.
12. Schultz–Larsen F, Hanifin JM. Epidemiology of atopic dermatitis // Immunol. Allergy Clin. North Am. –2002. –Vol.22. –P.1–24.
13. Stuetz A et al. Pimecrolimus does not affect Langerhans’ cells in murine epidermis, in contract to corticosteroids // J. Invest. Dermatol. – 2002. –Vol.119. P. 347
14. Tofte S.J., Hanifin J..M. Current management and therapy of atopic dermatitis // J. American Acad. Dermatol. –2001. –Vol. 44 (1). –Р. 13–16.
15. Wahn U et al. Efficacy and safety of pimecrolimus cream in the long–term management of atopic dermatitis in children // Pediatrics.– 2002. –Vol.110. –P.158–159.
Опубликовано с разрешения администрации Русского Медицинского Журнала.
Фармакокинетика
Взрослые. Концентрацию пимекролимуса в крови определяли у 12 взрослых пациентов с атопическим дерматитом (экземой) при поражении 15–59% площади поверхности тела, получавших лечение кремом Элидел 2 раза в сутки на протяжении 3 нед. В 77,5% наблюдений концентрация пимекролимуса в крови была ниже 0,5 нг/мл (минимальная определяемая концентрация), а в 99,8% — ниже 1 нг/мл. Cmax пимекролимуса в крови, зарегистрированная у 1 пациента, составила 1,4 нг/мл.
У 98% из 40 взрослых больных с исходным поражением 14–62% площади поверхности тела после 1 года лечения кремом Элидел концентрации пимекролимуса в крови оставались на низком уровне и в большинстве случаев были ниже минимальной определяемой концентрации.
Значение Cmax, составившее 0,8 нг/мл, было зарегистрировано после 6 нед лечения только у 2 пациентов. Ни у одного из пациентов не было отмечено нарастания концентрации на протяжении 12 мес лечения. За 3-недельный период лечения кремом Элидел 2 раза в сутки у 13 взрослых пациентов с дерматитом кистей (с применением крема на область ладоней и тыльную сторону кистей и бинтованием на ночь) максимальное зарегистрированное значение концентрации пимекролимуса в крови составило 0,91 нг/мл.
У 8 пациентов с содержанием пимекролимуса в крови выше минимальной определяемой концентрации значение AUC составляло 2,5–11,4 нг/мл.
Дети. Фармакокинетические исследования пимекролимуса были проведены у 58 детей в возрасте от 3 мес до 14 лет с атопическим дерматитом (экземой) при поражении 10–92% площади поверхности тела, получавших лечение кремом Элидел 2 раза в сутки на протяжении 3 нед. Пятеро детей получали лечение в течение 1 года по мере необходимости.
Концентрации пимекролимуса в крови были на стабильно низком уровне, независимо от площади поражения кожных покровов и длительности терапии и находились в том же диапазоне значений, что и у взрослых пациентов, получавших терапию кремом Элидел в тех же дозах. В 97% случаев концентрации пимекролимуса в крови были ниже 2 нг/мл, а в 60% — ниже 0,5 нг/мл (минимальная определяемая концентрация). Cmax пимекролимуса, зарегистрированная у 2 пациентов в возрасте 8 мес и 14 лет, составила 2 нг/мл.
Среди детей самого младшего возраста (от 3 до 23 мес) Cmax пимекролимуса составила 2,6 нг/мл и была зарегистрирована у 1 пациента.
У 5 детей, получавших лечение кремом Элидел в течение 1 года, концентрации пимекролимуса находились на стабильно низком уровне. Максимальное значение, зарегистрированное у 1 ребенка, составило 1,94 нг/мл. На протяжении всего периода лечения рост концентраций препарата не наблюдался ни у одного из пациентов.
У 8 детей в возрасте от 2 до 14 лет с содержанием пимекролимуса в крови выше минимальной определяемой концентрации при трехкратном измерении значение AUC составляло от 5,4–18,8 нг/мл. Значения AUC у пациентов с площадью поражения кожных покровов менее или более 40% были сопоставимы.
В исследованиях in vitro связывание пимекролимуса с белками плазмы (в основном с различными липопротеинами) составило 99,6%.
Поскольку при местном применении концентрации пимекролимуса в крови очень низкие, определение параметров метаболизма не представляется возможным.
Фармакокинетика в особых клинических случаях
Атопический дерматит (экзема) редко наблюдается у больных в возрасте 65 лет и старше. Количество пациентов такого возраста в клинических исследованиях 15% крема Элидел было недостаточным, чтобы выявить какие-либо различия в эффективности лечения по сравнению с молодыми пациентами.
Рекомендации по дозированию для младенцев (3–23 мес), детей (2–11 лет) и подростков (12–17 лет) не отличаются от рекомендаций для взрослых пациентов.
Противопоказания
повышенная чувствительность к тимекролимусу или любым компонентам препарата;
детский возраст до 3 мес (безопасность и эффективность применения крема Элидел у детей младше 3 мес не изучалась);
наличие острой вирусной, бактериальной или грибковой инфекций кожи.
С осторожностью:
пациенты с синдромом Нетертона (данных по безопасности применения нет) — возможен риск повышения системной абсорбции препарата;
тяжелые формы воспаления или поражения кожи, в т.ч. генерализованная эритродермия (данных по безопасности применения нет) — возможен риск повышения системной абсорбции препарата;
ослабленный иммунитет — т.к. эффективность и безопасность использования не изучались.
Данные по безопасности длительного применения крема Элидел отсутствуют.
Поскольку влияние длительного применения препарата на иммунную защиту кожи и частоту развития злокачественных новообразований не изучено, крем Элидел не следует наносить на поврежденные участки кожного покрова с возможным озлокачествлением или диспластическими изменениями.
В случае бактериального или грибкового поражения кожи применение крема Элидел на пораженных участках возможно только после излечения инфекции.
Применение при беременности и кормлении грудью
Данных по применению препарата у беременных женщин нет. В экспериментальных исследованиях при местном применении препарата прямого или опосредованного повреждающего действия крема Элидел на течение беременности, развитие эмбриона/плода, течение родов и постнатальное развитие потомства не выявлено. Следует соблюдать осторожность при назначении беременным женщинам. Однако учитывая минимальную степень всасывания пимекролимуса при местном применении, потенциальный риск у человека считается незначительным.
Выделение препарата с грудным молоком после местного применения на экспериментальных моделях не изучалось. Данных по содержанию пимекролимуса в грудном молоке кормящих женщин нет.
Поскольку многие препараты выделяются с грудным молоком, следует соблюдать осторожность при назначении 1% крема Элидел кормящим женщинам. Однако учитывая минимальную степень системного всасывания пимекролимуса при местном применении, потенциальный риск для человека считается незначительным.
Кормящие женщины не должны наносить 1% крем Элидел на область молочных желез.
Влияние крема Элидел на фертильность у мужчин и женщин не установлено.
Фармакологические свойства препарата Элидел
Пимекролимус — производное макролактама аскомицина. Селективно ингибирует продукцию и высвобождение цитокинов и медиаторов из Т-лимфоцитов и тучных клеток. Обладает противовоспалительными свойствами. Пимекролимус в значительной степени специфически связывается с макрофилином-12 и ингибирует кальцийзависимую фосфатазу кальциневрин. В результате, блокируя транскрипцию ранних цитокинов, пимекролимус подавляет активацию Т–лимфоцитов. В частности, в наномолярных концентрациях пимекролимус ингибирует синтез в человеческих Т-лимфоцитах интерлейкина-2, интерферона гамма (Th1-тип), интерлейкина-4 и интерлейкина-10 (Th2-тип). Кроме того, in vitro после взаимодействия с комплексом антиген/IgE-пимекролимус предотвращает антиген/IgE-опосредованное высвобождение цитокинов и медиаторов воспаления из тучных клеток. Пимекролимус не влияет на рост кератиноцитов, фибробластов и эндотелиальных клеток. Препарат сочетает высокую противовоспалительную активность и незначительное влияние на системные иммунные реакции. При местном применении пимекролимуса его концентрация в крови очень низкая, поэтому определить параметры метаболизма невозможно. В коже людей in vitro метаболизма препарата не отмечали.
Побочные действия
Применение крема Элидел может вызывать незначительные преходящие реакции в месте нанесения, такие как чувство тепла и/или жжения. При значительной выраженности этих реакций пациенты должны проконсультироваться у врача.
Наиболее часто реакции в месте применения препарата отмечались у 19% пациентов, получавших лечение кремом Элидел, и у 16% пациентов контрольной группы. Эти реакции в основном возникали на раннем этапе лечения, были незначительными/умеренными и непродолжительными.
Определение частоты побочных реакций: очень часто (≥1/10); часто (≥1/100, <1/10); иногда (≥1/1000, <1/100); редко (≥1/10000, <1/1000); очень редко (<1/10000), включая отдельные сообщения.
Очень часто — жжение в месте нанесения крема.
Часто — местные реакции (раздражение, зуд и покраснение кожи), кожные инфекции (фолликулит).
Иногда — нагноение, ухудшение заболевания, простой герпес, дерматит, обусловленный вирусом простого герпеса (герпетическая экзема), контагиозный моллюск; местные реакции, такие как сыпь, боль, парестезии, шелушение, сухость, отечность, кожные папилломы, фурункулы.
Представленные ниже нежелательные реакции отмечались при постмаркетинговом применении препарата (оценка частоты по количеству случаев развития нежелательных явлений в неустановленной популяции).
Со стороны иммунной системы: очень редко — анафилактические реакции.
Со стороны обмена веществ (метаболические нарушения): редко — непереносимость алкоголя.
Со стороны кожи и ее придатков: редко — аллергические реакции (сыпь, крапивница, ангионевротический отек); изменения цвета кожи (гипопигментация, гиперпигментация).
В большинстве случаев сразу же после приема алкоголя развивалось покраснение лица, сыпь, жжение, зуд или припухлость.
При применении крема Элидел в редких случаях отмечалось развитие злокачественных новообразований, включая кожные и другие типы лимфом, рак кожи. Причинно-следственная связь между данными нежелательными явлениями и применением препарата не установлена.
Побочные эффекты препарата Элидел
Часто: ощущение жжения в месте нанесения крема, реакции в месте нанесения (раздражение, сыпь, эритема), кожные инфекции (фолликулит). Редко: импетиго, ухудшение состояния, простой и опоясывающий герпес, герпесный дерматит, вариолиформный пустулез Капоши, контагиозный моллюск, нарушение в месте нанесения — боль, парестезия, шелушение, сухость, отек, папиллома кожи, фурункул, непереносимость алкоголя (в большинстве таких случаев после приема алкоголя возникали ощущения притока крови, сыпь, зуд или отечность), аллергические реакции (кожная сыпь, крапивница, ангионевротический отек) и изменения цвета кожи (гипо- или гиперпигментация). Очень редко: анафилактические реакции. В единичных случаях у пациентов, применявших крем на основе пимекролимуса, отмечали злокачественные новообразования, включая кожные и другие виды лимфом, а также рак кожи, хотя причинная связь не была установлена.
Взаимодействие
Потенциальное взаимодействие крема Элидел с другими препаратами не изучалось. Учитывая, что системная абсорбция пимекролимуса очень незначительна, какое-либо взаимодействие крема Элидел с препаратами для системного применения маловероятно.
При применении крема Элидел у детей в возрасте 2 лет и старше препарат не оказывал влияния на эффективность вакцинации.
Не рекомендуется нанесение крема на области введения вакцины до полного исчезновения местных проявлений поствакцинальной реакции.
Несовместимость. Поскольку исследования совместимости не проводились, не рекомендуется применять препарат совместно с другими средствами для местного применения.
Способ применения и дозы
Наружно.
Лечение следует начинать при первых проявлениях заболевания для предотвращения резкого развития его обострения.
Крем наносят тонким слоем на пораженную поверхность 2 раза в сутки и осторожно втирают до полного впитывания.
Крем можно наносить на кожу любых частей тела, включая голову, лицо, шею, а также на области опрелостей. Крем Элидел следует применять 2 раза в сутки, до полного исчезновения симптомов заболевания. При сохранении выраженности симптомов через 6 нед применения препарата необходимо провести повторное обследование пациента для подтверждения диагноза атопического дерматита. После прекращения лечения, во избежание последующих обострений, при первых признаках рецидива атопического дерматита терапию следует возобновить. Смягчающие средства можно применять сразу после нанесения 1% крема Элидел. Однако после водных процедур смягчающие средства следует применять перед нанесением крема Элидел.
Учитывая очень незначительное системное всасывание пимекролимуса, ограничений общей суточной дозы наносимого препарата, площади обрабатываемой поверхности кожи или длительности лечения не существует. При попадании крема Элидел в глаза, на слизистые оболочки (ротовой или носовой полости) следует немедленно удалить крем и промыть глаза и слизистые оболочки проточной водой.
Особые указания
При лечении ингибиторами кальциневрина для местного применения, включая Элидел, в редких случаях отмечалось развитие злокачественных новообразований (например кожных опухолей и лимфом). Причинно-следственная связь между данными нежелательными явлениями и применением препарата не установлена.
В клинических исследованиях при применении крема Элидел у 0,9% пациентов (14 из 1544) отмечалось развитие лимфаденопатии. Обычно лимфаденопатия была обусловлена инфекционными заболеваниями и исчезала после проведения курса соответствующей антибиотикотерапии. У всех пациентов или удавалось выявить причину развития лимфаденопатии, или отмечалось исчезновение данного нежелательного явления. У больных, получающих лечение Элиделом, при развитии лимфаденопатии необходимо установить этиологию процесса и обеспечить наблюдение за пациентами до полного исчезновения данного нежелательного явления. При неустановленной этиологии лимфаденопатии или при наличии у пациента острого мононуклеарного воспаления препарат следует отменить.
При лечении кремом Элидел пациентам рекомендуется уменьшить до минимума искусственную или естественную инсоляцию кожи или полностью исключить УФ облучение. Возможное влияние применения препарата при поражениях кожи, вызванных УФ облучением, неизвестно.
Влияние на способность к вождению автотранспорта и управлению механизмами. Влияние применения крема Элидел на способность к управлению автотранспортом или работе с механизмами не установлено.
Особые указания по применению препарата Элидел
Не следует наносить на пораженные острой вирусной инфекцией кожные покровы. В случае бактериального или грибкового поражения кожи применение крема возможно после излечения инфекции. Если инфекционный процесс не уменьшается, применение крема нужно отменить до купирования симптомов инфекции. Поскольку влияние Элидел 1% крема при длительном применении на местный иммунитет и на проявления злокачественных новообразований кожи не известно, его не следует применять при потенциально злокачественных новообразованиях кожи или при возможности таких заболеваний. Хотя причинная связь не установлена, однако имели место редкие случаи злокачественных новообразований кожи и лимфомы у пациентов, местно применявших ингибиторы кальциневрина, в том числе Элидел 1% крем. Данное лекарственное средство не рекомендуется пациентам с синдромом Нетертона или генерализованной эритродермией, когда существует риск повышенного всасывания, поскольку не установлена безопасность применения Элидел 1% крема у пациентов с данными заболеваниями. Безопасность и эффективность Элидел 1% крема у пациентов с иммунодефицитом также не изучена, поэтому применение препарата у этой группы больных не рекомендовано. При клинических исследованиях Элидел 1% крема отмечено 0,9% случаев лимфаденопатии. Как правило, они были связаны с инфекциями и исчезали при соответствующей терапии антибиотиками (большинство из них имели известную этиологию или исчезали сами по себе). Поэтому при появлении лимфаденопатии у пациентов, применявших Элидел 1% крем, нужно уточнить этиологию данного процесса. При неясной этиологии лимфаденопатии или при появлении острого инфекционного мононуклеоза лечение препаратом следует прекратить. Необходимо наблюдение в динамике пациентов с симптомами появившейся лимфаденопатии для контроля ее излечения. На протяжении лечения Элидел 1% кремом целесообразно, чтобы пациенты максимально ограничивали пребывание при естественном или искусственном солнечном освещении или вообще избегали его, даже когда крем не нанесен на пораженные участки кожи. Потенциальное влияние Элидел 1% крема на пораженную кожу, которая находится под действием ультрафиолетового облучения, не известно. У пациентов в возрасте 65 лет и старше случаи атопического дерматита (экземы) отмечаются редко. В клинические исследования по изучению Элидел 1% крема не было включено достаточного количество пациентов данной возрастной категории для определения отличается ли их реакция на препарат от таковой у пациентов более молодого возраста. Применение крема может вызывать незначительные преходящие реакции в месте нанесения, такие как ощущение тепла и/или жжения. При значительной выраженности этих реакций пациенты должны проконсультироваться у врача. Крем нельзя наносить на слизистые оболочки. При случайном попадании препарата на слизистую оболочку или в глаза следует немедленно промыть их водой. Период беременности и кормления грудью. Нет данных по применению крема Элидел в период беременности. Следует соблюдать осторожность при назначении 1% крема Элидел в указанный период. Неизвестно, проникает ли пимекролимус в грудное молоко, поэтому следует соблюдать осторожность при назначении 1% крема Элидел в период кормления грудью. Матери в период кормления грудью нельзя наносить 1% крем Элидел на область молочных желез. Влияние на способность управлять транспортными средствами и работу с механизмами: не установлено.