Что общего у препаратов
Чтобы понять, в чем разница и какой препарат лучше – Розувастатин или Аторвастатин, необходимо провести сравнительный анализ. Оба рассматриваемых препарата являются представителями статинов нового поколения. Необходимо подобрать такой из них, чтобы наряду с ощутимым лечебным действием он оказывал минимальные побочные эффекты.
Механизм их действия примерно одинаков, но имеются небольшие отличия. Если понимать разницу между ними, то можно скорректировать лечение конкретного пациента, что значительно улучшит прогноз на его выздоровление. Общим между Розувастатином и Аторвастатином является то, что оба препараты имеют двойное действие – снижают уровень плохого и повышают содержание хорошего холестерина.
Также общим для этих двух препаратов является то, что они:
- улучшают состояние внутренней оболочки сосудов при ее дисфункции;
- улучшают текучесть крови по сосудам;
- благотворно влияют на сосудистую стенку.
Оба препарата имеют общие показания к применению. Поскольку они относятся к статинам последнего поколения, их можно назначать не только для лечения заболеваний, но и для их профилактики, что было затруднительно со статинами первого и второго поколения ввиду множества побочных эффектов от них.
Поэтому рассматриваемые лекарственные средства рекомендуется применять пациентам, у которых повышенный риск развития ишемической болезни сердца. К факторам, повышающим этот риск, относятся:
- возраст старше 55 лет;
- наличие в анамнезе сахарного диабета;
- пристрастие к курению;
- повышенное артериальное давление;
- наследственная предрасположенность к повышению холестерина;
- сниженное содержание липопротеинов высокой плотности в крови.
Аторвастатин и Розувастатин не назначаются для лечения детей и подростков, в период кормления грудью и беременности, при острой стадии заболевания печени. Их применяют с осторожностью, если пациент страдает алкоголизмом, предрасположен к миопатии или в анамнезе имеется почечная недостаточность.
Максимальный лечебный эффект от приема статинов нового поколения достигается через 4 недели от начала приема. Если лекарство принимает женщина, сохранившая репродуктивные возможности, то ей и рекомендуется наряду со статинами позаботиться о надежных средствах контрацепции.
Оба препарата оказывают минимальное количество побочных эффектов, поэтому имеют хорошую переносимость пациентами. Их можно принимать независимо от поглощения пищи и без привязки к определенному времени суток.
Высокий уровень «вредного» холестерина приводит к закупорке сосудов
Розувастатин (Rosuvastatin)
Нарушение функции почек
У пациентов, получавших высокие дозы розувастатина (в частности 40 мг/сут), наблюдалась канальцевая протеинурия, которая выявлялась при помощи тест-полосок и в большинстве случаев была периодической или кратковременной. Такая протеинурия не свидетельствует об остром заболевании или прогрессировании сопутствующего заболевания почек. Частота серьезных нарушений функции почек, отмеченная при постмаркетинговом изучении розувастатина, выше при приеме дозы 40 мг/сут. У пациентов, принимающих препарат Розувастатин в дозе 30 или 40 мг/сут, рекомендуется контролировать показатели функции почек во время лечения (не реже чем 1 раз в 3 месяца).
Влияние на опорно-двигательный аппарат
При применении розувастатина во всех дозах, но в особенности в дозах, превышающих 20 мг/сут, сообщалось о следующих воздействиях на опорно-двигательный аппарат: миалгия, миопатия, в редких случаях рабдомиолиз. Отмечены очень редкие случаи рабдомиолиза при одновременном применении ингибиторов ГМГ-КоА-редуктазы и эзетимиба. Такая комбинация должна применяться с осторожностью, так как нельзя исключить фармакодинамического взаимодействия.
Как и в случае других ингибиторов ГМГ-КоА-редуктазы, частота развития рабдомиолиза при постмаркетинговом применении розувастатина выше при применении дозы 40 мг/сут.
Определение сывороточной активности КФК
Сывороточную активность КФК нельзя определять после интенсивных физических нагрузок и при наличии других возможных причин повышения ее активности, это может привести к неверной интерпретации полученных результатов. В случае, если исходная сывороточная активность КФК существенно превышена (в 5 раз выше верхней границы нормы), через 5-7 дней следует провести повторный анализ. Нельзя начинать терапию, если результаты повторного анализа подтверждают исходную высокую сывороточную активность КФК (более чем 5-кратное превышение верхней границы нормы).
Перед началом терапии
В зависимости от суточной дозы препарат Розувастатин должен назначаться с осторожностью пациентам с имеющимися факторами риска миопатии/рабдомиолиза.
К таким факторам относятся:
— нарушение функции почек,
— гипотиреоз,
— заболевания мышц в анамнезе (в том числе в семейном анамнезе),
— миотоксические явления при приеме других ингибиторов ГМГ-КоА-редуктазы или фибратов в анамнезе,
— чрезмерное употребление алкоголя,
— возраст старше 65 лет,
— состояния, при которых может повышаться концентрация розувастатина в плазме крови,
— одновременное применение фибратов.
У таких пациентов необходимо оценить риск и возможную пользу терапии. Также рекомендуется проводить клинический мониторинг. Если исходная сывороточная активность КФК выше более чем в 5 раз по сравнению с верхней границей нормы, терапию препаратом Розувастатин начинать нельзя.
В период терапии препаратом
Следует проинформировать пациента о необходимости немедленного сообщения врачу в случае неожиданного появления мышечных болей, мышечной слабости или спазмов, особенно в сочетании с недомоганием и лихорадкой. У таких пациентов следует определять сывороточную активность КФК. Терапия должна быть прекращена, если сывороточная активность КФК значительно увеличена (более чем в 5 раз по сравнению с верхней границей нормы), или если симптомы со стороны мышц резко выражены и вызывают ежедневный дискомфорт (даже, если сывороточная активность КФК не более чем в 5 раз превышает верхнюю границу нормы). Если симптомы исчезают, и сывороточная активность КФК возвращается к норме, следует рассмотреть вопрос о возобновлении применения препарата Розувастатин или других ингибиторов ГМГ-КоА- редуктазы в меньших дозах при тщательном медицинском наблюдении. Контроль сывороточной активности КФК при отсутствии симптомов нецелесообразен.
Отмечены очень редкие случаи иммуноопосредованной некротизирующей миопатии с клиническими проявлениями в виде стойкой слабости проксимальных мышц и повышения активности КФК в сыворотке крови во время терапии или при прекращении применения ингибиторов ГМГ-КоА-редуктазы, в том числе розувастатина. Может потребоваться проведение дополнительных исследований мышечной и нервной системы, серологических исследований, а также терапия иммунодепрессивными средствами. Признаков увеличения воздействия на скелетную мускулатуру при приеме розувастатина и сопутствующей терапии не отмечено. Однако сообщалось об увеличении числа случаев миозита и миопатии у пациентов, принимавших другие ингибиторы ГМГ-КоА-редуктазы в сочетании с производными фиброевой кислоты (например, гемфиброзил), циклоспорином, никотиновой кислотой в липидснижающих дозах (более 1 г/сут), противогрибковыми средствами — производными азола, ингибиторами протеазы ВИЧ и макролидными антибиотиками.
При одновременном применении с некоторыми ингибиторами ГМГ-КоА-редуктазы гемфиброзил увеличивает риск развития миопатии. Таким образом, одновременное применение препарата Розувастатин и гемфиброзила не рекомендуется. Преимущества дальнейшего изменения плазменной концентрации липидов при комбинированном применении препарата Розувастатин с фибратами или никотиновой кислотой в липидснижающих дозах должны быть тщательно взвешены с учетом возможного риска. Препарат Розувастатин в дозе 40 мг/сут противопоказан для комбинированной терапии с фибратами.
Препарат Розувастатин не следует применять одновременно или в течение 7 дней после прекращения терапии препаратами фузидовой кислоты системного действия. У пациентов, у которых применение фузидовой кислоты считается необходимым, следует прекратить терапию статином на весь период терапии фузидовой кислотой. Были получены сообщения о рабдомиолизе (в том числе со смертельным исходом в некоторых случаях) у пациентов, получающих фузидовую кислоту одновременно со статинами. Пациенту следует немедленно обратиться за медицинской помощью при появлении любых симптомов мышечной слабости, боли или болезненности.
Терапия препаратом Розувастатин может быть возобновлена через 7 дней после применения последней дозы фузидовой кислоты.
В исключительных случаях, когда требуется длительное применение фузидовой кислоты системного действия, например, при лечении тяжелых инфекций, необходимость одновременного применения препарата Розувастатин и фузидовой кислоты следует рассматривать индивидуально и при условии тщательного врачебного наблюдения.
В связи с увеличением риска рабдомиолиза препарат Розувастатин не следует применять пациентам с острыми состояниями, которые могут привести к миопатии или состояниям, предрасполагающим к развитию почечной недостаточности (например, сепсис, артериальная гипотензия, обширные хирургические вмешательства, травмы, тяжелые метаболические, эндокринные или электролитные нарушения, неконтролируемые судороги).
Через 2-4 недели после начала лечения и/или при повышении дозы препарата Розувастатин необходим контроль показателей липидного обмена (при необходимости требуется коррекция дозы).
Печень
В зависимости от суточной дозы препарат Розувастатин должен с осторожностью применяться у пациентов с чрезмерным употреблением алкоголя и/или у пациентов, имеющих в анамнезе заболевания печени, или его применение противопоказано (см. разделы «Противопоказания» и «С осторожностью»).
Рекомендуется проводить определение функциональных проб печени до начала терапии и через 3 месяца после ее начала. Применение препарата Розувастатин следует прекратить или уменьшить дозу препарата, если активность «печеночных» трансаминаз в сыворотке крови в 3 раза превышает верхнюю границу нормы.
У пациентов с гиперхолестеринемией вследствие гипотиреоза или нефротического синдрома до начала лечения препаратом Розувастатин должна проводиться терапия основных заболеваний.
Этнические особенности
В ходе фармакокинетических исследований у представителей монголоидной расы по сравнению с представителями европеоидной расы отмечено увеличение плазменной концентрации розувастатина.
Интерстициальное заболевание легких
При применении некоторых ингибиторов ГМГ-КоА-редуктазы, особенно в течение длительного времени, сообщалось о единичных случаях интерстициального заболевания легких. Проявлениями заболевания могут являться одышка, непродуктивный кашель и ухудшение общего самочувствия (слабость, снижение веса и лихорадка).
При подозрении на интерстициальное заболевание легких следует прекратить терапию ингибиторами ГМГ-КоА-редуктазы.
Сахарный диабет 2 типа
У пациентов с концентрацией глюкозы от 5,6 до 6,9 ммоль/л терапия розувастатином ассоциировалась с повышенным риском развития сахарного диабета 2 типа.
Ингибиторы протеазы ВИЧ
Не рекомендуется одновременное применение препарата с ингибиторами протеазы ВИЧ (см. раздел «Взаимодействие с другими лекарственными средствами»).
Специальная информация по вспомогательным веществам
Препарат Розувастатин содержит лактозу, поэтому противопоказан пациентам с непереносимостью лактозы, дефицитом лактазы, синдромом глюкозо-галактозной мальабсорбции.
В чем разница
Сравнение препаратов Аторвастатин и Розувастатин выявило, что несмотря на некоторую их схожесть они принадлежат к статинам разного поколения. Розувастатин – это новейшая разработка, а Аторвастатин предшествует ему. Преимуществом последнего поколения является то, что можно снизить дозировку препарата, поскольку он обладает высокой эффективностью.
Ловастатин и его аналоги
В отличие от Аторвастатина 90% Розувастатина выводится из организма через органы пищеварения, а 5% – через мочу. Кроме того, если сравнить между собой лекарственные средства по показателю снижения холестерина низкой плотности, то Аторвастатин немного уступает Розувастатину.
Первый снижает максимум на 54%, а второй – на 63%. Они отличаются также периодом полувыведения. Если для Аторвастатина этот промежуток времени занимает от 15 до 30 часов, то для Розувастатина – 19 часов.
Препарат новейшего поколения отличается более высоким показателем биодоступности. Это означает, что он лучше усваивается организмом. Но разница между ними не столь существенная: Аторвастатин – 12% а Розувастатин – 20%.
Чем отличаются эти препараты еще, так это характером растворимости. Так, Розувастатин является гидрофильным препаратом, а Аторвастатин – липофильным. Это означает, что Аторвастатин растворяется в жирах, а Розувастатин – в воде. Если предстоит сделать выбор между Аторисом и Розувастатином, то необходимо иметь в виду, что Аторис является разновидностью Аторвастатина, поэтому сходства и отличия будут примерно те же.
По степени безопасности оба рассматриваемых препарата примерно одинаковы. Но, например, при диабете 2 типа предпочтение следует отдать Розувастатину, поскольку он меньше оказывает влияние на углеводный обмен.
Если сравнивать эти препараты по стоимости, то в общем цена Аторвастатина значительно ниже, чем стоимость Розувастатина. В этом смысле значение имеет дозировка препарата и количество таблеток в упаковке. Например, 90 таблеток по 20 мг Аторвастатина будет стоить около 800 руб., в то время как за такую же упаковку Розувастатина придется заплатить больше 1000 руб.
Если судить об эффективности этих лекарственных средств, то практика показывает, что Розувастатин оказывает более выраженное действие по сравнению с Аторвастатином. Эффективность у них выше, а способность оказывать побочные эффекты ниже, чем у статинов, относящихся к первому поколению, например, Симвастатин.
Особенности Аторвастатина
Препарат Аторвастатин относится к категории статинов третьего поколения. Лекарственное средство выпускается в различных дозировках – по 10, 20, 40 и 80 мг. В аптечной сети представлены 2 вида этого препарата – российского (Аторвастатин) и израильского производства (Аторвастатин-Тева). Активным действующим веществом Аторвастатина является аторвастатин кальций тригидрат.
Препарат снижает концентрацию липопротеинов низкой плотности и одновременно увеличивает содержание липопротеинов высокой плотности. Также эффективен при семейных и гомозиготных гиперхолестеринемиях. Эффективность лекарства проявляется через 2 недели регулярного приема. Уже через 30 дней достигается максимальный эффект антихолестеринового средства, который сохраняется в течение всего времени лечения.
Аторвастатин так же, как и Розувастатин принадлежит к новому поколению статинов
Прием Аторвастатина необходимо сочетать с соблюдением диеты. Согласно диете, пациент должен исключить из рациона продукты, богатые животными жирами, а также блюда, приготовленные посредством жарки. Пить таблетки можно независимо от времени приема пищи. Дозировка подбирается индивидуально лечащим врачом по результатам липидограммы.
Начальная дозировка –10 мг, в последующем по необходимости ее можно увеличивать до 80 мг в сутки. Пациенты, страдающие почечной или печеночной недостаточностью, принимают Аторвастатин все время в этой начальной дозировке. Показаниями к назначению Аторвастатина является комплексное лечение высокого уровня общего холестерина и ЛПНП и повышение уровня триглицеридов.
На фоне приема Аторвастатина могут развиться следующие побочные реакции:
- нарушение сна;
- головная боль и головокружение;
- анемия или тромбоцитопения;
- диспепсические расстройства;
- артрит и миалгия;
- аллергия;
- отеки;
- облысение;
- повышенное потоотделение;
- чувствительность к свету.
Аторвастатин не назначают к применению при повышенной активности печеночных ферментов, почечной недостаточности, в период беременности и кормления грудью, при индивидуальной непереносимости компонентов препарата, тяжелых патологиях печени. Лекарственное средство также противопоказано пациентам, не достигшим 18 лет.
Стоимость препарата в аптеках зависит от дозировки и производителя и варьируется в пределах от 130 до 400 рублей. Его аналогами являются препараты Аторис, Липримар, Тулип.
В настоящее время в развитых странах мира до 80–95 % больных ишемической болезнью сердца (ИБС) принимают статины. Эти цифры свидетельствуют о том, что у кардиологов не осталось сомнений в целесообразности такого лечения. Действительно, за последние годы опубликованы данные сразу нескольких очень крупных исследований, которые однозначно свидетельствуют о снижении смертности (как сердечно-сосудистой, так и общей) на фоне терапии этими лекарствами. Кроме того, описано много дополнительных эффектов статинов, которые могут использоваться самостоятельно. Это, например, значимое антиишемическое действие, наблюдаемое при длительном приеме этих препаратов. Противовоспалительные эффекты статинов столь велики, что предпринимаются попытки лечить с их помощью ревматоидный артрит. Появились сообщения о клинической эффективности статинов при демиелинизирующих заболеваниях.
Однако, несмотря на широкое применение статинов, целевые уровни липидов (прежде всего, атерогенных фракций) достигаются далеко не всегда. В то же время снижение частоты осложнений коронарного атеросклероза связывают с коррекцией именно этого фактора риска. Попытки комбинировать статины с другими гиполипидемическими препаратами не всегда удачны, так как могут приводить к развитию выраженных побочных эффектов (как это было в случае с церивастатином, который в комбинации с фибратами привел к развитию большого числа случаев рабдомиолиза). Есть данные о совместном использовании статинов и никотиновой кислоты. Однако сама никотиновая кислота обладает весьма широким спектром побочных эффектов.
В настоящее время активно рекомендуется применять максимальные дозировки статинов. Однако при этом лечение становится настолько дорогим, что даже в развитых странах такой подход не используется повсеместно. Так, месячное лечение аторвастатином (самый популярный в США статин) в дозе 80 мг (без учета стоимости контроля параметров безопасности) обойдется почти в 400 долл. США. В нашей стране, где такая дозировка не зарегистрирована, прием 8 таблеток (по 10 мг) аторвастатина в сутки обойдется больному в 400–500 долл. ежемесячно. Но даже такие дозы не всегда приводят к достижению целевого уровня липопротеидов низкой плотности (ЛПНП).
Сопоставление статинов, умеренно и агрессивно снижающих липиды
В течение 2004 г. были опубликованы результаты 2 интересных исследований по сопоставлению статинов – правастатина, действующего на уровень ЛПНП весьма умеренно, и аторвастатина, снижающего уровень ЛПНП в значительно большей степени. Полученные данные свидетельствуют о том, что назначение статинов, интенсивно снижающих уровень липидов, приводит к более выраженному клиническому эффекту.
Исследование REVERSAL
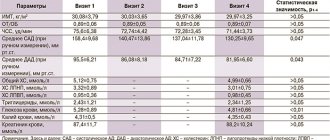
В этом исследовании (Reversal of Atherosclerosis with Aggressive Lipid Lowering) сопоставляли действие 40 мг правастатина и 80 мг аторвастатина в сутки на динамику атеросклеротического поражения коронарного русла по изменению объема коронарной атеромы [1]. Из 2163 скринированных больных были рандомизированы и получали исследуемые препараты 654 пациента. Из их числа 502 больным удалось выполнить внутрисосудистое ультразвуковое исследование удовлетворительного качества исходно и через 18 месяцев терапии, при этом 249 пациентов вошли в группу правастатина, 253 – в группу аторвастатина. Исходный уровень ЛПНП в обеих группах составил 150,2 мг/дл (3,89 ммоль/л). На фоне лечения правастатином содержание этой фракции снизилось до 110 мг/дл (2,85 ммоль/л), а при применении аторвастатина – до 79 мг/дл (2,09 ммоль/л). По этому показателю различия оказались высокодостоверными (р
Исследованные статины по-разному влияли на объем атеромы. Если фоне лечения правастатином атеросклеротическое поражение прогрессировало (рост на 2,7 %, р = 0,001), то в группе аторвастатина его объем не менялся.
Исследование PROVE-IT – TIMI-22
В исследовании Pravastatin or Atorvastatin Evaluation and Infection Therapy – Thrombolysis in Myocardial Infarction 22 (PROVE-IT – TIMI-22) также сопостав-ляли эффекты аторвастатина (80 мг/сут) и правастатина (40 мг/сут) [2].
Рандомизации были подвергнуты 4162 больных – мужчины и женщины старше 18 лет, госпитализированные по поводу острого коронарного синдрома (с подъемом сегмента ST или без него) либо перенесшие эпизод нестабильной стенокардии высокого риска в течение 10 дней до включения в исследование. Уровень общего холестерина не должен был превышать 240 мг/дл (6,21 ммоль/л) или 200 мг/дл (5,18 ммоль/л), если больные ранее получали статины. В исследование не включали пациентов, ранее получавших статины в дозе 80 мг/сут, и больных, использующих лекарства, метаболизируемые изоферментом 3А4 системы цитохрома Р450.
В группу правастатина были включены 2063 больных, в группу аторвастатина – 2099. Группы были полностью сопоставимы по всем основным клинических характеристикам, за исключением частоты встречаемости периферического атеросклероза, который чаще отмечался среди пациентов, получавших правастатин (р = 0,03). Срок наблюдения составил от 18 до 36 месяцев (в среднем – 24 месяца). После того как было зафиксировано 925 конечных точек, исследование было остановлено.
В качестве конечных точек регистрировали смерть от любых причин, инфаркт миокарда, документированную нестабильную стенокардию, потребовавшую госпитализации, реваскуляризацию (ангиопластика или аортокоронарное шунтирование), проведенную более чем через 30 дней после рандомизации, и инсульт.
Достоверное различие между группами в уровне ЛПНП отмечалось уже с 30 дня лечения. На фоне применения правастатина его средняя концентрация была равна 95 мг/дл (2,46 ммоль/л), а в группе аторвастатина – 62 мг/дл (1,60 ммоль/л). У ранее получавших статины больных правастатин дополнительного не снижал уровень ЛПНП, тогда как аторвастатин снижал их концентрацию еще на 32 %. У пациентов, ранее не принимавших статины, при лечении правастатином уровень ЛПНП снизился на 22 %, а при применении аторвастатина – на 51 %. В то же время уровень липопротеидов высокой плотности (ЛПВП) в большей степени повышался в группе правастатина (8,1 против 6,5 %, р
Высокодостоверными оказались и различия в степени снижения уровня СРБ. Хотя его содержание достоверно снижалось в обеих группах, однако на фоне правастатина его уровень снизился до 2,1 мг/л, а на фоне приема аторвастатина – до 1,3 мг/л (исходный уровень – 12,3 мг/л в обеих группах).
Основной результат исследования состоял в меньшей на 16 % (р = 0,005) частоте развития конечных точек в группе аторвастатина. В течение 2 лет наблюдения частота развития неблагоприятных исходов при применении правастатина составила 26,3 %, и только 22,4 % при лечении аторвастатином. Различие между группами начало отмечаться на 30 день лечения и сохранялось на всем протяжении исследования.
На фоне лечения аторвастатином достоверно меньшими оказались частота развития нестабильной стенокардии, требовавшей госпитализации (на 29 %, р = 0,02), и необходимость проведения реваскуляризации (на 14 %, р = 0,04). Снижение, хотя и недостоверное, отмечалось также в отношении риска смерти от любых причин (на 28 %, р = 0,07) и комбинированной конечной точки смерть + инфаркт миокарда (на 18 %, р = 0,06). Инсульт в обеих группах встречался редко, значимого различия по этой конечной точке между группами отмечено не было.
В наибольшей степени преимущества аторвастатина проявились у больных с исходным уровнем ЛПНП выше 125 мг/дл (снижение риска комбинированной конечной точки на 34 %, р = 0,02), а также у пациентов, ранее не получавших статины.
Важность результатов, демонстрирующих явное преимущество аторвастатина, состоит еще и в том, что они были получены в исследовании, проводившемся компанией-производителем правастатина, специалисты которой имели основания предполагать совершенно другие итоги. Основная гипотеза, лежавшая в основе протокола, предполагала отсутствие различий в клинических эффектах двух статинов, несмотря на различия в гиполипидемическом действии.
Концепция чем ниже, тем лучше”
В июле 2004 г. в журнале Circulation [3] были опубликованы поправки к 3 сообщению Национальной образовательной программы США по холестерину. На основании результатов, опубликованных в последнее время исследований, было принято решение существенно ужесточить требования к уровню ЛПНП крови (табл. 1).
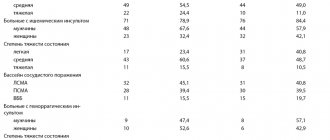
Предложено выделить 4 группы риска в отношении развития коронарной смерти в течение ближайших 10 лет. К группе высокого риска отнесены состояния, соответствующие риску инфаркта или коронарной смерти более чем в 20 % случаев за последующие 10 лет. Это наличие анамнеза ИБС (перенесенный инфаркт миокарда, нестабильная стенокардия, стабильная стенокардия, процедуры реваскуляризации), признаки значимой ишемии миокарда. Кроме того, к такому риску ведет наличие у больного так называемых эквивалентов ИБС по риску. Это клинически значимый некоронарный атеросклероз, сахарный диабет или сочетание состояний, при которых риск превышает 20 %.
У этой группы больных уровень ЛПНП должен быть ниже 100 мг/дл (2,6 ммоль/л). Однако существуют данные, что такой целью может стать снижение концентрации ЛПНП ниже 70 мг/дл (1,8 ммоль/л), особенно у больных с очень высоким риском (перенесших острый коронарный синдром). Если уровень ЛПНП у таких больных больше либо равен 2,6 ммоль/л, одновременно с изменением образа жизни требуется назначение гиполипидемической терапии. Однако существуют доказательства того, что таким пациентам терапия статинами показана и вслучаях, когда исходный уровень ЛПНП ниже 2,6 ммоль/л. Высокий уровень триглицеридов или низкий уровень ЛПВП являются показанием для дополнительного назначения фибратов или никотиновой кислоты. Причем если концентрация триглицеридов выше 2,3 ммоль/л, то одной из целей терапии становится достижение уровня атерогенных фракций холестерина (холестерин всех фракций за исключением ЛПВП) ниже 3,4 ммоль/л (на 0,8 ммоль/л выше целевого уровня ЛПНП).
Следующая градация – высокий промежуточный риск – предполагает сочетание 2 и более факторов риска, при которых частота развития инфаркта миокарда или коронарной смерти за последующие 10 лет составляет 10–20 %. К такому риску ведет сочетание курения, повышения АД более 140/90 мм рт. ст., низкого уровня ЛПВП (
Риск на основании этих факторов рассчитывается при помощи специальных программ-калькуляторов (в Интернете такой калькулятор находится по адресу www.nhlbi.gov/guidelines/cholesterol).
Промежуточный риск – сочетание 2 и более факторов риска, при которых рассчитанный с помощью калькулятора 10-летний риск – не превышает 10 %.
В случае когда в группах высокого и промежуточного риска применяются гиполипидемические препараты, уровень ЛПНП должен снижаться, по крайней мере, на 30–40 %.
Важно также, чтобы всем больным активно корректировали образ жизни (увеличение физической активности); проводили терапию, направленную на снижение избыточной массы тела и лечение метаболического синдрома, устранение гипертриглицеридемии и повышение уровня ЛПВП в случае его снижения.
В группе низкого риска (0–1 фактор риска) рассчитывать риск ИБС не следует.
Европейские рекомендации по профилактике сердечно-сосудистых заболеваний основываются не на расчете риска осложнений коронарного атеросклероза, а на учете суммарного риска сердечно-сосудистых заболеваний, включая инсульт.
Место противовоспалительного эффекта в антиатерогенном действии статинов
Большое число эффектов статинов, не связанных со снижением уровня атерогенных липопротеидов, позволяет всерьез обсуждать вопрос о том, что важнее – их действие на синтез холестерина или другие последствия блокады метаболизма мевалоновой кислоты.
Наибольшее внимание привлекает противовоспалительное действие статинов. Участие реакций воспаления в атерогенезе считается сегодня доказанным. Установлено, что прогноз при атеросклеротическом поражении различной локализации можно в значительной степени уточнить, измеряя уровень маркеров воспаления в системном кровотоке. Наиболее часто для этого используют определение уровня СРБ с помощью высокочувствительной методики. На основании данных крупных эпидемиологических исследований уровень СРБ предложено разделять на 3 диапазона: низкий – менее 1,0 мг/л, средний – 1,0–3,0 мг/л и высокий – более 3,0 мг/л. Уровень СРБ выше 10 мг/л указывает на наличие причин для системной воспалительной реакции, таких как инфекция, травма и т. п. Для оценки риска атеросклероза этот анализ следует повторить через 2 недели после купирования указанных состояний.
СРБ – негликозилированный белок, основным регулятором синтеза которого считается интерлейкин 6. Стимулом, провоцирующим синтез СРБ, могут быть окисленные липопротеиды. До недавнего времени считалось, что СРБ синтезируется гепатоцитами, однако в последнее время обнаружено, что он может продуцироваться и в атеросклеротических бляшках, почках, нервной ткани и альвеолярных макрофагах. Недавно появились сведения, что СРБ – не только маркер воспалительного процесса при атеросклерозе, но и сам по себе активный фактор атеротромбоза.
Воздействие СРБ на клетки эндотелия приводит к снижению активности эндотелиальной NO-синтетазы, уменьшению синтеза простациклина, увеличению продукции ингибитора активатора плазминогена 1 типа, эндотелина-1, интерлейкинов 6 и 8, некоторых молекул клеточной адгезии, провоцирующих миграцию макрофагов в субэндотелиальный слой. Проатерогенное действие СРБ на гладкомышечные клетки проявляется ускорением их пролиферации, усилением экспрессии рецепторов ангиотензина 1 типа и повышением уровня индуцибельной NO-синтетазы. Последняя синтезирует оксид азота, расходуемый в основном на образование весьма агрессивного радикала – пероксинитрита. Макрофаги под воздействием СРБ более активно продуцируют свободные радикалы, цитокины (интерлейкины 1 и 6, фактор некроза опухолей), тканевой фактор и др. [4]. Все это подтверждает непосредственное участие СРБ в процессах атерогенеза. Поэтому снижение его уровня можно рассматривать в качестве одной из основных целей патогенетического лечения атеротромбоза.
К настоящему времени опубликовано несколько работ по сопоставлению действия разных режимов приема статинов на уровень СРБ. В рандомизированном, плацебо-контролируемом исследовании, включавшем 110 больных, сравнивали эффекты терапии аторвастатином (10–80 мг, целевой уровень ЛПНП менее 2,1 ммоль/л) и ловастатином (5–10 мг, целевой уровень ЛПНП менее 3,4 ммоль/л). Достоверное снижение уровня СРБ (с 2,6 до 1,7 мг/л, р = 0,002) было достигнуто только при проведении интенсивной гиполипидемической терапии аторвастатином. Иными словами, между действием статинов на липиды и маркеры воспаления существует параллель.
Розувастатин – наиболее эффективный статин
Розувастатин (Крестор) – полностью синтетический препарат группы статинов, разрешенный для клинического применения в 2003 г. В силу очевидных достоинств востребованность розувастатина оказалась очень высокой. Об этом свидетельствует тот факт, что с момента регистрации он уже назначен более чем 2,5 млн больных, несмотря на наличие на фармацевтическом рынке 5 других статинов.
Фармакокинетические характеристики розувастатина и других применяемых в настоящее время статинов представлены в табл. 2. После однократного приема розувастатина его максимальная концентрация в крови достигается примерно через 5 часов. Препарат имеет самый длительный период полувыведения – 19 часов. Это может быть связано с феноменом кишечно-печеночной рециркуляции, продемонстрированной в эксперименте. Примерно на 88 % розувастатин обратимо связывается с белками плазмы крови, преимущественно с альбумином.
На фармакокинетические характеристики розувастатина не влияют возраст, пол, время приема лекарства или сопутствующий прием пищи, а также наличие умеренно выраженной печеночной недостаточности.
Молекула розувастатина гидрофильна, что делает ее более селективной по отношению к гепатоцитам, чем к другим тканям. Еще одним следствием гидрофильности этого препарата является его существенно меньшее влияние на синтез холестерина в миоцитах скелетных мышц. В исследованиях, проведенных на культуре клеток скелетной мускулатуры, розувастатин и другой гидрофильный статин правастатин снижали активность синтеза холестерина в значительно меньшей степени (в 50–1000 раз), чем липофильные аторвастатин, симвастатин и церивастатин. Этот факт позволяет считать розувастатин потенциально более безопасным по сравнению с другими препаратами из группы статинов.
Показано, что 90 % препарата выделяется с фекальными массами, а 10 % – с мочой. Метаболизируется лишь 10 % розувастатина, его главный метаболит – N-десметилрозувастатин – примерно в 2 раза менее активен, чем основное вещество. В отличие от большинства статинов (в частности, аторвастатина и симвастатина) розувастатин в минимальной степени взаимодействует с ферментами системы цитохрома Р450, в связи с чем вероятность его взаимодействия с множеством широко назначаемых лекарственных препаратов (антигистаминные, противогрибковые, противоязвенные, ряд антибиотиков, антидепрессантов, сердечные гликозиды и т .д.) минимальна. В частности, препарат не оказывает ингибирующего действия на изоферменты 1А2, 2С19, 2D6, 2E1 и 3А4. Только в отношении изофермента 2С9 отмечено снижение его активности на 10 %. При совместном назначении розувастатина с флуконазолом (мощный ингибитор изофермента 2С9) наблюдалось лишь небольшое повышение концентрации статина.
Клиническая эффективность розувастатина активно изучается в целой серии исследований, программа проведения которых получила название GALAXY (45 тыс. участников). В рамках этой программы исследуют действие розувастатина на липиды, маркеры воспаления, динамику атеросклеротического процесса и на так называемые фиксированные (или “твердые”) конечные точки. Программа охватывает большую часть состояний, при которых в настоящее время применяются статины.
Однако наибольший интерес вызывают исследование AURORA, посвященное изучению действия препарата у больных, находящихся на гемодиализе; исследование CORONA, включающее больных сердечной недостаточностью, и исследование JUPITER, посвященное первичной профилактике у больных с нормальным уровнем ЛПНП и повышенным содержанием СРБ. Все эти исследования продолжаются и их результаты позволят решить ряд неизученных вопросов.
Из числа законченных большое значение для оценки эффективности розувастатина имело исследование MERCURY I (Measuring Effective Reductions in Cholesterol Using Rosuvastatin therapy). В это открытое рандомизированное исследование был включен 3161 пациент с гиперлипидемией [5]. Его целью являлось сопоставление эффективности розувастатина, аторвастатина и других статинов с точки зрения снижения концентрации ЛПНП. Главным критерием оценки эффективности было достижение целевого уровня ЛПНП. Исследование продолжалось 16 недель.
Результатом исследования стала демонстрация существенного преимущества розувастатина перед другими статинами по действию на липиды. Целевой уровень ЛПНП на фоне приема розувастатина в дозе 10 мг/сут достигался у 86 % больных в сравнении с 80 % при применении аналогичной дозы аторвастатина (р
В настоящее время розувастатин рекомендовано использовать в дозировках 10–40 мг в сутки. При этом уровень ЛПНП снижается на 52–63 %, т. е. в значительно большей степени, чем при применении других статинов в аналогичных дозах. Кроме того, при лечении розувастатином достоверно повышалась концентрация ЛПВП на 14 % и снижался уровень триглицеридов на 28 %.
Снижение уровня атерогенных фракций холестерина (прежде всего, холестерина ЛПНП) – не единственная цель гиполипидемической терапии. Оно должна быть также направлено на коррекцию содержания ЛПВП – потенциально антиатерогенной фракции липопротеидов, уровень которой у многих пациентов снижен.
На последнем Европейском кардиологическом конгрессе (2004) были представлены результаты крупнейшего популяционного исследования INTER-HEART. В нем было показано, что 9 потенциально модифицируемых факторов на 90 % определяют риск развития инфаркта миокарда, причем наиболее значимым из них является соотношение АпоВ/АпоА1. На втором месте по значимости стоит курение, затем следуют сахарный диабет, артериальная гипертензия, абдоминальный тип ожирения, психосоциальные факторы, количество потребляемых фруктов и овощей, гиподинамия и потребление алкоголя [6].
Тот факт, что наиболее значимым являлось отношение АпоВ – единственного белка, входящего в состав ЛПНП, к АпоА1 – белку ЛПВП, – еще раз подтверждает особую важность поддержания этой фракции липопротеидов на оптимальном уровне. Главный конкурент розувастатина – аторвастатин – весьма незначительно влияет на концентрацию ЛПВП. Более того, с увеличением дозы аторвастатина степень его воздействия на ЛПВП снижается.
Противоположным образом ведет себя розувастатин. В исследовании STELLAR [7] показано, что различия между ним и аторвастатином в действии на ЛПВП проявлялись уже при применении этих препаратов дозе 10 мг, а на фоне приема статинов в дозе 20 мг различие становилось высокодостоверным. При использовании розувастатина в дозе 10 мг уровень АпоВ снижался на 38 %, а концентрация АпоА1 повышалась на 5 %. В результате отношение АпоВ/АпоА1 уменьшалось на 40 %.
Выраженное гипотриглицеридемическое действие розувастатина может считаться доказанным у больных с исходным уровнем триглицеридов в диапазоне от 3,4 до 9 ммоль/л [8]. В рандомизированном, плацебо-контролируемом исследовании, включавшем 156 таких больных, показано, что 6-недельный курс терапии розувастатином приводит к снижению уровня триглицеридов на 37–40 %, а холестерина всех атерогенных фракций – на 42–51 %. Параллельно этому на 6–18 % повышается уровень ЛПВП. Эта особенность действия розувастатина позволяет рассчитывать на то, что его широкое внедрение в клиническую практику существенно уменьшит потребность в комбинированном назначении статинов и фибратов.
Безопасность розувастатина
Проблема безопасности лечения – важнейший аспект применения любого лекарства. Особую важность она приобретает при введении в клиническую практику препарата, предназначенного для очень большого количества больных. Внимание к вопросам безопасного применения статинов резко возросло после отзыва с рынка церивастатина, бесконтрольное применение которого привело к большому числу фатальных осложнений.
Появление нового препарата этого класса – розувастатина – открыло дискуссию о целесообразности регистрации нового лекарства в условиях, когда значительное число статинов уже существует и активно применяется. Именно поэтому розувастатин подвергся весьма тщательному изучению с точки зрения безопасности. Информация в отношении этого препарата анализировалась по вдвое большему числу пациентов, чем требовалось для регистрации других статинов. Одним из следствий этой проверки стала некоторая задержка с выходом лекарства на рынок. С другой стороны, ее результаты позволяют смело утверждать, что при соблюдении дозировок и правил назначения розувастатина его применение, по крайней мере, так же безопасно, как и других статинов.
Тем не менее при использовании розувастатина необходимо предпринимать некоторые меры предосторожности, общие для всех статинов. Так, у некоторых больных на фоне применения высоких доз розувастатина может отмечаться протеинурия, связанная с развитием своеобразной тубулопатии, в 0,2–0,6 % случаев наблюдаемой и при применении других статинов. Поэтому препарат нельзя назначать в дозе 40 мг пациентам с клиренсом креатинина менее 60 мл/мин и в любых дозировках при клиренсе креатинина ниже 30 мл/мин. В любом случае при назначении 40 мг розувастатина необходимо контролировать уровень протеинурии.
Как и другие статины, розувастатин необходимо осторожно использовать у пациентов, злоупотребляющих алкоголем и имеющих заболевания печени. Всем больным необходимо определять уровень печеночных трансаминаз исходно и через 3 месяца терапии. Увеличение их уровня более чем в 3 раза – повод для снижения дозы или отмены препарата.
Фармакокинетические исследования показали, что больные, принадлежащие к монголоидной расе, более чувствительны к действию статинов. Поэтому при назначении розувастатина таким пациентам следует использовать несколько меньшие дозировки и не применять препарат в дозе 40 мг.
Наиболее серьезным, хотя и чрезвычайно редким, побочным эффектом любого статина считается развитие рабдомиолиза. Перед началом применения розувастатина необходимо измерить исходный уровень креатинфосфокиназы. В случае его повышение более чем в 5 раз через 5–7 дней анализ необходимо повторить – если повышение сохраняется, терапию розувастатином не начинают. Обнаружено, что миопатия и рабдомиолиз чаще встречаются у пациентов с повреждениями почек, гипотиреозом; при наличии врожденных мышечных заболеваний у родственников; у больных, имевших признаки поражения мышечной ткани на фоне приема других статинов и фибратов; у лиц, злоупотребляющих алкоголем; в случаях, когда препарат используется в сочетании с фибратами. Таким больным не следует назначать розувастатин в дозе 40 мг. Наличие миопатии является противопоказанием к применению препарата во всех дозировках.
Розувастатин также противопоказан женщинам во время беременности и лактации. Его не следует назначать пациенткам с сохраненной репродуктивной функцией, если они не используют контрацепцию.
В целом профиль безопасности розувастатина не отличается от такового других статинов. На сегодняшний день его безопасность изучена более чем у 15 тыс. пациентов, 1500 больных принимали препарат больше 2 лет. В контролируемых исследованиях розувастатина в настоящее время участвуют более 45 тыс. человек.
Таким образом, целесообразность самого широкого применения статинов в клинической практике не вызывает сегодня никаких сомнений. В нашей стране, как и во всем мире, практически не осталось врачей, незнакомых с терапевтическими возможностями, предоставляемыми препаратами этого класса. К большому сожалению, статины далеко не всегда используются правильно, в адекватных дозировках, что, безусловно, существенно снижает эффективность их применения в качестве средств профилактики тяжелых осложнений атеросклероза. Новый представитель этого класса розувастатин (Крестор), доступный теперь и в России, превосходит все другие статины по способности снижать уровень проатерогенных липопротеидов. Важнейшими его достоинствами являются также благоприятное влияние на антиатерогенные фракции липопротеидов (прежде всего, ЛПВП) и мощное гипотриглицеридемическое действие. Это позволяет снизить потребность в комбинированном назначении статинов и фибратов, что существенно повышает безопасность гиполипидемической терапии. Кроме того, эффективность препарата у большинства пациентов в начальной дозе 10 мг позволяет уменьшить потребность в титровании по сравнению с другими статинами, повысить приверженность к лечению, уменьшить стоимость терапии. Некоторые особенности фармакокинетики и фармакодинамики розувастатина позволяют рассчитывать на лучшую переносимость этого препарата по сравнению с другими статинами.
Особенности Розувастатина
Розувастатин является гиполипидемическим средством и назначается для нормализации уровня триглицеридов и фосфолипидов и липопротеинов в крови. Основным активным действующим веществом является розувастатин. Его назначают для лечения и профилактики гиперхолестеринемии, атеросклероза и его осложнений, тромбоза вен.
Розувастатин снижает высокую концентрацию холестерина низкой плотности, общего холестерина, триглицеридов, аполипротеина. При этом способствует повышению уровня липопротеинов высокой плотности. На фоне приема этого препарата снижается индекс атерогенности. Такой эффект указывает на нормализацию липидного профиля.
Показания для назначения этого препарата следующие:
- наследственная склонность к повышению холестерина;
- первичное выявление высокого уровня холестерина в крови;
- повышенное содержание триглицеридов в крови;
- профилактика осложнений атеросклероза, а именно стенокардии, гипертонической болезни, инфаркта миокарда и инсульта у пациентов старше 50 лет.
Поскольку Розувастатин не метаболизируется в печени, его влияние на этот орган минимально. После 90% препарата выводится через кишечник с калом, остальная часть через почки с мочой. Препарат не назначают лицам младше 18 лет, пациентам с непереносимостью лактозы, женщинам в период беременности и грудного вскармливания.
Он противопоказан пациентам на острой стадии заболеваний печени, больным с миопатией, при индивидуальной непереносимости компонентов препарата. Комбинация Розувастатина с Циклоспорином недопустима. Во время лечения этим статином врачи рекомендуют соблюдать антихолестериновую диету. При назначении препарата в дозировке больше 40 мг лечащий врач учитывает абсолютные и относительные показания к этому.
Розувастатин лучше всех других аналогичных препаратов снижает уровень холестерина
Оба препарата – и Аторвастатин и Розувастатин – имеют хорошие отзывы пациентов. Поскольку данные медикаменты имеют схожее действие, они являются взаимозаменяемыми. Но выбор конкретного из них должен определяться врачом в соответствии с диагнозом и индивидуальными особенностями.
Розувастатин – оптимальный препарат для лечения и профилактики атеросклероза
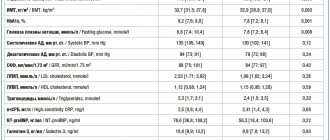
Коррекция нарушений липидного обмена в этой сфере занимает лидирующие позиции [1]. Препаратами первой линии в лечении дислипидемии у пациентов c факторами риска развития ССЗ, связанных с атеросклерозом, безусловно, являются статины (ингибиторы 3–гидрокси–3–метилглутарил–коэнзим А редуктазы – ГМГ–КоА– редуктазы). Главной целью применения статинов у всех больных является замедление прогрессирования атеросклероза, что, в свою очередь, снижает риск развития осложнений и улучшает прогноз. В настоящее время препараты этого класса получают миллионы пациентов с целью вторичной и первичной профилактики [2]. За последние 20 лет статины неоднократно демонстрировали свою эффективность в различных крупных исследованиях. Так, в рандомизированных клинических исследованиях 4S, HPS, ASCOT–LLA, LIPID было показано, что длительное применение этих препаратов уменьшает число повторных осложнений ишемической болезни сердца (ИБС), инфаркта миокарда (ИМ), нестабильной стенокардии и смертельных исходов на 25–40%, ишемических инсультов – на 25–30% [3–6]. При этом происходит снижение уровней общего холестерина (ОХС) и холестерина липопротеидов низкой плотности (ХС ЛНП) на 25–30% и 30–35% соответственно. Тем не менее, несмотря на значительные успехи в терапии ССЗ, риск развития осложнений остается большим. В настоящее время общедоступным является применение шести статинов – ловастатина, правастатина, симвастатина, флувастатина, аторвастатина и розувастатина. Среди перечисленных препаратов особое место занимает розувастатин, что связано с наличием у него неоспоримых преимуществ в отношении фармакологических и клинических свойств по сравнению с другими статинами. Розувастатин представляет собой синтетический статин, который в большей степени взаимодействует с ГМГ– КоА–редуктазой, что связано с более высокой аффинностью к активному центру этого энзима [7]. Также этот препарат имеет наиболее длительный период полувыведения среди всех статинов и является единственным статином, который минимально метаболизируется системой ферментов цитохрома Р450 (СYР 450) без значимого вовлечения изофермента 3А4. В результате клинически значимых лекарственных взаимодействий розувастатина и других препаратов, которые ингибируют энзимы СYР 450, практически не происходит [8]. Это свойство розувастатина облегчает его назначение в составе комплексной терапии, например, с ингибиторами ангиотензин–превращающего фермента, нитратами, антагонистами кальция, диуретиками, β–адреноблокаторами. Что же касается безопасности и переносимости розувастатина, то она сравнима с таковыми и для других статинов – аторвастатина, симвастатина и правастатина – что было показано на более чем 12 тыс. больных [7]. Клинически значимые повышения уровня ферментов печени и креатинкиназы встречались нечасто – не более чем в 0,2% случаев, а миопатия имела место примерно в 0,03% случаев среди пациентов, принимавших розувастатин в дозе до 40 мг. При использовании розувастатина в дозе 5–40 мг не было зарегистрировано ни смертельных случаев, обусловленных приемом препарата, ни рабдомиолиза [9]. Молекула розувастатина гидрофильнее молекул других статинов, высокоселективна к мембранам гепатоцитов и оказывает гораздо более выраженное ингибирующее влияние на синтез ХС ЛНП, чем другие статины. Препарат быстро всасывается из кишечника, независимо от сопутствующего приема пищи и времени суток. Пиковая концентрация розувастатина в плазме достигается через 3–5 ч после приема, период полувыведения составляет 18–20 ч. До 90% принятого препарата выделяются в неизмененном виде через ЖКТ, около 10% выводится с мочой. Кишечно–печеночная рециркуляция обеспечивает сравнительно большую продолжительность полувыведения розувастатина, однако исходное снижение функциональной активности печени не влияет на фармакокинетику препарата. Одной из главных особенностей розувастатина следует считать его высокую гиполипидемическую эффективность уже в начальной суточной дозе (10 мг/сут.), которая возрастает с повышением дозы до максимальной. Установлено, что в дозе 10 мг/сут. розувастатин снижает уровень ХС ЛНП на 42–52% от исходного уровня и на 63% – при назначении максимальной разрешенной дозы (40 мг/сут.). Основная цель приема статинов – это достижение целевого уровня ХС ЛНП: менее 2,5 ммоль/л у пациентов с высоким риском ИБС и менее 1,8 ммоль/л у пациентов с очень высоким риском, и именно розувастатин наиболее эффективен в этом отношении у большинства пациентов по сравнению с другими статинами [10]. Этот вывод был сделан в ряде клинических исследований. Так как розувастатин появился на рынке позже других статинов, то в большинстве клинических исследований использовался аторвастатин как контрольный, более эффективный препарат. В рандомизированном двойном слепом мультицентровом исследовании сравнивали эффективность в снижении уровня ХС ЛНП аторвастатина и розувастатина у пациентов с гиперхолестеринемией и высоким риском ИБС. Оказалось, что на 12–й неделе терапии розувастатин в дозе 10 мг достоверно в большей степени снижал уровень ХС ЛНП, чем аторвастатин в дозе 10 мг (47% и 35% соответственно) [11]. В другом исследовании, в котором приняли участие более 3 тыс. пациентов с ИБС, атеросклерозом и сахарным диабетом 2–го типа, оценивали эффективность перевода на низкие дозы розувастатина с терапии аторвастатином, симвастатином и правастатином. Эффективность терапии оценивали по количеству пациентов, достигших уровня ХС ЛНП <3 ммоль/л на 16–й неделе. Было показано, что перевод на розувастатин в дозе 10 мг позволил пациентам значительно быстрее достичь целевого уровня ХС ЛНП по сравнению с теми пациентами, которые продолжили лечение аторвастатином в дозе 10 мг (86% vs. 80%), симвастатином в дозе 20 мг (86% vs. 72%) и правастатином в дозе 40 мг (88% vs. 66%) [12]. В рандомизированном открытом мультицентровом исследовании SOLAR, которое проводилось в 145 центрах США, мужчинам и женщинам с высоким риском развития ИБС назначали стартовые дозы розувастатина (10 мг), аторвастатина (10 мг) или симвастатина (20 мг) в течение 6 нед. Тем пациентам, которые не достигали уровня ХС ЛНП <100 мг/дл к 6–й нед., дозу удваивали и наблюдали в течение последующих 6 нед. В целом, 1632 пациента были рандомизированы на три группы лечения. Спустя 12 нед. 76% пациентов, принимавших розувастатин, достигли целевого уровня ХС ЛНП по сравнению с 58% и 53% пациентов, получавших аторвастатин и симвастатин. Побочные эффекты встречались с одинаковой частотой во всех группах, и только 3% всех пациентов прекратили лечение из–за побочных явлений [13]. Что же касается влияния терапии розувастатином на уровень холестерина липопротеидов высокой плотности (ХС ЛВП), который является независимым маркером кардиоваскулярного риска, то был доказан благоприятный эффект этого препарата. Так, в рандомизированном открытом сравнительном исследовании у пациентов с метаболическим синдромом оценивали влияние терапии розувастатином и аторвастатином на уровень липидов плазмы у лиц с гиперхолестеринемией. В результате при лечении розувастатином отмечалось повышение уровня ХС ЛВП на 8–11% [14]. Эффективность применения розувастатина изучали также и у пациентов с тяжелой гетерозиготной семейной гиперхолестеринемией. В исследовании сравнивали эффективность розувастатина и аторвастатина в снижении уровня ХС ЛНП: 623 пациента были рандомизированы на 2 группы для лечения в дозе 20 мг аторвастатином (187 человек) или розувастатином (436 человек) и форсированным титрованием дозы с 6–недельными интервалами до 80 мг/сут. На 18–й нед. терапии розувастатином отмечались более значительное снижение уровня ХС ЛНП (–57,9% vs. –50,4%) и повышение уровня ХС ЛВП (12,4% vs. 2,9%), чем при терапии аторвастатином [15]. Также применение розувастатина оказалось эффективным и в плане первичной профилактики сердечно–сосудистых осложнений. Так, в рандомизированном двойном слепом плацебо–контролируемом исследовании JUРITER по изучению первичной профилактики у лиц с нормальным и низким уровнем ХС ЛНП и повышенным сердечно–сосудистым риском вследствие увеличения концентрации высокочувствительного С–реактивного белка (вч–СРБ) были получены благоприятные результаты [16]. Предпосылкой для проведения этого исследования явились данные о том, что около половины всех сердечно–сосудистых осложнений развиваются у практически здоровых лиц с нормальным или сниженным уровнем ХС ЛНП. У этих лиц необходимо установить новые прогностические маркеры для изучения риска развития ССЗ. Ранее было установлено, что вч–СРБ – это маркер сердечно–сосудистой патологии у лиц с нормальным или низким уровнем ХС ЛНП. Показатель признан маркером воспаления и ассоциируется с повышенным риском развития атеросклероза. Поэтому помимо улучшения выявляемости лиц из группы риска была поставлена цель изучить возможности липидоснижающей терапии в качестве одного из методов первичной профилактики сердечно–сосудистых осложнений. В исследование включили 17 802 пациента из 26 стран мира с ХС ЛНП <3,36 ммоль/л и уровнем вч–СРБ >2 мг/дл, которые были рандомизированы на 2 группы: в 1–й группе пациенты принимали розувастатин в дозе 20 мг/сут., во 2–й – плацебо. Большинство пациентов имели избыточный вес или страдали ожирением. В марте 2008 г. было принято решение о досрочном прекращении клинического исследования JUРITER ввиду того, что имелись явные доказательства уменьшения ССЗ и смертности среди пациентов, принимавших розувастатин, по сравнению с теми, кто принимал плацебо (средняя продолжительность составила приблизительно 2 года). Окончательные данные исследования JUРITER [17] говорят о том, что в группе розувастатина было отмечено достоверное снижение риска развития первичной конечной точки (ИМ, инсульт, реваскуляризация, госпитализация с нестабильной стенокардией, смерть от сердечно–сосудистых причин) на 44%; ИМ – на 54%; инсульта – на 48%; смерти от сердечно–сосудистых причин – на 47% и смерти от всех причин – на 20%. Таким образом, это исследование об эффективности первичной профилактики у лиц без гиперлипидемии, но с повышенным уровнем вч–СРБ продемонстрировало значительную эффективность розувастатина в снижении частоты больших кардиоваскулярных событий. В рандомизированном двойном слепом плацебо–контролируемом исследовании METEOR определяли, вызывает ли лечение розувастатином замедление прогрессирования и/или регресс атеросклероза (на основании показателя толщины комплекса интима–медиа (ТКИМ)) у лиц с низким риском и субклиническим атеросклерозом. В исследование было включено 984 пациента (мужчины и женщины в возрасте 45–70 лет) без ИБС, с умеренной гиперхолестеринемией (среднее значение ХС ЛПНП 154 мг/дл), имевшие исходные показатели ТКИМ в пределах 1,2–3,5 мм, у которых фактором риска был возраст или 10–летний фатальный риск менее 10% по Фрамингемской шкале. Пациенты получали розувастатин в дозе 40 мг или плацебо в течение 2 лет. В результате было показано, что в группе розувастатина средний уровень ХС ЛНП снизился на 49%. Изменения максимальной ТКИМ составили –0,0014 мм/год в группе розувастатина и +0,0131 мм/год в группе плацебо. В целом, у людей среднего возраста с риском <10% и субклиническим атеросклерозом терапия розувастатином по сравнению с плацебо в течение 2 лет значительно уменьшила степень прогрессирования атеросклероза [18]. Для изучения влияния розувастатина на каротидный атеросклероз, морфологию и состав атеросклеротической бляшки в рандомизированном двойном слепом исследовании ORION применяли неинвазивную визуализацию с помощью магнитно–резонансной томографии (МРТ). 43 пациента были разделены на 2 группы: первая принимала розувастатин в низкой дозе 5 мг, вторая – в высокой дозе 40/80 мг. МРТ выполняли в начале и через 24 мес. терапии. Через 2 года наблюдения было показано, что у пациентов с умеренной гиперхолестеринемией терапия розувастатином привела к относительному уменьшению богатого липидами некротического ядра бляшки без существенного изменения их количества [19]. Таким образом, можно предположить, что длительное лечение розувастатином приводит к стабилизации атеросклеротических бляшек. Также розувастатин продемонстрировал свое положительное влияние и в случае с коронарным атеросклерозом, что было выявлено в проспективном открытом исследовании АSTEROID. После 24 мес. терапии 349 пациентам было выполнено внутрисосудистое ультразвуковое исследование (ВСУЗИ). На фоне интенсивной терапии розувастатином в дозе 40 мг/сут. удалось достичь не только снижения уровня липидов крови – уровня ЛПНП на 60,8 мг/дл и повышения ЛПВП на 14,7%, но и вызвать существенный регресс атеросклеротических поражений коронарных артерий, что оценивалось по всем изучаемым показателям ВСУЗИ [20]. В этом же исследовании использовали коронароангиографию и определяли в процентах степень сужения и минимальный просвет коронарных артерий и их основных ветвей на разных уровнях, причем исходно стеноз составлял >25%. Для каждого пациента рассчитывали средние показатели пораженных участков в начале и в конце исследования. В целом, у 292 пациентов выявлено 613 стенозов. Терапия розувастатином вызвала регресс атеросклероза в виде уменьшения относительного диаметра стеноза и увеличения диаметра просвета сосуда по данным коронарографии у пациентов с ИБС [21]. Также эффективность применения розувастатина была изучена в большой клинической программе GALAXY, которая включила в себя 18 многоцентровых рандомизированных контролируемых исследований. В этой программе исследовалась связь между оптимальным контролем липидов, атеросклерозом и сердечно–сосудистой заболеваемостью и смертностью. Исследования можно разделить на три большие категории: 1) изучение влияния розувастатина на липиды и маркеры воспаления; 2) изучение влияния розувастатина на атеросклеротическое поражение коронарных и сонных артерий; 3) изучение влияния розувастатина на риск развития сердечно–сосудистых осложнений, сердечно–сосудистую и общую смертность. В результате были показаны преимущества розувастатина как в нормализации показателей липидного обмена, маркеров воспаления, так и в обратном развитии атеросклероза в коронарных и сонных артериях [2]. Таким образом, в сочетании с данными исследования JUPITER розувастатин в настоящее время является наиболее перспективным препаратом в профилактике развития и прогрессирования атеросклероза. Более чем 20–летний опыт применения статинов показал, что преобладающим большинством пациентов эти препараты хорошо переносятся. Проведено большое количество многоцентровых клинических исследований, в которых участвовало в общей сложности более 100 тыс. пациентов, длительность наблюдения достигала 5 лет и более. Не было указаний на развитие тяжелых побочных эффектов, непосредственно связанных с приемом этих препаратов. Не подтвердились опасения о возможности влияния статинов на центральную нервную систему, сон, об отрицательном влиянии на умственную деятельность человека. Более того, результаты исследований последних лет показали, что статины при длительном приеме способствуют предотвращению развития деменции и синдрома Альцгеймера. Среди всех статинов наиболее перспективным представляется применение розувастатина. В России зарегистрирован и с успехом применяется дженерик розувастатина Мертенил («Гедеон Рихтер», Венгрия). Появление Мертенила дает основание предполагать, что это эффективное средство станет доступным широкому кругу пациентов, ведь применение оригинального препарата не всегда возможно с экономической точки зрения. Мертенил по фармакологическим свойствам, лекарственной форме, силе действия, способу назначения и качеству нисколько не уступает оригинальному препарату. Также Мертенил является единственным розувастатином в России с полным спектром дозировок (5, 10, 20 и 40 мг), что очень удобно для подбора дозы и применения в различных клинических ситуациях. Удобная упаковка, рассчитанная на 1 месяц приема (30 табл.), повышает приверженность пациента к лечению. Немаловажную роль играет доступность цены для долгосрочного применения препарата. Таким образом, Мертенил можно рекомендовать пациентам для первичной и вторичной профилактики ССЗ, в том числе и лицам без клинических признаков ИБС. Литература 1. Диагностика и коррекция нарушений липидного обмена с целью профилактики и лечения атеросклероза. Российские рекомендации. // Кардиоваскулярная терапия и профилактика. – 2007. – № 6 (приложение 3). 2. Карпов Ю.А. Липидоснижающая терапия как важный компонент в лечении и профилактике сердечно–сосудистых заболеваний. // РМЖ – 2011. – Т. 19, № 7. – С. 450–456. 3. Scandinavian Simvastatin Survival Study Group: Randomised trial of cholesterol lowering in 4444 patients with coronary heart disease: The Scandinavian Simvastatin Survival Study. // Lancet 1994: 344: 1383–1389. 4. Heart Protection Study Collaborative Group. MRC/BHF Heart Protection Study of cholesterol lowering with simvastatin in 20536 high–risk individuals: a randomized placebo–controlled trial. // Lancet 2002; 360: 7–22. 5. Sever P.S., Dahlof B., Poulter N.R. et al. for the ASCOT investigators. Prevention of coronary and stroke events with atorvastatin in hypertensive patients who have average or lower–than–average cholesterol concentrations, in the Anglo–Scandinavian Cardiac Outcomes Trial – Lipid Lowering Arm (ASCOT–LLA): a multicentre randomized controlled trial. // Lancet 2003; 361: 1149–1158. 6. The Long–term Intervention with Pravastatin in Ischemic Disease (LIPID) Study Group. Prevention of cardiovascular events and death with pravastatin in patients with coronary heart disease and a broad range of initial cholesterol levels. // N Engl J Med. 1998;339:1349–1357. 7. P. Rubba, G. Marotta, M. Gentile. Efficacy and safety of rosuvastatin in the management of dyslipidemia. // Vasc Health Risk Manag. 2009; 5: 343–352. 8. McKenney J.M. Efficacy and safety of rosuvastatin in treatment of dyslipidemia. // Am J Health Syst Pharm. 2005;62:1033–1047. 9. Shepherd J., Hunninghake D.B., Stein E.A. et al. Safety of rosuvastatin. // Am J Cardiol. 2004;94:882–888. 10. LaRosa J.C. Low–density lipoprotein cholesterol reduction: the end is more important than the means. // Am J Cardiol. 2007;100:240–242. 11. Schwartz G.G., Bolognese M.A., Tremblay B.P. et al. Efficacy and safety of rosuvastatin and atorvastatin in patients with hypercholesterolemia and a high risk of coronary heart disease: a randomized, controlled trial. // Am Heart J. 2004;148–154. 12. Schuster H., Barter P.J., Stender S. et al. Effective Reductions in Cholesterol Using Rosuvastatin Therapy I study group Effects of switching statins on achievement of lipid goals: Measuring Effective Reductions in Cholesterol Using Rosuvastatin Therapy (MERCURY I) study. // Am Heart J. 2004;147:705–713. 13. Insull W., Jr, Ghali J.K., Hassman D.R. et al. SOLAR Study Group Achieving low–density lipoprotein cholesterol goals in high–risk patients in managed care: comparison of rosuvastatin, atorvastatin, and simvastatin in the SOLAR trial. Mayo Clin Proc. 2007;82:543–550. 14. Deedwania P.C., Hunninghake D.B., Bays H.E., Jones P.H., Cain V.A., Blasetto J.W., STELLAR Study Group Effects of rosuvastatin, atorvastatin, simvastatin, and pravastatin on atherogenic dyslipidemia in patients with characteristics of the metabolic syndrome. // Am J Cardiol. 2005;95:360–366. 15. Stein E.A., Strutt K., Southworth H., Diggle P.J., Miller E. HeFH Study Group Comparison of rosuvastatin versus atorvastatin in patients with heterozygous familial hypercholesterolemia. // Am J Cardiol. 2003;92:1287–1293. 16. Ridker P.M., Fonseca F.A., Genest J. et al. JUPITER Trial Study Group Baseline characteristics of participants in the JUPITER trial, a randomized placebo–controlled primary prevention trial of statin therapy among individuals with low low–density lipoprotein cholesterol and elevated high–sensitivity C–reactive protein. // Am J Cardiol. 2007;100:1659–1664. 17. Ridker P.M., Danielson E., Fonseca F.A. et al. the JUPITER Study Group Rosuvastatin to prevent vascular events in men and women with elevated C–reactive protein. // N Engl J Med. 2008;359(2):2195–2207. 18. Crouse J.R., Raichlen J.S., Riley W.A. et al. METEOR Study Group Effect of rosuvastatin on progression of carotid intima–media thickness in low–risk individuals with subclinical atherosclerosis: the METEOR Trial. // JAMA. 2007;297:1344–1353. 19. Underhill H.R., Yuan C., Zhao X.Q. et al. Effect of rosuvastatin therapy on carotid plaque morphology and composition in moderately hypercholesterolemic patients: a high–resolution magnetic resonance imaging trial. // Am Heart J. 2008;155:584.e1–e8. 20. Nissen S.E., Nicholls S.J., Sipahi I. et al. ASTEROID Investigators. // JAMA. 2006;295:1556–1565. 21. Ballantyne C.M., Raichlen J.S., Nicholls S.J. et al. ASTEROID Investigators Effect of rosuvastatin therapy on coronary artery stenoses assessed by quantitative coronary angiography: a study to evaluate the effect of rosuvastatin on intravascular ultrasound–derived coronary atheroma burden. // Circulation. 2008;117:2458–2466.
Отзывы
Оксана, 46 лет, г. Пятигорск: Для снижения холестерина принимала Аторвастатин. Снижает хорошо, но на себе почувствовала проявление побочных эффектов. За 3 месяца регулярного приема почти все показатели липидограммы, кроме триглицеридов, приблизились к норме. По результатам анализа врач дополнил лечение Дибикором, и триглицериды тоже снизились. Боялась за печень, но напрасно. Там все нормально.
Екатерина, 35 лет, г. Москва: Не могу сказать, что Аторвастатин значительно отличается по эффективности от предыдущих препаратов. Назначали отцу по 60 мг в сутки, у него высокий холестерин. Он говорит, что не замечает особых изменений состояния после курса лечения. Каким был холестерин, таким и остался. Видимо, это из-за наследственной предрасположенности.
Кирилл, 60 лет, г. Самара: При диагнозе «ишемическая болезнь сердца» врач назначил статины для профилактики осложнений. Выбор пал на препарат Розувастатин. Не ощущаю его влияния на себе, но по анализам холестерин соответствует норме для здорового человека. Перед началом приема Розувастатина он был повышен в несколько раз. Могу с уверенностью рекомендовать этот препарат для снижения высокого уровня холестерина другим.