Предпосылки к проведению исследования
Дапаглифлозин представляет собой селективный ингибитор натрий-глюкозного котранспортера (НГК) 2-го типа, который блокирует реабсорбцию глюкозы в проксимальных канальцах почек и способствует глюкозурии [1—3]. Ранее были получены данные о благоприятном влиянии применения ингибиторов НГК 2-го типа на риск развития осложнений сердечно-сосудистых заболеваний (ССЗ), включая снижение риска госпитализаций по поводу сердечной недостаточности (СН), преимущественно у больных с сахарным диабетом (СД) 2-го типа и установленным диагнозом ССЗ [4—6]. Кроме того, в ходе выполнения таких исследований были получены данные о замедлении прогрессирования хронической болезни почек (ХБП) за счет применения ингибиторов НГК 2-го типа [4, 5, 7—9].
Актуальность
У пациентов с хронической болезнью почек отмечается высокий риск развития неблагоприятных событий со стороны почек, сосудов и сердца.
До настоящего времени эффект дапаглифлозина у пациентов с хронической болезнью почек с или без сахарного диабета не был известен.
Больные
В исследование включали больных с СД 2-го типа в возрасте 40 лет, характеристики которых соответствовали следующим критериям:
— уровень гликированного гемоглобина (HbA1c) 6,5% и более, но менее 12%;
— клиренс креатинина 60 мл/мин и более;
— несколько факторов риска (ФР) развития ССЗОА или установленный диагноз ССЗОА, сосудисто-мозговое заболевание (клинически явная ишемическая болезнь сердца, сосудисто-мозговое заболевание ишемической природы или заболевание периферических артерий);
— при наличии только ФР развития ССЗОА возраст мужчин и женщин должен был быть не моложе 55 и 60 лет соответственно, если у них было не менее 1 известного ФР, включая артериальную гипертонию, дислипидемию (холестерин липопротеинов низкой плотности более 3,36 ммоль/л или применение гиполипидемической терапии) и использование табака.
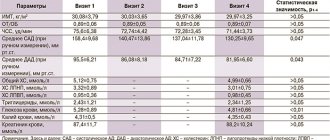
Подробно исходные характеристики участников исследования представлены в таблице.
Таблица. Исходные характеристики участников исследование Примечание. Данные представлены как среднее ± стандартное отклонение или * — медиана (минимальное значение — максимальное значение), если не указано другое. СД — сахарный диабет; АД — артериальная гипертония; СКФ — скорость клубочковой фильтрации; ППТ — площадь поверхности тела; ССЗОА — сердечно-сосудистое заболевание, обусловленное атеросклерозом; КБС — коронарная болезнь сердца; ЗПА — заболевание периферических артерий; СМЗ — сосудисто-мозговые заболевания; ДПП-4 — ингибиторы дипептидилпептидазы 4-го типа; ГПП-1 — глюкагоноподобный пептид 1-го типа; ССЗ — сердечно-сосудистое заболевание; АПФ — ангиотензинпревращающий фермент; БРА — блокаторы рецепторов ангиотензина II.
Материал и методы
Проведено одноцентровое проспективное исследование, одобренное этическим комитетом ФГБУ «НМИЦ им. В.А. Алмазова» Минздрава России. До вступления в исследование все пациенты подписывали информированное согласие. Включали пациентов с СД2 длительностью более 1 года, уровнем гликированного гемоглобина от 7% до 10%, без верифицированной атеросклеротической болезни сердца и сосудов, но с множественными факторами риска сердечно-сосудистых событий (дислипидемией, ожирением, артериальной гипертензией). Кроме того, критериями включения были возраст от 40 до 65 лет, стабильная сахароснижающая, гиполипидемическая и антигипертензивная терапия как минимум в течение 12 нед. до включения в исследование. В исследование не включали пациентов с фибрилляцией предсердий, клапанными пороками сердца, ревматологическими заболеваниями, обострением хронических заболеваний, сахарным диабетом 1 типа, симптомами гипотензии и уровнем систолического артериального давления (САД) ниже 95 мм рт. ст., уровнем N-концевого пропептида натрийуретического гормона (NT-proBNP) >125 нг/мл, скоростью клубочковой фильтрации (СКФ) <60 мл/мин/1,73 м2 и хронической болезнью почек, заболеваниями печени а также получающих инсулинотерапию, терапию глюкокортикостероидами, антагонистами минералокортикоидных рецепторов. Пациенты получали дапаглифлозин в дозе 10 мг/сут в течение 6 мес. в дополнение к базовой терапии СД2.
В ходе исследования проводили забор образцов крови до начала лечения дапаглифлозином и через 6 мес. лечения. Образцы крови забирали натощак (после 8 ч голодания), оценивали следующие показатели: гликированный гемоглобин (HbA1c), аланинаминотрансферазу, аспартатаминотрансферазу, креатинин, липидограмму (общий холестерин, липопротеины низкой плотности (ЛПНП), липопротеины высокой плотности (ЛПВП), триглицериды), NT-proBNP, вчСРБ, галектин-3, тканевой ингибитор матриксных металлопротеиназ-1 (TIMP-1), матриксную металлопротеиназу-9 (MMP-9), стимулирующий фактор роста, экспрессируемый геном 2 (ST2), карбокситерминальный фрагмент проколлагена I типа (PIСP). Уровень вчСРБ определяли на анализаторе Cobas Integra 400+ иммунотурбидиметрическим методом. Концентрацию NT-proBNP определяли электрохемилюминесцентным методом c применением тест-системы Elecsys (Roche Diagnostic). Оценку сывороточных уровней галектина-3 (R&D system), ММР-9 и TIMP-1 (R&D system), sST2 (Clinical diagnostics, Presage ST2 kit), PICP (USCN Life Science) проводили методом иммуноферментного анализа. Кроме того, в начале и в конце исследования оценивали массу тела, рост, окружность талии, уровень артериального давления (АД). С целью оценки нормальных значений биомаркеров фиброза в исследование дополнительно были включены 15 пациентов сходного возраста без СД2 и других хронических заболеваний, в том числе сердечно-сосудистых и заболеваний почек (группа контроля).
Для статистического анализа использовали программу SPSS Statistics. Количественные данные представлены в виде медианы и 25-го и 75-го квартилей — Me [Q25; Q75], качественные признаки — в виде абсолютного и относительного (%) показателей. Различия между количественными показателями выявляли с помощью критерия Вилкоксона. Корреляционный анализ проводили с использованием рангового коэффициента корреляции Спирмена. Нулевая гипотеза отвергалась при р<0,05.
Вмешательство
Во время вводного периода все участники принимали плацебо с использованием простого слепого метода и у них выполняли анализы крови и мочи. После завершения такого периода участников, характеристики которых продолжали соответствовать критериям включения и исключения, в соотношении 1:1 рандомизированно с использованием двойного слепого метода распределяли в группу приема дапаглифлозина по 10 мг 1 раз в сутки и группу плацебо. Другие гипогликемические препараты (кроме применяемых без использования слепого метода ингибировов НГК 2-го типа, пиоглитазона или розиглитазона) применяли по усмотрению лечащего врача. Участники должны были посещать исследовательский центр каждые 6 мес до завершения исследования и получения результатов лабораторной и клинической оценки безопасности и степени соблюдения предписанного режима терапии. Кроме того, в период между посещениями исследовательского центра с участниками каждые 3 мес связывались по телефону.
Критерии оценки/Клинические исходы
Основной комбинированный показатель безопасности: частота развития тяжелых осложнений сердечно-сосудистых заболеваний — ТОССЗ (смерть от осложнений ССЗ, инфаркт миокарда — ИМ или ишемический инсульт).
Основные комбинированные показатели эффективности:
— частота развития ТОССЗ (смерть от осложнений ССЗ, ИМ или ишемический инсульт);
— смертность от осложнений ССЗ и частота госпитализаций по поводу СН.
Дополнительные показатели эффективности:
— комбинированный показатель частоты развития ХБП (снижение на 40% и более расчетной скорости клубочковой фильтрации до менее 60 мл/мин на 1,73 м2, впервые развившаяся терминальная стадия почечной недостаточности или смерть от ХБП или ССЗ);
— общая смертность.
Методы статистического анализа
Безопасность оценивали с помощью анализа, выполняемого для проверки гипотезы о том, что прием дапаглифлозина не менее безопасен, чем прием плацебо, по влиянию на риск развития ТОССЗ. В соответствии с рекомендациями Администрации США по контролю за качеством пищевых продуктов и лекарственных препаратов результаты такого анализа должны свидетельствовать о том, что верхняя граница 95% ДИ отношения риска развития ТОССЗ для двустороннего критерия составляет 1,3 при одностороннем уровне α=0,023 (после учета результатов 2 промежуточных анализов). В случае подтверждения гипотезы о не меньшей безопасности применения дапаглифлозина по сравнению с плацебо предполагали оценивать 2 показателя эффективности: частоту развития ТОССЗ и комбинированный показатель частоты развития таких исходов, как смерть от осложнений ССЗ и госпитализация по поводу С.Н. Оценка этих показателей должна была быть параллельной при двустороннем уровне α=0,023 для каждого из них. В случае статистически значимого снижения любого из этих показателей уровень α мог быть изменен для проверки других показателей эффективности при уровне α=0,046 для двустороннего критерия. В случае статистически значимой эффективности по обоим показателям с использованием иерархического подхода анализировали дополнительные показатели при уровне α=0,046 для обоих показателей.
В соответствии с оригинальным протоколом исследования для развития не менее 1390 неблагоприятных клинических исходов в исследование требовалось включить примерно 17 150 участников при продолжительности наблюдения не менее 3 лет. Такое число участников обеспечивало 85% статистическую мощность исследования для выявления снижения на 15% частоты развития ТОССЗ в группе дапаглифлозина по сравнению с группой плацебо при уровне α=0,046 для двустороннего критерия, а также статистическую мощность более 99% для подтверждения гипотезы о не менее высокой безопасности применения дапаглифлозина по сравнению с плацебо, которую оценивали по влиянию на риск развития ТОССЗ.
В анализ основных показателей безопасности и эффективности включали данные о 17 160 участников, которые были рандомизированы. Из анализа были исключены данные 30 участников, включенных в исследование в одном центре. Причиной исключения этих данных были существенные нарушения принципов Качественной клинической практики в указанном центре в ходе выполнения другого исследования, что было основанием для сомнений в достоверности полученных данных.
Все виды анализа выполняли исходя из допущения, что у всех участников исследования применялось назначенное лечение, с использованием данных о подтвержденных клинических исходах. Для основных показателей предоставляли отношения рисков и 95% ДИ с указанием значений p, которые были получены в ходе выполнения анализа продолжительности периода до развития неблагоприятных клинических исходов. Такой анализ проводили с помощью модели пропорциональных рисков Кокса, в который включали данные обо всех участниках. Все виды анализа выполняли с использованием стратификации в зависимости от наличия или отсутствия при включении в исследование ССЗОА (установленный диагноз ССЗОА или несколько факторов риска развития ССЗОА) и гематурии. После выполнения анализа безопасности (частота развития ТОССЗ) оценивали другие показатели безопасности, в которые были включены данные об участниках, у которых оценивали безопасность (все участники, которые приняли хотя бы одну дозу дапаглифлозина или плацебо). Для показателей безопасности указывали значение p, рассчитанное без учета множественных сравнений.
Обсуждение
Преобладание синтеза коллагена I типа над его деградацией приводит к накоплению в миокарде избытка волокон коллагена и указывает на процесс фиброза, который происходит в интерстициальном и периваскулярном пространстве, в том числе при диабетической кардиомиопатии [9]. Уровни PICP, который является маркером образования и деградации коллагена I типа, надежно коррелируют с объемом образующегося коллагена как у пациентов с хронической сердечной недостаточностью (ХСН), так и без таковой [9].
В исследованиях показано, что концентрации PICP выше у пациентов с СД2, чем у пациентов без СД2 [10]. Сходные различия были продемонстрированы и в нашем исследовании. Терапия дапаглифлозином в течение 6 мес. приводила к значимому снижению уровня P1CP по сравнению с исходным. Сходная динамика была получена в исследовании другого ИНГТ2 у пациентов с СД2 и очень высоким риском сердечно-сосудистых событий [11].
В нашем исследовании не установлено значимого снижения концентраций NT-proBNP на фоне лечения дапаглифлозином в течение 6 мес., что можно объяснить включенной в исследование популяцией пациентов без ХСН и без высоких концентраций NT-proBNP. Поскольку NT-proBNP является маркером ХСН и его уровень коррелирует с ее тяжестью, даже в исследованиях пациентов с СД2 и ХСН с сохранной фракцией выброса не было выявлено значимого снижения концентрации NT-proBNP [12]. Тем не менее исследование DAPA-HF продемонстрировало, что риск ухудшения течения ХСН или смерти от сердечно-сосудистых заболеваний был ниже в группе дапаглифлозина, чем в группе плацебо [13]. Таким образом, несмотря на ограниченное влияние на уровень NT-proBNP, ИНГТ2 улучшают клинические исходы у пациентов с ХСН, что говорит о несоответствии между краткосрочными изменениями уровней NT-proBNP и клиническими исходами.
Концентрации ST2, вчСРБ, MMP-9 и ее ингибитора TIMP-1 значимо не изменились на фоне терапии дапаглифлозином, что согласуется с данными других исследований [11, 14, 15]. Вероятно, отсутствие значимой динамики показателей ряда маркеров в ходе нашего исследования связано с тем, что пациенты без ХСН и сердечно-сосудистых событий находятся на том этапе сердечно-сосудистого континуума, когда концентрации маркеров не могут в полной мере отражать тяжесть и прогноз у данных пациентов, а их изменения не могут быть зафиксированы за 6-месячный период наблюдения. Кроме того, отсутствие отрицательной динамики содержания данных биомаркеров может говорить о замедлении воспалительных и фиброзных процессов, имеющих место при СД2, и потенциально реализовываться в улучшении сердечно-сосудистых исходов. Также стоит принимать во внимание наличие ожирения и других неучтенных факторов, которые могут влиять на значения оцениваемых нами маркеров.
Основные результаты
В целом 25698 участников были включены во вводную фазу исследования с применением плацебо. После завершения такого периода выполнялась рандомизация, и 17 160 участников были включены в основную часть исследования с использованием двойного слепого метода (у 10 186 участников при включении не было диагностированных ССЗОА). В группу дапаглифлозина и группу плацебо были включены 8582 и 8578 участников соответственно.
Данные, полученные в ходе выполнения анализа основного показателя безопасности, свидетельствовали о том, что применение дапаглифлозина удовлетворяет заранее принятым требованиям к результатам анализа для проверки гипотезы о не менее высокой безопасности приема дапаглифлозина по сравнению с плацебо, которую оценивали по риску развития ТОССЗ (верхняя граница 95% ДИ отношения риска должна была быть менее 1,3 при p<0,001 для анализа, выполненного в целях проверки гипотезы о не менее высокой безопасности приема дапаглифлозина по сравнению с плацебо).
Результаты анализа двух основных показателей эффективности свидетельствовали о том, что прием дапаглифлозина по сравнению с плацебо не приводил к снижению частоты развития ТОССЗ (такие осложнения в группе дапаглифлозина и группе плацебо развились у 8,8 и 9,4% участников соответственно; отношение риска 0,93 при 95% ДИ от 0,84 до 1,03; p=0,17), но обусловливал снижение комбинированного показателя смертности от осложнений ССЗ и частоты госпитализаций по поводу СН (такие исходы в группе дапаглифлозина и группе плацебо развились у 4,9 и 5,8% участников соответственно; отношение риска 0,83 при 95% ДИ от 0,73 до 0,95; p=0,005), что отражало менее высокую частоту госпитализаций по поводу СН (отношение риска 0,73 при 95% ДИ от 0,61 до 0,88) в отсутствие статистически значимых различий между группами по смертности от осложнений ССЗ (отношение риска 0,98 при 95% ДИ от 0,82 до 1,17). Почечная недостаточность в группе дапаглифлозина и группе плацебо развивалась у 4,3 и 5,6% участников соответственно (отношение риска 0,76 при 95% ДИ от 0,67 до 0,87), а общая смертность достигала 6,2 и 6,6% соответственно (отношение риска 0,93 при 95% ДИ от 0,82 до 1,04). Частота развития диабетического кетоацидоза была выше в группе дапаглифлозина по сравнению с группой плацебо и составляла 0,3 и 0,1% соответственно (p=0,02), как и частота развития инфекции половых органов, которая приводила к прекращению применения исследуемого препарата или считалась тяжелым нежелательным явлением, — 0,9 и 0,1% соответственно (p<0,001).
Результаты исследования
В исследование включено 27 пациентов (возраст 56 [49; 61] лет), у большинства из которых были СД2 длительностью более 4 лет (7 [4; 12] лет) и ожирение I степени. Базовая сахароснижающая терапия включала комбинацию метформина с препаратами сульфонилмочевины или ингибиторами дипептидилпептидазы 4 типа (иДПП-4).
Основная характеристика пациентов и динамика изучаемых маркеров фиброза и воспаления представлена в таблице 1. За 6 мес. лечения дапаглифлозином наблюдалось значимое снижение уровня HbA1c с 8,2 [7,6; 8,8]% до 7,8 [7,2; 8,1]% (р=0,001), снижение ИМТ и уменьшение окружности талии. За время наблюдения не отмечено значимых изменений содержания липопротеинов и триглицеридов, СКФ и АД.
Содержание вчСРБ и NT-proBNP не отличалось от нормальных значений и не претерпело статистически значимых изменений по прошествии 6 мес. лечения дапаглифлозином. Исходно пациенты имели значимо бóльшие концентрации галектина-3, PICP и MMP-9 по сравнению с группой контроля (p=0,017, p=0,006 и p=0,008 соответственно). При оценке динамики содержания галектина-3, MMP-9, TIMP-1, ST2 не было получено значимых различий с исходными значениями (см. табл. 1). В то же время через 6 мес. лечения дапаглифлозином наблюдалось статистически значимое снижение концентрации PICP с 136,8 [100,4; 200,6] нг/мл до 104,8 [79,7; 162,0] нг/мл (р=0,019) и повышение концентрации TIMP-1 с 188 [138; 270] нг/мл до 234 [205; 315] нг/мл (р=0,011).