До XX века в терапии сахарного диабета 2-го типа (СД2) использовали производные сульфонилмочевины (псм) и бигуаниды (метформин); их механизм действия долго оставался неясным [1]. Открытие в 80–90-е годы особенностей деградации инкретинов и их влияния на секрецию инсулина у человека способствовало поиску препаратов, влияющих на это звено регуляции углеводного обмена. В 1998 г. был открыт первый ингибитор дипептидилпептидазы-4 (идпп-4) — вилдаглиптин, названный в честь Эдвина Б. Виллхауэра [2, 3], обнаружившего эту молекулу. После успешного завершения клинических исследований вилдаглиптин был впервые зарегистрирован в 2007 г. В России препарат зарегистрирован в 2008 г. Наряду с другими представителями класса идпп-4 вилдаглиптин сыграл ключевую роль в изменении парадигмы терапии CД2 с симптоматического снижения уровня глюкозы на патофизиологический подход [4, 5].
Фармакологические свойства
Инкретины — глюкозозависимый инсулинотропный полипептид (гип) и глюкагоноподобный пептид-1 (гпп-1) — гормоны кишечника, участвующие в гомеостазе углеводов. Они вызывают инсулино- и глюкагонотропный эффект.
Основное действие этих гормонов (инкретиновый эффект) — увеличение глюкозозависимой секреции инсулина β-клетками (инсулинотропный эффект) при приеме пищи. В норме вклад инкретинового эффекта в постпрандиальный подъем уровня инсулина составляет 50—70% [6, 7].
Инкретины обладают и глюкагонотропным эффектом: они снижают уровень глюкагона в постпрандиальный период (гпп-1) и сохраняют или усиливают его секрецию при снижении концентрации глюкозы (гип), препятствуя развитию гипогликемий [8, 9].
Уже со стадии нарушения толерантности к глюкозе регистрируется снижение инкретинового эффекта, что может быть ранним маркером дисфункции β-клеток [10]. Основанная на инкретинах терапия показала свою эффективность в отношении улучшения функции β-клеток [11—13]: глюкозозависимое действие идпп-4 способствует адаптации β-клеток к имеющейся инсулинорезистентности и усилению их чувствительность к глюкозе [14—17].
Прирост уровней гпп-1 и гип отмечается через 10—15 мин после приема пищи [18]. В норме только ~10% активных инкретинов достигает системного кровотока, так как они быстро разрушаются локальной (~75%) и печеночной дпп-4 (~15%).
Вилдаглиптин ковалентно связывается с активным центром дпп-4 и дольше других препаратов блокирует ее функцию (~55 мин); комплекс вилдаглиптин/ДПП-4 медленно диссоциирует, с активным центром фермента взаимодействует новая молекула препарата. Это обеспечивает продолжительное повышение концентрации инкретинов [11], за счет чего длительно стабилизируется уровень глюкозы; помимо постпрандиальной регуляции соотношения инсулин/глюкагон, снижается ночной глюконеогенез в печени и содержание глюкозы плазмы натощак (гпн). Благодаря оптимизации секреции глюкагона нивелируется риск развития гипогликемий.
Активность дпп-4 при СД2 связана с оксидативным стрессом, воспалением и нарушением чувствительности к инсулину [20]. Экспрессия дпп-4 в жировой ткани коррелирует с ИМТ, количеством висцерального жира, размером адипоцитов, воспалением и уровнем гликированного гемоглобина [21]. дпп-4, секретируемая адипоцитами, влияет на проведение сигнала инсулина в клетках жировой и мышечной ткани [22]. Экспрессия дпп-4 в печени коррелирует с резистентностью к инсулину [23]. Недавние исследования выявили корреляцию активности циркулирующей дпп-4 с риском развития СД2 и атеросклероза [24, 25].
Таким образом, кроме контроля гликемии, терапия идпп-4 может вызывать и экстрапанкреатические эффекты: способствует мобилизации липидов во время приема пищи, снижению секреции аполипопротеина b-48 в кишечнике, снижению липолиза натощак и содержания жиров в печени, а также повышению дисперсности ЛПНП и снижению воспалительного ответа при СД2.
Метаболический стресс при СД2 вызывает гиперактивацию иммунной системы, что проявляется повышением уровня маркеров острой фазы воспаления, факторов свертывания крови, провоспалительных цитокинов (ФНО-α, ИЛ-1β и ИЛ-6). Также известна связь инсулинорезистентности с переключением фенотипа макрофагов с противовоспалительного (M2) на провоспалительный (M1) [19]. Во многих исследованиях были показаны противовоспалительные эффекты сахароснижающих препаратов, однако эффекты снижения глюкозотоксичности следует отличать от влияния препаратов на компоненты иммунитета.
На поверхности иммунных клеток экспрессируются рецепторы гпп-1 и обладающие дпп-4 активностью CD26. идпп-4 повышают концентрацию активного гпп-1 и подавляют активность, сигналинг и экспрессию CD26. гпп-1 дает противовоспалительный эффект, связанный с обратным переключением макрофагов с M1- на M2-фенотип, снижает уровни простагландина E2, ИЛ-6 и гликированного альбумина; в связи с ингибированием CD26 снижается уровень C-реактивного белка, ФНО-α, ИЛ-1β и ИЛ-6, ТПР-4, ТПР-2 и IkB киназы β [19, 26].
Функция инкретинов напрямую зависит от баланса микрофлоры в кишечнике. При СД2 снижается количество бутиратпродуцирующих бактерий, метаболиты которых — короткоцепочечные жирные кислоты (КЦЖК) — являются важными регуляторами состояния кишечника [27]. КЦЖК через рецепторы (FFAR2 и FFAR3), экспрессирующиеся на энтероцитах, поддерживают локальный иммунитет и барьерную функцию кишечника, снижают эндотоксемию и провоспалительные процессы, ассоциированные с СД2. Кроме того, КЦЖК улучшают чувствительность периферических тканей к инсулину, участвуют в регуляции метаболизма и реакций пищевого поведения [28].
КЦЖК способствуют продукции и секреции гпп-1 и пептида Y. Активация FFAR2 адипоцитов подавляет аккумулирование жира в жировой ткани и усиливает синтез лептина [28].
Дисбаланс микрофлоры приводит к снижению экспрессии рецепторов гпп-1 (и нейрональной NO-синтазы) в энтеральных нейронах, что ведет к изменениям афферентных сигналов блуждающего нерва. Таким образом, состояние микробиоты влияет на резистентность к гпп-1 и имеет прямое отношение к физиологическим эффектам, реализуемым по оси кишечник-мозг [29].
Имеются данные о влиянии сахароснижающих препаратов на состояние микробиоты кишечника [30]. Было показано, что идпп-4 (в частности, вилдаглиптин) увеличивают количество бутиратпродуцирующих бактерий. Это связывают со снижением отека в стенке кишечника, подавлением пристеночных воспалительных процессов [31] и активности дпп-4 микроорганизмов [32, 33].
Таким образом, вилдаглиптин пролонгирует действие инкретинов, регулирует гомеостаз глюкозы глюкозозависимым способом (без гипогликемий и набора массы тела) и дополнительно влияет на метаболизм, воспаление и другие звенья патогенеза СД2 [2, 11].
Возможности и преимущества вилдаглиптина в комбинированной сахароснижающей терапии
В подавляющем большинстве обзорных работ, посвященных проблеме сахарного диабета типа 2 (СД2), прежде всего отмечается, что СД2 является гетерогенным заболеванием. При этом термин «гетерогенность» охватывает не только патогенетические основы СД2, но и особенности течения заболевания, в том числе реакцию на проводимую терапию. Безусловно, подобная гетерогенность присуща множеству других хронических заболеваний, например, артериальной гипертензии и т. д. Как справедливо отметили G. Leibowitz и соавт. (2009), биологическая вариабельность является одним из неотъемлемых проявлений как самой жизни, так и болезни.
Рис. 1. Программа изучения эффективности вилдаглиптина при СД типа 2
В течение многих лет исследователи не могли дать ответ, что первично в развитии СД2: инсулинорезистентность либо нарушение секреции инсулина. Лишь сравнительно недавно был сделан вывод о том, что характерные для диабета метаболические нарушения являются результатом устойчивого сочетания обоих факторов. Соответственно, залогом успешной терапии заболевания должен быть комплексный подход, воздействующий на все звенья патогенеза.
Метформин как универсальный препарат первой линии в лечении сахарного диабета типа 2
В европейских странах для лечения сахарного диабета типа 2 (СД2) метформин начал использоваться с конца 50‑х годов прошлого века. За прошедший период времени в ходе многочисленных клинических исследований было подтверждено не только лидерство метформина как сенситайзера инсулина, но и обнаружен целый ряд уникальных благоприятных эффектов препарата на сердечно-сосудистую систему, в том числе на липидный спектр, факторы свертывания крови и т. д. [24, 27].
Согласно последним рекомендациям Американской и Европейской ассоциаций диабетологов, метформин должен назначаться с момента диагностики сахарного диабета типа 2 на фоне изменения образа жизни [21]. Таким образом, в настоящее время среди пероральных сахароснижающих средств метформин является самым широкоиспользуемым препаратом.
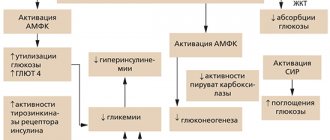
Основным механизмом действия метформина является уменьшение продукции глюкозы печенью, что способствует нормализации уровня глюкозы натощак. Этот эффект прежде всего осуществляется благодаря прямой блокаде ферментов, участвующих в глюконеогенезе (фосфоенолпируват-карбоксики-назы, фруктозо-1,6‑бифосфатазы и глюкозо-6‑фосфатазы), уменьшению захвата печенью необходимых для глюконеогенеза исходных продуктов (аланина, пирувата, глицерола и др.), а также усилению фосфорилирования рецептора инсулина и его субстратов (СИР-1, СИР-2). С другой стороны, метформин усиливает процесс утилизации глюкозы в печени путем активации гликолитических ферментов (гексокиназы, пируваткиназы). Кроме того, препарат подавляет активность печеночного фермента ацетил-КоА-карбоксилазы, что способствует уменьшению липогенеза, усилению окисления свободных жирных кислот (СЖК), предотвращению стеатоза и редукции синтеза триглицеридов [4, 9, 14, 20, 28].
Как стало известно сравнительно недавно, важнейшим медиатором влияния метформина на глюконеогенез и липогенез является аденозинмонофосфат-активиро-ванная протеинкиназа (АМПК).
Изначально АМПК была идентифицирована лишь как фермент, участвующий в синтезе холестерина и свободных жирных кислот. Исследования последних лет определили гораздо более широкий спектр действия АМПК: основной функцией оказались оценка и поддержание достаточных резервов энергии в различных клетках организма.
Активность фермента напрямую зависит от соотношения АМФ/АТФ. К состояниям, увеличивающим это соотношение (дефицит энергии), и соответственно, повышающим уровень АМПК, относятся физическая нагрузка, голод, гипоксия, ишемия, окислительный стресс и тепловой шок. Активированная АМПК способствует подавлению катаболических процессов, связанных с расходом АТФ, и стимулирует анаболические виды обмена, обеспечивающие регенерацию АТФ. В конечном итоге запасы энергии в клетке восстанавливаются. Таким образом, АМПК является своеобразным топливным сенсором («измерителем горючего») в клетках организма [29].
Как показали результаты фундаментальных исследований, метформин повышает активность АМПК, что приводит к супрессии генов, кодирующих ключевые ферменты глюконеогенеза и липогенеза, с последующим усилением синтеза гликогена в печени [30].
В клетках скелетной мускулатуры метформин усиливает как базальную, так и инсулин-стиму-лированную утилизацию глюкозы, что, в свою очередь, отражается на постпрандиальных значениях гликемии. Активация АМПК в мышцах под действием метформина способствует повышению утилизации глюкозы путем усиления транслокации транспортеров глюкозы ГЛЮТ4 [12, 30].
В жировой ткани путем активации АМПК метформин способствует угнетению липогенеза, усилению утилизации глюкозы и окисления СЖК, подавлению секреции провоспалительных диабетогенных цитокинов [10, 12, 22, 16].
Учитывая, что основной причиной летальных исходов при сахарном диабете типа 2 являются сердечно-сосудистые заболевания, крайне важно, чтобы сахароснижающие препараты оказывали как минимум нейтральное, а в приоритете – плейотропное положительное влияние на сер-дечно-сосудистую систему.
В определенной мере ренессанс метформина как бигуанида был обоснован результатами исследования UKPDS, которые впервые показали, что на фоне применения препарата по сравнению с использованием диетотерапии существенно снижается риск всех случаев смерти, а также смерти от диабета и ряда других неблагоприятных исходов заболевания (инфаркт миокарда, сердечная недостаточность и т. д.) [25]. Дальнейшие исследования позволили не только уточнить механизмы подобных эффектов метформина, но и, по выражению N. Wiernsperger (2007), охарактеризовать его как сердечно-сосудистый препарат, обладающий сахароснижающим действием.
Протективный эффект метформина в отношении сердечно-сосуди-стых заболеваний обусловлен непосредственным положительным действием препарата на тканевую перфузию, систему гемостаза, окислительный стресс, гликирование белков. Важно, что это действие проявляется при назначении препарата в гораздо меньших дозировках по сравнению с теми, которые предопределяют его сахаророснижающие эффекты [18, 26].
Терапия метформином характеризуется крайне низким риском развития побочных эффектов (в том числе в отношении развития гипогликемии и лактацидоза), не увеличивает массу тела.
Таким образом, эволюция метформина от рядового, старинного средства фармакопеи до препарата первой линии в структуре самых современных схем инициации терапии СД2 вполне обоснована.
Эффективность вилдаглиптина в комбинации с метформином
Причиной прогрессирующего течения СД2 является прежде всего усугубление нарушений секреторной функции β-клеток поджелудочной железы, соответственно, у большинства больных к терапии метформином на определенном этапе заболевания необходимо подключение препаратов, усиливающих продукцию инсулина. Идеальными лекарственными средствами, комбинируемыми с метформином, могут считаться препараты, обладающие комплементарным механизмом действия и обеспечивающие должный контроль показателей углеводного обмена при минимальном риске дополнительных побочных эффектов.
К числу новых перспективных ме-тодов лечения СД2 относятся препараты, действие которых сопря-жено с усилением эффектов глюкагоноподобного пептида-1 (ГПП-1) – гормона, вырабатываемого энтероэндокринными L-клетками ки-шечника.
Участие ГПП-1 в регуляции углеводного обмена осуществляется путем множества механизмов, важнейшими из которых являются:
- усиление секреции инсулина по глюкозозависимому механизму;
- подавление секреции глюкагона;
- уменьшение моторики желудка (замедление всасывания углеводов);
- снижение аппетита;
- подавление апоптоза β-клеток, усиление их пролиферации и неогенеза из расположенных в протоках поджелудочной железы клеток-предшественников.
Период пребывания гормона в активной форме – ГПП-17–36 либо ГПП-17–37 – составляет около 2 минут, затем он подвергается быстрому разрушению с образованием метаболитов ГПП-19–36 и ГПП-19–37 под действием фермента дипептидил-пептидазы-4 (ДПП-4). У больных СД2 содержание гормона ниже, чем у здоровых людей.
Препараты, ингибирующие активность ДПП-4 (глиптины), увеличивают продолжительность жизни эндогенного глюкагоноподобного пептида-1 [23].
Вилдаглиптин является мощным высокоселективным ингибитором ДПП-4, в течение суток он подавляет активность ДПП-4 на 97% [1, 3, 19].
В ходе многочисленных клинических исследований с участием свыше 22 тысяч больных СД2 показана эффективность вилдаглиптина при применении его как в виде монотерапии, так и в комбинации с другими сахароснижающими средствами. Программа клинических исследований по изучению эффективности и безопасности вилдаглиптина схематически представлена на рисунке 1.
Как стало известно в последние годы, метформин способствует увеличению уровня ГПП-1. Среди предполагаемых механизмов обсуждается роль бигуанида в непосредственном усилении секреторной функции L-клеток кишечника, активации транскрипции/трансляции гена проглюкагона, снижении почечной экскреции ГПП-1, блокаде дипептидил-пептидазы-4 [17]. Комбинация вилдаглиптина с метформином оказывает синергичное действие на усиление секреции ГПП-1.
К настоящему времени проведена целая серия работ, в которых продемонстрированы преимущества комбинированной терапии вилдаглиптином и метформином.
Вилдаглиптин в комбинации с метформином по сравнению с плацебо
В одном из наиболее ранних рандомизированных исследований было показано, что комбинация вилдаглиптина с метформином позволяет добиться значимого улучшения показателей углеводного обмена, причем эти результаты остаются стабильными в течение года. В данной работе вилдаглиптин в дозе 50 мг добавлялся к терапии метформином, что уже через 12 недель привело к снижению HbA1 с на 0,6% по сравнению с исходным уровнем (7,7%). В группе контроля (монотерапия метформином) существенных изменений не отмечалось. Все последующие 40 недель на фоне комбинированной терапии сохранялся положительный результат лечения, в то время как в контрольной группе наблюдалась прогрессирующая отрицательная динамика (увеличение HbA1 с на 0,066% ежемесячно). За счет этого разница между группами по HbA1 с изменилась с – 0,7% (12‑я неделя наблюдения) до –1,1% (40‑я неделя) [2].
В двойном слепом исследовании, выполненном E. Bosi с соавт. (2007), вилдаглиптин в дозе 50 мг однократно либо дважды в день комбинировали с метформином (> 1500 мг в сутки) у 416 больных. В среднем уровень HbA1 с, изначально составлявший 8,4%, через 24 недели возрос на 0,2% на фоне метформина в сочетании с плацебо. В группе, получавшей, помимо метформина, вилдаглиптин в дозе 50 мг либо 100 мг, показатели HbA1 с снизились на 0,5% и 0,9% соответственно, уровень гликемии натощак – на 0,8 ммоль/л и 1,7 ммоль/л [8]. Важно, что при сочетанном назначении вилдаглиптина и метформина побочные эффекты со стороны желудочно-кишечного тракта наблюдались реже, чем на фоне монотерапии метформином [11].
Вилдаглиптин по сравнению с тиазолиндионами при добавлении к метформину
Целью работы G. Boli и соавт. (2008) была оценка эффективности и переносимости вилдаглиптина по сравнению с пиоглитазоном у больных СД2 с неудовлетворительными показателями углеводного обмена (HbA1 с в пределах 7,5% – 11%) на фоне монотерапии метформином, применявшегося в средней дозе от 2000 мг в сутки. В многоцентровое рандомизированное двойное-слепое исследование длительностью 24 недели было включено 295 больных, получавших, помимо метформина, вилдаглиптин по 100 мг в день, а также 281 пациент, получавший на фоне метформина пиоглитазон в дозе 30 мг в день. К концу периода наблюдения уровень HbA1 с в группе, получавшей вилдаглиптин, уменьшился на 0,9%, при назначении пиоглитазона – на 1,0% (статистически значимой разницы по группам не выявлено). Серьезные побочные эффекты наблюдались у 2% человек на вилдаглиптине, и у 4,6% – на пиоглитазоне. Умеренная гипогликемия отмечена лишь у одного больного (0,3%), получавшего вилдаглиптин. Прием пиоглитазона привел к значимому увеличению массы тела (+1,9 кг в среднем, разница между изучавшимися группами составила 1,6 кг, р
Сходные результаты были получены в открытом многоцентровом исследовании GALIANT (GALvus In Addition to metformin vs. Tzd/metformin in lowering HbA1 с) с участием 2664 больных сахарным диабетом типа 2. Пациенты получали, помимо метформина в дозе от 1000 мг/день, вилдаглиптин либо тиазолидиндионы (выбор конкретного препарата – пиоглитазона либо розиглитазона – проводили исследователи в зависимости от опыта их практики). Через 12 недель было определено, что снижение HbA1 с было сходным по группам (–0,68% на вилдаглиптине vs. –0,57% на фоне приема тиазолидиндионов), не выявлено разницы по частоте побочных эффектов в целом (соответственно, 39,5% vs. 36,3%). Масса тела увеличилась в группе, получавшей глитазоны (+0,33 кг), и уменьшилась на фоне вилдаглиптина (-0,58 кг) [5].
Вилдаглиптин по сравнению с препаратами сульфонилмочевины (глимепиридом) при добавлении к метформину
В двойное слепое исследование были включены 2789 больных, получавших исходно монотерапию метформином в средней дозе 1900 мг в сутки (исходный HbA1 с в пределах 6,5% – 8,5%), с последующей рандомизацией на группы с подключением либо вилдаглиптина 100 мг в день, либо глимепирид до 6 мг в день. Через год наблюдения разницы по динамике HbA1 с не выявлено (-0,4% на вилдаглиптине vs. –0,5% на глимепириде). Целевых значений HbA1 с до 7% достигли 54% больных, получавших вилдаглиптин, и 56% человек на фоне терапии глимепиридом (p>0,05). Несмотря на сходство результатов, характеризующих динамику состояния углеводного обмена, количество побочных эффектов на вилдаглиптине было существенно меньше. Так, масса тела на фоне вилдаглиптина уменьшилась, но увеличилась у больных, получавших глимепирид (разница по группам составила 1,8 кг). Вилдаглиптин оказывал либо нейтральное, либо положительное влияние на показатели липидного спектра крови; прием глимепирида сопровождался умеренным возрастанием липопротеинов низкой плотности и триглицеридов. Частота эпизодов гипогликемии на вилдаглиптине за 52 недели составила 1,7% (ни одного тяжелого случая) и 16,2% на глимепириде (10 тяжелых случаев). Отчетливая положительная динамика показателей углеводного обмена в сочетании с низким риском гипогликемии даже у больных с относительно невысокими показателями HbA1 с свидетельствует о том, что сахароснижающее действие вилдаглиптина осуществляется прежде всего благодаря повышению чувствительности секреторного аппарата поджелудочной железы к глюкозе [13].
Комбинация вилдаглиптин/метформин по сравнению с монотерапией вилдаглиптином либо метформином
В 2009 г. E. Bosi с соавт. провели исследование длительностью 24 недели, в котором 1179 пациентов в зависимости от характера терапии были разделены на 4 группы: комбинация вилдаглиптина 50 мг с метформином 1000 мг дважды в день, комбинация вилдаглиптина 50 мг с метформином 500 мг дважды в день, монотерапия вилдаглиптином (по 50 мг дважды в день) либо монотерапия метформином по 1000 мг дважды. Динамика HbA1 с в изучавшихся группах составила соответственно –1,8%; –1,6%; –1,1%; –1,4%. Снижение гликемии натощак также было наиболее значимым в группах, получавших вилдаглиптин в сочетании с метформином по сравнению с пациентами, получавшими монотерапию каким-либо из препаратов. Все режимы терапии хорошо переносились пациентами и продемонстрировали сходные профиль и частоту побочных эффектов. Изменение массы тела (исходные значения – в среднем 88,3 кг) на вилдаглиптине составило –0,6 кг, –1,6 кг на фоне метформина и в среднем на –1,2 кг на обоих режимах комбинированной терапии [8].
Преимущества сочетанного назначения вилдаглиптина и метформина (аддитивное влияние на углеводный обмен и комлементарный механизм действия) предопределили необходимость создания фиксированной комбинации этих препаратов [17]. В странах Евросоюза вилдаглиптин/метформин (Eucreas) используется с 2007 г., в Российской Федерации препарат Галвус Мет зарегистрирован в 2009‑м.
Таким образом, возможность одномоментного воздействия на ключевые звенья патогенеза СД2 – инсулинорезистентность и нарушение функции островковых клеток поджелудочной железы, отчетливое улучшение показателей углеводного обмена при низком риске гипогликемии – обеспечивает высокий потенциал комбинированной терапии вилдаглиптином и метформином.
Эффективность
Влияние вилдаглиптина на уровень hba1c у человека было доказано в 4-недельном плацебо-контролируемом исследовании с участием пациентов с исходным уровнем hba1c 7,1—7,2. Были подтверждены эффекты, наблюдавшиеся в исследованиях на животных: увеличение гпп-1 и функции β-клеток поджелудочной железы — и впервые установлено снижение уровня глюкагона во время приема пищи [2].
Стартовая терапия
Монотерапия вилдаглиптином
По данным исследования с участием 354 наивных пациентов с СД2, монотерапия вилдаглиптином в течение 24 нед способствует снижению гликемии. У принимавших вилдаглиптин в различных дозировках ΔHbA1c составила 0,4—0,8%, в группе плацебо — лишь 0,1% [34].
Вилдаглиптин подобно метформину улучшал гликемический контроль. В 52-недельном исследовании прием вилдаглиптина обеспечивал ΔHbA1c — 1% (p
<0,001), а метформина — 1,4% (
p
<0,001). При пролонгации исследования до 104 нед результаты были аналогичными — 1,0 и 1,5% соответственно (
p
<0,001). Различий в динамике массы тела пациентов не было, частота гипогликемии была низкой в обеих группах (
p
<1%), а нежелательные явления (НЯ) со стороны ЖКТ проявлялись в 2 раза чаще при приеме метформина [35, 36].
В сводном анализе результатов монотерапии вилдаглиптином было продемонстрировано, что ΔHbA1c зависит от его исходного уровня. При исходном уровне гликированного гемоглобина 10,6% ΔHbA1c составила 2,1%; при 9,5% — 1,8%; при 8,5% — 1,2%; при 7,7% — 0,7% и при исходном уровне HbA1c 6,9% — 0,5% [37].
Комбинированная терапия вилдаглиптином с метформином
Стартовая комбинированная терапия вилдаглиптином с метформином (2 раза в сутки) изучалась в 24-недельном клиническом исследовании (n
=1179, hba1c=7,5—11%). Пациенты были рандомизированы в группы комбинированной терапии: вилдаглиптин+метформин в высокой (50+1000 мг) и низкой дозе (50+500 мг), а также в группы монотерапии: метформин (1000 мг) и вилдаглиптин (50 мг). ΔHbA1c в соответствующих группах составляла 1,8, 1,6, 1,4 и 1,1% (рис. 1).
Рис. 1. Изменение уровня HbA1c в группах с разной терапией СД2 [38]. В группах комбинированной терапии не отмечено эпизодов гипогликемии, повышения массы тела. Все виды терапии хорошо переносились и показывали сходную частоту НЯ [38].
Интенсификация терапии
Двухкомпонентная терапия
В мультицентровом рандомизированном клиническом исследовании (РКИ) к метформину ≥1500 мг/сут добавляли вилдаглиптин 50 мг/сут (n
=143), вилдаглиптин 50 мг 2 раза в сутки (
n
=143) или плацебо (
n
=130). Через 24 нед уровень hba1c в группах пациентов, получавших вилдаглиптин, снизился соответственно на 0,7 и на 1,1%, а гпн на 0,8 и 1,7 ммоль/л; в группе плацебо параметры гликемии не изменялись [39].
При сравнении эффектов вилдаглиптин+метформин и глимепирид+метформин в ходе 1- и 2-летнего исследования [12, 13] была показана сходная эффективность комбинаций, однако при приеме вилдаглиптина число гипогликемий было в 14 раз меньше (глимепирид: 554 события/10 тяжелых; вилдаглиптин: 39 событий/0 тяжелых) и не отмечен набор массы тела [40, 41].
Трехкомпонентная терапия
У пациентов, получавших метформин+псм, добавление вилдаглиптина улучшало гликемический контроль [42]. Через 24 нед терапии глимепирид+метформин с добавлением вилдаглиптина (n
=158) ΔHbA1c составила 1,01% (
p
<0,001), а в группе плацебо (
n
=160) — 0,25% (
p
<0,001). В группе вилдаглиптина целевого уровня hba1c достигли 28,3%, в группе плацебо — 5,6% пациентов (
p
<0,001); частота гипогликемий была низкой и не наблюдалось значимого увеличения массы тела. Положительный эффект добавления вилдаглиптина к метформину+псм связан не только с повышением глюкозозависимой секреции β-клеток, но и с нормализацией постпрандиальной секреции глюкагона α-клетками.
Комбинация с инсулином
У пациентов на инсулинотерапии вилдаглиптин улучшается гликемический контроль и позволяет снизить дозу инсулина [43]. Помимо этого, вилдаглиптин уменьшает частоту гипогликемий, что, вероятно, обусловлено повышением чувствительности α-клеток к глюкозе [43, 44].
Эффективность и безопасность вилдаглиптина в дозе 50 мг 2 раза в сутки (n
=144) в сравнении с плацебо (
n
=152) оценивались у пациентов на терапии инсулином-НПХ (доза >30 Ед/сут в течение 4 нед) с неудовлетворительным контролем гликемии (hba1c 7,5—11%). В группе вилдаглиптина ΔHbA1c составляла 0,5%, в группе плацебо — 0,2%, а у пациентов старше 65 лет — 0,7 и 0,1% соответственно. Вилдаглиптин снижал риск гипогликемий по сравнению плацебо: 113 (0 тяжелых) против 185 событий (6 тяжелых) соответственно [43].
В 12-недельном проспективном многоцентровом исследовании добавление 50 мг/сут вилдаглиптина позволило снизить среднюю суточную дозу инсулина с 36,26±18,21 до 26,87±16,49 Ед (p
<0,0001) [44].
По результатам описанных исследований вилдаглиптин был зарегистрирован для применения у больных с СД2 в качестве монотерапии (в сочетании с диетотерапией и физическими упражнениями); в комбинации с метформином (в качестве начальной медикаментозной терапии); в составе двухкомпонентной комбинированной терапии метформином, псм, тиазолидиндионами или инсулином, а также в составе тройной комбинированной терапии метформином+ПСМ или метформином+инсулином.
Ингибитор дипептидилпептидазы-4-вилдаглиптин — новый препарат в терапии сахарного диабета 2-го типа
У многих больных сахарным диабетом 2-го типа (СД 2-го типа) применение пероральных сахароснижающих препаратов (ПССП) не позволяет добиться необходимого контроля гликемии. По данным исследования UKPDS компенсация заболевания через 3 года после постановки диагноза при монотерапии ПССП достигалась только у 45% больных, а через 6 лет — лишь у 30%. Это обстоятельство диктует необходимость разработки и внедрения новых препаратов, позволяющих не только устранять метаболические нарушения, но и сохранять функциональную активность клеток поджелудочной железы, стимулируя и активируя физиологические механизмы секреции инсулина и контроля уровня глюкозы крови.
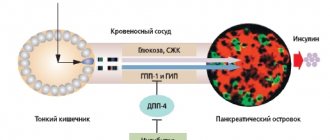
Регуляция гомеостаза глюкозы в организме осуществляется сложной полигормональной системой, включающей гормоны поджелудочной железы и гормоны инкретины, вырабатываемые в кишечнике в ответ на прием пищи. До 70% постпрандиальной секреции инсулина у здоровых людей обусловлено именно эффектом инкретинов () [1]. У больных СД 2-го типа этот эффект значительно снижен ().
Инкретинами, играющими основную роль в инсулиновом ответе на прием пищи, являются глюкозозависимый инсулинотропный полипептид (ГИП) и глюкагоноподобный пептид-1 (ГПП-1).
Поступление пищи в пищеварительный тракт быстро стимулирует выброс ГИП и ГПП-1, которые за счет совместного действия:
- стимулируют высвобождение инсулина бета-клетками и угнетают продукцию глюкагона альфа-клетками поджелудочной железы в ответ на повышение глюкозы крови;
- повышают концентрацию инсулина, способствуя утилизации глюкозы периферическими тканями;
- уменьшают высвобождение глюкозы печенью.
Инкретины могут снижать уровень гликемии также за счет «неинсулиновых» механизмов путем замедления опорожнения желудка и снижения потребления пищи.
При СД 2-го типа содержание инкретинов и их эффект снижен. Тем не менее, действие инкретинов у таких пациентов можно восстановить путем введения экзогенных препаратов [3]. Поэтому результатом выяснения роли желудочно-кишечных гормонов (инкретинов) в регуляции углеводного обмена явилось создание принципиально нового класса сахароснижающих препаратов — инкретиномиметиков (рис. 3).
В новых рекомендациях по выбору режимов терапии и алгоритмах по поддержанию гликемического контроля, представленных на конгрессе Международной федерации диабета (Монреаль, 18–23 октября 2009), была акцентирована значимость ингибиторов дипептидилпептидазы-4 (ДПП-4) и агонистов ГПП-1. Препараты этих групп рекомендуются практически на всех этапах терапии СД 2-го типа.
Одним из представителей класса ингибиторов ДПП-4 является препарат вилдаглиптин (Галвус®), зарегистрированный в России в ноябре 2008 г. Вилдаглиптин применяется у больных СД 2-го типа в виде монотерапии в дозе 50 мг или 100 мг в сутки либо в комбинации с метформином, препаратами сульфонилмочевины (ПСМ) или инсулином.
Селективное и обратимое ингибирование фермента ДПП-4 повышает концентрацию эндогенных ГИП и ГПП-1, а также продлевает период их присутствия в плазме. Вилдаглиптин, таким образом, усиливает физиологические эффекты обоих инкретиновых гормонов, улучшая глюкозозависимую секрецию инсулина и снижая повышенную секрецию глюкагона. Снижение избыточного уровня глюкагона во время еды, в свою очередь, вызывает уменьшение инсулинорезистентности.
Ингибирование ДПП-4 было показано после однократного приема вилдаглиптина у здоровых добровольцев и многократного приема у больных СД 2-го типа. При этом длительность ингибирования была дозозависимой. Дозы в 50 мг и 100 мг 1 раз в сутки были в равной степени эффективны в ингибировании ДПП-4 во время дневного приема пищи, однако доза в 100 мг была более эффективна в ночной период.
Повышение уровней ГПП-1 и ГИП было продемонстрировано у больных СД 2-го типа, получавших вилдаглиптин в течение 4 недель; отмечалось повышение уровней инкретинов после приема пищи и натощак. Повышенные уровни наблюдались как в течение дня, так и в ночные часы.
Основным клиническим эффектом препарата является улучшение контроля гликемии, снижение уровня гликированного гемоглобина HbA1c (интегрального показателя контроля углеводного обмена за 2–3 мес). Это позволяет большему количеству пациентов достичь терапевтических целей лечения. Эффекты снижения уровня гликемии и HbA1с изучались различными методами (уровень глюкозы в плазме натощак и после приема пищи, суточный гликемический профиль, продукция эндогенной глюкозы). Вилдаглиптин снижал уровень глюкозы в плазме после приема пищи у больных СД 2-го типа как в монотерапии, так и в комбинации с препаратами сулфонилмочевины или метформином, наиболее часто применяемыми ПССП [1]. Кроме того, на фоне приема вилдаглиптина (4 недели) у больных СД 2-го типа отмечалось снижение уровня триглицеридов сыворотки.
Таким образом, можно говорить о многокомпонентном действии вилдаглиптина, которое включает:
- ингибирование ДПП-4 (основное действие);
- повышение уровней ГПП-1 и ГИП (требуемый эффект);
- влияние на функции островков поджелудочной железы (усиление инсулинового ответа бета-клеток и уменьшение глюкагонового ответа альфа-клеток на глюкозу) и резистентность к инсулину;
- влияние на гликемический профиль (снижение уровня глюкозы натощак и после приема пищи) и эндогенную продукцию глюкозы;
- снижение уровня липидов после приема пищи;
- влияние на опорожнение желудка.
Более 20 тыс. пациентов принимали участие в клинических испытаниях вилдаглиптина, при этом 14 тыс. пациентов непосредственно получали препарат. Все исследования были контролируемыми, многоцентровыми, двойными слепыми в параллельных группах.
Вилдаглиптин в сравнении с росиглитазоном в качестве монотерапии
Проводилось сравнение эффективности и переносимости терапии вилдаглиптином и росиглитазоном в течение 24 недель терапии [8]. Пациенты, включенные в исследование, ранее не получавшие медикаментозной терапии, с исходным HbA1c 7,5–11,0% были рандомизированы на терапию вилдаглиптином (50 мг ´ 2 раза/сутки) или росиглитазоном (8 мг ´ 1 раз в сутки). В исследование включено 697 пациентов с СД 2-го типа (вилдаглиптин n = 459; росиглитазон n = 238). Основным параметром исследования была динамика HbA1c: исходно и через 24 недели. Вторичные параметры исследования: динамика глюкозы плазмы натощак, уровень липидов в плазме натощак, динамика массы тела, частота возникновения отеков на фоне проводимой терапии.
Результаты исследования показали достоверное снижение уровня HbA1c по сравнению с исходными значениями на -1,1% и -1,3% для вилдаглиптина и росиглитазона соответственно (р < 0,001 для обоих препаратов) ().
У пациентов с исходно высоким HbA1c (> 9%) была показана достоверно большая динамика снижения в обеих группах терапии: -1,8% в группе терапии вилдаглиптином (исходно 10,0%) и -1,9% в группе терапии росиглитазоном (исходно 9,9%). При этом отмечались статистически значимые (р < 0,001) различия по изменению массы тела между группами лечения: вилдаглиптин не влиял на массу тела, прием росиглитазона приводил к ее увеличению в среднем на 4,7 кг. Более высокая частота возникновения периферических отеков была выявлена в группе терапии росиглитазоном (11,1%) по сравнению с группой на терапии вилдаглиптином (4,6%). Результаты показали, что при равной сахароснижающей эффективности вилдаглиптин обеспечивает лучшую переносимость.
Добавление вилдаглиптина к терапии метформином в сравнении с терапией ПСМ или «ПСМ + метформин»
Эффективность и безопасность вилдаглиптина (50 мг ´ 2 раза/сутки) и глимепирида (препарата из группы сульфонилмочевины, использовался в дозе до 6 мг/сутки) изучалась при длительном применении (52 недели) у пациентов с недостаточно хорошим контролем гликемии (HbA1c 6,5–8,5%) при приеме метформина (постоянная доза ~1,9 г/сутки). Через год отмечалось снижение HbA1c в обеих группах (вилдаглиптин -0,4%; глимепирид -0,5%) () [9]. Таким образом, при добавлении к метформину вилдаглиптин показал эффективность, сходную с глимепиридом.
Кроме того, в течение исследования масса тела пациентов, принимавших вилдаглиптин, оставалась стабильной, тогда как у больных, принимавших глимепирид, отмечалась прибавка веса. Различия между группами через 52 недели составили 1,8 кг. Через 52 недели терапии у пациентов, получавших вилдаглиптин + метформин, прибавки веса отмечено не было.
Особое внимание уделялось сравнению числа гипогликемий в обеих группах: 1,7% пациентов из группы вилдаглиптина (n = 1389) и 16,2% пациентов из группы глимепирида (n = 1383) перенесли ≥ 1 гипогликемического эпизода ().
Было зарегистрировано 39 гипогликемических эпизодов в группе вилдаглиптина и 554 — в группе глимепирида. В группе вилдаглиптина не было отмечено тяжелых (2-й или близких ко 2-й степени) гипогликемических эпизодов, тогда как в группе глимепирида зарегистрировано 10 тяжелых гипогликемических эпизодов. К концу 52 недели в группе вилдаглиптина было отмечено меньше гипогликемических эпизодов [10].
Вилдаглиптин + инсулин НПХ
В исследовании длительностью 24 недели сравнивались эффекты терапии вилдаглиптином (50 мг ´ 2 раза/сутки, n = 144) или плацебо (n = 152) у пациентов с СД 2-го типа, получавших инсулинотерапию (как минимум в течение 3 мес в дозе > 30 Ед/сутки) и не достигших адекватного контроля гликемии (исходный HbA1c 7,5–11%). Основным параметром данного исследования являлась оценка эффективности добавления вилдаглиптина к инсулину в плане влияния на снижение HbA1c в сравнении с монотерапией инсулином ().
В целом, добавление вилдаглиптина к инсулину достоверно снизило уровень HbA1c в сравнении с исходными значениями и с группой монотерапии. Межгрупповая разница составила -0,3% (P = 0,01). У пациентов в подгруппе старше ≥ 65 лет также было отмечено достоверное и более выраженное снижение гликемии, чем в группе «вилдаглиптин + инсулин»: -0,7% HbA1c в сравнении с исходными значениями (р < 0,001).
Кроме того, было доказано, что достоверно меньшее число пациентов в группе терапии «вилдаглиптин + инсулин» имело эпизоды гипогликемии (23% пациентов сообщили о 113 эпизодах; P < 0,01) в сравнении с терапией «плацебо + инсулин» (30% пациентов сообщили о 185 эпизодах). В группе терапии «вилдаглиптин + инсулин» не было ни одного эпизода тяжелой гипогликемии в сравнении с терапией «инсулин + плацебо», где было отмечено 6 эпизодов (). Таким образом, несмотря на выраженный сахароснижающий эффект, вилдаглиптин обеспечивает снижение частоты гипогликемических реакций, особенно тяжелых.
Вилдаглиптин + метформин
Комбинация «вилдаглиптин + метформин» позволила достичь снижения уровня HbA1c на 1,1% по сравнению с группой, принимавшей метформин + плацебо [2, 3]. Пациенты, недостаточно контролирующие уровень гликемии на монотерапии метформином, при комбинированном применении метформина и вилдаглиптина в 4 раза чаще достигают компенсации заболевания по сравнению с комбинацией «метформин + плацебо» [4]. Помимо этого, добавление вилдаглиптина к терапии метформином продемонстрировало такую же эффективность, как и применение метформина с тиазолидиндионами (ТЗД). При этом не наблюдалось набора веса [5] ().
Эффективность длительного применения вилдаглиптина подтверждена исследованием моно- и комбинированной терапии, продолжительностью 52 недели ().
Результаты, полученные при совместном использовании вилдаглиптина и метформина, обосновали идею создания комбинированного препарата ГалвусМет® (вилдаглиптин + метформин), который зарегистрирован в России в марте 2009 года. ГалвусМет® назначается в тех случаях, когда монотерапия метформином не дает существенного результата. Вилдаглиптин в комбинации с метформином обеспечивает надежный контроль уровня глюкозы в крови. ГалвусМет® выпускается в трех дозировках: 50 мг вилдаглиптина + метформин в дозе 500 мг, 850 мг или 1000 мг. Принимается 2 раза в день.
Частота развития нежелательных побочных эффектов на фоне терапии вилдаглиптином
Общая частота нежелательных явлений была сравнимой в группах «вилдаглиптин + метформин» и «плацебо + метформин». Снижение частоты нарушений со стороны желудочно-кишечного тракта (ЖКТ) отмечалось при комбинации «вилдаглиптин + метформин» в 15% случаев по сравнению с комбинацией «плацебо + метформин» — 18%. Частота нежелательных явлений не увеличивалась с продолжительностью терапии. Частота серьезных нежелательных явлений была низкой и сравнимой для обеих групп. Из клинически значимых нежелательных явлений головная боль встречалась более часто при приеме вилдаглиптина, чем при приеме «плацебо + метформин». Не отмечено ухудшения побочных эффектов метформина при добавлении к терапии вилдаглиптина.
В исследованиях комбинированной терапии применение вилдаглиптина не было связано с повышением частоты гипогликемий при комбинации с метформином. Процент пациентов с гипогликемическими явлениями в группе «вилдаглиптин + глимепирид» был слегка выше, чем в соответствующей группе плацебо (2,4% по сравнению с 0,6%). Отмечавшиеся явления гипогликемии были легкой степени тяжести и не приводили к прекращению приема препарата. Как и ожидалось, значительно большая частота гипогликемии наблюдалась в исследовании с инсулином, но ее частота была ниже в группе «вилдаглиптин + инсулин» (23%), чем в группе «плацебо + инсулин» (30%). В группе «плацебо + инсулин» большее количество гипогликемических реакций имело среднюю степень тяжести. В этой же группе было отмечено несколько тяжелых эпизодов.
По сравнению с метформином, пациенты с уже существующими факторами сердечно-сосудистого риска (сердечно-сосудистые заболевания, гипертензия и/или дислипидемия) не показали более высокой частоты смертей, инфаркта миокарда (ИМ) или инсульта при приеме вилдаглиптина. Отдельные сердечно-сосудистые нарушения (гипертензия, значимые отклонения ЭКГ) не увеличивались при моно- или комбинированной терапии.
Таким образом, основными свойствами вилдаглиптина в отношении нежелательных побочных эффектов являются:
- переносимость и безопасность, схожие с плацебо, без увеличения общей частоты нежелательных явлений в отношении основных систем и органов как при моно-, так и комбинированной терапии;
- лучшая переносимость со стороны ЖКТ по сравнению с метформином;
- отсутствие увеличения риска гипогликемий: препарат не повышал частоту гипогликемии при монотерапии и в комбинации с инсулином, демонстрировал меньшее количество и более легкую степень тяжести эпизодов гипогликемии, чем инсулин + плацебо, не показал увеличения частоты эпизодов гипогликемии в комбинации с метформином.
Кроме того, вилдаглиптин не повышает сердечно-сосудистый риск, не вызывает увеличения массы тела, повышения частоты возникновения отеков или сердечной недостаточности, обладает нейтральным эффектом в отношении уровня липидов натощак и оказывает положительное влияние на липидный профиль после приема пиши.
Заключение
Современная эпидемиологическая ситуация характеризуется, с одной стороны, значительным ростом заболеваемости СД 2-го типа, а с другой стороны, недостаточной эффективностью существующих методов терапии. В этой ситуации все актуальнее становятся разработка и внедрение новых препаратов для лечения СД 2-го типа. Роль инновационных препаратов с оригинальными механизмами действия будет все более значимой, так как они открывают новые возможности коррекции дисфункции островков поджелудочной железы при СД 2-го типа и влияния на прогрессирование заболевания. Вилдаглиптин, являясь представителем нового класса препаратов для лечения СД 2-го типа, обладает рядом достоинств по сравнению с традиционной терапией. За счет подавления активности ДПП-4 препарат повышает уровень инкретиновых гормонов (ГПП-1 и ГИП). В свою очередь, их повышенные уровни, увеличивая уровень инсулина и снижая уровень глюкагона, позволяют добиться более эффективного контроля глюкозы крови и снижения продукции глюкозы печенью. Это приводит к наиболее важному клиническому эффекту — достижению компенсации заболевания (снижение HbA1с).
Литература
- Garber A. et al. Effects of Vildagliptin on Glucose Control in Patients with Type 2 Diabetes Inadequately Controlled with a Sulphonylurea // Diabetes, Obesity and Metabolism. 2008; 10: 1326–1463.
- Bosi E. et al. Effects of Vildagliptin on Glucose Control Over 24 Weeks in Patients with Type 2 Diabetes Inadequately Controlled with Metformin // Diabetes Care. 2007; 30: 890–895.
- Stratton I. et al. Association of Glycaemia with Macrovascular and Microvascular Complications of Type 2 Diabetes (UKPDS 35): Prospective Observational Study // BMJ. 2000; 321: 405–412.
- Dejager S. et al. Achievement of Glycemic Targets with Vildagliptin // Presented at EASD, 17–21 September 2007 (Abstract A-07–899).
- Bolli G. et al. Efficacy and Tolerability of Vildagliptin vs. Pioglitazone when Added to Metformin: A 24-Week, Randomized, Double-Blind Study // Diabetes, Obesity and Metabolism. 2008; 10: 82–90.
- Garber A. et al. Efficacy and Tolerability of Vildagliptin Added to a Sulfonylurea (SU) in Patients with Type 2 Diabetes (T2 DM) // Presented at ADA, 22–26 June 2007 (Abstract 501-P).
- Rosenstock J. et al. Efficacy and Tolerability of Initial Combination Therapy with Vildagliptin and Pioglitazone Compared with Component Monotherapy in Patients with Type 2 Diabetes // Diabetes, Obesity and Metabolism. 2007; 9 (2): 175–185.
- Rosenstock J., Baron M. A., Dejager S. et al. Comparison of vildagliptin and rosiglitazone Monotherapy in patients with Type 2 Diabetes: a 24-week, double-blinde, randomized trial // Diabetes Care. 2007, 30: 217–223.
- Ferrannini E. et al. 52-week efficacy and safety of vildagliptin versus glimepiride in patients with type 2 diabetes mellitus inadequately controlled on metformin monotherapy. Diabetes Obes Metab. 2009 (in press).
- Fonseca V. et al. Addition of vildagliptin to insulin improves glycaemic control in type 2 diabetes // Diabetologia. 2007; 50: 1148–1155.
М. Б. Анциферов, доктор медицинских наук, профессор Л. Г. Дорофеева, доктор медицинских наук
Эндокринологический диспансер Департамента здравоохранения, Москва
Контактная информация об авторах для переписки
Метаанализы и сравнительныеисследования
В метаанализ эффективности инкретиновой терапии было включено 79 РКИ (n
~40 000). Исходный уровень hba1c составлял 7,2—9,3%, а ΔHbA1c — 0,6—1,1%. Эффекты разных идпп-4 были схожими, однако вилдаглиптин показал наиболее выраженное снижение HbA1c и гпн (рис. 2)
Рис. 2. Среднее изменение уровня HbA1c (A) и ГПН (B) на фоне приема иДПП-4 [45]. [45].
Для прогнозирования ΔHbA1c при выборе идпп-4 на основе систематического обзора 98 РКИ (n
~24 000) была разработана номограмма. При прочих равных (hba1c и гпн) наибольшая ΔHbA1c ожидалась при выборе вилдаглиптина (рис. 3)
Рис. 3. Номограмма для оценки ΔHbA1c при выборе ДПП-4. Как пользоваться: (1) выбрать ингибитор и (2) исходный уровень HbA1c, затем (3) опустить перпендикуляр на шкалу «баллы», (4) аналогично для ГПН. (5) Сумма баллов исходного HbA1c и ГПН соответствуют предполагаемому снижению уровня HbA1c при приеме выбранного ингибитора [46]. [46].
Эффективность терапии в основном оценивают по уровню hba1c и гпн. Однако средняя амплитуда колебаний глюкозы (САКГ) имеет даже большее влияние на окислительный стресс, чем гипергликемия, и связана с развитием микро- и макрососудистых осложнений [47, 48]. Это подтверждено в двух субанализах исследования DEVOTE, в котором показано, что САКГ ассоциирована с тяжелыми гипогликемиями, а также с риском смерти от любых причин [49].
В 12-недельном исследовании пациенты с СД2 (n
=90, hba1c >7,5%), получавшие метформин в дозе 2000 мг/сут, были рандомизированы в группы интенсификации терапии ситаглиптином 100 мг/сут и вилдаглиптином 50 мг 2 раза в сутки. Показатели гликемии были сходными в обеих группах, однако САКГ была меньше в группе вилдаглиптина [13]. В группе вилдаглиптина было сильнее выражено снижение уровня нитротирозина и маркеров воспаления, а многофакторный анализ продемонстрировал более тесную корреляцию этих показателей с САКГ, чем с постпрандиальной гликемией. Кроме того, повышение активного гпп-1, ответ β-клеток (aucинсулина /aucглюкозы) и снижение уровня глюкагона (в прандиальный и межпрандиальный периоды) были более выраженными в группе вилдаглиптина, чем в группе ситаглиптина (рис. 4)
Рис. 4. Динамика уровня ГПП-1 и глюкагона в течение суток [50]. [50].
В другом исследовании (n
=73, терапия метформин+псм) изучалось влияние добавления вилдаглиптина и саксаглиптина на САКГ. При сходной эффективности и безопасности обоих препаратов вилдаглиптин снижал САКГ больше, чем саксаглиптин. В группе вилдаглиптина ΔСАКГ=1,74±0,48 ммоль/л (
p
<0,001), а в группе саксаглиптина — 0,87±0,40 ммоль/л (
p
=0,003).
Терапия вилдаглиптином в сравнении с ситаглиптином и саксаглиптином ассоциирована с меньшей САКГ. К тому же при приеме вилдаглиптина отмечено большее снижение уровня глюкагона, а гликемия пациентов дольше находилась в заданных диапазонах [50, 51].
Поддержание уровня глюкозы в физиологическом диапазоне, согласно эффекту метаболической памяти, способствует снижению риска осложнений СД2 и, возможно, снижению дисфункции β-клеток.
В исследование VERIFY впервые оценивается влияние ранней терапии вилдаглиптином с метформином на ифункцию β-клеток. Изучается стойкость эффекта у пациентов с впервые или недавно диагностированным СД2, имеющих небольшое повышение уровня hba1c (6,5—7,5%). Результаты исследования должны показать, обладает ли ранняя двухкомпонентная терапия длительными эффектами: увеличением времени до развития неэффективности лечения или до начала инсулинотерапии, а также влиянием на сосудистые изменения у пациентов с СД2. Результаты ожидаются в 2022 г. [52].
Безопасность. Применениев особых популяциях
Пожилые пациенты
Пожилые пациенты с СД2 имеют высокий риск микро- и макрососудистых осложнений и когнитивных нарушений, и им необходима эффективная, безопасная и удобная терапия.
В исследовании INTERVAL продемонстрированы безопасность и эффективность идпп-4 у пациентов старше 70 лет. Скорректированное отношение шансов достижения индивидуально подобранной гликемической цели составило 3,16 (1,81—5,52; p
<0,0001) в пользу вилдаглиптина, а переносимость и эффективность гликемического контроля у пожилых пациентов были аналогичны таковым у молодых.
В сводном анализе баз данных применения вилдаглиптина у пациентов старше 75 лет было продемонстрировано снижение уровня HbA1c на 0,9% при монотерапии и на 1,1% при комбинированной терапии с метформином. Среди получавших вилдаглиптин НЯ встречались реже, чем среди получавших препарат сравнения [53].
Пациенты с хронической почечной недостаточностью (ХПН)
У пациентов с умеренными и тяжелыми нарушениями функции почек вилдаглиптин показывает хороший профиль безопасности при приеме на фоне инсулинотерапии; у пожилых пациентов (≥75 лет); пациентов с впервые выявленным сахарным диабетом после трансплантации; пациентов на гемодиализе [5].
В фармакокинетических исследованиях у пациентов с нарушениями функции почек была продемонстрирована сходная концентрация инсулина в плазме при увеличенной в 2 раза экспозиции вилдаглиптина в сравнении с пациентами с сохранной функцией почек [4]. Поскольку вилдаглиптин выводится через почки на 23% в неизмененном виде и на 77% в виде неактивных метаболитов и не оказывает повреждающего действия на почки при средней (30 <�СКФ <50 мл/мин) и тяжелой (CКФ <30 мл/мин) ХПН, дозу вилдаглиптина можно уменьшить до 50 мг/сут, при этом сохранить эффект и в 2 раза снизить стоимость терапии.
У пациентов с СД2 со средней и тяжелой ХПН терапия вилдаглиптином (50 мг/сут) снижала уровень HbA1c на 0,57 и 0,81% соответственно. Отмечен низкий риск гипогликемий (26% в группе средней тяжести и 18% в группе тяжелой ХПН). По окончании 52 нед терапии вилдаглиптином не наблюдалось ухудшения функции почек независимо от исходной степени ХПН [5].
Прием 50 мг/сут вилдаглиптина хорошо переносился пациентами старше 75 лет (n
=105) со средней или тяжелой ХПН: ΔHbA1c составила 1%, не наблюдалось повышения частоты гипогликемии, частота других НЯ не возрастала [54].
Пациенты с хронической сердечной недостаточностью (ХСН)
Безопасность вилдаглиптина у пациентов с ХСН (I—III функционального класса по классификации NYHA) изучалась в 52-недельном двойном слепом РКИ (n
=254). Было установлено, что лечение вилдаглиптином не влияет на функцию левого желудочка и не ухудшает течение ХСН. ΔHbA1c составила 0,62% [55].
Согласно сетевому метаанализу результатов 50 РКИ [56], наименьшие шансы в плане нарастания сердечной недостаточности демонстрирует вилдаглиптин (ОШ=0,71).
Вилдаглиптин
Международное наименование лекарственного вещества:
Вилдаглиптин (Vildagliptin) Перечень препаратов, содержащих действующее вещество Вилдаглиптин, приведен после описания.
Фармакологическое действие:
Гипогликемическое средство, стимулятор островкового аппарата поджелудочной железы, селективный ингибитор фермента дипептидилпептидазы-4 (ДПП-4). Быстрое и полное ингибирование активности ДПП-4 (более 90%) вызывает повышение как базальной, так и стимулированной (приемом пищи) секреции глюкагоноподобного пептида 1 типа и глюкозозависимого инсулинотропного полипептида из кишечника в системный кровоток в течение всего дня. Повышая концентрации глюкагоноподобного пептида 1 типа и глюкозозависимого инсулинотропного полипептида, вилдаглиптин вызывает повышение чувствительности бета-клеток поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой секреции инсулина. При применении в дозе 50-100 мг в сутки у больных сахарным диабетом 2 типа отмечается улучшение функции бета-клеток поджелудочной железы. Степень улучшения функции бета-клеток островков поджелудочной железы зависит от степени их исходного повреждения; так у лиц, не без сахарного диабета (с нормальной концентрацией глюкозы в плазме крови) препарат не стимулирует секрецию инсулина и не снижает концентрацию глюкозы. Повышая концентрацию эндогенного глюкагоноподобного пептида 1 типа, вилдаглиптин увеличивает чувствительность альфа-клеток островков поджелудочной железы к глюкозе, что приводит к улучшению глюкозозависимой регуляции секреции глюкагона. Снижение концентрации избыточного глюкагона во время еды, в свою очередь, вызывает снижение инсулинорезистентности. Увеличение соотношения инсулин/глюкагон на фоне гипергликемии, обусловленное повышением концентрации глюкагоноподобного пептида 1 типа и глюкозозависимого инсулинотропного полипептида, вызывает уменьшение продукции глюкозы печенью (в прандиальный период и после приема пищи), что приводит к снижению концентрации глюкозы в плазме крови. На фоне применения вилдаглиптина отмечается снижение концентрации липидов в плазме крови, однако этот эффект не связан с его действием на глюкагоноподобный пептид 1 типа или глюкозозависимый инсулинотропный полипепдид и улучшением функции бета-клеток поджелудочной железы. Повышение концентрации глюкагоноподобного пептида 1 типа может приводить к замедлению опорожнения желудка, однако на фоне применения вилдаглиптина подобного эффекта не наблюдается. При применении вилдаглиптина в качестве монотерапии или в комбинации с метформином, производными сульфонилмочевины, тиазолидиндионом, или инсулином отмечается достоверное длительное снижение концентрации гликозилированного Hb и глюкозы крови натощак.
Фармакокинетика:
AUC прямо пропорционально повышению дозы препарата. При приеме с пищей скорость абсорбции снижается незначительно, Cmax уменьшается на 19%, TCmax — увеличивается до 2.5 ч; степень абсорбции и AUC не меняются. Связь с белками низкая — 9.3%. Распределяется эквивалентно между плазмой и эритроцитами. Объем распределения (при в/в введении) — 71 л. Распределение предположительно происходит экстраваскулярно. Основным путем выведения является биотрансформация. Превращению подвергается 69% дозы ЛС. Основной метаболит — LAY151 (57% дозы) фармакологически неактивен и является продуктом гидролиза циано-компонента. Около 4% дозы подвергаются амидному гидролизу. Отмечается положительное влияние ДПП-4 на гидролиз препарата. Вилдаглиптин не метаболизируется при участии изоферментов цитохрома P450 и не является субстратом для них, не ингибирует и не индуцирует их. T1/2 — 3ч. Выводится почками — 85% (в т.ч. в неизмененном виде 23%), кишечником — 15%. При печеночной недостаточности легкой (5-6 баллов по Чайлд-Пьюга) и умеренной степени (6-10 баллов по Чаилд-Пьюга) после однократного применения препарата отмечается снижение биодоступности на 20% и 8%, соответственно. При тяжелой печеночной недостаточности (12 баллов по Чаилд-Пьюга) биодоступность повышается на 22%. Повышение или снижение максимальной биодоступности, не превышающее 30%, не является клинически значимым. Корреляции между степенью тяжести нарушений функции печени и биодоступностью препарата не выявлено. У пациентов с легкими, умеренными, тяжелыми нарушениями функции почек, с терминальной стадией ХПН (на гемодиализе) отмечается повышение Сmax на 8%-66% и AUC на 32%-134%, не коррелирующее с тяжестью нарушения, а также увеличение AUC неактивного метаболита LAY151 в 1.6-6.7 раза, зависящее от тяжести нарушения. T1/2 не изменяется. Максимальное повышение биодоступности на 32% и Сmax на 18% (у пациентов старше 70 лет) не является клинически значимым и не влияет на ингибирование ДПП-4.
Показания:
Сахарный диабет 2 типа: монотерапия (в сочетании с диетотерапией и физическими упражнениями) и комбинированная терапии (в сочетании с метформином, производными сульфонилмочевины, тиазолидиндионом, инсулином) в случае неэффективности диетотерапии, физических упражнений и монотерапии этих препаратов.
Противопоказания:
Гиперчувствительность, тяжелые нарушения функции печени (повышение активности АЛТ и АСТ в 2.5 раза выше верхней границы нормы), умеренные или тяжелые нарушения функции почек (включая терминальную стадию ХПН на гемодиализе), беременность, период лактации, детский возраст (до 18 лет). Для ЛФ содержащих лактозу (дополнительно): непереносимость галактозы, дефицит лактазы или нарушение всасывания глюкозы-галактозы.
Побочные действия:
Частота: очень часто (1/10 и более), часто (более 1/100 и менее 1/10), нечасто (более 1/1000 и менее 1/100), редко (более 1/10000 и менее 1/1000), очень редко (менее 1/10000). При монотерапии: со стороны нервной системы — часто — головокружение, нечасто — головная боль. Со стороны пищеварительной системы: нечасто — запоры. Со стороны ССС: нечасто — периферические отеки. При применении в дозе 50 мг (1-2 раза в сутки) в комбинации с метформином: со стороны нервной системы — часто — головокружение, головная боль, тремор. При применении в дозе 50 мг/сут в комбинации с производными сульфонилмочевины: со стороны нервной системы — часто — головокружение, головная боль, астения, тремор. При применении в дозе 50 мг 1-2 раза в сутки в комбинации с производными тиазолидиндиона: со стороны ССС — часто — периферические отеки. Прочие: часто — увеличение массы тела. При применении в дозе 50 мг 2 раза в сутки в комбинации с инсулином: со стороны нервной системы — часто — головная боль. Со стороны пищеварительной системы: часто — тошнота, метеоризм, гастроэзофагеальная рефлюксная болезнь. Со стороны обмена веществ: часто — гипогликемия. При проведении монотерапии или в комбинации с др. препаратами побочные реакции были слабо выражены, имели временный характер и не требовали отмены ЛС. Частота развития ангионевротического отека (редко — более 1/10000 и менее 1/1000) была сходна с таковой в контрольной группе. Наиболее часто ангионевротические отеки отмечались при комбинации с ингибиторами АПФ, были умеренно выражены и исчезали при продолжении терапии. Редко отмечались нарушения функции печени (в т.ч. гепатит) бессимптомного течения, которые в большинстве случаев разрешились самостоятельно после прекращения терапии препаратом.
Взаимодействие:
Обладает низким потенциалом лекарственного взаимодействия. Вилдаглиптин не является субстратом изоферментов цитохрома Р450, не ингибирует и не индуцирует эти ферменты; его взаимодействие с ЛС, которые являются субстратами, ингибиторами или индукторами цитохрома Р450, маловероятно. При одновременном применении вилдаглиптин не влияет на скорость метаболизма ЛС, являющихся субстратами изоферментов CYP1A2, CYP2C8, CYP2C9, CYP2C19, CYP2D6, CYP2E1 и CYP3A4/5. Клинически значимых взаимодействий с ЛС, наиболее часто используемых при лечении сахарного диабета 2 типа (глибенкламидом, пиоглитазоном, метформином) или обладающих узким терапевтическим диапазоном (амлодипином, дигоксином, рамиприлом, симвастатином, валсартаном, варфарином) не установлено.
Особые указания:
В редких случаях при применении вилдаглиптина отмечается повышение активности аминотрансфераз (как правило, без клинических проявлений). Перед назначением ЛС и в ходе первого года лечения (1 раз в 3 мес), рекомендуется определять биохимические показатели функции печени. При повышении активности аминотрансфераз, результат следует подтвердить повторным исследованием, а затем регулярно проводить определение биохимических показателей функции печени до тех пор, пока они не нормализуются. Если превышение активности АСТ или АЛТ в 3 раза выше верхней границы нормы подтверждено повторным исследованием, препарат рекомендуется отменить. При развитии желтухи или др. признаков нарушения функции печени прием препарата следует немедленно прекратить и не возобновлять после нормализации показателей функции печени. При необходимости инсулинотерапии вилдаглиптин применяют только в комбинации с инсулином. Препарат не следует применять при сахарном диабете 1 типа или для лечения диабетического кетоацидоза. В период лечения (при развитии головокружения) необходимо воздержаться от управления транспортными средствами и занятий потенциально опасными видами деятельности, требующими повышенной концентрации внимания и быстроты психомоторных реакций.
Препараты, содержащие действующее вещество Вилдаглиптин:
Вилдаглиптин Медисорб, Галвус
Информация, приведенная в данном разделе, предназначена для медицинских и фармацевтических специалистов и не должна использоваться для самолечения. Информация приведена для ознакомления и не может рассматриваться в качестве официальной.
Общая безопасность
Сводный анализ данных 58 исследований (вилдаглиптин, n
=10 331; препараты сравнения,
n
=8068) показал сходную частоту развития НЯ, серьезных НЯ (СНЯ), досрочного прекращения лечения и смертельных исходов в обеих группах. Эти данные подкреплены результатами исследования EDGE (
n
=45 868), в котором частота развития НЯ была аналогичной в группах лечения вилдаглиптином (5,3%) и препаратом сравнения (5,7%) [5].
Сердечно-сосудистая безопасность
Сердечно-сосудистая безопасность вилдаглиптина была подтверждена в метаанализе (40 исследований III и IV фазы, n
=17 000), который включил пациентов со стажем СД2 >10 лет, пациентов старше 65 лет, с нарушениями функции почек и сердечной недостаточностью. Показано, что при лечении вилдаглиптином и препаратами сравнения были сходные риски в отношении комбинированной конечной точки и ее компонентов (смерть от сердечно-сосудистых заболеваний, нефатальный инфаркт миокарда, нефатальный инсульт) (рис. 5)
Рис. 5. Отношения рисков Мантеля—Хензеля комбинированной конечной точки и отдельных ее компонентов при лечении вилдаглиптином и препаратами сравнения [57]. [57].
Нежелательные явления со стороны кожи
В сводном анализе не выявлено повышенной частоты развития НЯ со стороны кожи при применении вилдаглиптина в сравнении с другими препаратами. Однако исследования баз данных фармаконадзора указывают на повышенную частоту буллезного пемфигоида у пожилых пациентов, получавших идпп-4, что соответствует эпидемиологическим наблюдениям: зрелый возраст — фактор риска развития подобных поражений. При применении идпп-4 у пациентов с СД2 рекомендован мониторинг кожных поражений [5].
Безопасность в отношении иммунной системы
CD26-рецептор (c дпп-4 активностью) экспрессируется на Т-лимфоцитах и играет роль в иммунном ответе. Отмечена сходная частота инфекционных НЯ и СНЯ при применении вилдаглиптина и всех препаратов сравнения. Согласно всестороннему обзору, вилдаглиптин не повышает частоту назофарингита (ОШ=1,06 [0,93—1,21]), инфекций верхних дыхательных путей (ОШ=1,19 [0,98—1,45]) или инфекций мочевыводящих путей (ОШ=0,94 [0,57—1,56]) [5].
Безопасность в отношении поджелудочной железы
Метаанализ 69 исследований показал отсутствие повышенного риска панкреатита на фоне лечения вилдаглиптином по сравнению с препаратами сравнения (ОШ=0,97 [0,37—2,53]). Риск развития острого панкреатита при приеме идпп-4 (кроме вилдаглиптина) в сравнении с плацебо был установлен в метаанализе (ОШ=1,79 [1,13—2,82]), хотя абсолютное повышение риска было невысоким (0,13%) [5].
Безопасность в отношении печени
Риск трехкратного повышения уровня АЛТ и АСТ, так и риск развития НЯ и СНЯ со стороны печени при лечении вилдаглиптином и препаратами сравнения были сходными [5].
В исследовании REDIRECT у пациентов с СД2 (hba1c ≤7,6%) лечение вилдаглиптином приводило к снижению уровня триглицеридов в печени и снижению АЛТ. Также была отмечена сильная положительная корреляция (r
=0,83;
p
<0,0001) между снижением уровня АЛТ и содержанием жира в печени [58].
Вилдаглиптин в реальной клинической практике (РКП)
Наиболее крупномасштабным исследованием эффектов идпп-4 в условиях ркп (n
=45 000, 27 стран) является исследование EDGE [59]. В российской части исследования (
n
=1650) через 12 мес наблюдения первичной конечной точки достигли 744 (81%) пациента из группы вилдаглиптина и 460 (64%) из группы сравнения. На фоне приема вилдаглиптина уровень HbA1c снижался на 1,3% (с 8,1 до 6,8%), в группе сравнения — на 0,8% (с 8,0 до 7,2%) (
р
<0,0001). Частота гипогликемий — 1,1 и 3,4 соответственно. Большинство гипогликемий в группе вилдаглиптина возникали при комбинированной терапии с ПСМ. На терапии вилдаглиптином большее число пациентов достигали целевого уровня hba1c (<7%) без гипогликемий и без набора массы тела: 48,7% против 19,1% [59].
Было проведено ретроспективное сравнение результатов терапии метформином+вилдаглиптином и метформином+ПСМ. В обеих группах степень снижения hba1c коррелировала с его исходным уровнем. Однако на фоне приема ПСМ эффективность, продемонстрированная в РКИ (ΔHbA1c =1,2%), не воспроизводилась в полной мере в РКП (ΔHbA1c 0,9%): разница между РКИ и РКП была тем больше, чем меньшим был исходный уровень hba1c. В то же время у пациентов группы вилдаглиптина ΔHbA1c (1,2% в РКИ, 1,1% в РКП) была одинаковой при всем диапазоне колебаний исходного уровня hba1c (рис. 6).
Рис. 6. Эффективность вилдаглиптина в сравнении с ПСМ при дополнении к метформину — сравнение результатов РКИ и РКП [53]. Расхождение эффективности ПСМ в РКИ и РКП могло быть связано с низкой приверженностью пациентов к лечению и медленным титрованием дозы, возможно, из-за боязни развития гипогликемии или набора массы тела.
В исследовании GUARD оценивали эффективность, безопасность и переносимость вилдаглиптина при монотерапии или комбинации с метформином в РКП (n
=19 000). Снижение уровня hba1c имело место на всех стадиях СД2 (рис. 7)
Рис. 7. Средняя ΔHbA1c по данным исследования GUARD; *p<0,0001 по сравнению с исходным уровнем [60]. независимо от пола, возраста и степени ожирения пациентов [60].
В другом исследовании (PROVIL) сравнивались эффективность и безопасность комбинации вилдаглиптин+метформин и другой сахароснижающей терапии в условиях РКП. Пациенты (n
=3648, длительность СД2 ~6 лет, уровень hba1c 7,6—7,9%) были распределены в три группы терапии: 1-я — вилдаглиптин+метформин (
n
=603); 2-я фиксированная комбинация вилдаглиптин+метформин в одной таблетке (
n
=2198) и 3-я — другие ПССП (ПСМ+метформин, тиазолидиндионы+метформин, другие идпп-4+метформин) (
n
=847). Через 6 мес во всех группах наблюдалось статистически значимое снижение уровня HbA1c, но при терапии вилдаглиптином эффект был более выраженным (ΔHbA1c=0,9%). У пациентов, получавших вилдаглиптин, было отмечено снижение массы тела на 1,4 и на 1,7 кг (на 0,8 кг в группе сравнения); число НЯ и гипогликемий было сравнимо во всех группах. Результаты исследования подтвердили эффективность комбинированной терапии вилдаглиптином и метформином в условиях РКП без увеличения числа НЯ [61].
В ретроспективном когортном исследовании с участием более 20 тыс. пациентов с СД2 было показано, что терапия вилдаглиптином в сравнении с ПСМ ассоциирована со значительно более низким риском развития ретино- и нейропатий, а также наблюдалась тенденция к снижению нефропатий и изъязвлений на фоне диабетической стопы (рис. 
Рис. 8. Отношение рисков осложнений СД2 при приеме вилдаглиптина и ПСМ [62]. [62].
При анализе данных 52 750 пациентов с СД2 (шведские регистры назначаемых препаратов, причин смерти и пациентов) было заключено, что комбинация метформин+псм ассоциирована с бо́льшим риском развития тяжелой гипогликемии, сердечно-сосудистых событий и смерти по любым причинам, чем комбинация метформин+идпп-4 [63].
В ретроспективном аналитическом исследовании 5 европейских баз данных была оценена сердечно-сосудистая безопасность вилдаглиптина в сравнении с другими ПССП. В анализ были включены данные более 730 тыс. пациентов с СД2. Результаты показали отсутствие увеличения риска инфаркта миокарда, острого коронарного синдрома, инсульта, ХСН при приеме вилдаглиптина по сравнению с другими ПССП [64].
Вилдаглиптин Медисорб
При применении вилдаглиптина в монотерапии или в комбинации с другими препаратами большинство нежелательных реакций были слабо выражены, имели временный характер и не требовали отмены терапии. Корреляции между частотой нежелательных реакций (HP) и возрастом, полом, этнической принадлежностью, продолжительностью применения или режимом дозирования не выявлено.
Частота развития ангионевротического отека на фоне терапии вилдаглиптином составляла ≥1/10000,
Наиболее часто случаи ангионевротического отека отмечались при применении препарата в комбинации с ингибиторами ангиотензинпревращающего фермента. В большинстве случаев ангионевротический отек был средней степени тяжести и разрешался самостоятельно в ходе продолжения терапии вилдаглиптином.
На фоне терапии вилдаглиптином редко отмечались нарушения функции печени (включая гепатит) бессимптомного течения. В большинстве случаев данные нарушения и отклонения показателей функции печени от нормы разрешились самостоятельно без осложнений после прекращения терапии препаратом. При применении вилдаглиптина в дозе 50 мг 1 или 2 раза в сутки частота увеличения активности ‘печеночных’ ферментов (АЛТ или ACT ≥ЗхВГН) составляла 0,2% или 0.3% соответственно (по сравнению с 0.2% в контрольной группе). Увеличение активности ‘печеночных’ ферментов в большинстве случаев было бессимптомным, не прогрессировало и не сопровождалось холестазом или желтухой.
HP сгруппированы в соответствии с классификацией органов и систем органов MedDRA. В пределах каждой группы органов и систем органов HP перечислены в порядке уменьшения частоты встречаемости. В пределах каждой группы частоты встречаемости HP указаны в порядке уменьшения тяжести.
Для оценки частоты встречаемости HP использовались следующие критерии: очень часто (≥1/10), часто (≥1/100,
При применении вилдаглиптина в монотерапии
При применении вилдаглиптина в дозе 100 мг в сутки частота отмены терапии в связи с развитием нежелательных реакций (0,3%) была не выше таковой в группе плацебо (0,6%) или препарата сравнения (0,5%).
На фоне монотерапии вилдаглиптином в дозе 100 мг в сутки частота развития гипогликемии без увеличения степени тяжести состояния составляла 0,4%, что сопоставимо с препаратом сравнения и плацебо (0,2%).
Масса тела не изменялась по сравнению с исходной в клинических исследованиях, когда вилдаглиптин 100 мг в сутки применяли в качестве монотерапии (-0,3 кг и -1,3 кг в группах вилдаглиптина и плацебо соответственно).
Инфекционные и паразитарные заболевания: очень редко — инфекции верхних дыхательных путей, назофарингит.
Нарушения со стороны обмена веществ и питания: нечасто — гипогликемия.
Нарушения со стороны нервной системы: часто — головокружение; нечасто — головная боль.
Нарушения со стороны желудочно-кишечного тракта (ЖКТ): нечасто — запор.
Нарушения со стороны сосудов: нечасто — периферические отеки.
Нарушения со стороны скелетно-мышечной и соединительной ткани: нечасто -артралгия.
Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в монотерапии.
При применении вилдаглиптина в дозе 100 мг в сутки в комбинации с метформином
При применении вилдаглиптина в дозе 100 мг/сут в комбинации с метформином или плацебо в сочетании с метформином случаев отмены терапии в связи с развитием нежелательных реакций не отмечалось.
При применении вилдаглиптина в дозе 100 мг в сутки в комбинации с метформином гипогликемия отмечалась в 1 % случаев (в группе плацебо + метформин нечасто (0,4%)). В группе применения вилдаглиптина не наблюдалось развития гипогликемии тяжелой степени.
Масса тела не изменялась по сравнению с исходной в клинических исследованиях при применении комбинации вилдаглиптина 100 мг в сутки и метформина (+0,2 кг и -1,0 кг в группах вилдаглиптина и плацебо соответственно).
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
Нарушения со стороны нервной системы: часто — тремор, головная боль, головокружение; нечасто — повышенная утомляемость.
Нарушения со стороны ЖКТ: часто — тошнота.
Долгосрочные клинические исследования продолжительностью до 2 лет не выявили каких-либо дополнительных отклонений профиля безопасности или непредвиденных рисков при применении вилдаглиптина в комбинации с метформином.
Изучение применения комбинации вилдаглиптина и метформина в качестве стартовой терапии при СД 2 не выявило отклонений профиля безопасности или непредвиденных рисков.
При применении вилдаглиптина в дозе 50 мг/сут в комбинации с производными сульфонилмочевины
При применении вилдаглиптина в дозе 50 мг/сут в комбинации с глимепиридом частота отмены терапии в связи с развитием HP составляла 0,6% (по сравнению с 0% в группе глимепирид + плацебо).
Частота развития гипогликемии пациентов, получавших вилдаглиптина в дозе 50 мг/сут вместе с глимепиридом, составила 1,2% (по сравнению с 0,6% в группе плацебо + глимепирид). В группе применения вилдаглиптина не наблюдалось развития гипогликемии тяжелой степени.
Масса тела не изменялась по сравнению с исходной в клинических исследованиях, когда вилдаглиптин в дозе 50 мг один раз в сутки добавляли к глимепириду (-0,1 кг и -0,4 кг в группах вилдаглиптина и плацебо соответственно).
Инфекционные паразитарные заболевания: очень редко — назофарингит.
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
Нарушения со стороны ЖКТ: нечасто — запор.
Нарушения со стороны нервной системы: часто — тремор, головокружение, головная боль, астения.
При применении вилдаглиптина в дозе 100 мг в сутки в комбинации с тиазолидиндионом
При применении вилдаглиптина в дозе 100 мг/сут + тиазолидиндион и плацебо + тиазолидиндион случаев отмены терапии в связи с развитием HP не отмечалось.
При применении вилдаглиптина в дозе 100 мг в сутки + пиоглитазон отмечалось развитие гипогликемии в 0,6% случаев, а у пациентов, получавших плацебо + пиоглитазон — в 1,9% случаев. В группе применения вилдаглиптина не наблюдалось развития гипогликемии тяжелой степени.
В исследовании применения вилдаглиптина в качестве дополнительной терапии к пиоглитазону абсолютное увеличение массы тела в группе плацебо и вилдаглиптина 100 мг в сутки составило 1,4 и 2,7 кг соответственно.
При добавлении вилдаглиптина в дозе 100 мг в сутки к пиоглитазону в дозе 45 мг/сут частота развития периферических отеков составляла 7% (по сравнению с 2,5% на фоне монотерапии пиоглитазоном).
Нарушения со стороны сосудов: часто — периферические отеки.
Нарушения со стороны обмена веществ и питания: часто — увеличение массы тела; нечасто — гипогликемия.
Нарушения со стороны нервной системы: нечасто — головная боль, астения.
При применении вилдаглиптина в дозе 50 мг 2 раза в сутки в комбинации с инсулином (с метформином или без него)
При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) частота отмены терапии вследствие развития побочных эффектов была равна 0,3% в группе терапии вилдаглиптином, в группе плацебо случаев отмены терапии не было.
При применении препарата в комбинации с инсулином (в комбинации с метформином или без метформина) не отмечалось увеличения риска развития гипогликемии по сравнению с комбинацией плацебо + инсулин (14% в группе вилдаглиптина и 16,4% в группе плацебо). У 2 пациентов в группе вилдаглиптина и у 6 пациентов в группе плацебо развилась гипогликемия тяжелой степени.
На момент завершения исследования препарат не оказывал влияния на среднюю массу тела (масса тела увеличилась на +0,6 кг по сравнению с исходной в группе вилдаглиптина, а в группе плацебо осталась неизменной).
Нарушения со стороны нервной системы: часто — головная боль, озноб.
Нарушения со стороны ЖКТ: часто — тошнота, гастроэзофагеальный рефлюкс; нечасто -диарея, метеоризм.
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
При применении вилдаглиптина в дозе 50 мг два раза в день в комбинации с препаратами сульфонилмочевины и метформином
Случаев отмены препарата, связанных с HP в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом, отмечено не было. В группе комбинированной терапии плацебо, метформином и глимепиридом частота отмены препарата, связанной с HP, составила 0,6%.
Гипогликемия отмечалась часто в обеих группах (5,1% в группе комбинированной терапии вилдаглиптином, метформином и глимепиридом и 1,9% в группе комбинированной терапии плацебо, метформином и глимепиридом). В группе вилдаглиптина отмечен один эпизод гипогликемии тяжелой степени.
На момент завершения исследования значимого влияния на массу тела выявлено не было (+0,6 кг в группе вилдаглиптина и -0,1 кг в группе плацебо).
Нарушения со стороны нервной системы: часто — головокружение, тремор.
Нарушения со стороны обмена веществ и питания: часто — гипогликемия.
Нарушения со стороны кожи и подкожных тканей: часто — гипергидроз.
Общие расстройства и нарушения в месте введения: часто — астения.
Пострегистрационные исследования
Во время проведения пострегистрационных исследований были выявлены следующие побочные реакции (поскольку сообщения получены в добровольном порядке от популяции неопределенного размера, достоверно определить частоту развития данных HP не представляется возможным, в связи с чем они классифицированы как ‘частота неизвестна’).
Нарушения со стороны ЖКТ: частота неизвестна — панкреатит.
Нарушения со стороны печени и желчевыводящих путей: частота неизвестна — гепатит (разрешившийся самостоятельно после отмены лекарственного препарата), повышение активности ‘печеночных’ ферментов (разрешившееся самостоятельно после отмены лекарственного препарата).
Нарушения со стороны скелетно-мышечной и соединительной ткани: частота неизвестна — миалгия.
Нарушения со стороны кожи и подкожных тканей: частота неизвестна — крапивница, эксфолиативное и буллезное поражения кожи, включая буллезный пемфигоид.
Если у Вас отмечаются побочные эффекты, указанные в инструкции или они усугубляются, или Вы заметили любые другие побочные эффекты не указанные в инструкции, сообщите об этом врачу.
Дополнительная информация
Источник финансирования.
Поисково-аналитическая работа и подготовка статьи осуществлена автором на личные средства.
Конфликт интересов.
Демидова Т.Ю. — лектор, участник экспертных советов, клинических исследований компаний Astra Zeneca, Novo Nordisk, Sanofi, Novartis, Boehringer Ingelheim, Takeda, Berlin Chemi.
Сведения об авторах
Демидова Татьяна Юльевна
— д.м.н., проф. [TatianaYu. Demidova, MD, PhD, Professor]; Адрес: Россия, 117997, Москва, ул. Островитянова, д. 1, [address: 1 Ostrovitianova street, 117997 Moscow, Russia]; телефоны,; SCOPUS: 7003771623; SPIN-код: 9600-9796; e-mail