Метформин (Metformin)
Лактоацидоз
Лактоацидоз является редким, но серьезным (высокая смертности при отсутствии неотложного лечения) осложнением, которое может возникнуть из-за кумуляции метформина. Случаи лактоацидоза при приеме метформина возникали в основном у пациентов с сахарным диабетом с выраженной почечной недостаточностью.
Следует учитывать и другие сопряженные факторы риска, такие как декомпенсированный сахарный диабет, кетоз, продолжительное голодание, алкоголизм, печеночная недостаточность, любое состояние связанное с выраженной гипоксией и одновременный прием препаратов, которые могут вызывать развитие лактоацидоза (см. раздел «Взаимодействие с другими лекарственными средствами»). Это может помочь снизить частоту случаев возникновения лактоацидоза.
Следует учитывать риск развития лактоацидоза при появлении неспецифических признаков, таких как мышечные судороги, сопровождающиеся диспептическими расстройствами, болью в животе и выраженной астенией. Лактоацидоз характеризуется ацидотической одышкой, болью в животе и гипотермией с последующей комой. Диагностическими лабораторными показателями являются снижение pH крови (менее 7,35), содержание лактата в плазме крови свыше 5 ммоль/л, повышенные анионный промежуток и отношение лактат/пируват. При подозрении на метаболический ацидоз необходимо прекратить прием препарата и немедленно обратиться к врачу.
Хирургические операции
Применение метформина должно быть прекращено во время проведения хирургических операций под общей, спинальной или эпидуральной анестезией. Терапия метформином может быть продолжена не ранее чем через 48 часов после хирургической операции или возобновления приема пищи при условии, что функция почек была обследована и признана нормальной.
Функция почек
Поскольку метформин выводится почками, перед началом лечения и регулярно в последующем, необходимо определять клиренс креатитнана:
— Не реже одного раза в год у пациентов с нормальной функцией почек;
— Каждые 3-6 месяцев у пациентов с клиренсом креатинина 45-59 мл/мин.
— Каждые 3 месяца у пациентов с клиренсом креатинина 30-44 мл/мин.
В случае клиренса креатинина менее 30 мл/мин применение препарата противопоказано.
Следует проявлять особую осторожность при возможном нарушении функции почек у пожилых пациентов, при дегидратации (хроническая или тяжелая диарея, многократные приступы рвоты), при одновременном применении гипотензивных лекарственных средств, диуретиков или нестероидных противовоспалительных препаратов.
Сердечная недостаточность
Пациенты с сердечной недостаточностью имеют более высокий риск развития гипоксии и почечной недостаточности. Пациентам с хронической сердечной недостаточностью следует регулярно проводить мониторинг сердечной функции почек во время приема метформина.
Прием метформина при сердечной недостаточности с нестабильными показателями гемодинамики противопоказан.
Дети и подростки
Диагноз сахарного диабета 2 типа должен быть подтвержден до начала лечения метформинаом.
В ходе клинических исследований продолжительность 1 год было показано, что метформин не влияет на рост и половое созревание. Однако в виду отсутствия долгосрочных данных, рекомендован тщательный контроль последующего влияния метформина на эти параметры у детей, особенно в период полового созревания. Наиболее тщательный контроль необходим детям в возрасте 10-12 лет.
Применение йодсодержащих рентгеноконтрастных средств
Внутрисосудистое введение йодсодержащих рентгеноконтрастных средств может привести к развитию почечной недостаточности и кумуляции метформина, что повышает риск развития лактоацидоза. Метформин необходимо отменить, в зависимости от функции почек, за 48 ч до или во время рентгенологического исследования с применением йодсодержащих рентгеноконтрастных средств, и не возобновлять прием ранее 48 ч после него, при условии, что в ходе обследования функция почек была признана нормальной.
Другие меры предосторожности:
— Пациентам рекомендуется продолжать соблюдать диету с равномерным потреблением углеводов в течение дня. Пациентам с избыточной массой тела рекомендуется продолжать соблюдать гипокалорийную диету (но не менее 1000 ккал/сут).
— Рекомендуется регулярно проводить стандартные лабораторные анализы для контроля сахарного диабета.
— Метформин при монотерапии не вызывает гипогликемию, однако рекомендуется проявлять осторожность при его применении в комбинации с инсулином или другими гипогликемическими средствами (например, производными сульфонилмочевины, репаглинидом и др.).
Применение препарата Метформин рекомендовано для профилактики сахарного диабета 2 типа лицам с предиабетом и дополнительными факторами риска развития явного сахарного диабета 2 типа, такими как:
— Возраст менее 60 лет;
— Индекс массы тела (ИМТ) ≥ 30кг/м:;
— Гестационный сахарный диабет в анамнезе;
— Семейный анамнез сахарного диабета у родственников первой степени;
— Повышенная концентрация холестерина ЛПВП;
— артериальная гипертензия.
— Метформин не влиял на фертильность самцов и самок крыс при применении в дозах, втрое превышающих максимальную рекомендованную суточную дозу для человека.
Метформин: новые преимущества в свете доказательной медицины
Более 50 лет метформин используется для лечения сахарного диабета типа 2. Его эффективность и высокий профиль безопасности доказаны результатами Британского проспективного исследования сахарного диабета. Сегодня метформин является препаратом первой линии у данной категории больных. Установлено, что помимо антигипергликемического метформин обладает и другими эффектами. Например, способен ингибировать пролиферацию опухолевых клеток и в условиях in vivo
, и в условиях
in vitro
, а также замедлять процессы старения. Однако для подтверждения этих эффектов необходимо проведение дальнейших исследований.
Введение
Бигуаниды для лечения сахарного диабета (СД) используются более 50 лет. Основными представителями этой группы препаратов являются метформин и фенформин. Однако фенформин был отозван из-за увеличения риска развития лактатацидоза на фоне его приема. Метформин повышает окисление лактата, но при этом не изменяет его высвобождение из мышц или плазменную концентрацию [1, 2]. В связи с этим лактатацидоз, индуцированный метформином, встречается крайне редко.
С 2005 г. метформин является препаратом первой линии фармакологического лечения СД типа 2 (СД 2) согласно рекомендациям Международной диабетической федерации (International Diabetes Federation – IDF), с 2006 г. – препаратом первой линии в комплексе с нефармакологическими методами лечения согласно рекомендациям Американской диабетической ассоциации (American Diabetes Association – ADA) и Европейской ассоциации по изучению диабета (European Association for the Study of Diabetes – EASD).
В настоящее время метформин – наиболее часто назначаемый пероральный сахароснижающий препарат во многих странах мира [3]. Именно поэтому особый интерес представляют данные о новых свойствах препарата [4].
Механизм действия
Механизм антигипергликемического действия метформина достаточно хорошо изучен. Установлено, что препарат не влияет на секрецию инсулина бета-клеткой, его воздействие экстрапанкреатическое. Метформин вызывает:
- снижение всасывания углеводов в кишечнике;
- повышение превращения глюкозы в лактат в желудочно-кишечном тракте;
- усиление связывания инсулина с рецепторами;
- экспрессию гена – транспортера глюкозы (ГЛЮТ) 1 (секреция);
- усиление транспорта глюкозы через мембрану в мышцах;
- перемещение (транслокацию) ГЛЮТ-1 и ГЛЮТ-4 из плазменной мембраны к поверхностной мембране в мышцах;
- снижение глюконеогенеза;
- гликогенолиза;
- уровня триглицеридов и липопротеинов низкой плотности;
- повышение уровня липопротеинов высокой плотности.
Действие метформина направлено на преодоление резистентности периферических тканей к инсулину, прежде всего мышечной и печеночной.
Важной мишенью метформина является аденозинмонофосфат-активируемая протеинкиназа (АМФК) – клеточный энергетический сенсор, активирующийся при метаболическом стрессе. В результате активации АМФК ингибируется продукция глюкозы печенью, повышается чувствительность к инсулину и поглощение глюкозы мышцами, а также происходит окисление жирных кислот. Для этого необходимо фосфорилирование треонина-172, ответственной киназой считается ген LKB1. Нижестоящая цель АМФК – «мишень рапамицина у млекопитающих». Это киназа, которая регулирует клеточный рост и ингибируется АМФК, что приводит к снижению синтеза белка [5].
АМФК может быть активирована физическими нагрузками, гормонами, цитокинами и лекарственными препаратами [5].
Активация АМФК на фоне приема метформина носит время- и дозазависимый характер. Она приводит к ингибированию продукции глюкозы печенью, увеличению поглощения ее мышцами, ингибированию ацетил-КоА-карбоксилазы и снижению экспрессии синтетазы жирных кислот в гепатоцитах крыс [6] и, возможно, увеличению утилизации глюкозы печенью через инсулиннезависимые пути [7]. Активация АМФК метформином, по всей видимости, не зависит от изменения соотношения аденозинмонофосфат/аденозинтрифосфат (АМФ/АТФ) [7, 8] вследствие ингибирования комплекса митохондриальной дыхательной цепи и увеличения активных форм азота [8, 9]. В то же время исследование на мышах показало, что метформин может ингибировать глюконеогенез по АМФК-независимому пути – через изменение соотношения АМФ/АТФ [10].
Еще один возможный механизм антигипергликемического действия – влияние на инкретиновые пути. A. Maida и соавт. установили, что метформин резко повышал уровень глюкагоноподобного пептида 1 (ГПП-1) у мышей без сопутствующего введения глюкозы, но не влиял на другие кишечные пептиды, такие как пептид YY и глюкозозависимый инсулинотропный полипептид. При этом метформин снижал скорость опорожнения желудка и улучшал толерантность к глюкозе, но это действие не было опосредовано ГПП-1 [11]. Влияние метформина на активность дипептидилпептидазы 4 не установлено [11].
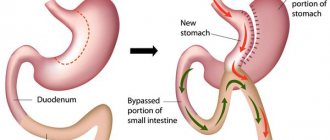
Метформин изменяет метаболизм желчных кислот, влияя на увеличение дыхательного СО14 и фекального СО14 у больных СД 2 после введения СО14-гликохолата [12]. Исследования на животных показали, что это действие, вероятно, связано с уменьшением абсорбции солей желчных кислот в подвздошной кишке [13] за счет уменьшения активного транспорта независимо от Na-K-АТФазы [14]. Это могло бы объяснить желудочно-кишечные эффекты метформина и его гиполипидемические свойства. Следовательно, он может быть вовлечен в контроль глюкозы, так как желчные кислоты активируют сопряженный с G-белком рецептор TGR5, который способен стимулировать высвобождение ГПП-1 из L-клеток [15]. В исследовании M.E. Patti и соавт. отмечено, что у пациентов, перенесших шунтирование желудка, был более высокий уровень желчных кислот по сравнению с пациентами с избыточной массой тела или ожирением и этот уровень положительно коррелировал с постпрандиальным пиком ГПП-1 и отрицательно с уровнем глюкозы. Следовательно, желчные кислоты могут стимулировать ГПП-1 [16].
Антигипергликемический эффект метформина можно объяснить и его влиянием на изменение островковых амилоидных отложений. Известно, что отложение амилоида приводит к уменьшению массы бета-клеток, которое является обычным при СД 2. В исследовании на трансгенных мышах (экспрессирующих островковый амилоидный пептид) метформин снижал распространенность и тяжесть островкового амилоидоза, хотя и не влиял на образование амилоида. Установлено, что этот эффект может быть связан с изменениями жировой массы тела и секреции инсулина [17].
Британское проспективное исследование сахарного диабета
Наиболее полная оценка лечения метформином по сравнению с другими видами лечения дана в Британском проспективном исследовании сахарного диабета (United Kingdom Prospective Diabetes Study – UKPDS). В работу были включены пациенты с впервые выявленным СД 2 в период 1977–1991 гг. Количество участников – 5102. Из них 59% мужчин и 41% женщин. Индекс массы тела больных – 28 кг/м2, уровень гликемии натощак (медиана) – 11,5 ммоль/л, гликированного гемоглобина (медиана) – 9,1%. Повышенное артериальное давление (АД) отмечено у 39% пациентов.
Основная идея UKPDS – изучить влияние гипергликемии, повышенного уровня АД и основных методов их коррекции на развитие осложнений СД. Исследование состояло из двух частей: изучение контроля гликемии и контроля АД. Изучение контроля гликемии преследовало две задачи: первая – оценить, может ли улучшение уровня глюкозы крови при СД 2 предотвратить развитие клинических осложнений заболевания, вторая – оценить, имеет ли какие-либо преимущества/недостатки терапия препаратами сульфонилмочевины (генерации I или II), инсулином или метформином.
Через три года на фоне применения метформина было достигнуто такое же снижение уровня глюкозы плазмы натощак и гликированного гемоглобина, как и на фоне применения производных сульфонилмочевины или инсулина. Кроме того, метформин снижал уровень инсулина плазмы натощак и не повышал массу тела [18]. Терапия метформином сопровождалась меньшей частотой гипогликемических эпизодов по сравнению с терапией препаратами сульфонилмочевины и инсулином, однако по сравнению с диетотерапией была выше [19].
Десятилетний анализ показал, что в группе метформина достигнут сопоставимый с другими группами гликемический контроль без значимых различий в массе тела, но при более низком уровне инсулина плазмы натощак и меньшей частоте гипогликемических эпизодов (по сравнению с группами производных сульфонилмочевины и инсулина) [20].
При оценке влияния терапии на развитие осложнений СД в группе метформина был ниже риск любой связанной с заболеванием конечной точки (32%): связанных с диабетом смертей (42%), общей смертности (36%), инфаркта миокарда (39%) и всех макрососудистых заболеваний (30%) – по сравнению с группой диетотерапии. В группе метформина по сравнению с группой традиционной терапии отмечен более низкий риск прогрессирования ретинопатии. В отношении нефропатии существенных различий не выявлено. При сравнении с группами производных сульфонилмочевины и инсулина в группе метформина достоверно более низкими были только риски связанных с диабетом конечных точек и смерти от всех причин [20].
Преимущества метформина оценивались только у пациентов с избыточной массой тела. Результаты наблюдательного ретроспективного исследования, в котором анализировалась база данных пациентов, получавших метформин или производные сульфонилмочевины не менее шести месяцев, свидетельствовали, что метформин может быть так же эффективен, как и сульфонилмочевина, у пациентов с ожирением и без ожирения [21].
Таким образом, UKPDS доказало, что метформин столь же эффективен в отношении контроля гликемии, как производные сульфонилмочевины и инсулин, при более низком риске развития гипогликемии.
Метформин и рак
В последние годы активно изучается способность метформина снижать риск злокачественных новообразований или смерти от них у больных СД 2.
По данным эпидемиологических исследований, проведенных за последние десятилетия, лица, страдающие СД (в первую очередь СД 2), в большей степени предрасположены к развитию рака. Чаще у них диагностируется рак печени, почек, поджелудочной и молочной железы, колоректальный рак и рак тела матки. Необходимо отметить, что величина относительного риска варьируется в зависимости от локализации опухоли – от 1,4 до 4,5 [22–24]. Это может быть объяснено гиперинсулинемией и инсулинорезистентностью, характерными для СД 2. Известно, что инсулин обладает митогенными эффектами.
J.M. Evans и соавт. (2005) впервые обратили внимание на то, что прием метформина может снижать риск злокачественных новообразований [25]. Так, анализ базы данных 11 876 жителей района Тейсайд (Шотландия), заболевших СД 2 с 1993 по 2001 г., показал, что 923 человека не менее чем через год после постановки диагноза были госпитализированы по поводу рака. Средний возраст пациентов – 73 года, длительность СД – 8,4 года. Последующий анализ, учитывающий и некоторые «мешающие» факторы (курение, индекс массы тела, АД и др.), свидетельствовал, что у больных, получавших метформин, относительный риск злокачественных новообразований снижался на 23% по сравнению с больными, не принимавшими этот препарат. Данные о локализации опухолей авторы не приводили.
В другом эпидемиологическом исследовании S.L. Bowker и соавт. (2006) показали, что частота смерти, ассоциированной с раком, была значительно ниже в группе метформина по сравнению с группой производных сульфонилмочевины [26].
Наконец, в работе G.W. Landman и соавт. (2010) отмечено, что у 1353 больных СД, наблюдавшихся в среднем 9,5 года, смертность от злокачественных новообразований, природа которых не уточнялась, среди принимавших метформин была достоверно ниже, чем среди тех, кто данное средство не использовал. Указанный эффект был тем выше, чем больше была суточная доза препарата [27].
Эпидемиологические данные стали поводом для изучения роли метформина при различных типах рака.
В ретроспективное когортное исследование, проведенное в США, было включено 191 233 больных СД. Средний возраст – 56 лет, 49% женщин. В среднем за 3,9 года наблюдения выявлено 813 случаев рака. Среди пациентов была выделена группа получавших монотерапию метформином. В данной группе влияние приема препарата на риск развития рака мочевого пузыря не зафиксировано, однако отмечена тенденция к повышению риска развития рака поджелудочной железы и снижению риска развития колоректального рака и рака печени [28]. В двух других, относительно немногочисленных по количеству пациентов, исследованиях, проведенных в США и Италии, на фоне приема метформина, наоборот, наблюдалось снижение риска развития рака поджелудочной железы [29] и подтверждено снижение риска развития гепатобластомы – по большей части за счет мужчин [30]. В исследовании J.L. Wright и соавт. прием метформина ассоциировался со снижением риска развития рака предстательной железы у пациентов европеоидной расы [31]. Еще один важный, но не понятный до конца факт – отсутствие влияния метформина на риск развития рака молочной железы [28, 32], чего можно было ожидать на основании некоторых предклинических испытаний и что может объясняться различными причинами [33, 34].
Тем не менее в работе G. Libby и соавт. (длительность наблюдения – 10 лет) применение метформина больными СД (свыше 4000 человек) привело к уменьшению на 37% риска развития новообразований в целом и опухолей легких, толстой кишки и молочной железы в частности [35].
Исследования в условиях in vitro
и с участием животных подтверждают, что метформин может предотвращать развитие рака.
Метформин и старение
Исследовательская группа Левенского католического университета (Бельгия) продемонстрировала, что метформин способен приостанавливать процесс старения организма и продлевать жизнь. Ученые провели серию экспериментов с круглыми червями (Caenorhabditis elegans). Указанный вид служит идеальной моделью для изучения процессов старения, поскольку продолжительность жизни его представителей всего три недели. В ходе работы установлено, что метформин повышал количество токсичных соединений, высвобождаемых из клеток. Возможно, именно это увеличивало продолжительность жизни червей. «По мере старения черви становятся меньше, сморщиваются и начинают мало двигаться. Но черви, которым мы давали метформин, демонстрировали очень ограниченное уменьшение в размере и не сморщивались. Они не только медленнее старели, но и дольше оставались здоровыми», – отметил автор исследования W. de Haes. Такое действие метформина ученые объясняют тем, что клетки тела получают энергию из митохондрий – микроскопических «электростанций», которые генерируют очень слабый электрический ток. Этот процесс сопровождается образованием высокоактивных форм кислорода (радикалов). Они способны повреждать протеины и ДНК, мешая нормальному функционированию клеток. Однако в маленьких концентрациях эти молекулы могут быть полезны. Метформин вызывает незначительное увеличение их количества.
В Национальном институте старения США установили, что метформин повышает продолжительность жизни лабораторных мышей. Средняя продолжительность жизни животных – 150 дней. На фоне приема метформина она увеличилась в среднем до 160 дней. При этом у животных, получавших метформин, физическая форма была значительно лучше, а также ощутимо снижался риск развития возрастной катаракты.
Однако биомолекулярный механизм описанного действия препарата не установлен. Отмечается лишь сходство с действием низкокалорийной диеты. В результате торможения транспорта электронов дыхательной цепи митохондрий уменьшается концентрация внутриклеточной АТФ и запускается анаэробный гликолиз. Это способствует уменьшению окисления жиров метформином и синтеза свободных жирных кислот.
Для того чтобы добиться такого действия, ученым пришлось значительно увеличить дозу препарата (пропорционально человеческой), что может оказать токсическое воздействие на организм.
Директор Национального института старения США R. Hodes так прокомментировал полученные результаты: «Существует повышенный интерес к препаратам, которые можно переориентировать на другие цели. Это потрясающий успех – открыть, что давно используемый лекарственный препарат можно использовать для чего-то еще, например для здорового старения».
Заключение
На сегодняшний день метформин является основным препаратом для лечения СД 2. Хотя в клинической практике он используется более 50 лет, интерес к препарату не ослабевает. Во многих исследованиях последнего десятилетия, посвященных различным аспектам применения метформина, демонстрируется уникальность препарата, раскрываются его потенциал и новые возможности для применения.
Введение
Сахарный диабет (СД) – острейшая медико-социальная проблема современности, касающаяся многих людей, поскольку рост заболеваемости позволил говорить о глобальной эпидемии диабета. По данным Международной федерации диабета (IDF), на 2022 г. в мире насчитывают 425 млн больных СД [1]. На долю СД 2 типа (СД2) приходится 90% случаев заболевания. При недостаточно эффективном лечении СД2 может значительно ограничивать жизнь пациентов, приводить к ранней инвалидизации и преждевременной смертности из-за развития сосудистых осложнений, которые и определяют тяжесть недуга и ущерб, причиняемый обществу. Последствия СД обусловливают огромные экономические затраты для систем здравоохранения, поскольку около 80% затрат на лечение СД связано именно с терапией сосудистых осложнений. Так, присоединение диабетических осложнений в среднем удорожает лечение в 3–10 раз [2].
Среди патогенетических механизмов развития гипергликемии инсулинорезистентность (ИР) играет ключевую роль, поэтому неудивительно, что успехи, достигнутые в лечении СД, в значительной мере связаны с использованием лекарственных средств, улучшающих чувствительность к инсулину [3]. Установлена существенная роль ИР в преждевременном развитии сердечно-сосудистых заболеваний (ССЗ), связанных с атеросклерозом, а также в повышении риска острых макроваскулярных осложнений вне зависимости от других значимых факторов риска, включая гипергликемию, дислипидемию, курение [4, 5].
Выбор ИР, ключевого патофизиологического звена СД2, в качестве стратегической мишени лечения позволяет улучшать чувствительность к инсулину и позитивно воздействовать на сопутствующие метаболические нарушения. Фармакологическая коррекция ИР увеличивает эффективность сахароснижающей терапии, направленной на другие патофизиологические звенья развития СД2 [6–8]. Выраженным ингибирующим воздействием на ИР обладают бигуаниды. История их применения началась еще в средние века с применения гуанидина, который получали из растения Galega officinalis (галега лекарственная, французская лилия). Однако выраженная токсичность препятствовала клиническому применению этого вещества [9].
В настоящее время метформин является единственным бигуанидом, рекомендованным для фармакотерапии больных СД2. Благодаря высокой клинической эффективности, уникальным терапевтическим свойствам, хорошему профилю безопасности, доказанными в клинических исследованиях и подтвержденными многолетним опытом применения, в современных клинических рекомендациях метформин закрепил ведущую позицию в лечении СД2 (при условии отсутствия противопоказаний к нему) и применяется на всех этапах течения заболевания [8, 10, 11]. Впервые клинические эффекты метформина были представлены после завершения многолетнего исследования UKPDS (United Kingdom Prospective Diabetes Study) в 1998 г. [12]: снижение риска сосудистых осложнений на 32%, инфаркта миокарда на 39%, смертности от диабета на 42% и общей смертности на 36%. С 2005 г. метформин считается препаратом первой линии фармакологического лечения СД2 в комплексе с нефармакологическими методами, согласно рекомендациям IDF, с 2006 г. – согласно рекомендациям Американской диабетической ассоциации (American Diabetes Association – ADA) и Европейской ассоциации по изучению диабета (European Association for the Study of Diabetes – EASD) [13].
Механизм действия и сахароснижающий (антигипергликемический) эффект метформина
Антигипергликемические эффекты метформина – это результат воздействия препарата на тканевую чувствительность к инсулину. Хотя преобладающим является влияние метформина на гепатическую продукцию глюкозы, именно комбинация эффектов на уровне печени, мышечной и жировой тканей в целом обеспечивает благоприятный фармакологический профиль [6, 7, 9]. Известно, что последствия избыточной эндогенной продукции глюкозы печенью особенно неблагоприятны ввиду стимуляции процессов атерогенеза и развития резистентности к действию сахароснижающих препаратов в течение дня. В частности, при повышении концентрации глюкозы крови натощак (ГКН) >6,1 ммоль/л риск развития сердечно-сосудистых событий в последующие 12,4 года возрастает в 1,33 раза [14]. Применение метформина приводит к снижению на 25–30% уровня ГКН, постпрандиальной гликемии (табл. 1) [8, 13].
За антитипергликемический эффект метформина ответственны несколько механизмов, причем основное его действие осуществляется на уровне митохондрий гепатоцитов [9, 13]. Молекулярной мишенью действия метформина служит аденозинмонофосфат-активируемая протеинкиназа (АМФК), известная как ключевой фермент клеточного метаболизма и энергетического баланса (см. рисунок). Опосредованная метформином активация АМФК приводит к восстановлению энергетического гомеостаза путем увеличения поглощения глюкозы в скелетных мышцах и подавления глюконеогенеза в печени [15, 16]. Под воздействием метформина активируется сигнальный путь печеночной киназы В1(LKB1)/AMФK; в котором LKB1 является восходящим активатором AMФK, отвечающим за фосфорилирование Thr 172 каталитической α-субъединицы этой киназы. Активация АМФК вторична по отношению к влиянию метформина на митохондриальную дыхательную цепь. Как наиболее вероятный механизм, объясняющий активацию AMФK, рассматривается следующий. АМФК активируется путем фосфорилирования LKB1-киназы в ответ на повышение соотношения АМФ/АТФ внутри клетки посредством ингибирования митохондриальной дыхательной цепи и увеличения активных форм азота под влиянием метформина. Активация АМФК подавляет экспрессию генов, отвечающих за ферменты глюконеогенеза [15, 17].
Усиливаются эффекты инсулина на транскрипцию, трансляцию и синтез фосфатидилинозитол-3-киназы, ответственной за транслокацию переносчиков глюкозы к плазматической мембране, что приводит к увеличению поглощения глюкозы печеночными, мышечными и жировыми клетками [6, 8]. Параллельно с этим происходит окисление жирных кислот.
В мышечной и жировой ткани метформин повышает связывание инсулина с рецепторами, также наблюдается повышение их числа и аффинности. Кроме того, происходит активирование пострецепторных механизмов действия инсулина, в частности тирозинкиназы и фосфотирозин фосфатазы [7, 10].
Изучение клеточно-молекулярных механизмов, лежащих в основе действия метформина, показало, что ингибирование экспрессии генов глюконеогенеза не единственный механизм гепатических эффектов метформина (AMPK-независимые механизмы) [17]. Другая концепция основывается на тесной взаимосвязи энергетического профиля гепатоцитов и гепатической продукции глюкозы – процесса энергозатратного. На фоне снижения уровня АТФ, вызываемого метформином, гепатоцитам приходится, соответственно, уменьшать продукцию глюкозы [18].
Заслуживает обсуждения и еще один механизм антигипергликемического действия препарата. Метформин модулирует активность инкретиновой оси и повышает уровень глюкагоноподобного пептида-1 (ГПП-1) [17, 19, 20]. Существует несколько гипотез по поводу того, как метформин способствует секреции ГПП-1. В частности, метформин стимулирует секрецию ГПП-1 через активацию Wnt-сигнальных путей в L-клетках кишечника у мышей линии db/db. Кроме того, стимулирует экспрессию генов, кодирующих рецепторы ГПП-1 и глюкозозависимый инсулинотропный полипептид (ГИП) в островках Лангерганса, увеличивает экспрессию генов белков-предшественников – преглюкагона, проглюкагона [19]. Данные относительно влияния метформина на активность дипептидилпептидазы-4 (ДПП-4) противоречивы. В исследованиях in vivo в отличие от in vitro показано, что применение метформина ассоциируется со снижением уровня ДПП-4 (возможно, через влияние на гепатическую продукцию ДПП-4).
Есть мнение о непрямых действиях метформина на секрецию ГПП-1, которые опосредуются изменением энтерогепатической циркуляции желчных кислот. Метформин подавляет ядерные фарнезоидные Х-рецепторы (FXR) AMPK-зависимым механизмом. Выступая как АМРК-активатор, метформин подавляет транскрипционную активность FXR. В результате снижается кишечная абсорбция желчных кислот и возрастает их пул в подвздошной кишке. Желчные кислоты являются естественными лигандами мембранного рецептора желчных кислот или TGR5 энтерохромофинных клеток кишечника. В свою очередь стимуляция TGR5 индуцирует секрецию ГПП-1 L-клетками. Активация TGR5 увеличивает расход энергии и потребление кислорода, тем самым улучшая чувствительность к инсулину [21].
Метформин и функция β-клеток
СД2 считается хроническим прогрессирующим заболеванием, поэтому крайне важно сохранение функциональной активности β-клеточного аппарата поджелудочной железы [22]. Принципиально важно, что, повышая печеночную и периферическую чувствительность к инсулину, метформин не влияет на секрецию инсулина [6, 10, 17]. Вместе с тем повышая чувствительность тканей к действию инсулина, снижая глюко- и липотоксичность, препарат опосредованно улучшает секрецию инсулина и способствует сохранению функциональной активности β-клеток. Благодаря всем указанным эффектам метформина снижение уровня глюкозы происходит без риска гипогликемических состояний, что считается несомненным достоинством препарата [23].
В этом плане интересны результаты ретроспективного исследования S.A. Berkowitz и соавт., в котором была проанализирована сахароснижающая терапия на этапе ее инициации и интенсификации с оценкой данных более чем 15,5 тыс. пациентов [24]. Согласно дизайну, пациентов, которым впервые назначались пероральные сахароснижающие препараты (ПСП) в период с 2009 по 2013 г., классифицировали в зависимости от получаемого лечения на несколько групп: только метформин или препараты сульфонилмочевины (ПСМ), или тиазолидиндионы, или только ингибиторы ДПП-4.
Целью данного исследования стало определить время интенсификации терапии (путем добавления другого сахароснижающего средства, включая инсулин) у пациентов с СД2, которым впервые были назначены ПСП. Как оказалось, несмотря на существующие алгоритмы лечения СД2, только 57,8% пациентов начинали терапию заболевания с приема метформина. С помощью регрессионного анализа Кокса в обширной популяции пациентов авторами показано, что старт терапии с метформина ассоциировался с меньшей необходимостью интенсификации терапии в будущем по сравнению с другими ПСП (табл. 2). В частности, доля пациентов, которым потребовалось назначение второго сахароснижающего средства и получавших на старте терапии метформин, составила 24,5%, ингибиторы ДПП-4 – 36,2%, ПСМ – 37,1%, тиазолидиндионы – 39,6%.
Снижая концентрацию и окисление свободных жирных кислот (СЖК) на 10–17 и 10–30% соответственно, активизируя их реэстерификацию, метформин не только улучшает тканевую чувствительность к инсулину, но и препятствует прогрессированию нарушений секреции инсулина у больных СД2 [7, 10, 13]. Последствия избыточной продукции СЖК сводятся к нарушению их компенсаторного окисления. Как следствие – к активации неокислительных путей метаболизма с образованием метаболитов, оказывающих липотоксическое действие на ткани (печень, сердце, мышечная ткань, поджелудочная железа). В частности, избыток СЖК подавляет активность пируватдегидрогеназы, нарушает транспорт и фосфорилирование глюкозы в скелетных мышцах. Повышенная концентрация СЖК на уровне печени стимулирует глюконеогенез. В свою очередь нормализация концентрации СЖК на фоне применения метформина приводит к устранению эффектов липотоксичности на всех уровнях, включая печень, жировую и мышечную ткани и островки Лангерганса. Снижение поступления СЖК к печени, синтеза триглицеридов и повышение чувствительности к инсулину сопровождаются уменьшением отложения жира в этом органе [17, 18].
Как известно, глюкозотоксичность служит ключевым фактором прогрессирования дисфункциb β-клеток [22]. Оказывая влияние на всасывание углеводов в желудочно-кишечном тракте, замедляя его скорость, а также снижая аппетит, метформин способствует уменьшению постпрандиальной гликемии, что также способствует устранению глюкозотоксичности. Кроме того, метформин повышает утилизацию глюкозы в кишечнике, усиливая в нем анаэробный гликолиз как в состоянии насыщения, так и натощак. В результате на фоне терапии метформином постпрандиальная гликемия снижается в среднем на 20–45% [17, 23].
Метформин и масса тела
Важной задачей лечения СД2 является снижение и поддержание нормальной массы тела. Согласно данным клинических исследований, терапия метформином препятствует увеличению массы тела либо способствует ее снижению, в т.ч. и в комбинации с инсулином. В зависимости от длительности приема препарата снижение массы тела у больных СД2 составляет от 0,5 до 6,0 кг [9, 10, 13]. Это остается значимым преимуществом препарата, поскольку применение ПСМ обычно вызывает увеличение массы тела. Интересный факт: терапия метформином сопровождается снижением висцерального отложения жира, которое является независимым фактором ССЗ [25].
Потенциальное влияние метформина на массу тела обусловлено несколькими механизмами, в т.ч. снижением концентрации инсулина, увеличением секреции ГПП-1. Согласно результатам экспериментальных исследований на животных моделях, метформину присущ анорексигенный эффект, по-видимому опосредованный центральным действием препарата на уровне гипоталамических нейронов [26]. Улучшение чувствительности к инсулину на фоне метформина устраняет причину для гиперинсулинемии, что также способствует снижению аппетита и уменьшению потребления энергии (в среднем – 104,5 ккал/сут) [27].
Применение метформина сопровождается подавлением выработки орексигенного пептида грелина, повышением концентрации ГПП-1, обладающего анорексигенным действием, что отчасти объясняет некоторые метаболические эффекты [17, 20, 25]. Кроме того, модулируя экспрессию орексигенного нейропептида Y, препарат способствует снижению массы тела [28].
Внегликемические эффекты метформина
В настоящее время немалое внимание уделяется внегликемическим эффектам сахароснижающей терапии, поскольку важно не только достигать контроля гликемии, но и воздействовать на другие модифицируемые факторы риска развития сердечно-сосудистой патологии для улучшения прогноза жизни.
Оценивая эффективность метформина, чаще обращаются к гликемическому контролю, однако немалое значение приобретают и иные эффекты (гиполипидемические, вазопротекторные и др.) препарата [6, 7, 10]. Примерно половина пациентов с СД2 имеют атерогенную дислипидемию, что неблагоприятно влияет на кардиоваскулярный прогноз. Эффекты метформина в отношении метаболизма липидов плазмы обусловлены его гиполипидемическим и антиатерогенным действиями. Как уже говорилось, метформин активирует АМФК, в результате подавляется экспрессия генов липидного метаболизма, таких как синтетазы СЖК (G001196), ацетил-CoA-карбоксилазы (G000684), S14, белка, связывающего стерол-регулирующий элемент – 1 (SREBP-1c) [29]. Помимо сказанного метформин влияет на процесс биосинтеза мононенасыщенных жирных кислот из насыщенных жирных кислот через АМФК-опосредованное фосфорилирование рецептора тиреоидных гормонов 4 (TR4) [17].
Кроме влияния на метаболизм СЖК лечение метформином ассоциируется с позитивными изменениями в липидном спектре; в частности снижением на 10–20% концентрации триглицеридов, на 10% – липопротеидов низкой плотности и повышением на 10–20% концентрации липопротеидов высокой плотности [13, 17, 23]. Подобные эффекты служат дополнительным преимуществом метформина с позиции основной цели терапии СД2 – снижение кардиоваскулярной заболеваемости и смертности.
Информация была бы неполной, если не привести результаты экспериментальных работ, свидетельствующие о влиянии метформина на метаболизм липидов сосудистой стенки. В частности, препарат снижает аккумуляцию эфиров холестерина в аорте, увеличивает содержание фосфолипидов и уменьшает содержание сфингомиелина. Наряду с этим метформин уменьшает пролиферацию гладкомышечных клеток (ГМК) сосудов. Снижая отложение липидов в сосудистой стенке, уменьшая пролиферацию ГМК, нарушая адгезию, трансформацию моноцитов и способность захватывать липиды, метформин активно воздействует на ранние стадии развития атеросклероза [30]. Следует отметить, что, подавляя повышенную адгезию моноцитов к эндотелию сосудов, липоидоз, метформин влияет на пусковые механизмы развития атеросклеротического поражения, снижает экспрессию рецепторов, вовлеченных в процессы внутриклеточного накопления липидов [31]. Кроме того, метформин подавляет процессы дифференциации моноцитов в макрофаги, активно секретирующие проатерогенные факторы. In vitro показано ингибирующее влияние метформина на лейкоцит-эндотелиальное взаимодействие, а также экспрессию на поверхности эндотелия таких молекул адгезии, как внутриклеточная молекула адгезии 1, сосудисто-клеточная молекула адгезии 1 и Е-селектин [10, 31].
Дополнительные кардиопротективные эффекты метформина обусловлены и его влиянием на систему гемостаза, реологию крови (антитромбическое действие), функцию эндотелия и сосудистую реактивность (табл. 3).
В частности, метформин снижает уровень маркеров активации тромбоцитов (тромбоцитарного фактора 4 и β-тромбоглобулина), концентрацию ингибитора активатора плазминогена-1, выработку молекул адгезии и фибриногена, тормозит активность XIII и VII факторов свертывания [8, 13, 30].
Вазопротективные свойства метформина многоплановые: нормализация цикла сокращение/расслабление артериол, уменьшение проницаемости сосудистой стенки и торможение процессов неоангиогенеза, улучшение эндотелийзависимой вазодилатации и транспорта глюкозы в эндотелиоцитах, ГМК сосудов, а также в миокарде [23, 32].
Метформин обладает прямым противовоспалительным действием на сосудистую стенку, что в основном обусловлено подавлением сигнальных путей образования NF-kB, активация которого приводит к инициации транскрипции генов ряда цитокинов и молекул адгезии [17].
В совокупности гликемические эффекты и дополнительные свойства (антисклеротические, вазопротективные, антивоспалительные, антиоксидантные) метформина важны для снижения риска возникновения ССЗ и увеличения продолжительности жизни пациентов с СД2. В настоящее время СД2 рассматривается как эквивалент наличия у больного клинически выраженного ССЗ, что выдвигает серьезные требования к долгосрочной кардиоваскулярной безопасности сахароснижающих препаратов [5]. Хорошая иллюстрация кардиопротективных свойств метформина – это результаты исследования UKPDS, касающиеся общих и сердечно-сосудистых исходов. Впервые благоприятное воздействие метформина на частоту развития ССЗ у больных СД и ожирением установлено в исследовании UKPDS [12]. В дальнейшем и другие исследования показали снижение сердечно-сосудистой и общей смертности среди больных СД2, получавших метформин в монотерапии или в комбинации с другими сахароснижающими препаратами [33–35]. В частности, результат Канадского ретроспективного анализа базы данных пациентов (Saskatchewan Health databases, n=12 272) показал значительное сокращение общей и сердечно-сосудистой смертности на 40 и 36% соответственно [33]. В исследовании PRESTO (Prevention of Restenosis with Tranilast and its Outcomes) применение метформина ассоциировалось с улучшением прогноза – снижением риска развития всех клинически значимых событий (28%), инфаркта миокарда (69%) и смертности от всех причин (61%) [34].
Недавно были опубликованы результаты ретроспективного анализа сердечно-сосудистой безопасности 12 020 тыс. пациентов с СД2 (the UK Clinical Practice Research Datalink), которым начиная с 2000 г. была назначена инсулинотерапия [35]. Первичной конечной точкой исследования была смертность от любой причины, вторичная конечная точка включала инфаркт миокарда и инсульт. В результате применение инсулина в комбинации с метформином ассоциировано с 40%-ным снижением риска смерти от всех причин по сравнению с монотерапией инсулином (отношение рисков – ОР=0,60, 95% доверительный интервал [ДИ] – 0,52–0,68). Среди пациентов, получавших инсулин в комбинации с метформином, по сравнению с пациентами на монотерапии инсулином (n=6484) отмечено снижение риска инфаркта миокарда, инсульта на 25% (ОР=0,75, 95% ДИ – 0,52–0,68).
В научных публикациях появляется все больше информации о новых мишенях метформина. Стало очевидным, что метаболические эффекты метформина отчасти связаны с изменением кишечной микробиоты [17, 20]. В частности, применение метформина сопровождается повышением количества видов бактерий рода Escherichia, Akkermansia muciniphila, Subdoligranulum, в т.ч. бактерий, продуцирующих короткоцепочечные жирные кислоты (бутират), которые стимулируют синтез инкретинов. Микробный анализ показал достоверное снижение потенциала микробиоты к производству бутирата у больных СД2 [33, 37].
Другие области применения метформина
Результаты многочисленных экспериментальных и клинических исследований позволили раскрыть новые аспекты действия метформина, полнее оценить его практическую значимость, а также расширить показания к его назначению [15, 17, 18, 20].
В последние годы большое внимание уделяется антиканцерогенному действию метформина, которое скорее всего осуществляется через активацию АМФК. Это приводит к ингибированию активности M-TOR (mammalian target of rapamycin), центрального регулятора синтеза белка и клеточного роста, с последующим восстановлением чувствительности к инсулину и снижением гиперинсулинемии [17, 39]. Эффект снижения уровня инсулина метформином может играть важную роль в противоопухолевой активности, т.к. инсулин обладает митогенными и пролиферативными свойствами и опухолевые клетки часто экспрессируют высокие уровни рецептора инсулина [38–40]. Метформин является также эффективным в лечении синдрома поликистозных яичников [41].
Практические аспекты применения метформина
Благодаря отсутствию длинных гидрофобных боковых цепей ограничивается как способность препарата к связыванию с клеточной мембраной, так и активное накопление внутри клетки, что определяет низкую вероятность лактат-ацидоза и высокую безопасность терапии метформином [6, 9, 10]. Лечение препаратом инициируют с 500–850 мг, принимаемыми за ужином или на ночь. Во избежание побочных эффектов метформина (диспепсические явления, диарея, абдоминальный дискомфорт) необходима постепенная титрация дозы препарата, увеличение на 500–850 мг каждые 1–2 недели, а в некоторых случаях временное снижение до предыдущей дозы. Побочные эффекты обычно исчезают при снижении дозы препарата. Максимальная рекомендованная доза больным метаболическим синдромом составляет 2500–3000 мг/сут в 2–3 приема.
Прием метформина может быть продолжен до скорости клубочковой фильтрации >45 мл/мин/1,73 м² в отсутствие других противопоказаний:
- заболевания, сопровождающиеся тканевой гипоксией (сердечная или легочная недостаточность, инфаркт миокарда, анемия и др.);
- почечная недостаточность или нарушение функции почек (клиренс креатинина <45 мл/мин/1,73 м²);
- печеночная недостаточность, алкоголизм;
- беременность, лактация;
- острые состояния, которые могут нарушать функцию почек (обезвоживание, острая инфекция, шок, внутрисосудистое введение рентгеноконтрастных средств);
- диабетический кетоацидоз.
Следует воздержаться от назначения препарата в период беременности и лактации.
Результаты клинических исследований свидетельствуют, что метформин снижает уровень гликированного гемоглобина (НbА1с) на 0,6–2,4% [6–9]. Такая вариабельность степени снижения гликемии связана с исходной концентрацией глюкозы в крови до инициации лечения этим препаратом. Отсутствие достижения целевого уровня НbА1с на фоне монотерапии метформином свидетельствует о значительном нарушении секреторной активности β-клеток. В этих случаях необходимо применение комбинации метформина с сахароснижающим препаратом иного механизма действия. Механизм действия метформина позволяет успешно комбинировать метформин со всеми сахароснижающими препаратами (сульфонилмочевиной, меглитинидами, тиазолидиндионами, агонистами ГПП1, ингибиторами ДПП4), что повышает общую терапевтическую эффективность и улучшает гликемический контроль [8, 18, 23]. Отдельно следует отметить, что рациональна комбинация метформина и инсулина, при таком варианте значительно улучшается чувствительность тканей и к экзогенному инсулину. В результате суточная доза инсулина снижается в среднем на 17–30%, уменьшается риск гипогликемий, не увеличивается риск прибавки массы тела [13].
Заключение
Очевидно, что СД2 представляет серьезную проблему здоровья населения Российской Федерации. Решение этой проблемы требует повышения эффективности сахароснижающей фармакотерапии, в которой большое значение имеет применение лекарственных средств, воздействующих на ИР. Метформин – высокоэффективный и безопасный сахароснижающий препарат с обширной доказательной базой и огромным опытом применения в условиях российской клинической практики.
Метформин во время беременности: каких результатов стоит ожидать?
Актуальность
В последние годы повсеместно увеличилось распространение сахарного диабета (СД) 2 типа у беременных женщин.
Инсулинотерапия является стандартом лечения СД во время беременности. Возрастание инсулинорезистентности во время беременности требует увеличения доз инсулина, что в свою очередь сопряжено с прибавкой веса у пациенток, большим количеством болезненных инъекций, большими затратами на лекарственные средства и низким комплаенсом.
На данный момент имеется недостаточно данных об особенностях терапии СД 2 типа метформином у беременных женщин.
Ученые из Канады изучили действие метформина в контексте возможного снижения риска неблагоприятных исходов для матери и плода.
Материалы и методы
Было проведено рандомизированное контролируемое исследование MiTy.
Результаты исследования были представлены на профессиональной конференции Diabetes UK: Online Series 17 ноября и недавно опубликовано в The Lancet Diabetes & Endocrinology.
Было исследовано 502 женщины из 29 центров Канады и Австралии, у которых СД 2 типа был диагностирован до беременности или во время беременности до срока 20 недель гестации.
Пациентки были рандомизированы для приема метформина 1 г два раза в день или плацебо в дополнение к их обычному режиму приема инсулина на сроках от 6 до 28 недель беременности.
Результаты
- СД 2 типа был диагностирован до беременности у 83% женщин в группе метформина и у 90% женщин, получавших плацебо.
- Средний уровень гликированного гемоглобина (HbА1С) при рандомизации составил 47 ммоль / моль (6,5%) в обеих группах.
- Средний возраст матерей составил приблизительно 35 лет, а средний гестационный возраст — 16 недель.
- Средний ИМТ до беременности составил приблизительно 34 кг / м2.
- Примечательно, что только 30% исследуемых принадлежали к европеоидной расе.
- Значительных различий между группами с точки зрения комбинированного первичного исхода в виде невынашивания беременности, преждевременных родов, родовой травмы, респираторного дистресс-синдрома, неонатальной гипогликемии или госпитализации новорожденных в отделение интенсивной терапии продолжительностью более суток не было (P = 0,86).
- Женщины в группе метформина имели значительно меньшую общую прибавку в весе во время беременности, чем женщины в группе плацебо, -1,8 кг (P <0,0001).
- У беременных женщин в группе метформина также был значительно более низкий уровень HbА1С во время беременности — 41 ммоль / моль (5,9%) по сравнению с 43,2 ммоль / моль (6,1%) у тех, кто получал плацебо (P = 0,015); им требовалось меньшее количество доз инсулина, 1,1 по сравнению с 1,5 единицы / кг / день (P <0,0001), что привело к снижению дневной дозы почти на 44 единицы.
- У женщин, получавших метформин, врачи реже прибегали к родовспоможению в виде кесарева сечения: 53,4% против 62,7% в группе плацебо (P = 0,03).
- Значимых различий в отношении гестационной гипертензии или преэклампсии в сравниваемых группах получено не было
- Наиболее часто нежелательные побочные явления возникали со стороны желудочно-кишечного тракта: 27,3% у пациенток в группе метформина и у 22,3%, получавших плацебо.
- Не было значительных различий между группами по показателям невынашивания беременности (P = 0,81), преждевременных родов (P = 0,16), родовых травм (P = 0,37), респираторного дистресс-синдрома (P = 0,49) и врожденных аномалий (P = 0,16).
- Средний вес новорожденных, чьи матери получали метформин, был ниже и составил 3,2 кг по сравнению с 3,4 кг у рожденных от матерей из группы плацебо (P = 0,002).
- У женщин, получавших метформин, также с меньшей вероятностью рождался ребенок с массой тела при рождении 4 кг или более, 12,1% против 19,2%; относительный риск 0,65 (P = 0,046), или ребенок, который был чрезвычайно большим для гестационного возраста, 8,6% против 14,8%; относительный риск 0,58 (P = 0,046).
- Примечательно, что метформин также был связан с повышенным риском рождения детей с малым гестационным возрастом на 12,9% по сравнению с 6,6% в группе плацебо; относительный риск 1,96 (P = 0,03).
Заключение
Метформин в качестве терапии СД 2 типа во время беременности помимо контроля уровня гликемии обладает следующими плейотропными эффектами: снижение массы тела, снижение необходимой дозы инсулина, снижение риска развития большого для гестационного возраста плода.
Задержка внутриутробного развития, курение, серьезная патология почек, низкий индекс массы тела (ИМТ) – факторы риска для развития маленького для гестационного возраста плода на фоне приема метформина у беременных женщин, страдающих СД 2 типа.
Метформин ингибирует путь mTOR, который является первичным сенсором питательных веществ в плаценте и может ослаблять процессы роста плода.
Команда исследователей запустила исследование MiTy Kids, в котором будет проводиться наблюдение за детьми, рожденными от матерей, получавших метформин, чтобы определить, связан ли метформин во время беременности со снижением ожирения и улучшением инсулинорезистентности у детей в возрасте 2 лет.
Если прием метформина был начат до беременности на фоне проблем с фертильностью, его отмена рекомендована сразу после наступления беременности или в течение первого триместра.
medscape.com/viewarticle/941337
Метформин Лонг — старт терапии сахарного диабета 2 типа
Одним из наиболее распространенных заболеваний в современном обществе является сахарный диабет (СД). Медико-социальная значимость СД определяется неуклонным ростом количества больных, высоким риском макро- и микрососудистых осложнений, а также влиянием заболевания на качество и продолжительность жизни пациентов. Аналогичная общемировой тенденция устойчивого роста числа заболевших сахарным диабетом имеет место и в Республике Беларусь. За последние 10 лет количество таких больных в Беларуси увеличилось со 150 тысяч до 336 тысяч человек, 94% которых страдают диабетом 2-го типа (данные по состоянию на 01.01.2019). И ежегодно в стране пациентов с СД 2-го типа становится больше. В настоящее время центральное место во всех актуальных рекомендациях по управлению СД 2-го типа занимает лекарственное средство метформин.
Так, в согласованном алгоритме Американской и Европейской диабетических ассоциаций (ADA/EASD) 2022 г. настоятельно рекомендуется использовать метформин в качестве средства первой линии (при отсутствии противопоказаний или непереносимости), сразу при постановке диагноза СД 2-го типа, в дополнение к коррекции образа жизни (диетические рекомендации и физические упражнения). Предпочтение, отдаваемое этому лекарственному средству, не случайно: эффективность и безопасность метформина имеют огромную доказательную базу, стоимость его невысока, препарат снижает риск развития кардиоваскулярных осложнений, способствует уменьшению веса тела, риск гипогликемии при его приеме минимален. В 2022 г. Американская диабетическая ассоциация выпустила новые рекомендации, согласно которым метформин остается самым предпочтительным лекарственным средством для старта сахароснижающей терапии у пациентов с СД 2-го типа (уровень доказательности А). Однако, к сожалению, переносимость метформина ограничена побочными эффектами со стороны желудочно-кишечного тракта, которые, по некоторым данным, развиваются почти у 25% пациентов, что приводит к прекращению приема препарата 5-10% больных. Кроме того, дробление приема метформина в течение суток и большое количество таблеток при необходимости принимать и другие препараты для лечения сопутствующих заболеваний, создает дополнительные неудобства для пациентов. Недостаточно хорошая переносимость со стороны желудочно-кишечного тракта и необходимость приема более одного раза в сутки приводит к снижению приверженности к терапии метформином у некоторых пациентов. Новая лекарственная форма метформина – пролонгированного действия – создана для обеспечения пролонгированного высвобождения препарата с целью улучшить переносимость и обеспечить продленное действие препарата. Данная лекарственная форма помогает замедлить транзит таблетки из желудка через привратник, посредством чего значительно увеличивается время нахождения препарата в желудке. В исследованиях in vitro показано, что 90% метформина в обычной лекарственной форме высвобождается в течение 30 минут. И напротив, у метформина пролонгированного действия 90% препарата высвобождается в течение 10 часов, относительно независимо от рН и моторики желудочно-кишечного тракта. Таким образом, лекарственная форма Метформин Лонг обеспечивает более медленное, ровное и длительное поступление лекарства без начального быстрого подъема концентрации препарата в плазме. При назначении в вечернее время вместе с едой благодаря своей лекарственной форме Метформин Лонг действует синхронно с естественными физиологическими процессами, когда в ночное время замедляется гастроинтестинальное опорожнение. Это приводит к пролонгированной абсорбции метформина и обосновывает назначение 1 раз в день.
Однако следует иметь в виду и предупреждать пациентов, что неактивная часть таблетки метформина замедленного высвобождения выводится в неизменном виде. Иначе это может привести к ошибочным выводам и немотивированному отказу от использования данной лекарственной формы. Сахароснижающий эффект метформина с модифицированным высвобождением сравним с таковым у метформина немедленного высвобождения. Таким образом, метформин с модифицированным высвобождением, обладая всеми преимуществами обычной формы препарата, лишен значительной части его недостатков: прием метформина пролонгированного действия 1 раз в сутки значительно упрощает схему лечения и совместно со снижением частоты побочных эффектов повышает приверженность пациентов лечению. Метформин Лонг – первый в Республике Беларусь дженерик метформина пролонгированного действия – выпускается Открытым акционерным обществом «Борисовский завод медицинских препаратов» в дозировках 500мг, 750мг и 1000мг. Показанием к применению лекарственных средств Метформин Лонг 500, 750, 1000 является сахарный диабет 2 типа у взрослых (особенно у больных с избыточной массой тела) при неэффективности диетотерапии и физических нагрузок, в качестве монотерапии или в комбинации с другими пероральными гипогликемическими средствами или совместно с инсулином. При монотерапии или комбинированной терапии в сочетании с другими пероральными гипогликемическими средствами лекарственное средство Метформин Лонг применяется следующим образом:
- Рекомендуемая начальная доза – 1 таблетка Метформин Лонг 500 в сутки.
- Через 10-15 дней проведенного лечения дозу необходимо откорректировать в соответствии с результатами измерений уровня глюкозы в сыворотке крови. Медленное увеличение дозы способствует снижению побочных эффектов со стороны пищеварительного тракта. Максимальная рекомендованная доза – 4 таблетки Метформин Лонг 500 в сутки (2000 мг).
- Дозу лекарственного средства рекомендуется принимать 1 раз в сутки во время еды вечером, увеличивая на 500мг каждые 10-15 дней до максимальной дозы 2000 мг. Если при применении Метформин Лонг в максимальной дозе 2000 мг 1 раз в сутки необходимый уровень гликемии не удается достичь, принимаемую дозу можно разделить на 2 приема (утром и вечером во время приема пищи). Если после этого необходимый уровень гликемии не достигается, можно применять метформин в таблетках с немедленным высвобождением в максимальной рекомендованной дозе 3000 мг в сутки.
- Для пациентов, которые уже принимают метформин, начальная доза Метформин Лонг должна быть эквивалентна дозе таблеток с немедленным высвобождением. Пациентам, принимающим метформин в дозе выше 2000 мг, переход на Метформин Лонг не рекомендуется.
- В случае перехода на Метформин Лонг необходимо прекратить прием другого противодиабетического лекарственного средства.
- Метформин Лонг 750 и Метформин Лонг 1000 предназначены для пациентов, которые уже получают метформин в таблетках с немедленным высвобождением.
- Дозы Метформин Лонг 750 или Метформин Лонг 1000 должны быть эквивалентны суточной дозе метформина таблеток с немедленным высвобождением с величиной максимальной дозы 1500 мг или 2000 мг соответственно, которая принимается вечером во время еды.
При комбинированной терапии в сочетании с инсулином Метформин Лонг применяется следующим образом:
- Для достижения лучшего контроля за уровнем глюкозы в крови метформин и инсулин можно применять в виде комбинированной терапии. Обычно начальная доза Метформин Лонг 500 — 1 таблетка в сутки во время еды вечером, дозу инсулина необходимо подбирать в соответствии с результатами измерения уровня глюкозы в крови.
- Для пациентов, уже получавших метформин и инсулин в комбинированной терапии, доза Метформин Лонг 750 или Метформин Лонг 1000 должна быть эквивалентна суточной дозе метформина с величиной максимальной дозы 1500 мг или 2000 мг соответственно, вечером во время еды, в то время как доза инсулина корректируется на основе измерений уровня глюкозы в крови.
- Пожилым пациентам и пациентам со сниженной функцией почек дозу корректируют на основании оценки почечной функции, которую необходимо проводить регулярно.
- Из-за отсутствия данных по применению Метформин Лонг не следует применять у детей до 18 лет.
- Лекарственные средства Метформин Лонг 500, Метформин Лонг 750, Метформин Лонг 1000 отпускаются по рецепту врача.
Правила выписывания рецепта
Метформин отпускают в аптечном пункте при условии предоставления рецепта. Рецепт на латыни Метформина должен быть выписан правильно. Если в документе есть ошибки, он будет отклонен фармацевтом.
На латинском рецепт препарата Метформин позволяет прописать форму лекарственного средства, дозировку, правила приема. Начинается оформление документа со слова Recipe (возьми). Его пишут с новой строчки. Слово Recipe можно сократить следующим образом: Rp. После этого обозначения должна стоять точка и двоеточие (Rp.:).
После слова Recipe пишется название препарата на латинском, дозировка и форма лекарства. В данном случае врач напишет следующее: «Tabulettas Metformini 1.0». Слово Tabulettas можно сократить при помощи обозначения Tab.
После описания дозы, формы и названия лекарства доктор прописывает во второй строчке рецепта количество форм, которые должен выдать фармацевт. Пример: «Da tales doses numĕro 30» — выдай такие дозы числом 30. Это предложение можно сократить следующим образом: D. t. d. N 30.
После количества доз врач прописывает сигнатуру. Сигнатура раскрывает правила применения лекарственного препарата. Начинается третья строчка документа со слова Signa (обозначь). Его сокращают следующим образом: S. В сигнатуре доктор пишет сколько таблеток принимать больному, и как часто. На этом выписывание рецепта заканчивается. После сигнатуры ставят знак — #. Он обозначает, что рецепт закончен.
На латинском рецепт Метформина прописывается так:
- Rp.: Tab. Metformini 1.0
- D.t.d. N 30
- S. По 1 таблетке 2 раза в день во время еды
- #
Побочные действия метформина
- При длительном приеме метформина может наблюдаться снижение всасываемости витамина В12. При обнаружении мегабластной анемии необходимо дополнительное внутримышечное введение витамина В12.
- Довольно часто происходят проблемы с желудочно-кишечным трактом (тошнота, рвота, понос (диарея), вздутие живота, боли в животе, перемена вкусовых ощущений, потеря аппетита). В этом случае метформин следует принимать во время еды, чтобы уменьшить раздражение желудочно-кишечного тракта.
- При длительном применении, а также при приеме метформина с большими дозами спиртного, может появиться лактоацидоз — высокий уровень молочной кислоты в крови, что может угрожать жизни пациента. Возникает чаще при передозировке метформина и у пациентов с почечной недостаточностью.
- Очень редко кожные реакции — эритема, сыпь, зудящие дерматозы.
- Очень редко нарушения функций печени, гепатит, исчезающие при отмене препарата.
Метформин применяется только по назначению врача, и его отпуск предполагается только по рецепту.
Известные механизмы действия метформина
Самым важным действием метформина является подавление выработки глюкозы печенью.
Метформин активирует выделение печеночного фермента АМФК, отвечающего за процессы метаболизма глюкозы и жира. Эта активация ведет к действию подавления на продукцию глюкозы в печени. То есть лишней глюкозы засчет метформина не образуется.
Кроме этого, метформин увеличивает чувствительность к собственному инсулину и повышает периферический захват глюкозы (при помощи инсулина глюкоза доставляется во все клетки организма и становится источником энергии), повышает окисление жирных кислот, уменьшает всасывание глюкозы в желудочно-кишечном тракте.
Задержка метформином всасывания глюкозы в желудочно-кишечном тракте позволяет поддерживать более низкие уровни глюкозы в крови после приема пищи, а также повысить чувствительность клеток-мишеней к собственному инсулину. Это свойство метформина позволяет его использовать при предиабете — для предупреждения диабета при склонности к таковому.
После приема внутрь метформин всасывается в желудочно-кишечном тракте, его активное действие начинается через 2,5 часа. А выводится метформин почками через каких-то 9–12 часов. Надо обратить внимание, что метформин способен накапливаться в печени, в почках и в мышцах.
Применение метформина начинают с приема 500–850 мг 2–3 раза в сутки во время или после еды. Возможно дальнейшее постепенное увеличение дозы в зависимости от результатов анализов концентрации глюкозы в крови.
Поддерживающая доза метформина обычно составляет 1500–2000 мг/сут.
Для уменьшения побочных эффектов со стороны желудочно-кишечного тракта суточную дозу делят на 2–3 приема. Максимальная суточная доза 3000 мг/сут, поделенная на 3 приема.
Оригинальным препаратом метформина является французский Глюкофаж.
Дженерики Глюкофажа: Метформин фирмы Озон (Россия), Сиофор и др.
Все так же для уменьшения побочного действия метформина (желудочно-кишечных расстройств) и улучшения качества жизни пациентов с сахарным диабетом 2 типа во Франции был разработан и выпущен метформин пролонгированного действия под названием Глюкофаж Лонг с замедленным всасыванием активного метформина. Глюкофаж лонг можно принимать 1 раз в сутки, что конечно же, намного удобнее для пациентов.
Всасывание пролонгированного метформина идет в верхних отделах желудочно-кишечного тракта.
Характеристики лекарственного средства
Метформин считается гипогликемическим лекарством, которое часто назначают диабетическим больным. Препарат можно приобрести в аптечном пункте в виде таблетированных форм. Средство имеет среднюю стоимость — 93 – 465 рублей. Аналогами лекарства является Сиофор, Метформин – Тева. Действующей составляющей средства является метформина гидрохлорид. Таблетированные формы могут иметь следующие дозировки: 500 мг, 850 мг, 1000 мг.
Активное вещество тормозит процесс глюконеогенеза в печеночной ткани, снижает концентрацию жирных кислот. Лекарство препятствуют окислению жировых молекул. Средство облегчает усвоение молекул глюкозы. Метформин не способен изменять количество инсулина крови. Препарат способствует похудению.
Метформин разрешается применять у диабетических больных. Лекарство можно использовать у взрослых пациентов и детей старше 10-летнего возраста. Препарат допускается использовать одновременно с инсулином или как монотерапию.
Ограничения к назначению лекарства:
- метаболический ацидоз;
- кома, прекома у больных с диабетом;
- серьезное нарушение работы почек, печени;
- тяжелая инфекционная патология;
- гипоксические состояния (патологии сердца, нарушения дыхательной функции);
- внутривенное введение препаратов, имеющих в своем составе йод, для осуществления рентгеновского обследования и компьютерной томографии;
- отравление спиртосодержащими напитками и лекарствами;
- пациенты младше 10-летнего возраста;
- аллергия на составляющие препарата.
Лекарство нужно аккуратно использовать у пациентов с серьезной патологией почек и печени, пациентов старше 60-летнего возраста. Аккуратно применяют препарат у больных 10-12-летнего возраста.
Лекарство не назначают во время вынашивания плода и кормления грудью. У этой группы пациентов действие препарата на организм было изучено не полностью. Средство не совмещают с алкогольсодержащими лекарствами и напитками, глюкокортикостероидными гормонами, диуретическими лекарствами, гипотензивными средствами и другими препаратами.
Серьезным осложнением при передозировке Метформина является лактатацидоз. Высокие дозировки способны также спровоцировать гипогликемическое состояние. Лактатацидоз и гипогликемия могут привести к ухудшению состояния больного, что опасно для жизни.
Метформин — лекарство от всего? Да, но нет
Мы тут, в редакции «XX2 века»
, очень любим метформин и рассказываем о нём при любом удобном случае. Сегодня он подавляет рост раковых клеток, завтра — борется с воспалением, послезавтра — помогает похудеть, а на следующей неделе и вовсе продлевает жизнь. У читателей могло сложиться впечатление, что это лекарство побеждает любые болезни. К сожалению, это не совсем так и почти к каждой хорошей новости прилагается «да, но». Так что мы решили снова написать про метформин — на этот раз большой текст, который пояснит тем, кто всё пропустил, откуда взялся этот препарат, что им лечат и насколько успешно.
История
Всё началось с травы. Козлятник лекарственный, он же козья рута, он же итальянский хорёк, он же, по-научному, Galéga officinális
— многолетнее травянистое растение. В средневековой Европе им лечили частое мочеиспускание — один из симптомов диабета — и некоторые другие болезни. Как давно козлятник используют в народной медицине, сказать сложно, но известно, что знаменитый английский эскулап Николас Калпепер (Nicholas Culpeper) упоминал о нём ещё в 1652 году в книге «Английский врач».
В конце XIX века учёные вплотную занялись козлятником и выяснили, что он содержит большие количества гуанидина (это бесцветное кристаллическое вещество впервые синтезировали в 1861 году). В 1918 году в ходе опытов на кроликах учёные показали, что гуанидин снижает уровень глюкозы в крови. Но соединение оказалось слишком токсичным, и лечить людей им было нельзя, поэтому учёные начали экспериментировать с производными гуанидина. В 1922 году Эмиль Альфонс Вернер (Emil Alphonse Werner) и Джеймс Белл (James Bell) в процессе синтеза N, N-диметилгуанидина получили диметилбигуанидин, известный нам как метформин, а семь лет спустя немецкий учёный Карл Слотта (Karl Slotta) протестировал его на животных. Были и другие препараты на основе гуанидина — галегин (изоамилен-дигуанидин), бигуаниды Синталин A и B. Синталины даже какое-то время использовали в клиническое практике, но после того, как началось промышленное производство инсулина (в 1923 году компания Eli Lilly and Company
начала продавать его под названием «Илетин»), о производных гуанидина подзабыли.
Galega officinalis
или козлятник лекарственный — дедушка самого популярного антидиабетического препарата.
В 1949 году метформин попал в руки филиппинского инфекциониста Эусебио Гарсия (Eusebio Garcia). Он называл вещество «флумамином» (flumamine) и лечил им грипп и малярию. Год спустя в статье Fluamine, a new synthetic analgesic and antiflu drug (Флумамин: новый синтетический обезболивающий и противопростудный препарат) Гарсия рассказал, что одна-единственная инъекция лекарства облегчила головную боль тридцати пациентов и полностью вылечила их за 24 часа. Точного механизма действия врач не знал, и предположил, что флумамин снижает концентрацию сахара в крови, но никаких доказательств не предоставил.
Этих спекуляций хватило, чтобы заинтересовать другого медика — француза Жана Стерна (Jean Sterne), специалиста по диабетологии. Он провёл эксперименты на собаках, крысах и кроликах и обнаружил, что полугодовое лечение не отразилось ни на их развитии, ни на функции печени. Даже при вскрытии не удалось обнаружить никаких аномалий. Стерн провёл клинические испытания на людях, обозвал препарат «глюкофагом» («пожирателем сахара», по аналогии с бактериофагом) и начал лечить им диабетиков.
Французский врач Жан Стерн и госпиталь, в котором он изучал свойства метформина.
У метформина почти сразу появились конкуренты — более мощные феноформин и буформин. Но эти препараты вызывали лактатацидоз — опасное состояние, которое сопровождается угнетением ЦНС, нарушением дыхания, функций сердечно-сосудистой системы и мочевыделения. Поэтому к концу 70-х ими перестали пользоваться в большинстве стран. И вот тогда метформин стал основной альтернативой инсулину. В конце 50-х его продавали во Франции и в Великобритании, в 70-х — в Канаде, а на американский рынок он попал только после одобрения Управлением по санитарному надзору за качеством пищевых продуктов и медикаментов (Food and Drug Administration, FDA) в 1994 году. Там он довольно быстро стал «бестселлером»
Что мы знаем о метформине
Сейчас метформин считается «препаратом первой линии» для лечения диабета 2 типа. Основное его преимущество в том, что он практически не вызывает гипогликемии, это отличает его от инсулина и другого класса сахароснижающих средств — производных сульфонилмочевины. Метформин снижает концентрацию глюкозы в крови путём угнетения её образования в печени, в то время как препараты сульфонилмочевины увеличивают выделение инсулина из бета-клеток в поджелудочной железе. Кроме того, он не способствует набору веса. Побочные эффекты у него, конечно, тоже есть, неприятные, но не смертельные: самые распространённые — желудочно-кишечные расстройства, в частности — тошнота, рвота, метеоризм и диарея. А снижение аппетита даже полезно.
Многое из того, что нам известно о влиянии метформина на здоровье, мы знаем благодаря клиническим исследованиям. Этот препарат изначально разрабатывали для снижения сахара в крови, и изучали его, конечно, прежде всего, в контексте диабета. Для того чтобы говорить о преимуществах и недостатках метформина, нужно хотя бы немного рассказать о том, как медики добывали эти сведения — иначе история превратится в «учёные доказали». Вот некоторые из самых значимых клинических испытаний, посвящённых диабету 2 типа:
- The University Group Diabetes Program, UGDP (Диабетическая программа университетской группы)
- United Kingdom Prospective Diabetes Study, UKPDS (Британское проспективное исследование диабета)
- Diabetes Prevention Program, DPP (Программа по профилактике диабета)
UGDP было первым рандомизированным клиническим испытанием, посвящённым диабету. В нём приняли участие 1027 человек, исследование длилось 21 год, с 1960 по 1981, а первые результаты были опубликованы в 1970 году. Учёные хотели узнать, какое лекарство эффективнее всего предотвращает развитие сердечно-сосудистых осложнений. Клиническое испытание подверглось ожесточённой критике, в том числе из-за ошибок при рандомизации. Однако FDA не нашло оснований не доверять его выводам. Метформин участники не принимали, но UGDP объявило неэффективным другое лекарство того же класса — фенформин, и в результате лекарство «по аналогии» не одобрили для применения в США. Именно благодаря UGDP выход лекарства на рынок этой страны отложили на много лет. UKPDS стало самым крупным на тот момент клиническим исследованием — оно включало 5102 больных диабетом второго типа. Испытание длилось 20 лет, с 1977 по 1997 годы. UKPDS должно было ответить на вопрос: может ли интенсивный контроль уровня глюкозы в крови предотвратить развитие осложнений, и какое лекарство подходит для этого лучше всего? Участники принимали препараты сульфонилмочевины первого поколения, инсулин или соблюдали диету. После публикации результатов, медики стали чаще рекомендовать метформин.
В DPP приняли участие 3 234 человек. Целью исследования было найти самый эффективный способ профилактики диабета 2 типа у людей с предиабетом. Для этого одной группе предлагали диету, упражнения и изменение образа жизни, другой — метформин, а третьей — плацебо. После клинического испытания провели ещё одно — Diabetes Prevention Program Outcomes Study, DPPOS или, по-русски, «Программа по профилактике диабета: исследование последствий». Медики изучили состояние здоровья участников DPP спустя 15 лет.
В ходе UKPDS метформин получали только пациенты с лишним весом. Результаты показали, что лекарство снижает риск смерти от осложнений диабета на 42% и смертность от всех причин — на 36%. Хороший результат, но он не так впечатляет, если учесть, что лекарство сравнивали с обыкновенной диетой. Риск сердечно-сосудистых осложнений у пациентов на метформине, инсулине и препаратах сульфонилмочевины практически не отличался. В паре с производными мочевины лекарство даже увеличивало смертность. Зато, в отличие от остальных средств, метформин не способствовал набору веса и реже вызывал гипогликемию. Поэтому учёные предложили ни много ни мало назначить метформин препаратом первой линии при лечении больных с ожирением. Это и положило начало его популярности.
DPP/DPPOS показали, что приём метформина может снизить риск развития диабета у людей с предиабетом на 31%. Но лучше всё-таки изменить образ жизни — в таком случае заболеваемость снижается на 58%. Старая добрая физкультура и диета оказались почти в 2 раза эффективнее. Зато у лекарства обнаружилось другое преимущество — метформин помогал сбросить вес. Люди с предиабетом, принимавшие препарат, в среднем теряли около двух килограммов. Эффект сохранялся всё время, пока участники исследования пили таблетки, при этом лекарство хорошо переносилось.
Конечно, были и другие исследования метформина и даже метаанализы этих исследований. Однако о преимуществах и недостатках этого препарата мы знаем ещё не всё. Например, учёные до сих пор пытаются разобраться, как метформин влияет на развитие сердечно-сосудистых заболеваний и смертность — данные на этот счёт противоречивы. Обзор 30 работ от 2011 года показал, что лекарство от диабета не приносит сердцу ни существенного вреда, ни весомой пользы, и выглядит молодцом только по сравнению с плацебо или полным отсутствием лечения. Статья от 2016 года, в которой анализировали 300 исследований, говорит, что отношении смертности и сердечно-сосудистых заболеваний между девятью классами сахароснижающих средств вообще нет разницы. Однако авторы анализа признают, что в отобранных статьях был высок риск предвзятости — больше, чем в половине публикаций информация подавалась избирательно, а в работе над ними участвовали спонсоры. С другой стороны, свежее исследование на основе 17 публикаций показывает, что у пациентов с хронической болезнью почек, застойной сердечной недостаточностью и хронической печёночной недостаточностью метформин смертность всё-таки снижает.
Новое применение
В России и США метформин одобрен только для лечения диабета 2 типа, но им пытаются лечить и другие заболевания. И чем больше становится известно о механизмах действия и влиянии препарата на организм, тем активнее ему ищут новое применение.
О том, что приём метформина сопровождается снижением веса, известно давно. DDP и DDPOS не открыли врачам глаза, а только подтвердили предыдущие наблюдения. Поэтому медики попробовали лечить метформином здоровых людей с ожирением. Одно из первых таких исследований вышло в 1970 году в журнале Lancet
. Учёные сравнивали эффективность метформина и фенфлурамина на примере 34 женщин в возрасте 22— 59 лет. После 8 недель терапии они пришли к выводу, что фенфлурамин работает лучше, да и побочных эффектов у него меньше.
Работы от 1998 и 2001 года реабилитировали сахароснижающий препарат и показали, что он снижает вес и у недиабетиков, но позже вышел метаанализ, который поставил эти результаты под сомнение. Учёные отобрали 57 исследований и 48 из них исключили, потому что они не соответствовали стандартам проведения клинических испытаний. Осталось всего 9 — и после анализа стало ясно, что данных об эффективности метформина недостаточно. Спустя 3 года вышел ещё один обзор и подтвердил результаты предыдущего. Метформин, вроде бы, снижал вес на 3—9 килограммов, но выборка таких исследований была маленькой, продолжительность — короткой, а дизайн — «слабым». К тому же участники помимо приёма лекарства занимались физкультурой — попробуй разберись, что именно помогло им похудеть. Несколько более длительных испытаний, лишённые этих недостатков, показали только незначительное снижение веса.
Четыре года назад опубликовали результаты, пожалуй, самого масштабного клинического исследования, посвящённого лечению ожирения у недиабетиков. Если в предыдущих работах речь шла о трёх-четырёх десятках человек, то теперь добровольцев было 200. 20% вообще не смогли сбросить вес, а 9 человек его набрали. Оставшиеся участники исследования теряли, в среднем, 5% массы тела, и больше всего препарат помогал людям с нарушением восприимчивости к инсулину. Но и в это исследование вкрался методологический подвох: не было рандомизации контрольной группы.
Детей и подростков с лишним весом метформином тоже лечат, но не особенно успешно. В 2016 году Кокрейн (Cochrane) — международная НКО, которая изучает эффективность технологий здравоохранения — представила систематический обзор и показала, что не только метформин, но и остальные лекарства у этой категории населения неэффективны. Да и качество доступных данных ожидает желать лучшего. В общем, медики признают, что рекомендовать диабетический препарат для лечения ожирения и детям, и взрослым пока рано. Проблему по-прежнему решают, в основном, диетой и физкультурой.
Другое применение метформина — лечение синдрома поликистозных яичников (СПКЯ). СПКЯ — это состояние, при котором у женщин повышается уровень мужских гормонов (андрогенов), нарушается работа яичников и сбивается менструальный цикл. В результате овуляции не происходит, и забеременеть становится сложно (хотя и не всегда невозможно). У многих больных начинается избыточный рост волос на лице и теле, появляется акне, а примерно половина набирает лишний вес. До конца разобраться в причинах СПКЯ не удалось, и вылечить его раз и навсегда не получается. Но уже известно, что болезнь связана с нечувствительностью тканей к инсулину, а у женщин с этим синдромом повышен риск развития диабета 2 типа. Метформин, который борется с инсулинорезистентностью, здесь как будто кстати.
Но не всё так просто. В 1994 году препарат хорошо себя зарекомендовал — тогда венесуэльские учёные провели исследование с участием 29 женщин, у 7 из которых восстановился менструальный цикл, а трое спонтанно забеременели. «При помощи метформина можно обратить многие, если не все, метаболические расстройства СПКЯ», — писали авторы. Правда, тут же оговаривались, что не проводили рандомизацию и не использовали плацебо для сравнения. Однако более крупные и продуманные клинические испытания 2006—2007 годов не подтвердили оптимистичные предположения. Метформин стимулировал овуляцию не особенно эффективно и уступал кломифену (торговое наименование — Клостилбегит).
Согласно клиническим рекомендациям международного Общества эндокринологов (Endocrine Society), диабетический препарат помогает при нарушениях метаболизма и нерегулярных месячных, но ограниченно эффективен или не эффективен при лечении бесплодия, акне и избыточного роста волос. К аналогичному выводу пришли участники семинара, организованного Американского общества репродуктивной медицины (American Society for Reproductive Medicine). Они рекомендовали метформин только женщинам с нарушением толерантности к глюкозе. А вот кокрейновский обзор от 2014 года говорит, что лекарство эффективнее, чем плацебо и повышает шанс забеременеть. Правда, качество доказательной базы исследований признали низким, а вероятность ошибки — высокой.
А ещё метформин, теоретически, может помочь в борьбе с раком. Но насколько эти надежды оправданы, пока неизвестно. Всерьёз присматриваться к лекарству с этой стороны стали только 12 лет назад — ничтожный срок, если вспомнить, сколько времени длилось, к примеру, UKPDS. В 2005 году Джози Эванс (Josie Evans) и её коллеги из Университета Данди (University of Dundee) сообщили, что приём метформина на 23% снижает заболеваемость онкологическими заболеваниями среди диабетиков. К таким выводам они пришли после анализа данных электронной медицинской базы данных DARTS.
Публикация вдохновила остальных медиков, и они принялись перепроверять выводы коллег с помощью других медицинских реестров. Постепенно пользу метформина подтверждали всё больше исследований. Появились обзоры научных работ, которые показывали снижение заболеваемости на уровне 31—34%. Затем — эксперименты на клеточных культурах и мышах. Оказалось, что у грызунов под влиянием диабетического препарата рост опухолей замедляется аж на 50% — правда, лекарство им скармливали в дозах, превышающих человеческие.
Почему же нельзя порадовать читателей и сказать, что мы наконец нашли новое эффективное средство от рака? По двум причинам. Во-первых, абстрактного «рака» не существует — это совокупность разных онкологических заболеваний. Насколько эффективно метформин борется с каждым из них нужно проверить в ходе клинических испытаний, и этот процесс пока далёк от завершения. Во-вторых, достоверность данных, которые вызвали энтузиазм на раннем этапе, поставили под сомнение. В двух десятках работ нашли ошибки, которые могли исказить результаты. А там где не нашли, не нашли и связи между метформином и заболеваемостью раком. В общем, нужно больше времени, нужно больше исследований.
Метформин и старение
Если в СМИ упоминают метформин, речь в статье наверняка идёт о продлении жизни. Геронтологи смотрят на старое лекарство с надеждой, и у них есть для этого серьёзные основания. Во-первых, в последние годы учёные стали активно исследовать молекулярные и генетические механизмы старения. Исследования показывают, что ограничение потребления калорий увеличивает продолжительность жизни мышей и крыс примерно на 30—40%. Если верить статье, опубликованной в этом году, такое «лечебное голодание» продлевает жизнь и приматам. «При чём здесь метформин?», — спросите вы. По мнению некоторых учёных, метформин вызывает в организме приблизительно те же изменения, что и ограничение калорий: повышает чувствительность к инсулину, снижает уровень холестерина, улучшает физическое состояние. Да и экспрессия генов у грызунов, которых кормят метформином, напоминает таковую у животных, сидящих на низкокалорийной диете.
Так что учёные взялись проверить действие препарата на модельных организмах. Черви Caenorhabditis elegans, получавшие метформин, жили на 18—36% (в зависимости от дозы) дольше своих родичей из контрольной группы. Мыши — на 5%. Кстати, подобные эксперименты проводили и у нас в России, в НИИ онкологии им. Н. Н. Петрова. Учёные кормили метформином не обычных крыс, а породу, созданную специально для изучения гипертензии и сердечно-сосудистых заболеваний. У таких животных средняя продолжительность жизни увеличивалась на 37,8%. Геронтологи добрались даже до сверчков: у вида Acheta domesticus после лечения антидиабетическим препаратом максимальная продолжительность жизни составила 138% по сравнению с контрольной группой.
Следующим логичным шагом было бы проведение испытаний на людях. Результаты одного такого исследования уже опубликованы. Учёные проанализировали данные 180 000 человек: 78 000 болели диабетом и принимали метформин, 12 000 — пили препараты сульфонилмочевины и 90 500 были здоровы. Эти сведения получили не в ходе двойного слепого плацебо-контролируемого испытания, а из базы медицинской документации Clinical Practice Research Datalink. Результаты показали, что диабетики на метформине живут на 15% дольше здоровых людей. СМИ написали о лекарстве, способном продлевать жизнь, но некоторых учёных работа под названием «Могут ли люди с диабетом 2 типа жить дольше, чем здоровые люди?» совсем не впечатлила. Вот что сказал о ней профессор прикладной статистики британского Открытого университета (The Open University) Кевин Макконуэй (Kevin McConway):
«Заголовок статьи вводит в заблуждение, потому что тот, кто его прочтёт, может неверно его понять — на самом деле, это исследование не может ответить на заданный вопрос по причинам, которые я приведу ниже, и создаётся впечатление, словно у врачей есть основания рекомендовать метформин здоровым людям. Но в исследовании речь идёт вовсе не об этом.
В пресс-релизе Крейг Карри говорит «После того, как у человека развивается диабет, продолжительность его жизни, сокращается, в среднем, на 8 лет» и дальше объясняет, почему. Если жизнь диабетиков настолько короче, чем у здоровых людей, каким образом они могут «жить дольше, чем те, кто не болеет диабетом», как говорится заголовках статьи и пресс-релиза?
Дело в том, что исследование посвящено периоду времени, когда больные диабетом получали метформин в качестве терапии первой линии (эту группу также сравнивают с теми, кто в качестве терапии первой линии получал препараты сульфонилмочевины). В какой-то момент многих пациентов переведут на терапию второй линии из-за того, что диабет или его симптомы ухудшились. Но в этот момент исследование попросту заканчивается.
Так что в цитате о сокращении продолжительности жизни у пациентов с диабетом 2 типа на 8 лет речь идёт обо всей жизни пациента после постановки диагноза, включая тот период, когда он находится на более агрессивной терапии второй линии. Но исследование учитывает только промежуток времени до изменения режима лечения. В ёмкий заголовок это не поместится, но важно отметить, что здесь не всё так просто.
Но если выживаемость диабетиков, принимающих метформин, значительно выше, чем выживаемость здоровых людей, пусть и на протяжении ограниченного периода времени, не означает ли это, что людям, которые не болеют диабетом, следует принимать метформин, чтобы жить дольше? Нет, не означает. Такое явное различие может быть связано не с метформином, а с чем-то другим. […]
Разница в выживаемости между диабетиками на метформине и контрольной группой была статистически значимой, но, в сущности, довольно маленькой и, вероятно, находится в пределах, которые можно объяснить остаточным искажением (влиянием других переменных, которые не учитываются в ходе анализа)».
Кроме того, было бы нечестно не упомянуть о том, что исследование финансировали фармацевтические компании AstraZeneca
и
Bristol-Myers Squibb
. Сотрудники этих фирм имели доступ к данным исследования, хотя в статье говорится, что они не могли влиять на анализ, рецензирование или процесс публикации. Да и сами учёные довольно близко знакомы с фармацевтической индустрией. Пятеро работали в исследовательской консалтинговой компании
Pharmatelligence
, которая получает гранты от производителей лекарств. Ещё один был сотрудником
Bristol-Myers Squibb
. Само по себе это не делает результаты недостоверными, но, согласитесь, несколько настораживает. Особенно учитывая тот факт, что обе компании-спонсора производят метформин.
Так что без полноценных клинических испытаний в этом вопросе не разобраться. Одним из первых исследований о связи метформина и старения должно было стать Изучение влияния метформина на продолжительность жизни (Metformin in Longevity Study). Но с момента старта в 2014 году о нём не появилось никакой информации. Предварительные результаты предполагалось получить ещё два года назад, но с тех пор не вышло ни одной публикации.
На подходе ещё одно клиническое испытание — Борьба со старением при помощи метформина (Targeting age with Metformin, TAME). Это двойное слепое рандомизированное плацебо-контролируемое исследование — золотой стандарт, всё, как мы любим. В нём примут участие 3000 человек в возрасте от 65 до 79 лет. TAME довольно необычно по нескольким причинам. Во-первых, оно направлено на изучение того, чего как бы не существует. Старение, с медицинской точки зрения — не болезнь. Общепризнанного биомаркера, по которому можно было бы понять, замедляется ли этот процесс или нет, тоже нет. Поэтому цель исследования — определить, может ли метформин замедлить развитие возрастных заболеваний: сердечно-сосудистых, неврологических, онкологических, и так далее.
Учёные надеются, что им удастся создать прецедент, и в будущем FDA признает старение «показанием», состоянием, которое можно лечить. «Я думаю, что FDA скорее воспримет то, что называется «сопутствующие заболевания», чем нечто под названием «старение», — говорит руководитель научной группы Нир Барзилай (Nir Barzilai). — Даже по нашему… по моему мнению, старость — это не болезнь. Это, знаете ли, человеческая природа! Мы рождаемся, умираем, а в промежутке — стареем… Я имею в виду: „Мне всё равно, как это называть, если я могу это отсрочить“».
Ещё одна необычная деталь — исследование не спонсируют ни фармацевтические компании, ни государство. Средства собирает Американская федерация по изучению старения (American Federation for Aging Research), пожертвование может внести любой желающий. По словам Барзилая, проведение клинических испытаний будет стоить «50 миллионов долларов, плюс-минус 20 миллионов». Результаты будут не скоро: какое-то время уйдёт на сбор денег, само исследование продлится 3—4,5 года, плюс время на обработку и публикацию данных. Но когда речь идёт о продлении жизни, можно и подождать.
Вам может быть интересно:
Метформин может быть полезен при аутизме.