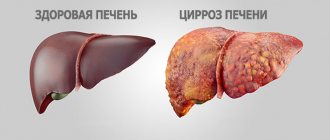
Алкогольная болезнь печени (АБП) — это комплекс патологических изменений в печени, развитие которых вызвано хроническим употреблением алкоголя в токсических дозах.
Около 30% всех диффузных поражений печеночной ткани связано именно с АБП1. Длительный прием алкогольных напитков негативно отражается на всех органах и системах, в том числе и печени. Дело в том, что этанол в клетках печени в процессе метаболизма превращается в ацетальдегид, который и оказывает токсическое действие на клетки.9 Стоит отметить, что у женщин в среднем отмечена более низкая активность фермента, обеспечивающего образование ацетальдегида, в сравнении с мужчинами, чем объясняется более тяжелое течение АБП среди женщин и развитие алкогольного повреждения печени в более короткий период времени и при более низких дозах потребляемого алкоголя1 (20 г/сутки для женщин в сравнении с 30 г/сутки для мужчин).10
Цирроз печени в России
В большинстве развитых стран АБП является одним из самых распространенных заболеваний, которое диагностируют у 10-25% мужчин и немного реже среди женщин2. Исследования ВОЗ (Всемирной организации здравоохранения) показали, что цирроз печени в России занимает шестое место среди всех причин смертности2.
АБП можно было бы назвать алкогольной жировой болезнью печени, что связано с развитием жировой дистрофии печени на первой стадии заболевания при систематическом употреблении этанола в высоких дозах.1 Такой феномен, накопление жира в клетках печени, происходит и при неалкогольной жировой болезни печени.
Факты
· Алкогольное повреждение возникает из-за токсического воздействия спирта на клетки органа.
· Наиболее распространенным повреждением является накопление жира. В ряде случаев развивается цирроз и асцит.
· До определенного момента поврежденная печень может восстанавливаться, при прекращении употребления алкоголя или сокращении его количества.
· Цирроз является серьезным хроническим заболеванием, которое у нас не лечится. Но его развитие можно замедлить, при отказе от употребления алкоголя и медикаментозной терапии.
· Лечение алкогольного повреждения печени — это, прежде всего, прекращение употребления алкоголя.
Методы лечения АБП
Можно выделить медикаментозные и немедикаментозные подходы к терапии.
Медикаментозные
Немедикаментозное лечение требует полного отказа от алкоголя.
Медикаментозные
Лекарство для лечения алкогольной болезни печени должно оказывать антиоксидантное действие, подавлять воспаление и препятствовать прогрессированию фиброза. Таким препаратом является Фосфоглив*
, продемонстрировавший все эти эффекты в клинических исследованиях. Его следует принимать по 2 капсулы 3 раза в день во время еды, не разжевывая, запивая небольшим количеством жидкости. Продолжительность курса обычно составляет 3 месяца.
При подозрении на развитие болезни печени следует обратиться к врачу.
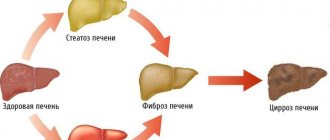
Динамика развития поражения печени алкоголем
При систематическом употреблении спиртного печень пациента претерпевает следующие изменения.
- На первом этапе образуется воспаление печени – гепатит.
- На втором этапе гепатит переходит в жировой гепатоз. На этой стадии происходит замещение клеток пени жировыми.
- Далее орган не успевает образовывать новые здоровые клетки и вместо них возникает соединительная ткань (аналогичная сухожилиям). Эта стадия поражения печени называется цирроз.
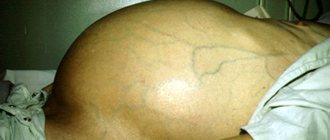
- Когда печень перестает полноценно выполнять свои функции, возникает заболевание асцит. При нем вода накапливается в брюшном пространстве. Такое состояние называется водянка брюшной полости.
Гепатит и алкогольное воспаление дают следующую симптоматику:
· Горечь во рту;
· Рвота;
· Вздутие живота;
· На запущенных стадиях проявляется желтуха – пожелтение кожи и склер.
Цирроз – это заболевание, которое не лечится. Из-за необратимых изменений в клетках органа происходит сильное отравление организма не только производными алкоголя, но и другими продуктами распада, образуемыми в организме человека. От этого страдает в первую очередь головной мозг.
Патогенез
Заболевание может развиваться длительно: месяцы и годы. Патологическое влияние вирусов на клетки печени, токсических веществ (лекарства, алкоголь), нарушение кровоснабжения органа, иммунные механизмы, влияние медиаторов воспаления приводят к массовой гибели гепатоцитов и замещению соединительной тканью. Этот процесс нарушает все жизненно-важные функции печени.
- 1. Жировая дистрофия. Начальные изменения в структуре и функции гепатоцитов, которые могут полностью исчезнуть за несколько недель при условии прекращения поступления алкоголя в организм.
- 2. Стеатогепатит. Развивается воспалительный процесс. Структура и размеры гепатоцитов меняются, в тяжелых случаях клетки погибают, что сказывается на общем состоянии печени. На этом этапе уже возникают нарушения в функционировании органа, а также требуется специализированное лечение.
- 3. Цирроз. Формирование необратимых фиброзных изменений в органе, нарушение общей структуры: появление бугристости, уменьшение размеров. При отсутствии лечения состояние прогрессирует, а функциональность печени снижается. Развиваются опасные осложнения не только в самом органе, но также в зависимых от него структурах.
Шансы избавиться от проблемы тем выше, чем раньше обратиться к врачу и, самое главное, перестать употреблять спиртное.
Развитие синдрома
Почти каждый, кто злоупотребляет алкоголем, подвержен риску ожирения печени, но только у небольшой части пациентов развивается воспаление органа, и еще меньший процент заболевает циррозом.
На начальных этапах, поврежденная алкоголем печень не дает ярко выраженных симптомов, но со временем начинает все больше беспокоить пациента.
Ярким признаком печеночной недостаточности является наличие желтушного симптома. При нем у пациента желтеет кожа и белки глаз, появляется горький привкус во рту.
Орган выполняет функцию очищения крови. В случае печеночной недостаточности повышенное количество токсинов распространяется по всему организму. Они оказывают вредное воздействие на мозг. Со временем это приводит к тому, что человек приобретает заболевания мозга. Это называется печеночной энцефалопатией или печеночной недостаточностью головного мозга.
Алкогольная жировая дистрофия (АЖД)
Данная патология является наиболее распространённым видом токсического поражения печёночной ткани. Ранняя диагностика нарушения затруднительна ввиду незначительной симптоматики. Пациенты практически не предъявляют никаких жалоб.
При опросе врачом они могут сообщить об:
- Апатии, плохом самочувствии, вялости.
- Периодическом ощущении переполнения желудка даже после приёма небольшого количества пищи.
- Вздутии кишечника.
- Выхождении зловонных газов.
- Диарее.
При осмотре и пальпации печени доктор выявляет:
- Увеличение органа.
- Закругленный край.
- Плотную консистенцию.
- Повышенную чувствительность.
Лабораторная диагностика не даёт никаких подтверждающих наличие патологии данных. Печёночные пробы остаются в пределах нормы, иногда незначительно выходя за границы. Единственным фактором, указывающим на болезнь, является бромсульфофталеиновая проба.
Патология выявляется при помощи:
- Данных УЗИ.
- Компьютерной и магнитно-резонансной томографии.
- Пунктационной биопсии. Патоморфологическое исследование позволяет выявить клетки, заполненные каплями жира, деформацию со смещением к периферии ядра и форменных элементов (митохондрий и лизосом).
АЖД является обратимым состоянием. Если пациент начнет вести трезвый образ жизни, то выявленные отклонения постепенно уйдут, начнется восстановление.
Симптоматика заболевания
Поврежденный орган на первых этапах не проявляет ярко выраженной симптоматики. Проблемы чаще всего обнаруживаются случайным образом, при сдаче анализов или начинают проявляться характерные симптомы на запущенных стадиях алкоголизма. Нарушения в работе органа проявляетс в виде:
- хронической усталости,
- проблем с пищеварением,
- кровавой рвоты,
- склонности к инфекциям;
- психических расстройств.
Алкогольное воспаление печени обычно проявляется внезапно и имеет аналогичную симптоматику.
Диагностика
Воздействие алкоголя на печень даёт настолько выраженную и характерную клиническую картину, что у врачей обычно не возникает проблем с выявлением формы и стадии заболевания.
Основная роль отводится:
- Опросу и сбору жалоб.
- Наличию длительного хронического алкоголизма.
- Анализам крови (описанным выше).
- Выявлению завышенных значений билирубина.
- Обнаружению высокого уровня иммуноглобулина А.
Современная диагностика основана на получении результатов компьютерной и микрорезонансной томографии, УЗИ. Эти методики позволяют находить нарушения в самом начале процесса. Полученные данные подтверждаются радионуклидными методами и биопсией.
Постановка диагноза
Врач определяет продолжительность употребления спиртного или степень алкоголизма. На основании этих данных пациенту назначается проведение медицинского обследования. Как при общей диагностике, так и при анализе крови можно определить степень повреждения печени. Для этого проводятся:
- Лабораторные анализы.
- Гистологические исследования.
- УЗИ. Чтобы иметь визуальное представление о картине болезни выполняется ультразвуковое исследование печени.
- Биопсия. Для ее проведения врач извлекает с помощью иглы образец ткани.
- Магниторезонансная и компьютерная томография.
Лечение алкоголизма в в Москве
Наркологическая клиника “АлкоЗдрав” осуществляет профессиональную терапию алкогольной зависимости в Москве. Мы используем сертифицированные лекарственные препараты, прибегаем к современным психотерапевтическим программам и руководствуемся принципами индивидуального подхода к каждому человеку. Важно заметить, что лечение в “АлкоЗдрав” осуществляется строго анонимно.
Диагностика
Диагностика является первым звеном в цепи лечения печеночных патологий. Для определения состояния железы необходимо сдать общий анализ крови и мочи, пройти УЗИ, сдать маркеры (цитолиз, холестаз). В тяжелых случаях необходима биопсия. После визуального обследования и изучения анамнеза врач определяет актуальный метод диагностики.
Детоксикация от алкоголя
К самым распространенным способам детоксикации от этилового спирта относятся:
- Постановка капельниц для очищения кровяного русла;
- Прием энтеросорбентов;
- Проведение инъекций;
- Прибегание к помощи специализированных аппаратов (плазмаферез, УБОД и т.д.).
Детоксикация необходима для выведения шлаков и токсинов из организма. Процедура должна осуществляться с участием медицинского персонала.
Медикаментозная терапия
Фармакотерапия осуществляется с целью ускорения процессов детоксикации, купирования симптомов заболевания и восстановления функций органов и систем. Актуальная группа препаратов определяется только врачом-наркологом. Самолечение может привести к появлению побочных реакций.
Реабилитация алкоголиков
Реабилитация в специализированном центре необходима для восстановления организма и психологического состояния человека.
В процессе реабилитации резидент клиники проходит интенсивную индивидуальную и групповую психотерапию, борется с психологической зависимостью от психоактивных веществ. Совместно со специалистом человек прорабатывает психологические проблемы, обучается принципам социальной адаптации, проявляет активную социальную позицию, учится жить в трезвости.
Причины возникновения алкогольного повреждения печени
Алкоголь влияет на метаболизм клеток органа. Это приводит к тому, что жир (жировые клетки) накапливается. В некоторых случаях это вызывает воспалительные реакции в печени, что приводит к образованию рубцовой или соединительной ткани.
Если воздействие (раздражение) происходит в течение длительного времени, соединительная ткань сокращается и разрушает структуру печени. Таким образом, отдельные клетки печени не будут функционировать нормально, и крови будет трудно течь через орган. Это приводит к тому, что кровь ищет другие пути, например, через пищевод. Так в результате заболевания печени могут возникать варикозные вены.
Алкогольный гепатит: современные алгоритмы диагностики и лечения
Для цитирования. Костюкевич О.И. Алкогольный гепатит: современные алгоритмы диагностики и лечения // РМЖ. 2016. № 3. С. 177–182.
Проблема алкогольного поражения печени (ПП) по-прежнему не утрачивает своей актуальности. Потребление алкоголя повсеместно остается на крайне высоком уровне. По последним данным, в нашей стране среднегодовое потребление этанола составляет 15,7 л на душу населения. Алкоголь является основной причиной ПП и вносит существенный вклад в генез общей заболеваемости и смертности [1]. Алкогольная болезнь печени (АБП) включает в себя целый спектр патологий, начиная от жирового гепатоза и завершая циррозом печени. Своевременная диагностика АБП крайне важна в клинической практике, т. к. ранняя абстиненция может существенно замедлить прогрессирование фиброза и развитие серьезных осложнений, а в некоторых случаях привести к выздоровлению. В то же время практикующему врачу хорошо известно, что сбор алкогольного анамнеза порой превращается в настоящий медицинский детектив. Во многих случаях пациенты либо приуменьшают, либо вовсе отрицают употребление алкоголя, направляя «следствие» по ложному следу. А иногда сами мы, из «жалости» к пациенту, при формулировке диагноза термин «алкогольный» подменяем на «пищевой» или «криптогенный», вводя в заблуждение коллег. Сейчас существует довольно большой спектр объективных и лабораторных маркеров хронической алкогольной интоксикации (ХАИ), специальные анкеты и шкалы, позволяющие оценить истинный вклад алкоголя в генез ПП и повреждения других органов. Внедрение их в клиническую практику позволяет гораздо шире использовать в диагнозе определение «алкогольный», даже при исходном отрицании пациентом факта злоупотребления спиртными напитками. Золотым стандартом диагностики АБП по-прежнему остается биопсия печени, хотя в реальной практике мы прибегаем к ней в крайних случаях сомнительного диагноза или для оценки степени фиброза. Сегодня все шире используются неинвазивные методики, такие как эластография и различные биохимические тесты.
Формы АБП
Алкогольное ПП имеет три последовательно сменяющие друг друга стадии-формы. 1.
Стеатоз
(жировой гепатоз) – присутствует в той или иной степени у 90% злоупотребляющих алкоголем пациентов (потребляющих этанола более 60 г/сут) и протекает, как правило, бессимптомно [2], обнаруживая себя лишь при ультразвуковом исследовании. Основной признак – гепатомегалия при нормальных трансаминазах. 2.
Алкогольный гепатит
(АГ) – стадия накопления цитокинов, повреждения мембран гепатоцитов при продолжительном употреблении алкоголя. Морфологически эта стадия характеризуется воспалительной инфильтрацией, дистрофией гепатоцитов, наличием алкогольного гиалина (тельца Мэллори), коллагенозом пространства Диссе, реже – наличием ступенчатых некрозов. Различают острый и хронический АГ. • Острый АГ нередко развивается после длительного употребления высоких доз этанола, может развиться на любой стадии АБП – и на фоне стеатоза, и на фоне уже имеющегося цирроза печени, что значительно ухудшает прогноз. Тяжелый АГ характеризуется крайне высокой смертностью, достигающей 50%. • Хронический АГ диагностируется у пациентов с нерезко выраженным цитолитическим и иммуновоспалительным синдромом, при отсутствии признаков цирротической трансформации. 3.
Цирроз печени
– развивается при длительном (более 10 лет) употреблении «опасных» доз алкоголя (в пересчете на этанол: 60–80 г/сут для мужчин и 20 г/сут для женщин) в 20–40% случаев [3]. Показано, что на чувствительность к гепатотоксическому действию этанола влияет целый ряд факторов и АБП развивается далеко не у всех «хронически злоупотребляющих» пациентов.
Факторы риска АБП:
• высокие дозы этанола; • генетическая предрасположенность; • женский пол; • применение препаратов, метаболизирующихся в печени; • вирусные гепатиты; • дефицит веса или ожирение.
Высокие дозы этанола.
Отличительной особенностью алкогольных ПП является высокая дозозависимость. Исследования последних лет показали, что риск развития АБП существенно возрастает при употреблении более 30 г этанола в сутки. Абсолютно гепатотоксичными считаются дозы более 120–160 г/сут. При этом ежедневное употребление даже небольших доз алкоголя более опасно, чем периодический прием высоких доз, когда печень имеет возможность регенерировать. Генетическая предрасположенность. Известен тот факт, что разные народы отличаются степенью элиминации алкоголя по меньшей мере в 3 раза. Это объясняется генетическим полиморфизмом ферментных систем (алкогольдегидрогеназы, цитохрома Р450 и альдегиддегидрогеназы).
Женский пол.
Доказано, что женщины в 2 раза более чувствительны к токсическому действию алкоголя, у них чаще развивается цирроз печени. Наиболее вероятная причина таких различий связана с разной активностью желудочной фракции алкогольдегидрогеназы, что обусловливает большую нагрузку на ферментные системы печени.
Гепатотропные препараты.
Необходимо помнить, что у лиц, злоупотребляющих алкоголем, многие лекарственные препараты становятся гепатотоксичными (парацетамол, ацетилсалициловая кислота, противотуберкулезные, антиретровирусные средства, противоопухолевые и психотропные препараты и др.), при этом риск ПП повышается в несколько раз. Объясняется данный феномен конкурентным метаболизмом в печени с участием системы цитохрома Р450.
Вирусные гепатиты.
При сочетании хронических гепатитов с употреблением алкоголя ПП прогрессирует заметно быстрее и повышается риск развития гепатоцеллюлярной карциномы.
Питание
. На сегодняшний день нет сомнений, что общее недоедание или недостаточность каких-либо нутриентов в дополнение к алкогольной зависимости приводят к большему ПП. С алкоголем поступает большое количество энергии (1 г этанола дает 7 ккал), но не поступают пластические вещества, что приводит к разрушению собственных белков и усугубляет питательную недостаточность. Неполноценное питание и гепатотоксичность этанола действуют как синергисты.
Патогенетические аспекты алкогольного повреждения печени
В основе ПП лежат сразу несколько механизмов. 1. Прямое гепатотоксическое воздействие этанола. Слабо поляризованный растворитель, этанол может растворять фосфолипиды мембран гепатоцитов и митохондрий. Именно повреждение митохондрий лежит в основе жировой дистрофии печени, т. к. последние теряют способность метаболизировать триглицериды. 2. Токсическое действие ацетальдегида. Ацетальдегид является крайне токсичным субстратом для гепатоцитов. Он накапливается в гепатоцитах и приводит к разрушению плазматических мембран путем деполимеризации белков и активации продуктов перекисного окисления липидов (ПОЛ). Кроме того, ацетальдегид активирует клетки, что приводит к избыточной продукции коллагена. Именно этим объясняется развитие фиброза печени при ХАИ. 3. Задержка белков и воды в гепатоцитах. Этанол подавляет секрецию из гепатоцитов вновь синтезированных белков, что приводит к накоплению белка, а вслед за этим и воды, – это ведет, наряду с жировой дистрофией, к развитию гепатомегалии. 4. Иммунное ПП. Именно иммунными механизмами можно объяснить случаи прогрессирования АБП, несмотря на прекращение употребления алкоголя.
Клиническая картина АГ
Различают 4 основные клинические формы АГ: латентную, желтушную, холестатическую и фульминантную. 1. Латентная форма не дает самостоятельной клинической картины и диагностируется по умеренному повышению трансаминаз у злоупотребляющего алкоголем пациента. Могут иметь место такие неспецифические жалобы, как слабость, снижение аппетита, неустойчивый стул, тупая боль в правом подреберье и т. д. 2. Желтушная форма встречается наиболее часто. У пациентов отмечаются выраженная слабость, анорексия, тупая боль в правом подреберье, тошнота, рвота, диарея, похудание, желтуха, у половины больных наблюдается лихорадка. 3. Холестатическая форма характеризуется значительным повышением гамма-глутамилтранспептидазы (ГГТП) и щелочной фосфатазы (ЩФ), сопровождается мучительным кожным зудом. Довольно редко, уже на стадии гепатита могут проявляться признаки транзиторной портальной гипертензии с развитием асцита. 4. Фульминантный (тяжелый) острый АГ характеризуется нарастающей энцефалопатией, выраженной желтухой, отечно-асцитическим и геморрагическим синдромами. Риск развития фульминантного АГ возникает при одновременном приеме гепатотоксичных лекарств (например, парацетамол). Характерен нейтрофильный лейкоцитоз до 15–25×109/л, повышение СОЭ до 30–50 мм/ч. Билирубин повышается преимущественно за счет прямой фракции. Уровень трансаминаз повышается в 5–10 раз. Возрастает активность ГГТП и ЩФ, повышена концентрация иммуноглобулина А (IgA).
Диагностика АГ
Диагностика АГ складывается из 4-х этапов: 1) верификация ПП (факт гепатита); 2) подтверждение факта злоупотребления алкоголем; 3) оценка тяжести гепатита и прогноз; 4) оценка степени фиброза. Оценка состояния печени включает в себя определение структурных (УЗИ, КТ и МРТ брюшной полости, биопсия печени) и функциональных (лабораторная диагностика, сцинтиграфия печени) изменений. Основными критериями гепатита являются гепатомегалия и повышение сывороточных трансаминаз. При УЗИ, КТ и МРТ печени выявляется гепатомегалия различной степени выраженности, в случае транзиторной портальной гипертензии может верифицироваться асцит, спленомегалия. Золотым стандартом диагностики АГ по-прежнему остается биопсия печени. Показаниями к биопсии печени служит необходимость дифференциальной диагностики между алкогольным и иными ПП, определения стадии АПБ, выявления перивенулярного фиброза как прогностически неблагоприятного фактора перехода заболевания в цирроз у лиц, продолжающих злоупотреблять алкоголем. На сегодняшний день точность диагноза алкогольного стеатогепатита может быть подтверждена только на основании биопсии печени (класс рекомендаций 1A). Морфологическими признаками острого АГ являются: • некрозы гепатоцитов; • воспалительная инфильтрация; • жировая и балонная дистрофия; • алкогольный гиалин (тельца Мэллори); • поражение центролобулярной области. Для острого АГ характерны признаки острой воспалительной реакции: лейкоцитоз, ускорение скорости оседания эритроцитов (СОЭ) (20–50 мм/ч), повышение С-реактивного белка. У пациентов с АГ можно выделить следующие клинико-лабораторные синдромы: 1) синдром цитолиза – собственно отражает факт повреждения гепатоцитов. Характеризуется повышением трансаминаз: аланинаминотрансферазы (АЛТ), аспартатаминотрансферазы (АСТ), лактатдегидрогеназы. Степень повышения ферментов, как правило, коррелирует со степенью тяжести гепатита; 2) синдром холестаза – верифицируется как минимум при 3-кратном увеличении ЩФ и ГГТП; 3) желтуха – повышение билирубина преимущественно за счет прямой фракции; 4) синдром печеночно-клеточной недостаточности – прогрессирует параллельно с тяжестью заболевания, его маркерами являются снижение альбумина, протромбина, нарастающая энцефалопатия; 5) портальная гипертензия – также имеет место при остром АГ и, как правило, носит обратимый характер. Наличие стойкой портальной гипертензии свидетельствует о возможном цирротическом поражении печени. Следующим
важнейшим этапом диагностики является
определение этиологического фактора гепатита. У всех без исключения пациентов, даже с указанием на злоупотребление алкоголем в анамнезе, обязательным является определение маркеров вирусных гепатитов и тщательный сбор лекарственного анамнеза. Факт употребления этанола, истинные дозы алкогольных напитков часто скрываются самими пациентами, что порой направляет лечащего врача по ложному пути и приводит к постановке ложного диагноза. Знание объективных критериев ХАИ помогает не только в диагностике АБП, но и многих других соматических заболеваний.
Выявление ХАИ
I. Существуют несколько опросников, позволяющих с высокой достоверностью не только выявить факт злоупотребления алкоголем, но и учесть
вклад ХАИ в генез соматической патологии.
1. Опросник CAGE (Cut down, Annoyed, Guilty, Eye-opener) – состоит всего из 4-х вопросов (табл. 1).
2. Опросник AUDIT (Alcohol Use Disorders Identification Test) – имеет международную стандартизацию, состоит из 10 вопросов (табл. 2).
II. К объективным критериям ХАИ
относят так называемые «алкогольные стигмы»: расширение сосудов лица и носа, инъекция склер, гипертрофия околоушных желез, атрофия мышц плечевого пояса, яркие телеангиоэктазии, гинекомастия, контрактура Дюпюитрена, атрофия яичек. 1. Большой чувствительностью для выявления ХАИ обладает анкета ПАС (определения выраженности постинтоксикационного алкогольного синдрома), которая включает 35 вопросов (табл. 3). Положительные ответы на 15 и более вопросов позволяют предположить высокую вероятность систематического употребления небезопасных доз алкогольсодержащих напитков [4]. 2. С целью выявления физикальных признаков ХАИ используется «Сетка LeGo» [4] (табл. 4). III.
Лабораторные признаки ХАИ.
Для алкогольного гепатита характерно превышение активности АСТ над АЛТ в 1,5–2,0 раза (коэффициент де-Ритиса), повышение ГГТП. Высокой чувствительностью и специфичностью обладает тест на определение углевододефицитного (десиализированного) трансферрина сыворотки крови — соединения трансферрина с ацетальдегидом, приводящего к накоплению железа в печени и ацетальдегид-модифицированного гемоглобина (табл. 5).
Оценка степени тяжести и прогностические критерии АГ
Для оценки степени тяжести АГ и прогноза используют различные шкалы. Наибольшей популярностью пользуются следующие (табл. 6):
1. Индекс Маддрея, или дискриминантная функция (mDF) [5]. Показатель более 32 свидетельствует о тяжелом течении АГ и характеризуется высоким риском летального исхода в текущую госпитализацию (>50%). 2. Шкала MELD (Model for End-Stage Liver Disease), первоначально разработанная для определения очередности трансплантации печени. 3. Шкала Глазго оценки тяжести АГ (Glasgow alcoholic hepatitis score – GAHS). При значениях более 9 баллов к 28-му дню выживают 46% [6]. 4. Шкала Лилль используется, как правило, для оценки целесообразности продолжения лечения кортикостероидами, т. к. при расчете используются лабораторные показатели до начала и через неделю терапии. При значении менее 0,45 выживаемость больных в течение 6 мес. составляет в среднем 25%.
Оценка степени фиброза
Выделяют инвазивные (биопсия печени) и неинвазивные методики: фибротест (определение сывороточных маркеров фиброза) и фиброскан, которые обладают довольно высокой чувствительностью и специфичностью.
Лечение АГ
Выбор лечебной тактики лечения АГ зависит, прежде всего, от степени тяжести заболевания. Поэтому перед началом терапии необходимо провести оценку тяжести и прогноза гепатита (индекс Маддрея). Рациональные подходы к лечению АГ: 1) отказ от алкоголя; 2) нутритивная поддержка; 3) тщательный подбор кандидатов для короткого курса кортикостероидов; 4) назначение пентоксифиллина при невозможности приема кортикостероидов; 5) назначение поддерживающей терапии при легком и среднетяжелом течении АГ; 5) лечение осложнений АГ (портальная гипертензия, печеночная энцефалопатия, инфекционные осложнения).
Отказ от алкоголя.
Обязательным условием лечения любой стадии АБП является абстиненция.
Нутритивная поддержка.
Показано, что питательная недостаточность присутствует в той или иной степени у всех пациентов с АБП. В случае выраженных нарушений питательного статуса решается вопрос о нутритивной поддержке специализированными энтеральными питательными смесями. Всем пациентам рекомендовано питание с суточной калорийностью 2000–3000 ккал, с содержанием белка не менее 1 г на 1 кг массы тела. Ограничение количества белка вводится только при явлениях печеночной энцефалопатии, в этом случае рекомендовано использовать аминокислоты с разветвленной цепью. Увеличение потребления белка с пищей способствует снижению катаболических процессов, нормализации иммунного статуса и непосредственно улучшению функции печени. Диета должна содержать достаточное количество витаминов (особенно группы В, фолиевой и липоевой кислот) и микроэлементов — цинка, селена. Установлено, что дефицит цинка (40% больных с АБП) занчительно усиливает проявления печеночной энцефалопатии. Известно также, что алкогольдегидрогеназа – цинкозависимый фермент, следовательно при дефиците цинка ее активность снижается.
Глюкокортикостероиды
Метаанализ 13 рандомизированных исследований, проведенный Mathurin в 2002 г., показал, что терапия глюкокортикоидными препаратами достоверно улучшает выживаемость пациентов с тяжелым острым АГ. На сегодняшний день ГКС являются препаратами первой линии терапии тяжелого АГ при индексе Маддрея более 32 (уровень доказательности 1В) [7]. Преднизолон назначается перорально 40 мг/cут сроком до 4-х нед. с последующей быстрой заменой на 5 мг/нед.; обязательное условие – нормальный уровень креатинина. Если в течение 7 дней снижения билирубина не произошло (оценка по шкале Лилль – 0,45), ГКС отменяют (уровень доказательности 1В). При наличии противопоказаний к назначению ГКС целесообразно назначение пентоксифиллина (1В) 1200 мг/сут per os или 400–600 мг/сут внутривенно. Терапия пентоксифиллином имеет меньшую доказательную базу и используется только при невозможности терапии ГКС.
Поддерживающая терапия АГ легкой и средней тяжести
Гепатопротекторы
Традиционно к гепатопротекторам относят довольно широкий спектр препаратов, различных по механизму действия, обладающих избирательным защитным действием на клетки печени. По происхождению гепатопротекторы можно разделить на несколько групп [8]: • растительные полифенолы (экстракт плодов расторопши пятнистой, комбинированный препарат, содержащий экстракт дымянки лекарственной и экстракт расторопши пятнистой, и др.); • синтетические препараты (морфолиний-метил-триазолил-тиоацетат); • фосфолипидные препараты; • органопрепараты (гидролизат экстракта печени со стандартизированным количеством цианокобаламина и др.). К сожалению, многие из этих препаратов еще не доказали свою эффективность в крупных клинических исследованиях. 1. Препараты силимарина. Механизм его действия связан с подавлением ПОЛ и синтеза коллагена клетками Ито (антифибротический эффект). Назначают силимарин в дозе 70–100 мг/сут курсом не менее 3-х мес, часто в рамках комбинированной терапии. 2. S-адеметионин. Его использование при АБП связано с необходимостью для организма восполнения эндогенного адеметионина, выполняющего одну из основных функций в промежуточном обмене. Его назначение особенно оправдано при наличии синдрома холестаза (повышение ГГТП и ЩФ). Рекомендуемые дозы адеметионина составляют 800 мг/сут – при парентеральном введении (в течение 2 нед.) и 1600 мг/сут – per os (от 2 до 4–8 нед.). Недостаток перпарата заключается в низкой биодоступности при пероральном введении (5%). 3. Имеются указания на улучшение клинико-биохимической и гистологической картины на фоне применения у больных АБП урсодезоксихолевой кислоты, что, вероятно, связано не только с ее антихолестатическим эффектом, но и с подавлением секреции противовоспалительных цитокинов. 4. Эссенциальные фосфолипиды (ЭФЛ). Мембраностабилизирующее и гепатопротективное действие ЭФЛ достигается путем непосредственного встраивания молекул в фосфолипидную структуру поврежденных гепатоцитов, замещения дефектов и восстановления барьерной функции липидного бислоя мембран. 5. Тиотриазолин (морфолиний-метил-триазолил-тиоацетат) обладает антиоксидантными и антигипоксантными свойствами. Поскольку в патогенезе алкогольного гепатита немалая роль отводится оксидативному стрессу, патогенетически оправданным является назначение препаратов, ингибирующих процессы ПОЛ [8]. В многочисленных исследованиях доказано, что при алкогольном гепатите происходит образование большого количества активных форм кислорода, таких как гидроксильный радикал (HO•), супероксид-анион (O2•), синглетный кислород (1О2) и т.д. Свободные радикалы способствуют окислению липидов мембран гепатоцитов, что приводит к образованию пор и выходу через поврежденную мембрану ферментов и прочих компонентов цитоплазмы. Тиотриазолин содержит в своей структуре тиоловую группу, которая способна принимать от активных форм кислорода электроны, при этом сера в тиольной группе переходит от двух- к четырехвалентному состоянию. Антиоксидантное действие препарата также проявляется в том , что он активирует антиоксидантные ферменты – супероксиддисмутазу, каталазу, глутатионпероксидазу, содействует более экономному расходу эндогенного антиоксиданта – -токоферола [9]. Также есть данные, свидетельствующие об ингибирующем действии Тиотриазолина на процессы окислительной модификации белка [10]. Показано, что у пациентов с заболеваниями печени Тиотриазолин снижает интенсивность эндогенной интоксикации, уменьшает выраженность цитолиза, предупреждает развитие осложнений и уменьшает длительность пребывания больных в стационаре [11]. Подбор доз препарата должен осуществляться дифференцированно, с учетом степени выраженности цитолиза. При заболеваниях печени Тиотриазолин в первые 5 дней заболевания вводят внутривенно медленно струйно или капельно по 4 мл 2,5% раствора, либо, при невозможности внутривенного введения, внутримышечно 1–2 раза в день. Поддерживающая терапия проводится до 3-х нед. из расчета 600 мг/сут (по 1 таб. 200 мг 3 раза в день). В настоящее время накоплен большой опыт клинического использования препарата не только при заболеваниях желудочно-кишечного тракта но и сердечно-сосудистых и неврологических заболеваниях. Тиотриазолин хорошо сочетается с другими фармакологическими средствами, что позволяет его использовать в комбинированной терапии. В заключение хочется отметить, что для решения проблемы алкогольного поражения печени, прежде всего важна своевременная диагностика «злоупотребления алкоголем» и хронической алкогольной интоксикации. Сами пациенты порой не осознают, что употребляют алкоголь в субтоксических и токсических дозах, отрицая связь симптомов «недомогания» с алкоголем. При этом показано, что 33% пациентов, обращающихся в поликлиники, злоупотребляют алкоголем, а среди поступивших в стационары их доля возрастает до 60% [12]. В этой связи крайне важно любому практикующему врачу уметь вовремя распознать признаки ХАИ и разъяснить пациентам истинные причины их недугов. Ведь в большинстве случаев алкогольному гепатиту предшествует длительный этап алкогольного гепатоза, который либо не был распознан, либо оставался без должного внимания. Если АГ уже развился и мы не смогли «предотвратить болезнь», на сегодняшний день все же имеется довольно широкий арсенал терапевтических средств для лечения пациента. Здесь необходимо грамотно оценить тяжесть заболевания и возможные риски для выбора оптимальной тактики лечения. Важно помнить, что до стадии цирроза, во многих случаях АБП обратима, конечно при условии абсолютной абстиненции.♦
Механизм лечения синдрома
Цель лечения — остановить дальнейшее развитие заболевания печени и прекратить некроз клеток органа. Самое главное, чтобы пациент полностью перестал употреблять алкоголь. Также весомым фактором в выздоровлении является соблюдение диеты. Больному нужно обеспечить хорошее питание с витаминными добавками и обильное питье.
В терапии также применяют мочегонными и гипотензивными средствами. Они снижают кровяное давление печени. Если функция печени настолько плохая, что отходы, например, аммиак, не удаляются естественным путем, они влияют на мозг, и развивается печеночная недостаточность (энцефалопатия печени). Так как аммиак вырабатывается в толстой кишке, его выведение можно увеличить с помощью слабительных препаратом. При лечении цирроза используются антибиотики и назначаются богатые белком диеты.
В случаях развития тяжелой желтухи и алкогольного воспаления их лечат корковым гормоном надпочечников – преднизолом.
Когда следует обратиться за помощью
Если вы или ваши родственники считаете, что существует проблемы с алкоголем, поговорите со своим семейным врачом или проконсультируйтесь с наркологом. Если вы подозреваете, что развилось заболевание печени, следует сообщить об этом доктору и пройти необходимые обследования.
Обратиться к специалисту нужно в следующих случаях:
· Систематическое употребление алкоголя на протяжении 1 года (Алкоголизм).
· Общее недомогание: сонливость, хроническая усталость.
· Перенесенные ранее заболевания печени.
· Наличие диспепсического синдрома: утренняя тошнота, несварение желудка, рвота, изменение стула.
· Тремор конечностей.
· Резкое изменение массы тела (дистрофия или ожирение).
· Увеличение околоушных лимфатических узлов (контрактура Дюпюитрена).
· Признаки гипогонадизма. У мужчин они проявляются как небольшая выраженность вторичных половых признаков: атрофия яичек, гинекомастия, женский тип роста волос.
· Боли в подреберье, тяжесть в желудке.
Симптомы болезни
АБП может протекать бессимптомно. Вместе с тем, симптомы алкогольного поражения печени могут быть неспецифическими. К ним относятся такие жалобы, как тяжесть или боль в правом подреберье, вздутие живота, нарушение стула, тошнота и др.
Кроме печени в патологический процесс могут вовлекаться и другие органы и системы. В частности, может отмечаться атрофия мышц плечевого пояса, нарушение чувствительности в конечностях (полинейропатия), заболевания сердца (кардиомиопатия), поджелудочной железы (панкреатит).
Как развиваются болезни печени
Жировое перерождение печени
Если это ожирение печени, то прекращения употребления алкоголя будет достаточно, чтобы предотвратить дальнейшее развитие недуга. Со временем количество жировых клеток уменьшится, и симптомы заболевания пройдут. Пациенту назначается полная отмена алкоголя, специальное диетическое питание и медицинские препараты для восстановления клеток органа.
Цирроз печени
Алкогольный цирроз печени — это опасное и неизлечимое заболевание с высокой смертностью и значительно сниженным качеством жизни. Цирроз начинается с ожирения печени и при отсутствии своевременного лечения приводит к необратимым последствиям и дальнейшей смерти.
Цирроз перерастает в хроническое заболевание, которое прогрессирует в асцит, если потребление алкоголя продолжается. Это приводит к значительному увеличению смертности и сложной жизни со следующими симптомами.
· Хроническая усталость и постоянное отсутствие сил.
· Склонность к варикозному расширению вен в пищеводе. Это явление перерастает в кровавую рвоту.
· Склонность к инфекциям (снижение иммунитета).
· Часто возникают психические расстройства, такие как трудности с концентрацией внимания, причудливые паттерны поведения, нарушения сна, депрессия.
Эти осложнения, существенно сокращают продолжительность жизни. В особо запущенных случаях проблема решается трансплантацией печени.
Алкогольное воспаление печени
Это заболевание возникает на фоне интенсивного употребления алкоголя в течение 1 и более года. Алкогольное воспаление без отказа от употребления спиртного и отсутствия лечения приводит пациента к смерти.
Причины, факторы риска
Основная причина развития АБП — злоупотребление алкоголем, однако прямой зависимости между дозами регулярно употребляемых спиртных напитков и возникновением болезни, степенью ее прогрессирования и прогнозом не установлено1,3. Основными факторами риска развития АБП являются:
- Ежедневный длительный прием алкоголя в токсических дозах: больше 30г этанола для мужчин10 (это 75 г водки или 600 мл пива), а для женщин — 20 г (примерно 200 мл вина) в сутки1. Допустимое к ежедневному потреблению количество алкоголя, расценивающееся как «безопасная доза», разнится: в европейских рекомендациях по диагностике и лечению АБП10, например, «безопасной дозой» для женщин считают прием 12 г этанола в сутки и 24 г/сутки для мужчин. Влияет и вид напитка: появились данные, что среди потребителей красного вина, риск развития алкогольного цирроза печени ниже, чем при употреблении пива или крепких спиртных напитков4. Однако, не стоит воспринимать такие новости как руководство к действию. В любом случае алкоголь — фактор токсического повреждения, поэтому следует осторожно относиться к употреблению алкогольных напитков даже в самых малых дозах.
- Наследственность. Предрасположенность к развитию алкогольной болезни печени объясняется генетически обусловленными различиями в работе ферментных систем, отвечающих за нейтрализацию этанола1.
- Этническая принадлежность. Недостаточная активность фермента, метаболизирующего этанол, наблюдается у 50% населения Азии.1
- Избыточный вес или ожирение. Является независимым фактором риска развития АБП.1
- Алкогольная зависимость у лиц с вирусными гепатитами (особенно В и С) ассоциировано с более выраженными патологическими изменениями в органе, а также с более высоким уровнем смертности в сравнении с пациентами, не страдающими вирусными гепатитами.1
- Аутоиммунные процессы. Патологические иммунные реакции могут обуславливать дальнейшее повреждение органа даже после прекращения действия алкоголя.1
Механизм развития АБП
Этанол в желудке и в печени окисляется до ацетальдегида, весьма реактогенного соединения, которое повреждает белки, нарушает их функции, что в свою препятствует нормальной функции клеток печени, стимулирует перекисное окисление липидов свободными радикалами.
При этом нарушается обмен жиров и отложение жировых капель в клетках печени. Токсическое действие ацетальдегида ведет также к повреждению мембран клеток и, в конечном счете, их гибели.1
Статистика заболеваемости
- Ожирение клеток – достаточно распространенная проблема среди населения постсоветских стран. Недугом страдают до 10% всех жителей России. Это в первую очередь связано с чрезмерным употреблением алкоголя, избыточным весом и высоким уровнем заболевания сахарным диабетом.
- Алкогольный цирроз возникает с вероятностью около 1000 новых случаев в год. Например, в Дании около 12 000 человек имеют эту болезнь, по Российской федерации это количество точно не определено. Известно, что показатели заболеваемости в разы выше, чем в европейских странах. Отсутствие точных данных по заболеваемости объясняется тем, что многие случаи диагностируются только после вскрытие умершего пациента.
- Алкогольное воспаление является более редким заболеванием и насчитывает меньшее количество новых случаев в год, чем цирроз.