Сабрил – Sabril (Вигабатрин)
Фармакологическое действие
Противоэпилептическое средство. Необратимый селективный ингибитор GABA-аминотрансферазы. Повышает концентрацию GABA в синапсах, увеличивая, тем самым, тормозные эффекты. Подавляет повышенную возбудимость нейронов, лежащую в основе возникновения и распространения эпилептических судорог.
Показания активного вещества ВИГАБАТРИН
Парциальные судороги, синдром Веста.
Режим дозирования
Внутрь взрослым по 500 мг 2 раза/сут, при необходимости дозу увеличивают до 1.5 г/сут.
Для детей рекомендуется начальная доза 40 мг/кг/сут, при необходимости доза может быть увеличена до 80-100 мг/кг/сут.
Побочное действие
Со стороны ЦНС и периферической нервной системы: беспокойство, раздражительность, агрессивность, психотические нарушения; редко – головные боли, нистагм, тремор, парестезии, нарушение способности к концентрации внимания, повышенная утомляемость, нарушения поля зрения; в единичных случаях – повышение частоты развития эпилептических припадков, включая эпилептический статус.
Прочие: редко – незначительно выраженные диспептические симптомы, увеличение массы тела; в единичных случаях – отеки.
Противопоказания к применению
Беременность, лактация (грудное вскармливание), повышенная чувствительность к вигабатрину.
Применение при беременности и кормлении грудью
Противопоказан к применению при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции почек
У пациентов пожилого возраста особенно при нарушениях функции почек (КК менее 60 мл/мин) требуется коррекция режима дозирования.
Применение у детей
Применение возможно согласно режиму дозирования.
Применение у пожилых пациентов
У пациентов пожилого возраста и особенно при нарушениях функции почек (КК менее 60 мл/мин) требуется коррекция режима дозирования.
Особые указания
С осторожностью применять у пациентов с психическими заболеваниям, указаниями в анамнезе на психозы и нарушения поведения.
В период лечения требуется тщательное медицинское наблюдение для выявления возможных побочных реакций со стороны нервной системы.
При необходимости прекращения лечения рекомендуется постепенно снижать дозу в течение 2-4 недель. Внезапная отмена лечения может привести к возобновлению судорог.
Перед началом и в процессе лечения требуются периодические консультации офтальмолога. При выявлении дефектов полей зрения вопрос о дальнейшем применении вигабатрина решается в зависимости от соотношения риска и пользы проводимой терапии. В случаях, когда выявление дефектов полей зрения не может быть выполнено соответствующим образом (например, у маленьких детей), решение о терапии вигабатрином должно базироваться на анализе клинических показателей, которые позволяют оценить соотношение риска и пользы лечения.
У пациентов пожилого возраста и особенно при нарушениях функции почек (КК менее 60 мл/мин) требуется коррекция режима дозирования.
В экспериментальных исследованиях показано, что вигабатрин вызывает обратимый отек миелиновых оболочек. В настоящее время отсутствуют подтверждения такого же феномена у человека.
Влияние на способность к управлению транспортными средствами и механизмами
С осторожностью применять у пациентов, деятельность которых связана с необходимостью высокой концентрации внимания и быстрых психомоторных реакций.
Лекарственное взаимодействие
При одновременном применении возможно уменьшение концентраций в плазме крови фенитоина, фенобарбитала, примидона.
Заказать товар
Применение антиконвульсантов в педиатрической практике
История лекарственного лечения эпилепсии начинается с середины XIX в., когда было открыто противосудорожное действие бромидов. Соли брома подавляли генерализованные тонико-клонические припадки, однако обладали сильным седативным эффектом и были токсичны при длительном применении [1]. С начала XX в. широко применяется первый противосудорожный препарат из группы барбитуратов — фенобарбитал. В дальнейшем в практику вошли и другие барбитураты — примидон (гексамидин) с 1952 г. и отечественный препарат бензонал. Однако седативный эффект барбитуратов по-прежнему был слишком высоким. В 1937 г. началось использование фенитоина. Положительным свойством фенитоина было отсутствие седативного действия, к недостаткам относились нелинейная кинетика и выраженные косметические побочные действия. На сегодняшний день барбитураты и фенитоин в России еще производятся и используются, однако в большинстве развитых стран препараты этих групп считаются устаревшими и применение их в детской практике не рекомендовано.
60-е годы XX в. — время, когда в развитых странах в практику вошли препараты, которые сейчас относят к базовым антиконвульсантам: вальпроаты, карбамазепин, этосуксимид, бензодиазепины, сультиам, ацетазоламид. Препараты этого поколения постепенно вытеснили более токсичные старые антиконвульсанты и доминировали на рынке до середины 1990-х. Бензодиазепины в дальнейшем перешли в разряд лекарственных средств третьей-четвертой очереди выбора из-за часто развивающейся толерантности приступов к ним.
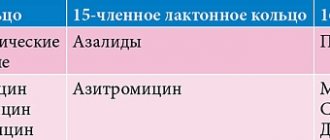
1990-е годы — время появления так называемых «новых» антиконвульсантов: окскарбазепина, ламотриджина, вигабатрина, габапентина, фелбамата, топирамата, тиагабина, зонисамида, стирипентола (препараты приведены в порядке появления на рынке). В России зарегистрирована часть этих препаратов, причем не все из них разрешены для применения у детей (табл. 1). Данный обзор касается применения в педиатрической эпилептологии как базовых, так и новых антиконвульсантов. Суточная доза антиконвульсантов в детской эпилептологии рассчитывается исходя из массы тела пациентов. Дозировки, в том числе и для устаревших антиконвульсантов, приведены в таблице 2.
Основные антиконвульсанты
Вальпроат натрия. История клинического применения вальпроата насчитывает более 35 лет, и за это время он стал одним из наиболее популярных антиконвульсантов [2]. Вальпроевая кислота и ее соли обладают широким спектром действия и могут назначаться практически при всех формах эпилепсии в качестве препаратов первой очереди выбора, даже до уточнения формы заболевания. Исключение составляет синдром Веста, при котором вальпроаты в значительной степени уступают по эффективности вигабатрину и гормональной терапии. Широкий спектр действия препарата обычно связывают со множественностью механизмов действия. Сообщалось, что вальпроат блокирует вольтажзависимые натриевые каналы нейронов, однако, в отличие от карбамазепина и фенитоина, не влияет на восстановление канала из инактивированного состояния. Вальпроат в высокой концентрации действует на кальциевые каналы T-типа, снижает концентрацию аспартата и увеличивает уровень содержания GABA [3].
Для вальпроатов также характерен низкий (2%) уровень аггравации приступов [4]. К достоинствам препарата относится возможность при необходимости назначить препарат сразу в минимальной терапевтической дозе, минуя период длительной титрации. Если минимальная терапевтическая доза неэффективна, следует перейти к средней и максимальной дозе, прежде чем заменять препарат или прибегать к политерапии. Поскольку действие вальпроата может быть отсроченным, промежуток между повышением дозы должен составлять от 2 нед до 1 мес.
В аптечной сети имеется в наличии большое количество детских (сироп, капли), делимых ретардированных форм (депакин хроно, конвулекс ретард), кишечно-растворимых форм (депакин энтерик). Предпочтение следует отдавать ретардированным формам, так как двукратный прием антиконвульсанта удобнее для родителей школьника. Индивидуальную дозу следует назначать из расчета на кг массы тела в сутки, но так, чтобы суточную дозу можно было легко подобрать с помощью мерной ложки или риски на делимой таблетке, поскольку любые неудобства, связанные с приемом лекарства, приводят к некомплаентности (пропуску приемов, самовольному изменению дозы). Длительное применение вальпроата требует контроля за ферментами печени (АЛТ, АСТ), поджелудочной железы (амилаза), уровня аммония в крови. Повышение содержания аммония встречается у 20–50% пациентов и чаще всего протекает бессимптомно, но в отдельных случаях может проявляться симптомами энцефалопатии. Другим серьезным осложнением терапии вальпроатом является гепатопатия, риск которой особенно высок у детей в возрасте до 2 лет, получающих политерапию. В качестве антидота при вальпроевой энцефалопатии и гепатопатии используется L-карнитин [2].
Терапевтическая концентрация препарата составляет 50–100 мг/л, однако потребность в ее измерении возникает либо при политерапии совместно с ферменто-индуцирующими препаратами, либо в случае резистентности приступов к терапии.
Карбамазепин. Считается, что карбамазепин (финлепсин, тегретол) стабилизирует в инактивированном состоянии вольтажзависимый натриевый канал, однако предполагаются и другие механизмы [3]. Карбамазепин эффективен при криптогенных и симптоматических парциальных эпилепсиях (при простых, сложных и вторично генерализованных припадках), при изолированных первично генерализованных тонико-клонических припадках. Применение его при идиопатических генерализованных эпилепсиях ограничено из-за аггравации карбамазепином абсансов и миоклонуса. В ряде случаев при наличии вторично-билатеральной синхронии на ЭЭГ при симптоматических лобных эпилепсиях карбамазепин также способен аггравировать приступы.
Риск атипичной эволюции, связанной с применением карбамазепина, привел к ограничению использования этого препарата при роландической эпилепсии. Однако карбамазепин высокоэффективен при детской затылочной эпилепсии с поздним дебютом (форма Гасто) и при аутосомно-доминантной лобной эпилепсии с ночными пароксизмами [5]. Его структурное сходство с трициклическими антидепрессантами позволяет использовать его в психиатрической практике, кроме того, препарат эффективен при невралгии тройничного нерва.
На практике имеет значение то, что карбамазепин полностью метаболизируется до 10–11-эпоксида карбамазепина, при этом индуцируя микросомальные ферменты печени. Это значит, что, определившись с целевой дозой (у детей обычно в пределах 10–30 мг/кг веса в сутки), необходимо начинать с назначения около 5 мг/кг веса в сутки и увеличивать дозировку постепенно, чтобы избежать дозозависимых побочных действий. Препарат способен снижать концентрацию вальпроатов, и хотя (при резистентных парциальных эпилепсиях) может использоваться в комбинации с ними, такая схема не считается рациональной и может потребовать контроля уровня препаратов в крови. Терапевтическая концентрация карбамазепина — 4–12 мг/л.
В педиатрии удобны для применения делимые ретардированные формы карбамазепина (финлепсин ретард, тегретол ЦР), позволяющие назначать препарат 2 раза в сутки, несмотря на короткий период полувыведения карбамазепина. При длительном лечении карбамазепином необходимо осматривать кожу и слизистые ребенка, контролировать гематологические показатели. Для своевременной диагностики вторично-билатеральной синхронии следует проводить контрольные ЭЭГ-исследования.
Этосуксимид. Единственный механизм действия этосуксимида (суксилеп) — это блокада вольтажзависимых кальциевых каналов T-типа [3]. Уникальность этого механизма обеспечивает его высокую эффективность при абсансах, как типичных (при идиопатических генерализованных эпилепсиях), так и атипичных (при синдроме Леннокса–Гасто, при атипичной доброкачественной парциальной эпилепсии, синдроме Ландау–Клеффнера и др.). Кроме того, этосуксимид эффективен при так называемых «лобных абсансах» и при негативном миоклонусе. Однако препарат неэффективен в отношении генерализованных тонических, тонико-клонических и всех видов парциальных приступов, что не позволяет использовать этосуксимид в качестве монотерапии; наиболее часто используется комбинация этосуксимида и вальпроата, обладающая истинным синергизмом при абсансах у детей [2].
К достоинствам препарата относится возможность назначения сразу в терапевтической дозе, к недостаткам — отсутствие в России детских и делимых форм.
Новые антиконвульсанты
Ламотриджин. Ламотриджин (ламиктал) блокирует вольтажзависимые натриевые каналы, однако иным образом, чем карбамазепин, что можно предположить, исходя из широкого спектра действия этого препарата. Сообщалось также о блокаде вольтажзависимых кальциевых каналов, приводящей к снижению возбуждающего действия глутамата [1, 3]. Спектр действия ламотриджина включает все типы приступов и практически совпадает со спектром действия вальпроата. Взаимодействие этих двух препаратов синергично, при этом вальпроат увеличивает концентрацию ламотриджина, что позволяет снизить дозу последнего и тем самым повлиять на общую стоимость лечения.
К недостаткам ламотриджина относятся развитие кожной сыпи (у 11% детей) и синдромов Стивенса–Джонсона и Лиелла [1]. Риск осложнений снижается при медленной титрации дозы, однако это ограничивает применение ламотриджина в качестве препарата первой очереди выбора при вновь диагностированной эпилепсии. При назначении препарата в первый раз необходимо увеличивать дозу строго в соответствии с инструкцией по применению препарата и обучить родителей ежедневно осматривать кожу и слизистые ребенка. В дальнейшем необходимость в таком контроле отпадает.
К положительным свойствам ламотриджина относится минимальное по сравнению с другими антиконвульсантами влияние на когнитивные функции и меньший, чем при использовании других препаратов, риск развития кистоза яичников у пациенток либо пороков развития нервной трубки у ребенка от матери с эпилепсией [6–9].
Ламотриджин аггравирует приступы при тяжелой миоклонической эпилепсии младенческого возраста (синдроме Драве) и категорически противопоказан при этой форме. Сообщалось о единичных случаях усиления миоклоний при юношеской миоклонической эпилепсии, однако это не препятствует назначению ламотриджина, наряду с вальпроатами и топираматом, при этой часто встречающейся форме эпилепсии, в особенности у лиц женского пола.
Топирамат. Топирамат (топамакс) считается одним из самых многообещающих антиконвульсантов благодаря множественным механизмам действия: блокаде вольтажзависимых натриевых каналов и вольтажзависимых кальциевых каналов; усилению действия GABA на GABAA-рецепторы; блокаде медиаторов возбуждения (глутамата); угнетению карбоангидразы II и IV типов [3].
Показано, что препарат обладает нейропротективным эффектом при экспериментальном эпилептическом статусе [10]. Показанием к применению топирамата являются большинство эпилепсий и эпилептических синдромов, за исключением абсансных эпилепсий: в этом случае он уступает вальпроату. Эффективность топирамата при резистентных формах эпилепсии несколько выше, чем у базовых антиконвульсантов [11, 12].
К недостаткам топирамата относится необходимость медленной титрации дозы (для детей — не быстрее чем 1 мг на кг массы тела в неделю). Такая титрация нужна для снижения риска возникновения побочных действий: гиперактивности, возбудимости, неусидчивости. С другой стороны, медленная титрация позволяет точнее подобрать индивидуальную дозу, так как «терапевтическое окно» препарата очень широко и контроль над приступами может быть достигнут как при дозе 1 мг на кг массы тела в сутки, так и 10–15 мг на кг массы тела в сутки. Верхняя граница дозы топирамата уточняется и у детей младше 2 лет может составить 20–25 мг на кг массы тела в сутки. В процессе лечения топираматом необходимо контролировать состояние почек.
Леветирацетам (кеппра). Как и многие новые антиконвульсанты, леветирацетам (на рынке присутствуют несколько лекарственных форм препарата) первоначально был зарегистрирован как препарат для дополнительного лечения криптогенных и симптоматических парциальных эпилепсий у взрослых. В дальнейшем препарат оказался эффективным и при идиопатических генерализованных эпилепсиях, включая юношескую миоклоническую эпилепсию [13].
При исследовании эффективности препарата у детей в качестве положительного эффекта отмечалось повышение концентрации внимания в 25% случаев. Наиболее частыми побочными действиями были возбудимость, агрессивность [14].
Механизм действия леветирацетама долгое время оставался неизвестным, однако в последнее время установлено, что леветирацетам связывается с пресинаптическим протеином SV2, находящимся в синаптических пузырьках. Функция протеина окончательно не выяснена, однако уникальность механизма действия леветирацетама и его структурное сходство с пирацетамом объясняют отличия в спектре действия леветирацетама и других новых антиконвульсантов. Леветирацетам в виде монотерапии или в комбинации с пирацетамом эффективно купировал миоклонус у пациентов с болезнью Унферрихта-Лундборга и другими прогрессирующими миоклоническими эпилепсиями [15 –17]. Несмотря на то что в России препарат не зарегистрирован для применения у детей, как можно более раннее назначение его как при прогрессирующих миоклонус-эпилепсиях, так и в лечении детей с непрогрессирующим миоклоническим статусом (при синдроме Ангельмана, постгипоксическом миоклонусе) представляется перспективным [15].
Возможна быстрая титрация дозы, однако на сегодняшний день границы дозировок в педиатрии точно не определены, существуют также единичные сообщения о парадоксальных реакциях на фоне приема высоких доз леветирацетама.
В заключение следует отметить, что сегодня на рынке антиконвульсантов в Российской Федерации представлено достаточное количество препаратов для лечения большинства форм эпилепсии у детей. Ограничительным фактором является высокая стоимость лечения новыми антиконвульсантами. Вместе с тем остаются незаполненными ниши применения препаратов, эффективных при отдельных формах детской эпилепсии. Это вигабатрин (сабрил) — эффективный при синдроме Веста (инфантильных спазмах), в особенности при туберозном склерозе; сультиам (осполот) — препарат, эффективный при синдромах, сочетающихся с электрическим эпилептическим статусом медленного сна (синдром Ландау–Клеффнера и др.), и роландической эпилепсии; клобазам (фризиум), бензодиазепин с наименьшей степенью развития толерантности. По-видимому, вопрос о регистрации в России этих препаратов должен быть поднят ассоциациями неврологов и родительскими организациями.
А. Ю. Ермаков, кандидат медицинских наук Московский НИИ педиатрии и детской хирургии, Москва
По вопросам литературы обращайтесь в редакцию.
Медицинские интернет-конференции
Туберозный склероз — генетически детерминированное заболевание, относится к группе нейроэктодермальных нарушений, характеризуется поражением нервной системы, кожи и наличием гамартом в различных органах. Наследуется по аутосомно-доминантному типу.
Клинический случай: пациентка М., 2 года 1 месяц, поступила в клинику с диагнозом: Туберозный склероз. Симптоматическая эпилепсия. Субэпендимальные гиганто-клеточные астроцитомы боковых желудочков головного мозга. Множественные рабдомиомы сердца.
В анамнезе: ребенок от 2 беременности, протекавшей без особенностей, физиологические роды на 38 неделе. Семейный анамнез не отягощен. Спорадический случай. По данным УЗИ на 30 неделе гестации, диагностирована рабдомиома сердца плода, туберозный склероз? При рождении на коже в области левой ягодицы 2 пигментированных пятна 3-5 мм, на передней поверхности брюшной полости 1 пятно 1,5 на 0,5 см. В области плеча справа- мелкий участок по типу шагреневой кожи, плотной консистенции, желтовато-коричневого цвета, умеренно выступает над поверхностью окружающей кожи.
На ЭХО-КГ: множественные рабдомиомы.
В 4 мес. появились кивательные движения головы, через 2 недели появились флексорные спазмы, через 2 недели приступы спонтанно прекратились. В возрасте 6 месяца отмечает появление «замираний», с отведением глаз и головы влево, напряжение мышц туловища и конечностей, длительностью до 2-х мин, до 2 раз в день. Наметилось отставание в развитии. Была назначена противосудорожная терапия: депакин хроносфера 100мг-2 р/д, на фоне которой удалось достичь положительной динамики. В 7 мес. при МРТ исследовании головного мозга был подтвержден диагноз Туберозный склероз. В 7,5 мес. появились серийные приступы тонического напряжения до 20 приступов в серию. В терапию был введен Сабрил (селективный необратимый ингибитор ГАМК-трансаминазы) — приступы купировались на дозе 500 мг в сутки по ½ табл утром и вечером через 12 часов. Приступов нет с 14.02.15г. В настоящее время – психомоторное развитие по возрасту.
Результаты: Сабрил обеспечил стойкий и положительный эффект, приступы купировались, состояние девочки улучшилось. Общее состояние удовлетворительное, сознание ясное. Обращенную речь понимает по возрасту. Общемозговые и менингеальные симптомы отсутствуют. Окружность головы 47,5 см. Движение глазных яблок: в полном объеме. Нистагма нет. Точки выхода тройничного нерва безболезненны. Лицо симметрично. Слух сохранен. Язык в полости рта по средней линии. Голова по средней линии. Пассивные движения в полном объеме, активные движения в полном объеме. Мышечная сила сохранена. Тонус мышц сохранен. Сухожильные рефлексы сохранены.
Международный неврологический журнал 5(21) 2008
В детской неврологии одной из самых сложных является проблема инфантильных спазмов, частота которых у детей может доходить до 250 приступов в сутки. Лечение больных с синдромом Веста сопряжено с рядом трудностей.
Под нашим наблюдением находятся 10 больных с синдромом Веста в возрасте от 2 месяцев до 3 лет, получающих вигабатрин (сабрил) и синактен депо. Судороги у детей раннего возраста были представлены инфантильными спазмами, а также сочетались с миоклониями, фокальными пароксизмами, генерализованными общесудорожными припадками, которые дебютировали в возрасте от 1 до 6 месяцев. С началом приступов у всех детей отмечалась задержка развития. Данные больные наблюдались по поводу эпилептического синдрома с приступами, резистентными к терапии. Частота серий в течение суток варьировала от 5 до 30, в серии насчитывалось до 64 инфантильных спазмов, максимальное количество приступов в сутки — до 242. У трех детей дебют судорожного синдрома совпал с началом вакцинации. Всем детям было проведено комплексное клиническое обследование, включавшее ЭЭГ, МРТ головного мозга, ЭКГ, ЭхоКГ, УЗИ внутренних органов, обследование на группу внутриутробных инфекций, консультирование в медико-генетическом центре. ЭЭГ выявила наличие гипсаритмии, высокоамплитудных комплексов пик- и полипик-волн, спайк-волн, что позволило подтвердить диагноз синдрома Веста. Проводимая ранее терапия не была эффективной.
Введение в терапию сабрила в комбинации с синактеном депо позволило добиться купирования приступов у 6 детей, при этом отмечаются улучшение когнитивных функций, положительная динамика по данным ЭЭГ. Удалось добиться урежения приступов, уменьшения их тяжести и улучшения когнитивных функций у 4 детей (в данной группе отмечалось сочетание инфантильных спазмов с другими видами приступов).
Приводим пример клинического наблюдения. Больной Б.Д., 9 месяцев. Дебют заболевания с 4 месяцев в виде серий инфантильных спазмов, до 5–7 серий в сутки (частота инфантильных спазмов в серии — до 15–19), сопровождающихся выраженным беспокойством ребенка. С началом приступов у ребенка отмечается задержка психомоторного развития. На фоне противосудорожной терапии частота приступов оставалась высокой (до 19–22 серий в сутки, частота инфантильных спазмов в серии — до 64, за сутки — до 242). Из анамнеза установлено: ребенок от I беременности с токсикозом, нефропатией, гипергликемией, I срочных родов, масса тела — 3600 г, ОША 8–9 баллов, на естественном вскармливании. Привит до 4 месяцев. Неврологический статус при поступлении: окружность головы — 44 см. Состояние ребенка тяжелое по заболеванию. Вяловат. Беспокоен периодически. Резко отстает в развитии. Голову держит, следит кратковременно, не переворачивается, не сидит, к игрушке не тянется, опора на ноги слабая. Большой родничок не напряжен. Глазные щели D = S, зрачки равны. Ng нет. Движения глазных яблок заметно не ограничены. Легкая асимметрия носогубных складок. Мышечный тонус в конечностях дистоничен. Сухожильные рефлексы повышены D > S.
Ребенок обследован в клинике с проведением ЭКГ, ЭхоКГ, УЗИ внутренних органов, обследован на внутриутробные инфекции. ЭЭ-картирование в июне 2008 г.: Сон. Фазы сна не определяются. На протяжении всей записи отмечается чередование низкоамплитудной медленноволновой полиморфной активности с периодами высокоамплитудных медленных полиморфных волн в сочетании с разрядами спайк-волн и острых волн, без четкой локализации. Можно предположить гипсаритмию, т.к. во сне паттерн гипсаритмии напоминает паттерн «вспышка — подавление». МРТ головного мозга 03.07.2008 г.: в белом веществе обеих гемисфер, перивентрикулярно и субкортикально визуализируются неправильной формы зоны. Срединные структуры не смещены. Умеренное расширение боковых желудочков мозга до 1,0 см, подоболочечные пространства выражено расширены в височно-лобно-теменных областях с обеих сторон (до 0,8 см). Определяется S-образная извитость экстракраниальных отделов обеих внутренних сонных артерий, с наличием слева в области извитости участка умеренного снижения интенсивности МР-сигнала (за счет изменения кровотока в области извитости (?)). Также отмечается умеренная извитость экстракраниальных отделов обеих ПА. Заключение: вышеописанные зоны в головном мозге могут быть обусловлены незавершенной миелинизацией (контроль в динамике). Умеренное расширение боковых желудочков мозга. Выраженное расширение подоболочечных пространств. S-образная извитость обеих ВСА, извитость обеих ПА.
Проведена терапия: сироп депакина (40 мг/кг в сутки), сабрил (60 мг/кг в сутки, дексаметазон, синактен депо, аспаркам, диакарб, никотиновая кислота. После введения в терапию синактена депо приступы купировались. После купирования приступов ребенок активнее следит, гулит, играет игрушками.
ЭЭ-картирование 09.09.2008 г.: Бодрствование. Регистрируется медленноволновая ЭЭГ с преобладанием дельта-активности и без признаков локальной патологии. Признаков пароксизмальной активности на момент обследования зарегистрировать не удалось. Функциональная незрелость.
Ребенок выписан из отделения в удовлетворительном состоянии. Ремиссия 1,5 месяца.
Таким образом, при лечении инфантильных спазмов препаратами выбора являются: депакин 30–50 мг/кг в сутки или вигабатрин (сабрил) в дозе 40–80 мг/кг в сутки в сочетании с гормональной терапией — синактен депо в дозе от 0,15 мл в сутки и далее по схеме. Данная комбинация продемонстрировала высокую эффективность у детей с синдромом Веста и способствовала ремиссии приступов до 2 лет, позволила улучшить развитие, когнитивные функции у детей.
Суд обязал выдать незарегистрированный в России «Сабрил» трем девочкам
Районный суд Рязани обязал региональный Минздрав выдать незарегистрированный в России препарат «Сабрил» трем тяжелобольным девочкам, сообщило рязанское общество «Мемориал».
«Больше года мамы девочек вместе с нашим юристом Петром Ивановым добивались выдачи препарата «Сабрил», который нужен для снижения частоты эпилептических приступов. Из-за того, что для закупки не зарегистрированного в России лекарства нужно запускать сложную процедуру, Минздрав под разными предлогами родителям отказывал, но суд посчитал такую позицию министерства незаконной», – говорится в сообщении.
Как рассказали «Милосердию.ru» в рязанском обществе «Мемориал», одной упаковки «Сабрила» пациенту хватает на 25 дней. Стоимость ее доходит до 7000 рублей. Принимать препарат нужно постоянно.
Согласно судебному решению, министерство должно начать закупку лекарства незамедлительно, так как промедление создает угрозу для здоровья детей, передает местное СМИ. «Для родителей такое решение суда – большая победа, но решение важно и для Рязанской области и России в целом. Долгое время Минздрав игнорировал закон и отказывался признать, что эти дети имеют право на бесплатное обеспечение «Сабрилом». Мы надеемся, что теперь тяжелобольные люди, которым по медицинским показаниям назначают незарегистрированные в России препараты, смогут своевременно получать лекарства согласно законной процедуре, а не тратить по несколько месяцев на прокуратуры и суды, как в этом случае», – отметил Петр Иванов, который представлял интересы родителей в суде.
Ранее Петр Иванов объяснил «Милосердию.ru», на какие нормативные акты опираются родители тяжелобольных детей, добиваясь предоставления им незарегистрированных лекарств. «После того, как в конце 2014 года был принят закон, который ввел в Уголовный кодекс и КоАП статьи, запрещающие ввозить в Россию незарегистрированные лекарства, родители какое-то время вообще не могли получать такие препараты, опасаясь условных сроков и огромных штрафов. Потом Минздрав дал разъяснение и сказал, что для личного пользования ввозить можно. То есть родители могут самостоятельно поехать за границу, купить лекарство и привезти для своего ребенка. Естественно, такие деньги есть только у единиц», – сказал Иванов.
Однако существует приказ Минздрава от 9 августа 2005 года № 494 «О порядке применения лекарственных средств у больных по жизненным показаниям». «В этом документе сказано, что если лекарственный препарат нужен по жизненным показаниям (без него наступит серьезное ухудшение здоровья или даже летальный исход), то консилиум врачей может его назначить», – пояснил юрист.
«Если консилиум такой препарат назначил, то здесь уже будет действовать другая норма – статья 80 федерального закона “Об основах охраны здоровья граждан”, – продолжил он. – В этой статье четко сказано, что не подлежат оплате за счет личных средств граждан препараты, не входящие в перечень ЖНВЛП, в случае их замены из-за индивидуальной непереносимости по жизненным показаниям.
То есть, если нельзя назначить препарат, входящий в перечень бесплатных лекарств, и этот препарат нужен по жизненным показаниям, в таком случае он предоставляется бесплатно».
Если лекарство назначено ребенку по жизненным показаниям, даже если оно не зарегистрировано в России, назначить его могут, и государство обязано его предоставить, резюмировал Петр Иванов.
Продержаться всего лишь один год!