Введение
Абдоминальная боль (АБ) является одним из распространенных поводов для обращения за медицинской помощью (после головной боли, болей в спине и головокружения) и может быть связана как с проходящими самостоятельно нарушениями, так и с тяжелыми, угрожающими жизни состояниями, требующими немедленного медицинского вмешательства. Установление правильного диагноза может быть затруднено в связи с наличием в брюшной полости множества систем органов, а также из-за того, что АБ могут вызывать многие болезни. В связи с этим АБ во всем мире занимаются врачи общей практики/семейные врачи, хирурги, терапевты, врачи неотложной помощи, педиатры, гастроэнтерологи, урологи и гинекологи.
Обычно АБ относится к одной из следующих категорий:
1. Процесс, приводящий к воспалению париетальной брюшины и/или связанный с воспалением паренхиматозных органов, обычно сопряжен с возникновением постоянной, ноющей боли, усиливающейся при изменении натяжения брюшины при надавливании/сдавлении, растяжении или изменении положения. Она часто сопровождается дефансом – сокращением мышц живота для уменьшения напряжения брюшины.
2. Боль, связанная с непроходимостью полого органа, часто схваткообразная или имеющая характер “колик”, что соответствует перистальтическим движениям органа, направленным на устранение обструкции.
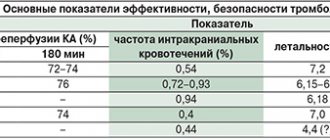
3. Боль, связанная с сосудистыми нарушениями в брюшной полости (тромбоз или эмболия), вызвана гипоксией/ишемией тканей дистальнее места окклюзии; может возникать резко или постепенно, быть сильной или легкой.
4. Функциональные желудочно-кишечные нарушения, такие как функциональная диспепсия и синдром раздраженного кишечника СРК [1]. 5. АБ может быть связана с поражением органов, не находящихся в брюшной полости (например, нижнедолевая пневмония).
По частоте встречаемости ведущее место при возникновении АБ занимает воспаление полых и паренхиматозных органов, сопровождающееся раздражением брюшины. Примерами могут служить такие распространенные заболевания, как гастрит, гастроэзофагеальная рефлюксная болезнь (ГЭРБ), пептическая язва, аппендицит, холецистит, гепатит, кишечная непроходимость, колики при уретрите, цистит, пиелонефрит и первичная дисменорея.
Ссылки [ править ]
- «2-Бром-2-метилпропан — Резюме соединения» . PubChem Compound
. США: Национальный центр биотехнологической информации. 26 марта 2005 г. Опознание . Проверено 16 июня 2012 года . CS1 maint: обескураженный параметр ( ссылка ) - Справочник CRC по химии и физике 65-е изд.
- Райнерс, Матиас; Эрлих, Нико; Уолтер, Марк Д. (2018). «Синтез 1,3,5- три- трет-
бутилциклопента-1,3-диена и его металлических комплексов Na {1,2,4- (Me 3 C) 3 C 5 H 2 } и Mg {η 5 -1 , 2,4- (Me 3 C) 3 C 5 H 2 ) 2 «.
Неорганические синтезы
.
37
: 199. DOI : 10.1002 / 9781119477822.ch8 . - «2-Бром-2-Метилпропан 135615.» H2NC6H4CO2C2H5, лекарства, www.sigmaaldrich.com/catalog/product/aldrich/135615?lang=en®ion=US.
- «Структуры 2-бром-2-метилпропана». Кембриджский центр структурных данных (CCDC), www.ccdc.cam.ac.uk/structures/search?id=doi:10.5517/ccvcqmj&sid=DataCite
Фармакологические свойства гиосцина бутилбромида
Гиосцина бутилбромид (ГББ) является производным гиосцина, получаемым из листьев дерева Дубоизия (Duboisia), произрастающего преимущественно в Австралии. ГББ также известен как скопаламина-N-бутилбромид, N-бутилскополаммония бромид и бутилскополамин. Молекулярная формула – C21H30BrNO4, молекулярный вес составляет 440,37.
ГББ содержит молекулу азота, связанную четырьмя различными связями с разными химическими группами; таким образом, это четвертичное аммониевое соединение. Молекула ГББ высокополяризована и в отличие от аммония и других подобных соединений сохраняет полярность независимо от рН среды. В связи с этим при пероральном применении происходит лишь частичная абсорбция препарата (8 %), а системная биодоступность составляет менее 1 %. Тем не менее, несмотря на низкие уровни в крови сразу после введения, ГББ и/или его метаболиты обнаруживаются в местах действия.
Препарат не проникает через гематоэнцефалический барьер и обладает низким связыванием с белками плазмы. Метаболизм осуществляется в основном путем гидролиза эфирной связи. После приема внутрь экскреция препарата происходит с калом и мочой.
Как известно, в парасимпатической нервной системе ацетилхолин (АЦХ) действует на два типа рецепторов, мускариновые и никотиновые холинергические рецепторы. В большинстве случаев нервная передача происходит в два этапа: при стимуляции преганглионарный нерв выделяет в ганглий АЦХ, который действует на никотиновые рецепторы постганглионарных нейронов. Затем постганглионарный нейрон выделяет АЦХ для возбуждения мускариновых рецепторов органа-мишени.
Хорошо изучены три основных типа мускариновых рецепторов:
• М1-мускариновые рецепторы, находятся в нервной системе.
• М2-мускариновые рецепторы, расположены в сердце.
• М3-мускариновые рецепторы, расположены во многих частях тела, особенно в гладкой мускулатуре кровеносных сосудов, бронхов и желудочно-кишечного тракта (ЖКТ), а также различных железах, связанных с дыхательным трактом и ЖКТ. Стимуляция этих рецепторов приводит к опосредованной вазодилатации (благодаря образованию оксида азота), бронхоконстрикции и усилению моторики кишечника, а также увеличению секреции желез. М3-рецепторы обнаружены также в цилиарном теле и мышцах радужки глаза, где они участвуют в аккомодации и позволяют контролировать размер зрачка.
Существуют также М4- и М5-рецепторы; последние обнаружены только в центральной нервной системе (ЦНС). Полная характеристика действия и локализация М5-рецепторов не до конца изучены.
Недавно проведенные исследования также показали, что ГББ является сильнодействующим неконкурентным блокатором никотиновых рецепторов in vitro. Если такой эффект имеет место и in vivo, он может вносить свой вклад в известный механизм спазмолитического действия препарата [2].
ГББ блокирует действие АЦХ в парасимпатических рецепторах гладких мышц и секреторных желез. На этом основан как механизм действия ГББ, так и его побочные эффекты. Таким образом, ГББ вызывает снижение моторики ЖКТ и мочеполового тракта, применяется для устранения спазмов этих систем, появление которых возможно при гастроэнтеритах, колитах, воспалительных заболеваниях кишечника, дивертикулите, желчных коликах, цистите, коликах при уретрите и первичной дисменорее. Также он используется для предотвращения спазмов ЖКТ перед радиологическими и диагностическими исследованиями, такими, как эндоскопическая ретроградная холангиопанкреатография и колоноскопия. Исходя из механизмов действия ГББ, возможно возникновение побочных явлений/нежелательных реакций.
Наиболее распространенные из них: кожные реакции (например, крапивница, сыпь, эритема, зуд) и другие виды гиперчувствительности, тахикардия, сухость во рту, задержка мочи. Многие из перечисленных нежелательных эффектов могут быть связаны с антихолинергическими свойствами препарата. Антихолинергические побочные эффекты обычно выражены слабо и проходят самостоятельно. Необходимо отметить, что как четвертичное аммониевое соединение ГББ не проникает через гематоэнцефалический барьер и поэтому не вызывает нежелательных явлений со стороны ЦНС.
Периферические антихолинергические эффекты развиваются из-за ганглиоблокирующего действия на стенки внутренних органов, а также благодаря антимускариновому действию.
Применение ГББ противопоказано при миастении и мегаколоне/болезни Гиршпрунга. Кроме того, его не следует назначать парентерально пациентам с некомпенсированной узкоугольной глаукомой, при тахикардии; гипертрофии простаты с задержкой мочи; при механическом стенозе ЖКТ.
Другие аспекты [ править ]
трет-
Бутилбромид, используемый для изучения массового деаденилирования нуклеозидов на основе аденина, индуцированного галогенированными алканами ( алкилгалогенидами ) в физиологических условиях. 2-Бром-2-метилпропан вызывает массивное дегуанилирование нуклеозидов на основе гуанина и массивное деаденилирование нуклеозидов на основе аденина. [4]
Фазовый переход от орторомбической фазы III Pmn21 при низких температурах (измерения от 95 К) к неупорядоченной ромбоэдрической фазе II при 205-213 К. Фаза II может существовать при 213-223 К, частично совпадая с фазой ГЦК I, которая может быть наблюдается между 210-250 К. Фазовые переходы изучались также при высоком давлении (до 300 МПа) [5]
Обзор клинического применения гиосцина бутилбромида
Боль в животе (неспецифические колики) и СРК
Способность ГББ устранять неспецифические коликообразные АБ объясняется его антимускариновым действием. Клинически это действие проявляется расслаблением гладкой мускулатуры ЖКТ, благодаря чему уменьшаются/исчезают спазмы/колики, ощущаемые пациентом. Данный эффект был объективно продемонстрирован в исследовании электрической и биомеханической активности желудка, в котором внутривенное введение 20 мг ГББ привело к уменьшению показателя механической моторики на 50,9 %, а показатель электрической моторики составил 36,5 % [3].
Основными областями клинического применения ГББ при АБ являлись неспецифическая абдоминальная боль по типу колик, СРК, желчные колики и ГЭРБ.
Применение ГББ при неспецифической АБ изучалось в ряде недавно проведенных исследований. В одном из последних крупных исследований производилось сравнение эффективности и переносимости 10 мг ГББ при применении 3 раза в сутки, 500 мг парацетамола 3 раза в сутки и их фиксированной комбинации по сравнению с плацебо у пациентов с периодической спастической болью в животе [4]. Всем 1637 пациентам в течение недели давали плацебо, после чего была проведена рандомизация на группы получающих один из 4 видов лечения в течение 3 недель. Выраженность боли (в соответствии с визуальной аналоговой шкалой и словесной оценочной шкалой) статистически значимо уменьшилась во всех группах лечения по сравнению с плацебо. Лечение хорошо переносилось во всех группах, частота возникновения побочных эффектов между группами существенно не различалась.
В другом исследовании, в котором принимали участие 204 ребенка, находившихся под наблюдением в течение недели, производилось сравнение ГББ с гомеопатическим средством. Оказалось, что оба препарата обеспечивали значительное уменьшение симптомов (выраженности спазмов, боли/колик, нарушений сна, затруднений при еде и питье, частого плача) по наблюдениям родителя/лица, осуществлявшего уход, и хорошо переносились [5].
Tytgat и соавт. опубликовали два обзора, касающихся применения ГББ перорально/энтерально для лечения спастических болей в животе и при ряде других клинических сценариев [6, 7]. В первом из них приведено 10 плацебо-контролируемых исследований, в которых производилось изучение эффективности и безопасности перорального и ректального применения ГББ. Установлена эффективность препарата во всех исследованиях, что рассматривается авторами как доказательство в поддержку применения лекарства при болях в животе, связанных со спазмами.
Во втором обзоре представлены данные об использовании ГББ для лечения колик/спазмов; в диагностических целях – при визуализации; в отношении терапевтической эффективности и безопасности парентерального введения ГББ для лечения желчных и почечных колик, резких спазмов мочеполового тракта; а также при родах и в качестве паллиативного лечения. Авторы пришли к выводу, что препараты ГББ обладают быстрым действием и высокоэффективны при хорошей переносимости, что поддерживает их применение при ряде показаний, связанных с резкими спазмами в животе, при родах, для паллиативного лечения, а также при проведении диагностических и лечебных процедур на органах брюшной полости, которые могут затруднять спастическое сокращение [7]. Фармакологический профиль ГББ предполагает возможность его применения при состояниях, сопровождающихся раздражением кишечника. Проведено двойное слепое рандомизированное сравнительное исследование в параллельных группах, в которое были включены 712 пациентов с СРК. Больным в течение 4 недель назначались: ГББ + парацетамол, ГББ, парацетамол или плацебо. Для оценки симптомов использовалась визуальная аналоговая шкала, к концу лечения у более чем 75 % пациентов в группе ГББ наблюдалось облегчение симптомов [8]. Отмечено также статистически значимое уменьшение интенсивности АБ в группе ГББ по сравнению с плацебо и парацетамолом. Другие исследователи подтвердили одинаковую эффективность ГББ и схожих с ним препаратов плюс их преимущество перед плацебо при лечении СРК [9–11].
Почечная колика
Почечная колика обычно является следствием нахождения конкремента (камня) в мочеточнике (реже в мочевом пузыре); сильная приступообразная боль, сопровождающая это состояние, вызвана периодическими спастическими сокращениями закупоренного полого органа, направленными на устранение блокады. Кажется логичным, что препарат, способный устранять такие спазмы в мочевыводящей системе, будет обладать хорошим обезболивающим действием, для оценки которого был проведен ряд исследований.
Было обнаружено 6 исследований с участием 755 пациентов, в которых производилась оценка ГББ в качестве дополнительного обезболивающего средства нестероидными противовоспалительными средствами (НПВС) [15–18] и другими противоспастическими препаратами [19]. Для сравнения: сочетание ГББ и петидина оказалось эффективнее, чем применение одного диклофенака натрия [15], хотя эффективность обоих препаратов в плане облегчения боли через 30 минут после введения была выше 90 %. Исследования показали, что монотерапия ГББ эффективно облегчает боль, хотя и уступает в этом отношении терапии с применением дипирона и диклофенака [17] или дипирона и трамадола [19]. Аналогичным образом исследования, проведенные для сравнения сочетания ГББ и дипирона с теноксикамом [16], а также с флурбипрофеном [18], подтверждали, что это сочетание обеспечивает значительное уменьшение боли.
Таким образом, имеющиеся данные говорят в пользу эффективности ГББ при лечении почечной колики как в качестве монотерапии, так и в сочетании с другими лекарственными средствами.
Дисменорея
В двух недавно проведенных исследованиях изучалось применение ГББ при первичной и вторичной дисменорее. В первом двойном слепом перекрестном исследовании, включившем 120 женщин, ГББ и парацетамол сравнивались с клониксинатом лизина и проприноксом, а также с плацебо [20]. В обеих группах лечения отмечено значительное уменьшение субъективной оценки боли по сравнению с плацебо.
Во втором продолжительном открытом исследовании изучалось сочетанное применение клониксината лизина и ГББ во время трех последовательных менструальных циклов у 30 женщин [21]. У всех женщин исходно отмечена очень сильная (10,7 %), сильная (42,9 %) или умеренная (46,4 %) боль. К концу исследования умеренная боль сохранилась у одной пациентки.
Роды
Обнаружено только одно исследование, в котором произведено изучение ГББ в первую очередь как обезболивающего средства при боли, связанной с родами. В исследовании произведено наблюдение за 104 первобеременными женщинами при родах в ходу; оказалось, что внутривенное введение ГББ приводит к уменьшению боли на 36 % по сравнению с плацебо [22].
Некоторые авторы изучали действие ГББ как средства, ускоряющего роды, ссылаясь на то, что, если боли в родах невозможно устранить безопасным способом, возможно безопасное уменьшение продолжительности родов (а значит, и боли). Было обнаружено пять подобных исследований, в трех из них произведено сравнение препарата с введением физиологического раствора или отсутствием лечения [22–24]. В одном исследовании ГББ сравнивали с другим спазмолитическим средством (дротаверином) [25], еще в одном – проведено сравнение ГББ, дротаверина и отсутствия терапии [26]. Препарат вводился внутривенно в 4 исследованиях в дозах от 20 до 40 мг, а одном исследовании – ректально [23]. В последних 4 исследованиях принимали участие 533 женщины, разделенные на почти равные группы; применение ГББ привело к статистически и клинически достоверному уменьшению периода между введением препарата и родоразрешением в отсутствие значимых побочных реакций со стороны матери или новорожденного.
Дискомфорт и боль, связанные с проведением манипуляций
ГББ изучался как средство для облегчения различных исследований ЖКТ и близкорасположенных структур.
В 3 исследованиях эффективность ГББ в сравнении с плацебо (2 исследования; 208 пациентов) и глюкагоном (1 исследование; 100 пациентов) оценивали при сигмоидоскопии и/или колоноскопии. В одном исследовании, в котором осуществлено сравнение препарата и плацебо, доказано уменьшение продолжительности процедуры в группе, получавшей ГББ [27].
Магнитно-резонансная визуализация может применяться для получения изображений верхнего отдела желудочно-кишечного тракта с высоким разрешением. Исследование, проведенное Wagner и соавт. [30], показало, что внутримышечное введение ГББ значительно улучшает качество изображения при Т2-взвешенной магнитно-резонансной визуализации брюшной полости. Кроме того, установлено, что магнитно-резонансная визуализация печени и поджелудочной железы несколько лучше при подавлении желудочно-кишечной перистальтики ГББ.
Пропедевтика лучевых методов обследования желчного пузыря
Ведущим методом диагностики патологических изменений желчного пузыря (ЖП) является ультразвуковое исследование (УЗИ).
Ультразвуковое исследование
Несомненными его преимуществами являются неинвазивность, возможность быстрого и портативного проведения исследования; отсутствие действия ионизирующей радиации и необходимости внутривенного введения контрастных веществ; независимость от физиологического состояния желудочно-кишечного тракта и гепатобилиарной системы [1–3].
Особенности синтопии желчного пузыря — прилежание его задней стенки в области тела и дна к правым отделам толстого кишечника и луковице двенадцатиперстной кишки диктуют необходимость подготовки пациентов к ультразвуковому обследованию с целью уменьшения пневматизации соответствующих отделов пищеварительного тракта. Для этого необходимо, как минимум, 6-часовое голодание накануне проведения диагностической манипуляции, а оптимальным считается проведение исследования натощак после ночного сна. Такие условия требуются еще и для наиболее детальной визуализации строения стенки желчного пузыря и его содержимого, поскольку он представляет собой полый орган, заполненный желчью и способный сокращаться в ответ на гуморальную стимуляцию при приеме пищи, что приводит к уменьшению его размеров, резкому утолщению стенок и невозможности детализировать внутрипросветные изменения [2, 3].
Анатомическое строение желчного пузыря несложно. В нем выделяют узкую шейку, соединяющуюся с пузырным протоком, тело пузыря, имеющее практически параллельные стенки, и куполообразное дно. В месте соединения шейки и пузырного протока стенка часто образует карман (или дивертикул) Гартмана, в котором могут скапливаться конкременты, блокирующие выход пузырной желчи [3–5] (рис. 1).
Для проведения ультразвукового исследования желчного пузыря датчик сканера (как правило, частотой 3,5 МГц) располагают в правом подреберье обследуемого — месте анатомической проекции. Улучшить визуализацию органа можно, уложив пациента на левый бок, что позволяет несколько оттеснить петли кишечника влево, этой же цели служит проведение исследование во время задержки дыхания при глубоком вдохе. Визуализация желчного пузыря через межреберья наиболее постоянна, но наименее информативна и используется в основном в ургентных ситуациях у неподготовленных пациентов. Для лучшей оценки характера внутрипузырных изменений (наличие мелких конкрементов, выявление их подвижности) возможно проведение обследования в вертикальном их положении или с наклоном туловища вперед [2–5].
В диагностике желчнокаменной болезни (ЖКБ) ультразвуковое сканирование по праву занимает ведущие позиции. Чувствительность ультразвукового исследования при выявлении желчных конкрементов превышает 95%, которые выглядят как гиперэхогенные структуры с акустической тенью [1, 5] (рис. 2).
В подавляющем большинстве случаев конкременты подвижны, но могут быть фиксированы к стенке или неподвижно располагаться в шейке пузыря. Другими инородными телами, имитирующими холелитиаз, могут быть сгустки крови или гноя, паразиты. Полипы желчного пузыря неподвижны или ограниченно подвижны в случае наличия у них ножки, всегда связаны со стенкой и, как правило, не дают акустической тени, обычно размер их не превышает 5 мм. Как правило, на фоне длительного отсутствия сокращений пузыря возможна визуализация расслоения желчи на два компонента с четкой границей раздела, один из которых анэхогенный и занимает верхние, по отношению к горизонтальной плоскости, отделы пузыря, другой — более плотный, располагающийся снизу. Это явление, называемое застоем желчи, или сладжем (англ. «sludge» — грязь, тина, ледяная каша, ил, взвесь), возникает вследствие присутствия в ней кристаллов холестерина и билирубината кальция и их способности обратимо формировать крупные агрегаты (рис. 3).
Наиболее частое осложнение желчнокаменной болезни — острый холецистит, причиной которого практически всегда является нарушение оттока желчи из желчного пузыря. Основными ультразвуковыми признаками этой патологии служат:
- наличие конкрементов в просвете пузыря (наиболее характерно обнаружение «вколоченного» конкремента в шейке) — рис. 4;
- утолщение стенки более 3 мм с появлением неоднородности ее структуры, расслоения (рис. 4);
- увеличение поперечного размера пузыря более 4 см; выявление наибольшей болезненности в месте ультразвуковой проекции желчного пузыря (ультразвуковой симптом Мерфи), которая может не определяться при гангренозном холецистите [3, 5] (рис. 4).
Сочетание указанных симптомов с обнаружением скопления жидкости около пузыря, особенно в сочетании с выявлением дефекта стенки, говорит о ее перфорации и, возможно, о формировании перипузырного абсцесса (рис. 5). Обнаружение ультразвуковых признаков скопления газа в просвете пузыря на фоне других признаков острого его воспаления указывает на такую тяжелейшую патологию, как эмфизематозный холецистит, вызываемый газообразующей анаэробной флорой [3, 5] (рис. 6).
Другое осложнение желчнокаменной болезни, проявляющееся нарушением пассажа желчи, — холедохолитиаз. Нарушение оттока желчи по общему желчному протоку вызывает его расширение более 7 мм, расширение внутрипеченочных желчных протоков (более 40% от диаметра прилежащей ветви воротной вены) (рис. 7). Бесспорным доказательством холедохолитиаза служит обнаружение конкрементов, которые чаще всего локализуются в дистальной части общего желчного протока, но могут быть визуализированы лишь в 70–80% случаев [1, 4, 5].
Расширение внутри- и внепеченочных желчных протоков отмечается и при таком осложнении желчнокаменной болезни, как синдром Мирицци (Mirizzi), который заключается в обструкции общего желчного протока в результате объемного эффекта воспалительной реакции тканей на камень, расположенный в шейке пузыря или пузырном протоке, при низком впадении его в холедох (рис.  [5].
[5].
Нередко образованию конкрементов в желчном пузыре сопутствуют доброкачественные изменения его стенок, одной из основных которых выступает нарушение обмена холестерина. Эти изменения называются гиперпластической холецистопатией. Один из ее вариантов — холестериновая дистрофия проявляется такими ультразвуковыми признаками, как выявление в стенке пузыря гиперэхогенных отложений размером не более 1 мм, не дающими акустической тени, но сопровождающимися эффектом реверберации (пузырь отдаленно напоминает клубнику), которые являются липидными отложениями (рис. 9). Более выраженные изменения стенки, называемые аденомиоматозом, проявляются в ее утолщении, образовании интрамуральных дивертикулов (синусы Ашоффа–Рокитанского), содержащих гиперэхогенные холестериновые отложения с эффектом реверберации («хвост кометы») и микролиты, дающие акустическую тень (рис. 9). Гиперпластическая холецистопатия может поражать как весь пузырь, так и часть его стенки [2, 5].
Известно, что удаление ЖП по поводу ЖКБ не избавляет больных от метаболических нарушений, в том числе от гепатоцитарной дисхолии, сохраняющейся и после операции [6]. Выпадение физиологической роли ЖП, а именно концентрация желчи в печени в межпищеварительный период и выброс ее в двенадцатиперстную кишку во время еды, сопровождается нарушением пассажа желчи в кишечник и расстройством пищеварения [6, 7].
Изменение химического состава и объема желчи, хаотическое ее поступление в двенадцатиперстную кишку после холецистэктомии (ХЭ) нарушают переваривание и всасывание жира и других веществ липидной природы, уменьшают бактерицидность дуоденального содержимого, что приводит к микробному обсеменению и нарушению моторики двенадцатиперстной кишки, развитию синдрома избыточного бактериального роста в кишечнике (особенно в подвздошной кишке), расстройству печеночно-кишечной циркуляции и снижению синтеза желчных кислот в печени [6]. Как следствие — синдром нарушенного пищеварения, симптомы которого часто ошибочно трактуются как постхолецистэктомический синдром (ПХС), ассоциирующийся хирургами в первую очередь с нераспознанными до операции или не устраненными во время ХЭ механическими препятствиями желчеоттоку (оставленными или возникшими вновь камнями в холедохе, стенозом фатерова сосочка и т. д.) [6].
При подготовке к операции ХЭ большое внимание всегда уделяется диагностике механических препятствий желчеоттоку в двенадцатиперстную кишку. Совершенно иное дело обстоит с дооперационной верификацией внепеченочных билиарных дисфункций. Отсутствие косвенных признаков функциональных нарушений сфинктера Одди в виде расширения общего желчного протока при УЗИ, повышения печеночных ферментов, болевых приступов и т. д. совсем не исключает дисфункций фатерова сосочка, формирующихся задолго до поступления пациента. По нашим данным, у 45% пациентов с желчнокаменной болезнью при радионуклидной гепатобилисцинтиграфии (ГБСГ) устанавливаются функциональные нарушения транспорта радиофармпрепарата из общего желчного протока в двенадцатиперстную кишку, не требующие проведения ретроградной панкреатохолангиографии и эндоскопической коррекции.
Радионуклидные методы в ряде случаев являются просто безальтернативными из-за строгой специфичности включения радиофармпрепарата (РФП) в различные метаболические процессы (ГБСГ). Функциональное состояние гепатобилиарной системы при любой патологии гепатобилиарной системы, в том числе и при ЖКБ, изучается с помощью стандартной ГБСГ.
Гепатобилисцинтиграфия
ГБСГ позволяет объективно оценивать наиболее важные с позиций функционирования пищеварительно-транспортного конвейера процессы: желчесинтетическую и желчеэкскреторную функции печени, а также транспорт желчи в двенадцатиперстную кишку. Метод основан на регистрации пассажа короткоживущих радионуклидов Тс-99м+бромезида по билиарному тракту.
Исследование проводится натощак, в горизонтальном положении пациента после введения 3 мКм Тс-99м+бромезида внутривенно. Длительность процедуры составляет 60 минут. В качестве желчегонного завтрака пациенты принимают желтки куриных яиц или 200 мл 10% сливок через 30 минут от начала исследования.
Нормальными показателями ГБСГ считаются:
1) время полувыведения (Т1/2) радиофармпрепарата (РФП) из печени менее 35 минут; 2) время полувыведения (Т1/2) РФП из холедоха менее 50 минут; 3) время поступления РФП в двенадцатиперстную кишку менее 40 минут; 4) адекватным поступлением РФП в кишечник является преобладание активности РФП в двенадцатиперстной кишке по сравнению с таковой в холедохе к концу исследования.
Общепринятая стандартная методика радиоизотопного исследования с желчегонным завтраком не всегда позволяет конкретизировать характер функциональных изменений желчеоттока. Это объясняется тем, что пищевая нагрузка оказывает свое действие как посредством активации поступления в кровоток холецистокинина (ХК) при раздражении I-клеток слизистой оболочки двенадцатиперстной кишки и интрамурального нервного сплетения [8]. Активность пищеварительных ферментов и чувствительность сфинктерного аппарата желчевыводящих путей к интестинальным гормонам вариабельна и на практике трудноопределима [9]. Тонус интрамуральных нервных волокон зависит от физиологической активности органов верхних отделов пищеварительного тракта [10, 11].
В этой связи при радионуклидной диагностике внепеченочных билиарных дисфункций (ВБД) достаточно часто применяется внутривенное введение гормона холецистокинина, но релаксирующий эффект этого препарата зависит от состояния центральной нервной системы, гормонального фона пациента и нарушается при холестерозе ЖП, поскольку локализация рецепторов к холецистокинину совпадает с местами отложений эфиров холестерина в стенке пузыря и желчных протоках, что затрудняет точное определение дозы вводимого гормона [8, 10].
Для уточнения характера нарушений желчеоттока по общему желчному протоку в клинике факультетской хирургии им. С. И. Спасокукоцкого РНИМУ им. Н. И. Пирогова на базе Первой Градской больницы выполняются ГБСГ с аминокислотным холекинетическим тестом (ГБСГ-АХТ) и ГБСГ с Бускопан®-тестом (патент РФ № 2166333).
ГБСГ с аминокислотным холекинетическим тестом
Исследование проводится натощак. Через 30 минут после введения РФП и начала исследования в периферическую вену вводится раствор аминокислот Вамин-14 или Фреамин, не содержащие глюкозы и электролитов. Последнее условие мы считаем весьма важным, так как возникающая при инфузии глюкозы гипергликемия полностью или частично ингибирует секрецию холецистокинина [8]. Доза препарата выбиралось из расчета 1,5–2 мл/кг массы тела (80–130 мл). Продолжительность инфузии составляет 5–7 минут, поскольку введение раствора аминокислот более 10 минут (независимо от дозы) не приводит к увеличению выброса эндогенного холецистокинина, а наоборот, снижает инкрецию гормона [9]. ВБД и причина замедленной экскреции радиофармпрепарата гепатоцитами оценивается на основании различий показателей стандартной ГБСГ и ГБСГ-АХТ (рис. 10).
ГБСГ с использованием гиосцина бутилбромида
Гиосцина бутилбромид (Бускопан®) — производное третичного аммониевого соединения гиосцина. Гиосцин — алкалоид, присутствующий в растении рода Duboisia. Его химически перерабатывают с помощью добавления бутиловой группы для получения четвертичной аммониевой структуры. Эта модификация формирует молекулу, которая по-прежнему обладает антихолинергическими свойствами, сравнимыми со свойствами гиосцина.
Но, в отличие от гиосцина, четвертичные аммониевые соединения, такие как гиосцина бутилбромид, ограничивают системное поглощение и значительно уменьшают число побочных реакций. Гиосцина бутилбромид — антихолинергический препарат с высокой степенью сродства к мускариновым рецепторам, расположенным на клетках гладких мышц желудочно-кишечного тракта, вызывает спазмолитический эффект. Кроме того, препарат связывается с никотиновыми рецепторами, что определяет эффект блокировки нервных узлов, что обуславливает его антисекреторное действие.
Техническая сторона исследования мало отличается от вышеизложенного АХТ-теста. По окончании стандартной гепатобилисцинтиграфии пациент вместо инфузии раствора аминокислот принимает per os 20 мг гиосцина бутилбромида. Через 20 минут выполняется повторная запись и обработка данных (рис. 11). Таким образом, применение Бускопан®-теста позволяет сократить время диагностики для врача и упрощает диагностическую процедуру для пациента.
Наиболее эффективно ГБСГ с Бускопан®-тестом зарекомендовала себя при исследовании пациентов после холецистэктомии (рис. 12).
Ведущими факторами нарушения функции печени после холецистэктомии являются наличие и продолжительность дискинезии сфинктерного аппарата желчных путей. У пациентов значительно преобладает парадоксальный спазм сфинктера Одди как причина задержки РФП в холедохе. Функциональные нарушения оттока желчи обусловлены холестерозом желчных путей, в частности сфинктера Одди (рис. 13, 14).
Рентгенологические методы
Рентгенологические методы исследования желчного пузыря и внепеченочных желчных протоков сегодня практически не применяются, поэтому приводим их краткое описание в качестве исторической справки.
Обзорная рентгенография
Обзорная рентгенография брюшной полости проводится намного реже, чем УЗИ, из-за лучевой нагрузки. Но, тем не менее, она являлась достаточно информативным методом диагностики желчекаменной болезни. На рентгенограмме можно увидеть наличие, месторасположение и количество рентгенпозитивных камней, содержащих соли кальция (рис. 15).
Пероральная холецистография
Пероральная холецистография проводится при подозрении на рентгеннегативные (холестериновые) камни. Метод основывается на всасывании в желудочно-кишечном тракте и выведении с желчью контрастного вещества (рис. 16).
При нарушении всасывания в кишечнике, снижении выделительной функции печени, закупорке пузырного протока камнем и прочем пероральная холецистография может быть отрицательной, т. е. на ней не определяется тень желчного пузыря.
Внутривенная холецистография
Внутривенная холецистография выполняется при отрицательном результате перорального рентгеноконтрастного метода. С помощью данной методики удается контрастировать желчный пузырь в 80–90% случаев (рис. 17).
Компьютерная томография и магнитно-ядерная (магнитно-резонансная) томография
Недостатки классических рентгенологических исследований желчного пузыря с успехом восполняют компьютерная томография (КТ) и магнитно-ядерная томография (магнитно-резонансная томография, МРТ). При калькулезном холестерозе конкременты визуализируются в виде теней однородной структуры (холестериновые камни) (рис. 18) или представлены неоднородными тенями с чередованием участков смешанных камней — холестериновое ядро с кальциево-билирубиновой оболочкой (рис. 19).
Компьютерная томография и магнитно-ядерная томография позволяют заподозрить желчекаменную болезнь у пациентов, обследуемых по поводу другой патологии органов брюшной полости, так как описание изображения желчного пузыря является обязательной составляющей протокола этих исследований.
Литература
- Практическое руководство по ультразвуковой диагностике. Под ред. В. В. Митькова. М.: Видар-М, 2003. Т. 1. 720 с.
- Brant W. E., Helms C. A. Fundamentals of Diagnostic Radiology, 2 nd ed. Lippincott, Williams and Wilkins, p. 836–841.
- Kurtz A. B., Middleton W. D. Ultrasound: The Requisites. Philadeiphia, Hanley&Belfus, 1996, p. 35–71.
- Parulekar S. G. Transabdominal sonography of bile ducts // Ultrasound Q. 2002, (18) 3: 187–202.
- Rumack C. M., Wilson S. R., Charboneau J. W. (eds). Diagnostic Ultrasound, 2 nd ed. St. Louis, Mosby, 1998, p. 172–195.
- Савельев В. С., Петухов В. А. Желчекаменная болезнь и синдром нарушенного пищеварения. М.: БОРГЕС, 2010. 258 с.
- Савельев В. С., Петухов В. А., Болдин Б. В. Холестероз желчного пузяря. М.: ВЕДИ, 2002., 176 с.
- Высоцкая Р. А. Простагландины и гастроинтестинальные гормоны при хронических заболеваниях печени. Дисс. докт. биол. наук. М., 1992, 340 с.
- Houda R., Tooli J., Dodds W. J. Effect of enteric hormons on sphincter of Oddi and gastrointestinal myoelectric activity in fasted conscious opossums // Gastroenterol. 1983, vol. 84, p. 1–9.
- Weechsler-J. G. Bedeutung der Gallenblase in der Regulation des duodenogastralen Refluxes // Z-Gastroenterol. 1987, Aug. 25, Suppl 3: p. 15–21.
- Петухов В. А. Липидный дистресс-синдром. Под ред. В. С. Савельева, М.: МАКС ПРЕСС, 2010. 544 с.
В. А. Петухов*, 1, доктор медицинских наук, профессор Д. А. Чуриков**, кандидат медицинских наук
* ГБОУ ВПО РНИМУ им. Н. И. Пирогова МЗ РФ, Москва ** ГУЗ ГКБ № 1 им. Н. И. Пирогова, Москва
1 Контактная информация