Ламизил Таблетки, пачка, 14 шт, 250 мг, для приема внутрь, для взрослых
Побочное действие
Со стороны системы кроветворения: очень редко — нейтропения, агранулоцитоз, панцитопения. В очень редких случаях при применении препарата отмечалось развитие качественных или количественных изменений со стороны форменных элементов крови (нейтропения, агранулоцитоз, тромбоцитопения, панцитопения). В случае развития качественных или количественных изменений со стороны форменных элементов крови следует установить причину нарушений и рассмотреть вопрос о снижении дозы препарата или при необходимости о прекращении терапии препаратом Ламизил. Со стороны иммунной системы: очень редко — анафилактоидные реакции (включая ангионевротический отек), кожная и системная красная волчанка. Со стороны нервной системы: часто — головная боль; иногда — нарушения вкусовых ощущений, включая их утрату (обычно восстановление происходит в пределах нескольких недель после прекращения лечения); очень редко — головокружение, парестезии, гипестезии. Имеются отдельные сообщения о случаях длительных нарушений вкусовых ощущений. В отдельных случаях на фоне приема препарата отмечалось снижение потребления пищи, которое приводило к значительному уменьшению веса. Со стороны гепатобилиарной системы: редко — гепатобилиарная дисфункция (преимущественно холестатической природы), включая очень редкие случаи развития тяжелой печеночной недостаточности (некоторые со смертельным исходом или требующие трансплантации печени). В большинстве случаев, когда развивалась печеночная недостаточность, пациенты имели серьезные сопутствующие системные заболевания и причинно-следственная связь печеночной недостаточности с приемом препарата Ламизил была сомнительной. Со стороны пищеварительной системы: очень часто — чувство переполнения желудка, потеря аппетита, диспепсия, тошнота, слабо выраженные боли в животе, диарея. Со стороны кожи и подкожной клетчатки: очень часто — нетяжелые кожные реакции (сыпь, крапивница); очень редко — серьезные кожные реакции (в т.ч. синдром Стивенса-Джонсона, токсический эпидермальный некролиз); псориазоподобные высыпания на коже или обострения псориаза. Очень редко отмечались случаи выпадения волос, хотя причинно-следственная связь этого явления с приемом препарата не установлена. В случае, если развивается прогрессирующая кожная сыпь, лечение следует прекратить. Со стороны скелетно-мышечной системы: очень часто — артралгия, миалгия. Прочие: очень редко — чувство усталости.
Ламизил таб 250мг N14 (Новартис)
ЛАМИЗИЛ — противогрибковое широкого спектра, фунгистатическое, фунгицидное.ФармакодинамикаТербинафин представляет собой аллиламин, который обладает широким спектром действия в отношении грибов, вызывающих заболевания кожи, волос и ногтей, в т.ч. дерматофитов, таких какTrichophyton (например Т. rubrum, Т. mentagrophytes, Т. verrucosum, Т. tonsurans, Т. violaceum),Microsporum (например М. canis), Epidermophyton floccosum, а также дрожжевых грибов рода Candida(например С. albicans) и Pityrosporum. В низких концентрациях тербинафин оказывает фунгицидное действие в отношении дерматофитов, плесневых и некоторых диморфных грибов. Активность в отношении дрожжевых грибов, в зависимости от их вида, может быть фунгицидной или фунгистатической.Тербинафин специфически подавляет ранний этап биосинтеза стеринов в клетке гриба. Это ведет к дефициту эргостерина и к внутриклеточному накоплению сквалена, что вызывает гибель клетки гриба. Действие тербинафина осуществляется путем ингибирования фермента скваленэпоксидазы в клеточной мембране гриба. Этот фермент не относится к системе цитохрома Р450.При назначении препарат Ламизил® внутрь в коже, волосах и ногтях создаются концентрации препарата, обеспечивающие фунгицидное действие.ФармакокинетикаПосле приема внутрь тербинафин хорошо абсорбируется (>70%); абсолютная биодоступность тербинафина вследствие эффекта первого прохождения составляет примерно 50%. После однократного приема тербинафина внутрь в дозе 250 мг его Cmax в плазме достигается через 1,5 ч и составляет 1,3 мкг/мл. При постоянном приеме тербинафина его Cmax увеличивалась в среднем на 25% , по сравнению с однократным приемом; AUC увеличилась в 2,3 раза. Исходя из увеличенияAUC, можно рассчитать эффективный T1/2 — 30 ч. Прием пищи в незначительной степени влияет на биодоступность препарата (AUC увеличивается менее чем на 20%), поэтому не требуется коррекция дозы препарата Ламизил® при одновременном приеме с пищей.Тербинафин в значительной степени связывается с белками плазмы крови (99%). Он быстро проникает через дермальный слой кожи и концентрируется в липофильном роговом слое. Тербинафин также проникает в секрет сальных желез, что приводит к созданию высоких концентраций в волосяных фолликулах, волосах и в коже, богатой сальными железами. Показано также, что тербинафин проникает в ногтевые пластинки в первые несколько недель после начала терапии.Тербинафин метаболизируется быстро и в существенной степени при участии как минимум 7 изоферментов цитохрома Р450, при этом основную роль играют изоферменты CYP2C9, CYP1A2,CYP3A4, CYP2C8 и CYP2C19. В результате биотрансформации тербинафина образуются метаболиты, не обладающие противогрибковой активностью и выводящиеся преимущественно с мочой.Не выявлено изменений равновесной концентрации тербинафина в плазме в зависимости от возраста.В фармакокинетических исследованиях разовой дозы препарата Ламизил® у больных с сопутствующими нарушениями функции почек (Cl креатинина
Ламизил в лечении онихомикоза
О
нихомикоз является одним из наиболее частых заболеваний человека. В настоящее время считается, что заболевания ногтей, вызванное грибами, встречается у 50% пациентов с поражениями ногтевых пластинок. В России число больных онихомикозами варьирует от 4,5 до 15 миллионов человек.
Возбудителями онихомикозов являются дерматофиты, дрожжи, плесени, однако, их соотношение в спектре заболеваемости оценивается исследователями по–разному. У подавляющего большинства (91,3%) больных идентифицируются дерматофиты – прежде всего, Tr. rubrum
(72%), реже –
Tr. menthagrоphytes
(19,3%) [1, 15, 21] (рис. 1.). В частности,
Tr. rubrum
, как правило, является причиной поражения ногтевых пластинок стоп; дрожжи обычно поражают ногти на кистях, а недерматофитные плесени, вызывающие 3–5% онихомикозов, – на стопах [23]. В основном дрожжевые и плесневые грибы встречаются в сочетании с
Тr. rubrum
.
Рис. 1. Доли возбудителей в этиологии онихомикозов
К предрасполагающим факторам развития микотической инфекции следует отнести заболевания сосудов нижних конечностей (облитерирующий эндартериит, тромбофлебит, варикозное расширение вен, синдром Рейно), систематические микротравмы ногтевой пластинки, а также дистрофические состояния. Обычно эти факторы затрудняют лечение онихомикоза, в особенности, если у больного имеет место сочетанная патология ногтя (например, микоз на фоне псориаза).
В патогенезе онихомикозов существенная роль принадлежит патологии углеводного обмена, эндокринным и неврологическим изменениям, нарушениям иммунной системы. Заболевание нередко развивается на фоне длительного приема лекарственных препаратов, подавляющих защитные силы организма (глюкокортикоидов, цитостатиков, антибиотиков широкого спектра действия). По данным литературы [8, 23], онихомикоз в 40% случаев регистрируется у лиц старше 65 лет, имеющих обусловленную возрастом иммунодепрессию.
Подавляющее большинство случаев онихомикоза характеризуется хроническим персистирующим течением. Считают, что при поражении Tr. rubrum
это связано с невозможностью выработки специфического иммунного ответа против гриба за счет активности специальных Т–супрессорных клеток. Подавление клеточной и отсутствие воспалительной реакции на возбудитель также может быть обусловлено его преимущественной локализацией в роговом слое эпидермиса и ногтевых пластинах.
В литературе приводятся многочисленные данные о сравнительной эффективности различных методов терапии онихомикозов: локального применения антимикотиков в виде мазей, пластырей, лаков, хирургического удаления ногтевой пластины с последующим лечением ногтевого ложа противогрибковыми препаратами, а также системными антимикотиками [1, 2, 12, 28]. Анализ публикаций по проблеме свидетельствует о том, что в мировой медицинской практике еще нет идеального средства и метода лечения онихомикоза, которые подходили бы всем без исключения пациентам, не давали бы никаких побочных эффектов и в короткое время обеспечивали 100% клинико–этиологическое излечение больного. Поэтому и сегодня оправдан поиск и всестороннее изучение новых эффективных антимикотиков, отвечающих этим требованиям.
Представителем класса аллиламинов – химических соединений, вошедших в арсенал наиболее эффективных средств лечения дерматомикозов, является тербинафин (Ламизил, созданный в 1982 году швейцарской компанией “Новартис”).
К настоящему времени после многосторонних клинических испытаний Ламизил прочно вошел в практику лечения больных микозами [11, 22, 29, 31]
Это препарат с широким спектром противогрибковой активности [16, 34]. В терапевтических концентрациях он оказывает прямое фунгицидное действие на дерматофиты, дрожжеподобные и плесневые грибы как при пероральном, так и при местном применении. Местом приложения препарата является цитоплазматическая мембрана грибковой клетки. Преимуществом тербинафина является действие его на ранних стадиях стерольного метаболизма, на уровне скваленового эпоксидазного цикла. Подавляя фермент скваленэпоксидазу, тербинафин тормозит формирование эргостерола – основного компонента клеточной стенки грибов, препятствуя их дальнейшему размножению [15, 19, 22].
Препарат обладает двойным механизмом действия: фунгицидным и фунгистатическим, причем фунгицидный эффект – основной. Он обусловлен накоплением в грибковой клетке скваленов, которые, подобно своеобразной липидной губке, экстрагируют из мембран липидные компоненты. Накапливающиеся внутри клетки липидные гранулы, постепенно увеличиваясь в объеме, разрывают ущербные цитоплазматические мембраны, приводя грибковую клетку к гибели [11, 17]. Фунгистатический эффект обусловлен ущербностью мембран грибковой клетки вследствие подавления синтеза эргостерола, что приводит к утрате способности грибковой клетки к развитию – она лишь выживает.
Преимущественное фунгицидное действие ламизила, отличающее его от ранее созданных системных антимикотиков, обусловливает более высокую эффективность препарата, а также меньшее число рецидивов при его применении, за счет чего лечение обходится дешевле, чем другими системными антимикотиками [9, 14].
Препарат хорошо всасывается из желудочно–кишечного тракта: через 2 часа после однократного приема в дозе 250 мг его концентрация в плазме составляет 0,8–1,5 мг/мл. Благодаря липофильности, он накапливается в дерме, эпидермисе, жировой ткани, откуда медленно всасывается в кровь [19]. Тербинафин также проникает в секрет сальных желез, что приводит к созданию максимально высоких концентраций в волосяных фолликулах, волосах и коже, богатой сальными железами. Препарат обнаруживают в роговом слое эпидермиса уже через несколько часов после перорального приема, что достигается путем его экскреции сальными железами и в меньшей степени – путем пассивной диффузии [11, 17]. Для тербинафина характерна длительная персистенция в крови благодаря непрерывной схеме приема препарата, что составляет важный компонент его выраженной эффективности. В дистальных частях ногтей его концентрация сохраняется в течение 48 недель после окончания курса терапии, что обусловливает положительный фунгицидный эффект и делает возможным излечение онихомикоза без удаления ногтевых пластин [19, 29]. Биотрансформация приводит к образованию не обладающих антимикотической активностью метаболитов, которые выводятся из организма преимущественно с мочой [9].
К особенностям распространения тербинафина относится его лимфатический транспорт благодаря липофильности и связи с хиломикронами. По лимфатическим сосудам тербинафин непосредственно достигает инфильтративно–нагноительных и абсцедирующих очагов поражения, осложненных лимфангоитами. Такой характер транспорта тербинафина в сочетании с его антибактериальными свойствами, сравнимыми с таковыми гентамицина, приводит к достаточно быстрому разрешению осложненных форм дерматофитий [23].
Препарат не подавляет ферменты печени, мало связываясь с цитохромом р–450, вследствие чего практически не влияет на метаболизм медикаментозных средств, т. е. риск лекарственных взаимодействий минимален. Это является важным достоинством препарата, т. к. обеспечивает безопасность при лечении больных, получающих сопутствующую терапию по поводу интеркуррентных заболеваний (сахарный диабет, заболевания сердечно–сосудистой, нервной систем и т.д.) [21, 31]. Биодоступность тербинафина в результате совместного приема с другими лекарственными средствами и пищей не изменяется. В концентрации, в 5 раз превышающей терапевтическую, тербинафин не угнетает хемотаксис, фагоцитоз и метаболическую активность лейкоцитов, т.е. не обладает иммуносупрессивным эффектом [34]. Более того, в работе Barbareschi, 1993 г. [13] показано, что инкубация in vitro полиморфноядерных нейтрофилов с тербинафином приводит к повышению их активности [13].
Ламизил имеет прекрасный профиль безопасности [20, 36, 39, 40]. Его безопасность сопоставима с плацебо [29]. Согласно данным, представленным рядом авторов [16,27], по результатам анализа историй болезни 25884 пациентов, принимавших таблетки, побочные эффекты, возникшие при приеме ламизила, крайне редки и относятся преимущественно к слабо выраженным явлениям со стороны желудочно–кишечного тракта (табл. 1).
Все отмеченные свойства препарата способствовали его быстрому внедрению в клиническую практику более чем в 80 странах мира [17, 21, 25, 27]. Приведенные в таблице данные зарубежных исследователей свидетельствуют о высокой эффективности ламизила в терапии онихомикозов. Положительный опыт лечения ламизилом отмечают и многие отечественные ученые, демонстрируя весьма впечатляющие показатели.
Так, по данным А.А. Кубановой [4], положительное клиническое действие и микробиологическое излечение отмечено у 94,4% больных. Показательны результаты Ю.В. Сергеева [9], который демонстрирует клинико–микологическое излечение у 82% больных. Данные Н.С. Потекаева [8] свидетельствуют о высокой эффективности ламизила: микологическое излечение получено у 96% больных (см. табл. 2). В.М. Лещенко и Г.М. Лещенко [6] оценивают результаты лечения пациентов с онихомикозом стоп и кистей, сочетающимся с поражением гладкой кожи, как положительные. По окончании традиционного курса лечения (по 250 мг однократно в течение 12 недель) клиническое выздоровление отмечено у 96% больных. Переносимость препарата была хорошей. У 478 пациентов после лечения ламизилом в материале с ногтевых пластинок микроскопически грибы не были обнаружены, и через 6 мес после начала лечения у всех констатировано клиническое и микробиологическое излечение.
По данным В.А. Молочкова [5], при лечении больных онихомикозом применение ламизила оказалось высокоэффективным положительное клиническое действие и микробиологическое излечение отмечено у 95,2% больных. Интересные данные об использовании ламизила у больных сахарным диабетом, получены С.А. Буровой [3]. Представленные отдаленные результаты (через 6 мес после окончания лечения ламизилом) свидетельствуют о том, что клиническое выздоровление отмечается у 85,7% пациентов, микробиологическая санация у 89,3%. О.Н. Позднякова демонстрирует эффективность и безопасность ламизила у 48 пациентов с хроническими заболеваниями печени вне обострения [8] в компенсированной и субкомпенсированной стадиях: после окончания терапии микологическое излечение отмечено у 100% больных. Обнадеживающими представляются сведения об использовании ламизила при иммунодефицитных состояниях, учитывая, что число этих больных с каждым годом увеличивается. К настоящему времени описано 82 случая применения таблеток ламизила при иммунодефицитах: СПИДе [26, 37, 38], синдроме Дауна, после трансплантации органов [18, 24, 27].
Ю.К. Скрипкин и Ж.В. Степанова [10], обобщая опыт отечественных и зарубежных исследователей, еще раз подчеркнули эффективность и безопасность применения ламизила, хорошую переносимость, удобную схему применения. Эффективность лечения, по их данным, составила 94%.
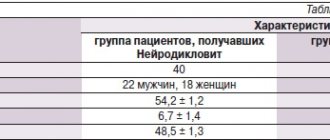
Под нашим наблюдением находилось 32 больных онихомикозом стоп (18 мужчин, 14 женщин) в возрасте от 25 до 55 лет с продолжительностью болезни от 1 года до 15 лет. Сопутствующие заболевания выявлены у 28% больных, в том числе гастриты, колит, дисфункция щитовидной железы; 50% пациентов считали себя практически здоровыми. Предрасполагающие факторы, обусловливающие развитие микотического процесса, выявлены у 100% больных. Так, 26 пациентов были постоянными посетителями бассейнов, 18 – саун; 14 больных занимались профессиональным спортом, что сопряжено с постоянной травматизацией ногтевых пластинок. Диагноз онихомикоза устанавливали в каждом случае на основании клинической картины заболевания и обнаружения грибов при микроскопическом исследовании пораженных ногтевых пластинок. У 20 больных, помимо онихомикоза (поражение от 1 до 16 ногтевых пластин), имелось поражение кожи соответствующей локализации: стоп и кистей (4 больных), гладкой кожи туловища (6 больных), крупных складок (10 больных). По клинической картине ногтевые пластины были поражены в основном по смешанному типу, т.е. у одного и того же больного на разных пальцах они были изменены по гипертрофическому, нормотрофическому типу с явлениями онихолизиса и площадью поражения ногтя от краевого (5–10%) до тотального, с вовлечением в процесс кожи стоп и ладоней с изменениями кожи, характерными для руброфитии утрированностью кожных борозд, мелкопластинчатым (муковидным) шелушением, гиперкератозом, мацерацией эпидермиса, трещинами в межпальцевых складках кожи стоп.
Больные получали Ламизил внутрь по 250 мг в сутки в течение 12 недель, причем на фоне терапии исследовали общий анализ крови, мочи, функциональные пробы печени. В каждом случае проводили обработку обуви в домашних условиях 25% раствором формалина или 0,5% раствором хлоргексидина биглюконата дважды с интервалом 1 месяц. В целях увеличения интенсивности роста ногтевой пластинки 5 больным внутрь назначали фитин, цинксодержащие комплексы витаминов.
Лечение больные переносили хорошо. Из побочных действий у 1 больного отмечалась временная потеря вкусовых ощущений: это явление самостоятельно разрешилось, не требуя отмены препарата.
Контрольное микроскопическое исследование проводили через 3, 4, 6 мес после начала лечения, причем через 6 мес после окончания терапии в 100% случаев результаты микроскопического исследования были отрицательными. У 4 больных, несмотря на отсутствие при микроскопическом исследовании грибов, ногтевые пластинки остались дистрофически измененными, при этом в каждом случае в анамнезе у них имела место травма соответствующего ногтя.
В результате лечения высыпания на коже, особенно в крупных складках, разрешались уже через 2–3 недели. Пораженные ногти с площадью поражения до 60% на стопах были заменены визуально здоровыми через 5–6 мес, т.е. через 3–4 мес после окончания приема ламизила. Рецидивов заболевания выявлено не было (9–14 мес наблюдения).
Таким образом, на основании данных литературы и результатов собственных исследований можно утверждать, что появление ламизила привело к значительному улучшению прогноза больных, страдающих онихомикозом, который ранее трудно поддавался лечению и характеризовался упорным течением. Терапия ламизилом изменила точку зрения о том, что онихомикоз трудно излечить: препарат высокоэффективен, обеспечивает высокую частоту излечения за более короткий срок, чем антимикотики предыдущих поколений. Фунгицидный эффект, активное проникновение ламизила в кератин и длительное его сохранение в ногтевой пластинке в сочетании с относительной редкостью серьезных нежелательных эффектов и рецидивов сделали препарат средством выбора в лечении грибковых инфекций ногтей и гладкой кожи. Следует отметить, что в настоящее время он введен в список лекарств для льготного обслуживания инвалидов и пенсионеров за счет фонда страховых компаний.
Список литературы Вы можете найти на сайте https://www.rmj.ru
Тербинафин–
Ламизил (торговое название)
(Novartis Pharma)
Литература:
1. Афанасьев Д.Б. “Комплексное амбулаторное лечение онихомикоза с использованием биологически активных перевязочных средств”, автореферат диссертации канд.мед. наук, М., 1996, 23.
2. Бормотов В.Ю. “Амбулаторное лечение больных онихомикозом, обусловленным красным трихофитоном”, Автореферат диссертации канд.мед.наук., М., 1983; 19.
3. Бурова С.А., Талалаева С.М., “Отдаленные результаты лечения онихомикозов у больных сахарным диабетом” “Российский журнал кожных и венерических болезней” 2000 г, №5, стр.31–33.
4. Кубанова А.А., Суколин Г.И., Юсуф М., Язды М.Ш. “Вестник дерматологии и венерологии “ 1995, №6, стр. 42–43 “Применение Ламизила в микологической практике”.
5. Курчева О.П., Молочков В.А. “Ламизил – эффективное средство лечения онихомикозов” “Российский журнал кожных и венерических болезней” 1998 г, №1, 47–49.
6. Лещенко В.М., Лещенко Г.М. “Лечение онхомикозов Ламизилом” “Вестник дерматологии и венерологии” 1998 г., №2, стр.61–64.
7. Лыкова С. Г., Позднякова О. П. “Вестник дерматологии и венерологии”, 2000г., №4
8. Потекаев Н. С. “ Вестник дерматологии и венерологии”, 1999г., №5
9. Сергеев Ю.В., Потекаев Н.С., Лещенко В.М., Ларионова В.Н. “Вестник дерматологии и венерологии” 1995 №5 стр. 54–56 “Ламизил: совершенствование терапии онихомикозов, вызванных дерматофитами».
10. Скрипкин Ю.К., Степанова Ж.В. “Вестник дерматологии и венерологии” №6, 1999. 11 11. Alpsoy E., Yilmanz E., Basaran E. Intermettent therapy with terbinafine for dermatophyte toe onychomycosis a new approach.– J. Dermatol, 1996, 23:259–262
12. Back D.J., Tjia J.F., Abel S.M. Azoles, allylamines and drug metabolism. Br. J. Dermatol. 1992; 126 (Suppl. 33): 14–18.
13. Barbareschi M, Vago, Colombo D., Bevilacqua M. mycoses 36: 405–9 (1993), (LAS 360)
14. Clayton J.M. In vitro activity of terbinafine, Clin Ep.Dermatol. 1989; 14: 101–103.
15.Clayton J.M., Hay K.J., Bnt. J. Dermatol. 1994 vol.130 suppl.43, p.9–11.
16. De Cnyper “Long–term outcome of onychomycosis treatments” Cl. Dermal, 1998; T.Z.
17. Einarson T.R., Lupta А.К., Shear N.H., Arikian S. Clinical and economic factors in the treatment of onychomy costs. Pharmacoeconomics 1996: 307–320.
18. EnsenP. et al. ActaDermato–Venereologica76: 280–1 (1996)
19.Faergemann J., Lehender H., Milleriouv L. Levels of terbinafine in plasma, stratum comeum, dermis–epidermis (without stratum comeum), sebum, hair and nails during and after 250 mg terbinafme orally once daily for 7 and 14 days.– Clin. Exp. Dermatol. 19:121–6.
20. Hall M., Monka C., Krupp P., O’Sullivan Safety of oral terbinafme. Results of a Postmarketing Surveillance study in 25884 patients.–Archives of Dermal, 1997, v. 1213–1218.
21. Goodfield M.J.D., Br. J. Dermatol. 1992; 126 suppl. 33–35
22. Jones Т.С. Overview of the use of terbinafme (Lamisil) in children. Br. J. of Dermatology; 1995; 132: 683–689.
23. Lamisil (terbinafine hydrochloride tablets). Physicians’Desk Reference. 51 st col Montvale, N.J.: Medical Economics; 1997,2334–95.
24. La Placa M et al. J. Dermatol. Tream 6: 51–2(1995) (LAS 446)
25. Matsumoto Т., Januma H., Kaneko S., Jakasu H., Nishiyama S. Clinical and pharmacokinetic investigations of oral terbinafme in patients with tinea unguium. – Mycoses 1995; 38: 135–144.
26. Nandwani R. et al. Br J Dermatol. 134 ( suppl. 46) : 22–24 (1996) (LAS 563)
27. Norden J et al. Scand J Infect Lis 23: 377–82 ( 1991) (LAS 188) 2 8. Onychomy costs and terbinafine. Lancet 1990; 335:636
29. Polak A., Handbook of Experimental Pharmacology; Chemotherapy of Fungal Diseases 1990, p.96–153.
30. Roberts D.T. et al J. Amer. Assoc. Dermatol. 1994; 31 (suppl.2) 578–581.
31. Roberts D.T. Prevalence of dermatophyte onychomycosis in the United Kingdom: results of an omnibus survey.– Br. J. Dermatol. 1992; 126 (Suppl. 39): 23–7
32. Roberts Dabriol. Abstracts of the 19–th world congress of dermatology, 1997, Sydney, Australia
33. Rynder N. S. The mechanism of action of terbinafine. Clin. Exp. Dermatol. 1989; 14:98–100.
34.Shauder M. Mycoses 31: 259–67 ( 1988) (LAS 62)
35.Singer M.J. et al, J.Amer.Acad Dermatol. 1997, 37; 765–771.
36.Suhonen R. and Neuvonen P., Rev.Contemp.Pharmacother, 1997; 8; 373–386.
37. Villars V et al. Br J Dermatol 126 (suppl 39): 61–9 (1992) (LAS 208)
38. Velthuis PJ et al. Br J Dermatol 144–6(1995) (LAS 465).
39. Williams and Hall M. “A review of the Safety of oral terbinafine (Lamisil) when used with oral coutraceptives and in pregnancy in a Postmarketing Surveillance Study”.– Book of abstracts, poster №81, Sing., 1988, 12–20.06, p.l 18.
40. Williams Т., Lanslandt J. and Jones T. A review of the efficacy and tolerability of terbinafine in children. Poster presented at 8 th International Congress Paediatric Dermatology, 1998.