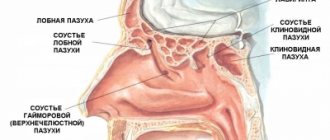
Термин «острый коронарный синдром» используется с тех пор, когда врачи стали выбирать активные методы терапии до подтверждения диагноза крупноочагового инфаркта миокарда.
- Классификация
- Патогенез
- Симптомы и диагностика
- Лечение острого коронарного синдрома
- Ведение больных после выписки из стационара
Термин ОКС означает сочетание определенного количества симптомов, которые указывают на нестабильную стенокардию или инфаркт миокарда. Острый коронарный синдром может обозначать несколько состояний больного:
- инфаркт миокарда без подъема сегмента 5Г;
- инфаркт миокарда с подъемом сегмента 5Г;
- нестабильную стенокардию;
- инфаркт миокарда, диагностированный по изменениям активно-сти кардиоспецифических ферментов, по биомаркерам, поздним ЭКГ-признакам.
На протяжении суток после помещения человека в больницу данный диагноз должен быть изменен на один из ниже перечисленных:
- «инфаркт миокарда с зубцом О»;
- «инфаркт миокарда без зубца О»;
- «нестабильная стенокардия»;
- «стабильная стенокардия напряжения» или «другое заболевание».
Классификация
По проявлениям и данным электрокардиограммы выделяют два вида острого коронарного синдрома:
• острый коронарный синдром без подъема сегмента 5Т (которые является следствием инфаркта миокарда (ИМ) без подъема сегмента 5Т или нестабильной стенокардии);
• острый коронарный синдром с подъемом сегмента 5Г.
Существует не одна классификация нестабильной стенокардии, часто применяется классификация 2000 года, авторство: Хамм-Браунвальд. Наихудший прогноз у нестабильной стенокардии, которая развилась за двео суток.
С клинической точки зрения прогностически наиболее неблагопри-ятна нестабильная стенокардия, развившаяся в течение 48 ч.
| А — развивается в присутствии экс-тракардиальных факторов, усиливающих ишемию миокарда(вторичная нестабильная стенокардия) | В — развивается без экстракарди-альных факторов (первичная нестабильная стенокардия) | С — развивается в пределах 2 нед после инфаркта миокарда (пост- инфарктная нестабильная стенокардия) | |
| I — первое появление тяжелой стенокардии, прогрессирующая стенокардия, без стенокардии покоя | 1А | № | 1С |
| II — стенокардия покоя в предшествующий месяц, но не в ближайшие 48 ч (стенокардия покоя, подострая) | НА | ИВ | НС |
| III — стенокардия покоя в предшествующие 48 ч (стенокардия покоя острая) | ША | ШВ ШВ тропонин (-) ШВ тропонин (+) | ШС |
Патогенез
В патогенезе острого коронарного синдрома имеют значение ниже перечисленные факторы.
- Тромбоз венечной артерии различной степени выраженности
- Надрыв или эрозия атеросклеротической бляшки
- Дистальная эмболизация венечных артерий
- Спазм венечной артерии
- Воспаление
Надрыв или эрозия атеросклеротической бляшки бывают, когда появляется ее нестабильность. А нестабильность, в свою очередь, может возникать из-за таких причин:
- тонкая фиброзная капсула с тонким слоем поверхностно поврежденного коллагена;
- большие размеры липидного ядра;
- высокая концентрация макрофагов и, соответственно, тканевых факторов (металлопротеиназ);
- низкая плотность гладкомышечных клеток.
Симптомы и диагностика
Проявления (клиника) острого коронарного синдрома без подъема сегмента 5Т делятся на две нозологические формы, которые отличаются в большинстве случаев лишь тяжестью симптомов:
- инфаркт миокарда без подъема сегмента 5Г;
- нестабильная стенокардия.
Инфаркт миокарда без подъема сегмента 5Т — острая ишемия миокарда, которая настолько тяжелая и длительная, что может вызвать некроз миокарда.
- На начальной стадии подъем сегмента 5Т на ЭКГ не регистрируется. У большинства пациентов далее также не появляются патологические зубцы 0. — у таких больных диагностируют инфаркт миокарда без зубца 0.
- Инфаркт миокарда без подъема сегмента 5Т отличается от нестабильной стенокардии лишь обнаружением в крови маркеров некроза миокарда.
Нестабильная стенокардия — острая ишемия миокарда, которая не может вызвать некроз миокарда. На электрокардиограмме подъем сегмента 5Т также не виден. Выброса в кровоток маркеров некроза миокарда не происходит по причине отсутствия явлений некроза.
Жалобы
Для диагностики острого коронарного синдрома имеет значение предшествующий анамнез ИБС. В типичных случаях острого коронарного синдрома у человека отмечается болевой синдром, который длится дольше, чем 15 минут. Для своевременной диагностики имеют значение жалобы больного на появление ночных приступов стенокардии, а также на развитие приступов стенокардии в состоянии покоя.
Атипичные нризнаки. В основном они бывают у людей в возрасте от 75 лет, молодых людей, которым менее 40 лет, больных с диагнозом «сахарный диабет», а также у женщин. Клиника может быть такой:
- Боль в районе эпигастрия
- Боль в покое
- Боль в грудной клетке с признаками, типичными для плеврита
- Колющая боль в грудной клетке
- Усиление одышки, ухудшение переносимости физической нагрузки
Электрокардиография
ЭКГ является очень значимым методом диагностики острого коронарного синдрома: характерны смещение сегмента 5Т и изменения зубца Г. Предпочтительно сделать запись электрокардиограммы на этапе проявления болевого синдрома. Необходимое условие диагностики острого коронарного синдрома — сравнение нескольких записей ЭКГ в динамике. Если при наличии типичного болевого синдрома на ЭКГ изменений нет, то некардиальные причины болей исключают.
Лабораторное исследование
Показаны:
- проведение общего анализа крови;
- определение биохимических показателей.
Для отличия инфаркта миокарда без подъема 5Т от нестабильной стенокардии в рамках острого коронарного синдрома нужно определить концентрацию сердечных тропонинов (качественно или количественно). Медики также определяют количество глюкозы в плазме крови, чтобы оценить углеводный обмен. При его нарушениях течение ОКС может ухудшиться.
Подготовка и практическая деятельность врача общей практики и врача, оказывающего специализированную медицинскую помощь пациентам кардиологического профиля на амбулаторном или стационарном этапе лечения, различны. Люди, которые обращаются к ВОП, нередко имеют иную клиническую картину, поскольку ранние проявления любого заболевания менее специфичны.
.
Актуальность проблемы
Более 10 лет назад J. Allen, советник Министерства здравоохранения Великобритании по первичной помощи, сказал: «Обучающийся предмету “Общая врачебная практика” должен быть там, где пациенты». Для врача любой специальности процесс непрерывного обучения является неотъемлемой составляющей профессии.
Обсуждая вопросы диагностики острого коронарного синдрома (ОКС), мы сосредоточимся на типичных клинических ситуациях, не забывая о том, что ежегодно во всем мире отмечается рост бессимптомных и атипичных форм инфаркта миокарда.
Одной из основных причин появления данной тенденции считается увеличение числа пациентов с коморбидной патологией, присутствие которой изменяет клиническую симптоматику при развитии ОКС. Оказание медицинской помощи при большом количестве сопутствующих заболеваний требует наличия у ВОП навыка выделения приоритетной проблемы. Он формируется по мере роста практического опыта при условии хороших теоретических знаний в области кардиологии и терапии.
Правильная оценка ранних неспецифических проявлений заболевания очень важна для врача первичного этапа оказания медицинской помощи. В подавляющем большинстве случаев развивающийся ОКС является наиболее опасным состоянием среди коморбидной патологии и требует быстрых профессиональных действий, а также наличия навыков общения с пациентом в критическом состоянии.
Ориентация на социально-экономические характеристики при обеспечении населения первичной медико-санитарной помощью включает умение согласовывать потребности отдельных пациентов в медицинской помощи с потребностями всей обслуживаемой группы населения и с имеющимися ресурсами системы здравоохранения.
Несмотря на совершенствование медицинских технологий, дифференциальный диагноз боли в грудной клетке остается сложной задачей, так как ее могут вызывать многие заболевания и состояния, а также их сочетания.
Особое значение имеет своевременное и точное распознавание прогностически неблагоприятных клинических ситуаций, требующих специальной тактики лечения. ОКС относится к патологии, актуальность максимально быстрой диагностики которой хорошо известна и не вызывает сомнений.
Однако гипердиагностика в данном случае также является существенной проблемой. За рубежом до 90 % лиц с острой болью в груди, направленных в отделения неотложной помощи, не имеют острой коронарной патологии. По данным российских специалистов, диагноз ОКС не подтверждается у трети пациентов, поступающих в стационар.
Необоснованное инвазивное и медикаментозное лечение значительно увеличивает затраты системы здравоохранения, ухудшает течение заболевания, приведшего к развитию болевого синдрома, а также создает дополнительные риски, связанные с госпитализацией и диагностическими манипуляциями, включая инфекционные и процедурные осложнения.
Основы диагностики
Термин «острый коронарный синдром» не является диагнозом и используется на этапе первичного медицинского контакта с пациентом до момента верификации основного заболевания. Это клинико-электрокардиографический феномен, который объединяет в себе единые по патогенезу нозологические формы (нестабильная стенокардия, острый инфаркт миокарда с подъемом или без подъема сегмента ST) и позволяет предположить наличие в коронарной артерии нестабильной атеросклеротической бляшки, частично или полностью окклюзирующей просвет сосуда.
Правильное понимание патогенеза ОКС обосновывает необходимость принятия ВОП быстрого решения о возможности и способах восстановления кровотока в инфаркт-связанной артерии. Достаточным информационным минимумом в данной ситуации являются клиническая картина развивающегося острого события и данные ЭКГ, которые должны быть записаны в течение 10 минут от момента первичного медицинского контакта с пациентом. В зависимости от регистрируемых изменений на ЭКГ, на догоспитальном этапе дифференцируется ОКС с подъемом или без подъема сегмента ST. Каждый вариант при общности клинической картины и патогенеза развития отличается индивидуальной тактикой и стратегией на догоспитальном и стационарном этапах лечения.
Клинически классический вариант ОКС проявляется развитием интенсивных болей в грудной клетке давящего, сжимающего или жгучего характера с возможной иррадиацией в левую или обе руки, межлопаточную область, шею, нижнюю челюсть продолжительностью более 15–20 минут.
Среди атипичных форм развивающегося инфаркта миокарда следует отметить:
- безболевую (отсутствует status anginosus, имеются ишемические изменения ЭКГ),
- астматическую (эквивалентом болевого синдрома является одышка или приступ острой левожелудочковой недостаточности),
- абдоминальную (болевые ощущения или дискомфорт локализованы в эпигастральной области),
- аритмическую (патогномоничными нарушениями ритма при ОКС считаются пароксизмы желудочковой тахикардии, фибрилляция желудочков, атриовентрикулярные блокады),
- периферическую (клиническим проявлением данного варианта является потеря сознания, обусловленная значительным снижением ударного объема).
Развитие ОКС со стойким подъемом сегмента ST в большинстве случаев предполагает наличие острой тромботической окклюзии коронарной артерии и требует максимально быстрого проведения реперфузионного вмешательства. Предпочтительным способом реперфузии в рассматриваемой ситуации является проведение первичного чрескожного коронарного вмешательства, что предполагает экстренную транспортировку пациента в стационар при прогнозируемом времени от первичного медицинского контакта до раздутия баллона в инфаркт-связанной артерии менее 90 минут. Если уложиться в указанный временной диапазон в силу разных обстоятельств не представляется возможным, пациентам с ОКС с подъемом сегмента ST в максимально ранние сроки должна быть проведена тромболитическая терапия при отсутствии противопоказаний для введения антитромботических лекарственных средств.
ОКС без подъема сегмента ST может проявляться депрессией сегмента ST, инверсией зубца T, отсутствием электрокардиографических изменений.
Реперфузионная стратегия ограничена проведением первичного чрескожного коронарного вмешательства, тромболитическая терапия при этом варианте ОКС не используется. Для решения вопроса о необходимости и срочности коронарного вмешательства на догоспитальном этапе должны быть оценены такие клинические факторы, как нестабильность гемодинамики, рефрактерный характер болевого синдрома, развитие жизнеугрожающих аритмий, кардиогенного шока, механических осложнений инфаркта миокарда, транзиторный подъем сегмента ST на ЭКГ покоя или сохраняющаяся депрессия сегмента ST.
При наличии у пациента с болевым синдромом в грудной клетке постинфарктного кардиосклероза, стабильной стенокардии напряжения или бессимптомной формы ИБС (безболевая ишемия миокарда) обнаружение отрицательного зубца Т или электрокардиографической картины рубцовых изменений может вызывать трудности при проведении дифференциальной диагностики со свежим некрозом миокарда. Особенно с случае, если отсутствуют записанные ранее электрокардиограммы.
Обычно внимательный опрос и осмотр пациента позволяют исключить острый инфаркт миокарда, но и здесь поначалу возможны трудности. Главным образом при «застывшей» форме ЭКГ и отсутствии достоверных сведений об особенностях ранее перенесенного инфаркта миокарда. Во всех этих случаях экстренная госпитализация пациентов с ишемической болезнью сердца оправдана — большинство из них проведет в отделении (блоке) интенсивной терапии и реанимации не более суток.
Выбор терапии
При появлении первых признаков ОКС пациенту необходимо прекратить физическую нагрузку, принять нитроглицерин сублингвально и при сохранении ангинозных болей в течение 15–20 минут или при возобновлении болевого синдрома в грудной клетке после приема нитроглицерина незамедлительно вызвать скорую медицинскую помощь.
В случае если первичный контакт с пациентом, у которого развивается ОКС, осуществляет ВОП, в его обязанности входит оценка клинических симптомов, запись ЭКГ, оказание первой медицинской помощи, вызов бригады скорой помощи. Правильность интерпретации данных ЭКГ в данном случае имеет принципиальное значение при выборе организационно-лечебной тактики.
Медикаментозная терапия, начинающаяся на догоспитальном этапе, направлена на купирование болевого синдрома, профилактику осложнений и создание оптимальных гемодинамических условий для максимального восстановления миокарда.
Используются следующие группы лекарственных средств:
- антикоагулянты,
- комбинированная дезагрегантная терапия,
- бета-адреноблокаторы,
- ингибиторы ангиотензинпревращающего фермента,
- статины (в соответствии с приложением 2 постановления Минздрава от 06.06.2017 № 59).
Выводы
Таким образом, для правильного врачебного заключения, определяющего выбор тактики ведения пациента с ОКС, необходим тщательный критический анализ всех имеющихся симптомов, данных анамнеза и ЭКГ, а также постоянная настороженность в отношении более редких причин развития болей в груди.
Проводя дифференциальный диагноз инфаркта миокарда с другими сердечными и внесердечными заболеваниями, необходимо руководствоваться некоторыми общими соображениями:
1. Соответствие диагноза инфаркта миокарда полу и возрасту пациента, наличию факторов риска.
2. Возникновение эпизодов загрудинных болей с аналогичной клинической картиной в прошлом и их исходы.
3. Наличие анамнестических указаний на заболевания, осложнения которых могут быть ошибочно приняты за инфаркт миокарда.
4. Во всех сомнительных случаях, за исключением острой хирургической патологии, гипердиагностика инфаркта миокарда — наименьшее зло.
Современные подходы к лечению пациентов с ОКС, использующие возможности интервенционных и при необходимости кардиохирургических методов лечения, а также эффективные медикаментозные технологии позволяют улучшить прогноз и качество жизни пациентов после перенесенного ОКС.
С другой стороны, нельзя забывать, что ишемическая болезнь сердца — это хроническое прогрессирующее заболевание сердечно-сосудистой системы, которое требует пожизненной медикаментозной терапии, отказа от курения, модификации образа жизни, ежедневной физической нагрузки на протяжении не менее 30 минут, нормализации массы тела, контроля артериального давления, достаточного ежедневного потребления овощей и фруктов, ограничения употребления соли и трансжиров.
В задачи ВОП входит необходимость обозначить перед пациентом абсолютную важность регулярного приема лекарственных средств для вторичной профилактики болезней системы кровообращения и предотвращения сердечно-сосудистых осложнений.
Лечение острого коронарного синдрома
Госпитализация
Больного с острым коронарным синдромом следует поместить в отделение реанимации или палату интенсивной терапии на сутки. Оставлять ли пациента там дальше, определяют медики, ориентируясь на показатели ЭКГ в динамике, на его состояние (степень тяжести), на анализы крови и пр.
Лекарства
Для лечения острого коронарного синдрома используют такие группы препаратов:
- р-Адреноблокаторы
- Нитраты
- Тромболитическую терапию, показанную при подъеме сегмента
- Блокаторы медленных кальциевых каналов
- Антитромботические антитромбиновые препараты: гепарин натрия, низкомолекулярные гепарины — надропарин кальция, эноксапарин натрия, далтепарин натрия
- Антитромботические антитромбоцитарные препараты: ацетилсалициловую кислоту, клопидогрел, абциксимаб, эптифибатид
Нитраты
Нитраты назначают тем, у кого сохраняются эпизоды ишемии миокарда (клиника в основном заключается в болевом синдроме). Вводятся внутривенно. Дозировку увеличивают, пока симптомы не исчезнут. Но клиника может сохраниться, а появятся побочные эффекты, тогда нитраты отменяют. Побочное действие проявляется в основном, головной болью, или повышением артериального давления. Если эффект от препаратов достигнут, далее назначают вместо них лекарства для приема внутрь, согласно рекомендациям ВНОК 2003 года.
Если вводить нитраты в/в, сначала скорость инфузии должна быть на уровне 10 мкг/мин. Далее дозу увеличивают на 10 мкг/мин каждые 3-5 минут, пока симптомы не начнут уменьшаться, или не отреагирует давление.
р-Адреноблокаторы
Препараты из этой категории оказывают такое действие:
- Снижают потребление кислорода миокардом из-за систолического АД и постнагрузки, уменьшения частоты сокращений сердца, а также ослабления сократимости миокарда.
- Увеличивают венечный кровоток за счет улучшения диастолической перфузии, увеличения дистальной венечной перфузии, благоприятного эпикардиально-эндокардиального сдвига.
Эффективно такое лекарство как Пропранолол, начальная доза которого составляет 0,5-1,0 мг. Спустя час лекарство больной должен принимать вовнутрь в дозе 40-80 мг каждые 4 часа до суммарной дозы 360-400 мг в сутки. Эффективен Метопролол, его начальная доза 5 мг, вводится внутривенно на протяжении 1-2 минут. Каждые 5 минут вводится повторная доза, пока общая не достигнет 15 мг. Через 15 мин после последнего внутривенного введения показан прием внутрь по 50 мг каждые 6 ч в течение 48 ч. Далее интервалы между приемами могут быть увеличены. Поддерживающая доза составляет 100 мг 2-3 раза в сутки. Нужный эффект дает еще один препарат из серии р-Адреноблокаторов — Атенолол, который вводится сначала в дозе 5 миллиграмм.
Гепарин
Нефракционированный гепарин применяют в качестве антикоагулянтного лечения. Но прием его может грозить кровотечениями из различных учасков тела и органов. Чтобы избежать этого, нужно наблюдать за свертывающей системой крови пациента. Стартовая доза колеблется от 60 до 80 ЕД/кг, она не может превышать 5000 ЕД.
Альтернативой нефракционированному гепарину являются низкомолекулярные гепарины. Введение их простое, чувствительность к тромбоцитарному фактору 4 меньшая, чем у нефракционированного гепарина, что относится к преимуществам данной группы препаратов. Актуальны такие средства:
- Далтепарин натрия
- Эноксапарин натрия
- Надропарин кальция
Ацетилсалициловая кислота
Терапия этим препаратов больше чем в два раза снижает риск смерти и развития ИМ у людей с ОКС без подъема сегмента 5Г. Первая доза составляет 250-500 мг, используют только таблетки без оболочки. Далее нужно принимать внутрь75-325 мг 1 раз в сутки.
Клопидогрел
Назначается этот препарат в основном пациентам с высоким риском инфаркта миокарда и летального исхода. В первые сутки нужно применить нагрузочную дозу, которая составляет 300 мг, потом в сутки доза составляет 75 мг. Курс лечения – 1-9 месяцев.
Проведение стресс-теста
Его проводят тем, кто находится в группе низкого риска, на 3-7-е сутки после характерного приступа при отсутствии повторных эпизодов ишемии миокарда в покое.
Диагностика и лечение острого коронарного синдрома: от понимания принципов к реализации стандартов
Определение
Согласно определению, приведенному в руководстве Американской коллегии кардиологов и Американской ассоциации сердца 2000 г., понятие «острый коронарный синдром» включает любые группы симптомов, позволяющие подозревать острый инфаркт миокарда (ИМ) или нестабильную стенокардию (НС). К основным клиническим вариантам ОКС относятся:
- ИМ с подъемом сегмента ST;
- ИМ без подъема сегмента ST;
- ИМ, диагностированный по изменениям ферментов или биомаркерам;
- ИМ, диагностированный по поздним ЭКГ–признакам;
- НС.
Следует подчеркнуть, что диагноз ОКС является временным, «рабочим» и используется для выделения категории больных с высокой вероятностью ИМ или НС при первом контакте с ними. Лечение больных с ОКС начинают до получения информации, необходимой и достаточной для уверенной постановки нозологического диагноза. После идентификации какого–либо из перечисленных выше клинических состояний на основе результатов диагностических тестов производится коррекция терапии.
Патогенез
Ведущим патогенетическим механизмом ОКС является тромбоз пораженной атеросклерозом коронарной артерии
. Тромб образуется в месте разрыва атеросклеротической бляшки. Вероятность разрыва бляшки зависит от ее расположения, размера, консистенции и состава липидного ядра, прочности фиброзной капсулы, а также выраженности местной воспалительной реакции и напряжения стенки сосуда. Непосредственными причинами повреждения оболочки бляшки являются механическое воздействие кровотока и ослабление фиброзной капсулы под влиянием протеолитических ферментов, выделяемых макрофагами. Содержимое бляшки характеризуется высокой тромбогенностью – его воздействие на кровь приводит к изменению функциональных свойств тромбоцитов и запуску коагуляционного каскада. Определенную роль в развитии ОКС играет спазм коронарной артерии в месте расположения поврежденной бляшки. В случаях, когда нарушение проходимости коронарной артерии вызывается ее спазмом и/или формированием тромбоцитарного агрегата (то есть является обратимым), развивается клиническая картина НС. Образование красного тромба, не полностью перекрывающего просвет сосуда, ведет к развитию ИМ без зубца Q. При полной тромботической окклюзии коронарной артерии формируется ИМ с зубцом Q.
Диагностика
Распознавание ОКС базируется на трех группах критериев. Первую группу составляют признаки, определяемые при расспросе и физикальном исследовании больного, вторую группу – данные инструментальных исследований и третью – результаты лабораторных тестов.
Типичными клиническими проявлениями ОКС являются ангинозная боль
в покое продолжительностью более 20 мин, впервые возникшая стенокардия III функционального класса, прогрессирующая стенокардия. К атипичным проявлениям ОКС относят разнохарактерные болевые ощущения в грудной клетке, возникающие в покое, боль в эпигастрии, острые расстройства пищеварения, боль, характерную для поражения плевры, нарастающую одышку. Физикальное исследование больных с ОКС нередко не выявляет каких–либо отклонений от нормы. Его результаты важны не столько для диагностики ОКС, сколько для обнаружения признаков возможных осложнений ишемии миокарда, выявления заболеваний сердца неишемической природы и определения экстракардиальных причин жалоб больного.
Основным методом инструментальной диагностики ОКС является электрокардиография
. ЭКГ больного с подозрением на ОКС, по возможности, следует сопоставлять с данными предыдущих исследований. При наличии соответствующей симптоматики для НС характерны депрессия сегмента ST не менее чем на 1 мм в двух и более смежных отведениях, а также инверсия зубца T глубиной более 1 мм в отведениях с преобладающим зубцом R. Для развивающегося ИМ c зубцом Q характерна стойкая элевация сегмента ST, для стенокардии Принцметала и развивающегося ИМ без зубца Q – преходящий подъем сегмента ST (рис. 1). Помимо обычной ЭКГ в покое, для диагностики ОКС и контроля эффективности лечения применяется холтеровское мониторирование электрокардиосигнала.
Рис. 1. Варианты ОКС в зависимости от изменений ЭКГ
Из биохимических тестов, применяемых для диагностики ОКС, предпочтительным считается
определение содержания в крови сердечных тропонинов T и I
, повышение которого представляет собой наиболее надежный критерий некроза миокарда. Менее специфичным, но более доступным для определения в клинической практике критерием является повышение в крови уровня креатинфосфокиназы (КФК) за счет ее изофермента МВ–КФК. Увеличение содержания МВ–КФК (предпочтительно массы, а не активности) в крови более чем вдвое по сравнению с верхней границей нормальных значений при наличии характерных жалоб, изменений ЭКГ и отсутствии других причин гиперферментемии позволяет с уверенностью диагностировать ИМ. Повышение уровня МВ–КФК и сердечных тропонинов регистрируется через 4–6 часов от начала формирования очага некроза миокарда.
Наиболее ранним биомаркером ИМ является миоглобин
– его содержание в крови повышается спустя 3–4 часа после развития ИМ. Для исключения или подтверждения диагноза ИМ рекомендуются повторные анализы крови в течение 6–12 часов после любого эпизода сильной боли в грудной клетке. Перечисленные тесты приобретают особенно важное значение при дифференциальной диагностике ИМ без зубца Q и НС.
Традиционные биомаркеры некроза миокарда, такие как аспарагиновая аминотрансфераза, лактатдегидрогеназа и даже общая КФК, в связи с недостаточной чувствительностью и специфичностью не рекомендуются для диагностики ОКС. В условиях практического здравоохранения средства, затрачиваемые на приобретение реактивов для их определения, целесообразно направить на внедрение рекомендованных диагностических тестов.
Оценка риска
В течение первых 8–12 часов после появления клинической симптоматики ОКС необходимо обеспечить сбор диагностической информации в объеме, достаточном для стратификации риска. Определение степени непосредственного риска смерти или развития ИМ принципиально важно для выбора лечебной тактики в отношении больного с ОКС без стойкого подъема сегмента ST.
К критериям высокого непосредственного риска смерти и развития ИМ относятся:
повторные эпизоды ишемии миокарда (повторяющиеся ангинозные приступы в сочетании и без сочетания с преходящей депрессией или подъемом сегмента ST); повышение содержания сердечных тропонинов (при невозможности определения – МВ–КФК) в крови; гемодинамическая нестабильность (артериальная гипотензия, застойная сердечная недостаточность); пароксизмальные желудочковые нарушения ритма сердца (желудочковая тахикардия, фибрилляция желудочков); ранняя постинфарктная стенокардия.
Признаками низкого непосредственного риска смерти и развития ИМ являются:
отсутствие повторных приступов боли в грудной клетке; отсутствие депрессии или подъема сегмента ST – изменения только зубца Т (инверсия, уменьшение амплитуды) или нормальная ЭКГ; отсутствие повышения содержания сердечных тропонинов (при невозможности их определения – МВ–КФК) в крови.
С целью подтверждения диагноза ИБС и оценки отдаленного прогноза у больных с низким непосредственным риском развития ИМ и смерти спустя 3–5 дней после эпизода с симптоматикой ОКС рекомендуется выполнение стресс–теста
. У больных с высоким непосредственным риском развития ИМ и смерти проведение стресс–теста для оценки прогноза и определения лечебной тактики считается возможным не ранее чем через 5–7 дней после стойкой стабилизации состояния. При подозрении на безболевую ишемию миокарда проведению стресс–теста должно предшествовать холтеровское мониторирование ЭКГ. Стандартный нагрузочный тест подразумевает регистрацию ЭКГ во время физической нагрузки на велоэргометре или тредмиле. У ряда больных тест с физической нагрузкой может быть недостаточно информативен. В этих случаях возможно выполнение
стресс–эхокардиографии с физической нагрузкой
. Фармакологические стресс–тесты с применением эхокардиографии или сцинтиграфии миокарда показаны пациентам, у которых имеются ограничения физической активности.
К критериям высокого риска неблагоприятного исхода, определяемым по результатам стресс–тестов, относятся: развитие ишемии миокарда при низкой толерантности к физической нагрузке; обширный стресс–индуцированный дефект перфузии; множественные стресс–индуцированные дефекты перфузии небольшого размера; выраженная дисфункция левого желудочка (фракция выброса менее 35%) в покое или при нагрузке; стабильный или стресс–индуцированный дефект перфузии в сочетании с дилатацией левого желудочка.
Пациентам, отнесенным к категории высокого риска по клиническим признакам, данным инструментальных и лабораторных тестов, а также больным с НС, перенесшим ранее коронарную баллонную ангиопластику (КБА) или коронарное шунтирование (КШ), показана коронарография
. На результатах последней основывается выбор дальнейшей тактики лечения больного – в частности, оценка целесообразности выполнения и определение вида операции реваскуляризации миокарда. Больным с упорно рецидивирующим болевым синдромом и выраженной гемодинамической нестабильностью коронарографическое исследование рекомендуется проводить в максимально сжатые сроки после появления клинической симптоматики ОКС без предварительного проведения стресс–тестов.
Медикаментозное лечение
С учетом представлений о механизмах развития главным направлением патогенетической терапии ОКС следует считать воздействие на систему свертывания крови
. К средствам, влияющим на процесс тромбообразования, относятся три группы лекарственных препаратов: тромболитики, антикоагулянты и антиагреганты.
Тромболитическая терапия (ТЛТ)
Показанием к ТЛТ является ангинозная боль длительностью более 30 мин, сохраняющаяся несмотря на прием нитроглицерина, в сочетании с элевацией на 1 мм и более сегмента ST не менее чем в 2–х смежных отведениях ЭКГ или появлением полной блокады левой ножки пучка Гиса. Анализ результатов плацебо–контролируемых исследований (GISSI–1, ISIS–2, ASSET, LATE) показал, что ТЛТ, выполненная в первые 6 часов после появления клинической симптоматики развивающегося ИМ, уменьшает смертность в течение первого месяца после развития ИМ в среднем на 30%. Проведение ТЛТ в сроки 6–12 часов от момента возникновения ангинозной боли уменьшает смертность в среднем на 20% и считается допустимым при наличии клинических и ЭКГ признаков расширения зоны некроза миокарда. ТЛТ, выполненная позже 12 часов от момента развития ИМ, позитивного влияния на смертность не оказывает. При отсутствии стойкой элевации сегмента ST, которая рассматривается как признак закупорки коронарной артерии фибринсодержащим тромбом, применение ТЛТ также нецелесообразно.
Абсолютными противопоказаниями к ТЛТ являются геморрагический инсульт в анамнезе, ишемический инсульт или динамическое нарушение мозгового кровообращения в течение последнего года, внутричерепная опухоль, активное внутреннее кровотечение, расслаивающая аневризма аорты.
Исследование GUSTO
доказало, что ускоренный режим введения
альтеплазы
является наилучшей стратегией тромболитической терапии в настоящий момент для пациентов с ИМ.
Схема ускоренного введения альтеплазы (100 мг) при ИМ в течение 6 часов от начала развития симптомов при массе тела более 65 кг следующая: 15 мг альтеплазы болюсно в течение 1-2 мин., затем инфузионно внутривенно 50 мг в течение 30 мин. и затем 35 мг в течение 60 мин. До начала внутривенное введение гепарина 5000 МЕ + внутривенная инфузия гепарина 1000 МЕ/ч в последующие двое суток.
Антикоагулянты
Из соединений, относящихся к данной фармакологической группе, в лечении больных с ОКС применяется главным образом нефракционированный гепарин
(НФГ). В отличие от тромболитических средств НФГ вводится не только больным со стойкой элевацией сегмента ST, но и пациентам с другими вариантами ОКС. Основными противопоказаниями к гепаринотерапии являются активное кровотечение и заболевания, сопровождающиеся высоким риском его возникновения.
Схема введения НФГ больным с ОКС без стойкого подъема сегмента ST: внутривенно – болюс 60–80 ЕД/кг (но не более 5000 ЕД), затем инфузия 12–18 ЕД/кг/ч (но не более 1250 ЕД/кг/ч) в течение 48 часов. Оптимальная скорость введения гепарина определяется по величине активированного частичного тромбопластинового времени (АЧТВ). Использование с этой целью времени свертывания крови не рекомендуется. Условием результативности гепаринотерапии считается увеличение АЧТВ в 1,5–2,5 раза по сравнению с нормальным значением этого показателя для лаборатории данного лечебного учреждения. АЧТВ рекомендуется определять через 6 часов после начала инфузии и затем – через 6 часов после каждого изменения скорости введения гепарина. Если при двух последовательных определениях АЧТВ сохраняется в желаемых пределах, следующий анализ может быть выполнен через 24 часа. Определение АЧТВ перед началом гепаринотерапии необязательно.
В случаях ОКС со стойким подъемом сегмента ST при отсутствии противопоказаний гепарин показан всем больным, не получавшим ТЛТ, а также больным, у которых планируется проведение реваскуляризации миокарда. НФГ рекомендуется вводить подкожно по 7500–12500 ЕД 2 раза в день или внутривенно. Рекомендуемая продолжительность терапии гепарином при его подкожном введении составляет 3–7 дней. Внутривенный путь введения НФГ является предпочтительным для больных с повышенным риском тромбоэмболических осложнений (обширный ИМ, передняя локализация ИМ, мерцательная аритмия, тромбоэмболии в анамнезе, документированный тромб в левом желудочке).
Целесообразность применения НФГ в сочетании с ТЛТ оспаривается. Согласно современным представлениям, если тромболизис проводится неспецифичными фибринолитическими препаратами (стрептокиназа, анистреплаза, урокиназа) на фоне применения ацетилсалициловой кислоты в полной дозе, введение гепарина необязательно. При применении альтеплазы внутривенное введение гепарина считается оправданным. Гепарин вводится внутривенно болюсом 60 ЕД/кг (но не более 4000 ЕД), затем – со скоростью 12 ЕД/кг/ч (но не более 1000 ЕД/кг/ч) в течение 48 часов под контролем АЧТВ, которое должно превышать контрольный уровень в 1,5–2 раза. Начинать гепаринотерапию рекомендуется одновременно с введением альтеплазы. Наличие критериев высокого риска развития тромбоэмболических осложнений рассматривается, как показание к гепаринотерапии больных, которым проводился тромболизис, вне зависимости от вида тромболитического препарата.
Низкомолекулярные гепарины (эноксапарин, фраксипарин) обладают рядом преимуществ по сравнению с НФГ: эти препараты имеют большую продолжительность действия и более предсказуемый антикоагулянтный эффект, вводятся подкожно в фиксированной дозе, не требуя применения инфузионного насоса и лабораторного контроля. Результаты исследований FRIC
,
FRAXIS
,
TIMI 11B
показали, что низкомолекулярные гепарины обладают не меньшей, но и не большей, чем НФГ, способностью снижать риск развития ИМ и смерти у больных с НС и ИМ без зубца Q. Лишь эноксапарин, по данным исследования
ESSENCE
, сильнее, чем НФГ, уменьшал риск развития суммы «коронарных событий» (смерть, ИМ, рецидив стенокардии) и частоту экстренных операций реваскуляризации миокарда. Объединенные результаты исследований ESSENCE и TIMI 11B подтвердили клинические преимущества эноксапарина перед НФГ. Длительность лечения больных ОКС низкомолекулярными гепаринами в среднем составляет 5–7 суток. Исследования FRIC, FRAXIS и TIMI 11B показали, что более продолжительное их применение не приводит к дополнительному снижению частоты «коронарных событий», но увеличивает риск кровотечений. Вместе с тем результаты, полученные в исследованиях TIMI 11B и FRISC II, позволяют предполагать, что увеличение длительности гепаринотерапии может оказаться полезным для пациентов, готовящихся к операции реваскуляризации миокарда.
Стоимость низкомолекулярных гепаринов превосходит стоимость НФГ. Вместе с тем их эффективное клиническое применение не требует дорогостоящего инструментального и лабораторного обеспечения. Если медицинское учреждение не располагает необходимыми материально–техническими ресурсами и не способно обеспечить введение НФГ в соответствии с изложенными выше требованиями, для лечения больных с ОКС рекомендуется использовать низкомолекулярные гепарины.
В последние годы было выполнено 4 крупных исследования (OASIS–2, ASPECT, APRICOT–2, WARIS), результаты которых дают основание полагать, что прогноз больных, перенесших ОКС, может быть существенно улучшен за счет включения в состав комплексной терапии непрямого антикоагулянта варфарина. Продолжительное (от 3 месяцев до 4 лет) применение варфарина (в дополнение к ацетилсалициловой кислоте) способствовало снижению частоты реокклюзий инфаркт–зависимой коронарной артерии у больных ИМ после успешной ТЛТ, уменьшению риска развития ИМ, мозгового инсульта и смерти без достоверного увеличения частоты геморрагических осложнений. Однако широкое применение варфарина во вторичной профилактике ИБС ограничивается необходимостью регулярного контроля антикоагуляционного эффекта по величине международного нормализованного отношения.
Антиагреганты
Наиболее широко используемым в клинической практике антиагрегантом является ацетилсалициловая кислота. Препарат показан при всех вариантах ОКС. Его применение отчетливо снижает риск смерти и развития ИМ. Так, по данным исследования ISIS II, в течение 35 суток после развития ИМ по сравнению с группой больных, получавших плацебо, летальность при лечении только ацетилсалициловой кислотой снижалась на 23%, только стрептокиназой – на 25% и ацетилсалициловой кислотой в сочетании со стрептокиназой – на 42%. Минимальная доза ацетилсалициловой кислоты, обеспечивающая уменьшение риска развития смерти и ИМ у больных с НС, составляет 75 мг/сут.
Среди противопоказаний к применению ацетилсалициловой кислоты в клинической практике чаще всего встречаются обострение язвенной болезни, геморрагические диатезы и повышенная чувствительность к салицилатам. В случаях непереносимости ацетилсалициловой кислоты рекомендуется применение препаратов из группы тиенопиридинов (тиклопидин, клопидогрель). Их основным недостатком является медленное развитие антиагрегационного эффекта. При ОКС с целью ускорения развития лекарственного воздействия в первые двое суток терапии допускается увеличение дозы тиклопидина до 1000 мг/сут с последующим переходом на прием стандартной дозы 500 мг/сут. В случаях индивидуальной непереносимости или развития побочных эффектов (аллергические реакции, желудочно–кишечные расстройства, нейтропения) тиклопидин может быть заменен на клопидогрель – 300 мг однократно, затем по 75 мг/сут.
Весьма перспективной считается концепция комбинированной антиагрегационной терапии, то есть одновременного блокирующего воздействия на различные пути активации тромбоцитов. В исследовании CURE
было показано, что лечение больных, перенесших ОКС без подъема сегмента ST, комбинацией ацетилсалициловой кислоты и клопидогреля по сравнению с терапией только ацетилсалициловой кислотой приводит к достоверно более выраженному снижению риска развития сердечно–сосудистых событий при отсутствии разницы по количеству жизнеугрожающих кровотечений.
Наиболее сильным антиагрегационным эффектом обладают блокаторы IIb/IIIa рецепторов тромбоцитов
(абциксимаб, эптифибатид, тирофибан, ламифибан), которые способны блокировать агрегацию тромбоцитов, вызываемую любым физиологическим индуктором. По данным многочисленных исследований (EPILOG, EPISTENT, EPIC, CAPTURE, PRISM–PLUS, PURSUIT, PARAGON и др.), внутривенное введение этих препаратов больным с ОКС без подъема сегмента ST в дополнение к ацетилсалициловой кислоте и НФГ значимо улучшало результаты КБА как в сочетании, так и без сочетания с установкой стента. Абциксимаб был эффективен только у больных, которым проводилась реваскуляризация миокарда, тирофибан и эптифибатид – как при проведении реваскуляризации, так и при медикаментозном лечении. Дополнительное снижение числа неблагоприятных исходов было особенно выраженным при добавлении антагонистов гликопротеиновых рецепторов IIb/IIIa к стандартному антитромботическому лечению у больных с повышенным уровнем сердечных тропонинов. В то же время длительное применение этих препаратов внутрь, по данным исследований OPUS–TIMI и SYMPHONY, не оказывало положительного влияния на результаты лечения больных с ОКС. Основным показанием к применению антагонистов гликопротеиновых рецепторов IIb/IIIa у больных с ОКС является отсутствие стойкого подъема сегмента ST в сочетании с высоким непосредственным риском смерти или развития ИМ при запланированном проведении процедуры реваскуляризации миокарда в ближайшие 24 часа.
Рекомендуемые дозы антагонистов гликопротеиновых рецепторов IIb/IIIa: абциксимаб – внутривенно болюс 0,25 мг/кг с последующей инфузией 0,125 мкг/кг/мин в течение 12–24 часов; эптифибатид – внутривенно болюс 180 мг/кг c последующей инфузией 2,0 мкг/кг/мин в течение 72–96 часов; тирофибан – внутривенная инфузия 0,4 мкг/кг/мин в течение получаса, затем 0,1 мкг/кг/мин в течение 48–96 часов.
Нитраты
На начальном этапе лечения больных с ОКС препараты нитроглицерина и изосорбида–динитрата применяются внутривенно. Начальная скорость инфузии составляет 10 мкг/мин. Каждые 3–5 мин скорость введения увеличивают на 10 мкг/мин. Выбор скорости инфузии и темпа ее увеличения определяется изменениями выраженности болевого синдрома и уровня артериального давления (АД). Не рекомендуется снижать систолическое АД более чем на 15% от исходного при нормотензии и на 25% при гипертензии. При достижении желаемого эффекта скорость инфузии стабилизируется, а затем постепенно снижается. В случае избыточного снижения АД продолжительность введения препаратов на каждой ступени дозирования и интервалы между ними увеличиваются. Помимо снижения АД, к наиболее частым побочным эффектам, препятствующим проведению эффективной антиангинальной терапии, относится головная боль. После завершения внутривенного введения препараты органических нитратов (предпочтительно производные изосорбида–динитрата или изосорбида–5–мононитрата) назначаются внутрь по асимметричной схеме с обеспечением «безнитратного» интервала.
b–адреноблокаторы
Препараты этой группы рекомендуется применять у всех больных с ОКС при отсутствии противопоказаний, к которым относятся бронхиальная астма, тяжелая обструктивная дыхательная недостаточность, брадикардия в покое менее 50 ударов в минуту, синдром слабости синусового узла, атриовентрикулярная блокада II–III степени, хроническая сердечная недостаточность IV функционального класса, выраженная артериальная гипотензия. Начинать лечение предпочтительно с внутривенного введения b–адреноблокаторов при постоянном мониторировании ЭКГ
. После внутривенной инфузии рекомендуется продолжить лечение b–адреноблокаторами путем приема внутрь. По данным мета–анализа выполненных к настоящему времени исследований, продолжительное лечение b–адреноблокаторами больных, перенесших ИМ с зубцом Q, позволяет уменьшить смертность на 20%, риск внезапной смерти на 34% и частоту нефатального ИМ на 27%. Наиболее эффективными и безопасными считаются b1–селективные соединения без собственной симпатомиметической активности.
Схемы применения: пропранолол
– внутривенно медленно 0,5–1,0 мг, затем внутрь по 40–80 мг каждые 6 часов;
метопролол
– внутривенно 5 мг за 1–2 мин трижды с интервалами между инъекциями по 5 мин, затем (через 15 минут после последней инъекции) внутрь по 25–50 мг каждые 6 часов;
атенолол
– внутривенно 5 мг за 1–2 мин дважды с интервалом между инъекциями 5 мин, затем (через 1–3 часа после последней инъекции) внутрь по 50–100 мг 1–2 раза в день. Индивидуальная доза b–адреноблокаторов подбирается с учетом частоты сердечных сокращений, целевое значение которой составляет 50–60 ударов в мин.
Антагонисты кальция
Производные дигидропиридина, бензодиазепина и фенилалкиламина, наиболее широко применяемыми представителями которых являются препараты первого поколения – соответственно нифедипин, дилтиазем и верапамил, различаются по выраженности вазодилатирующего действия, отрицательного инотропного и отрицательного дромотропного эффектов. Мета–анализы результатов рандомизированных исследований выявили дозозависимое негативное влияние нифедипина короткого действия на риск смерти больных с НС и ИМ. В связи с этим короткодействующие производные дигидропиридина не рекомендуются для лечения больных с ОКС. В то же время, по данным некоторых исследований, продолжительное применение дилтиазема (MDPIT, DRS) и верапамила (DAVIT II) препятствует развитию повторного ИМ и смерти у больных, перенесших ИМ без зубца Q. У больных с ОКС дилтиазем и верапамил применяются в случаях, когда имеются противопоказания к применению b–адреноблокаторов (например, обструктивный бронхит), но при отсутствии дисфункции левого желудочка и нарушений атриовентрикулярной проводимости. Рекомендуемые дозы препаратов составляют 180–360 мг/сут.
Ингибиторы ангиотензинпревращающего фермента
Положительное влияние ингибиторов ангиотензинпревращающего фермента (АПФ) на выживаемость больных, перенесших ИМ (в особенности осложненный застойной сердечной недостаточностью), доказана в ряде контролируемых исследований – GISSI–3
,
ISIS–4
,
AIRE
,
SAVE
,
TRACE
и др. Обширный ИМ с патологическим зубцом Q является показанием к применению ингибиторов АПФ даже при отсутствии клинических и эхокардиографических признаков дисфункции левого желудочка. Чем раньше начинается лечение ингибиторами АПФ, тем сильнее выражено их тормозящее влияние на процесс постинфарктного ремоделирования сердца. С другой стороны, как показали результаты исследования CONSENSUS II, которое было прервано досрочно в связи с тем, что смертность в группе больных, получавших эналаприл, превысила смертность больных контрольной группы, ингибиторы АПФ должны применяться в терапии больных ИМ с большой осторожностью. По возможности, терапию следует начинать после стабилизации гемодинамики в первые 48 часов от момента развития ИМ. Рекомендуются следующие начальные дозы препаратов: каптоприл – 25 мг/сут, эналаприл и лизиноприл – 2,5 мг/сут, периндоприл – 2 мг/сут. Увеличение дозы должно проводиться постепенно под контролем АД и функции почек. При достижении оптимальной дозы терапия должна продолжаться в течение многих лет.
Немедикаментозное лечение
КБА или КШ выполняются больным с рецидивирующей ишемией миокарда для предотвращения ИМ и смерти. Выбор метода реваскуляризации миокарда зависит от степени, протяженности и локализации стеноза коронарной артерии, количества пораженных сосудов, которые определяются по результатам ангиографии. Операция АКШ при НС и в остром периоде ИМ сопряжена с повышенным риском операционной летальности. Данная методика реваскуляризации миокарда оправдана при поражении ствола левой коронарной артерии или многососудистом поражении. У больным с поражением одного, реже двух сосудов реваскуляризация миокарда обычно достигается путем КБА.
Как указывалось выше, улучшение результатов КБА, а также процедуры стентирования коронарной артерии (исследование EPISTENT) может быть достигнуто с помощью блокаторов IIb/IIIa рецепторов. КБА все более широко применяется при лечении больных с элевацией сегмента ST вместо ТЛТ. Это позволяет не только получить дополнительное снижение больничной летальности, но и значительно уменьшить риск осложнений, обусловленных медикаментозным воздействием на свертывающую систему крови.
Тактика медицинской помощи больным с ОКС
Объем инструментальных и лабораторных исследований, а также выбор методов медикаментозного и немедикаментоного лечения больного с симптоматикой ОКС определяется условиями оказания медицинской помощи и возможностями конкретного медицинского учреждения. Предварительный диагноз устанавливается на основании жалоб больного. Следует подчеркнуть, что отсутствие патологических изменений на ЭКГ не исключает ОКС. При подозрении на связь болей в грудной клетке с острой коронарной недостаточностью больной должен быть срочно госпитализирован – по возможности, в специализированное отделение (палату) интенсивного наблюдения и терапии, где выполняются необходимые диагностические исследования.
Алгоритм медицинской помощи больным с ОКС представлен на рисунке 2. Первыми медикаментозными средствами, которые следует применить при подозрении на ОКС, являются ацетилсалициловая кислота – 325 мг внутрь (для ускорения всасывания таблетку следует разжевать) и нитроглицерин – 0,5 мг под язык (при необходимости возможен прием до 3 таблеток с интервалом 5 мин). Больные со стойкой элевацией сегмента ST или появлением блокады левой ножки пучка Гиса получают ТЛТ или подвергаются первичной КБА. Больные с депрессией сегмента ST, инверсией зубца Т или отсутствием изменений ЭКГ получают гепаринотерапию, b–адреноблокаторы, при сохранении болевого синдрома – нитраты внутривенно. В случаях непереносимости b–адреноблокаторов или наличии противопоказаний к их применению назначаются антагонисты кальция. Всем больным обеспечивается многоканальное мониторирование ЭКГ. После получения дополнительной информации (результаты клинического наблюдения, данные ЭКГ в динамике, анализ содержания сердечных тропонинов, КФК и МВ–КФК в крови) проводятся уточнение диагноза и оценка риска негативного развития событий, на основании чего принимаются дальнейшие тактические решения. Больным, у которых развился ИМ, но в остром периоде не была выполнена КБА, перед выпиской из стационара проводится проба с физической нагрузкой для определения прогноза и показаний к хирургическому лечению.
Рис. 2. Алгоритм медицинской помощи больным с ОКС
Больным с высоким непосредственным риском развития ИМ и смерти, при возможности, следует начать введение блокаторов IIb/IIIa рецепторов, выполнить коронарографию, КБА и продолжить терапию блокаторами IIb/IIIa рецепторов. В случаях, когда введение препаратов данной группы и выполнение процедуры реваскуляризации миокарда невозможно, осуществляется гепаринотерапия (НФГ или низкомолекулярные гепарины) в сочетании с ацетилсалициловой кислотой, b–адреноблокаторами и при необходимости нитратами внутривенно. После стабилизации состояния данной категории больных показано проведение пробы с физической нагрузкой для определения прогноза и показаний к КБА или КШ. Лечение больных с низким риском развития ИМ и смерти включает прием внутрь ацетилсалициловой кислоты, b–адреноблокаторов или антагонистов кальция и нитратов. При отсутствии изменений ЭКГ и повышения содержания в крови биохимических маркеров некроза миокарда по результатам двух определений введение НФГ или низкомолекулярных гепаринов может быть прекращено. Спустя 5–7 дней больным данной категории показано выполнение пробы с физической нагрузкой для уточнения диагноза ИБС, прогноза и дальнейшей тактики лечения.
Большая часть неблагоприятных событий приходится на первые месяцы после развития ОКС. В лечении больных, перенесших ОКС, помимо средств непосредственного воздействия на коронарное кровообращение, необходимо проведение мероприятий, направленных на ослабление действия модифицируемых факторов риска прогрессирования ИБС. Больные должны прекратить курение. В случаях, когда применение b–адреноблокаторов или антагонистов кальция и ингибиторов АПФ в средне–терапевтических дозах не позволяет скорректировать повышенное АД, следует увеличить дозы применяемых препаратов или назначить дополнительно антигипертензивные лекарственные средства. Больные должны соблюдать гиполипидемическую диету. Статины, согласно современным представлениям, показаны больным, перенесшим ОКС, даже при отсутствии повышения содержания в крови холестерина атерогенных липопротеидов низкой плотности. Все более веские подтверждения получает идея применения статинов с первых суток заболевания.
Показатели летальности при ОКС в России в 2–3 раза выше, чем в странах Западной Европы и Северной Америки. Главной причиной этого различия является неполноценное применение в отечественной клинической практике эффективных методов диагностики и лечения ОКС. К сожалению, многие учреждения здравоохранения современной России не располагают возможностями обеспечить выполнение рекомендаций по медицинской помощи больным с ОКС. Однако наряду с объективными трудностями (прежде всего, финансового характера) к причинам этого следует отнести и недостаточную профессиональную осведомленность врачей. Именно недостаточность профессиональных знаний является предпосылкой нерационального использования финансовых средств, выделяемых для оказания медицинской помощи больным с ОКС, значительная часть которых в настоящее время расходуется на обеспечение малоинформативных диагностических методик и приобретение малоэффективных лекарственных препаратов. Принятие врачами основных положений рекомендаций по диагностике и лечению ОКС является важнейшим условием их успешного внедрения в клиническую практику, а реализация согласованных стандартов представляет собой доказанную возможность существенного улучшения результатов медицинской помощи.
Санкт-Петербургская государственная медицинская академия им. И.И. Мечникова
Литература:
1. ACC/AHA guidelines for the management of patients with acute myocardial infarction: a report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on Management of Acute Myocardial Infarction). J Am Coll Cardiol 1996;28:1328–1428.
2. Update: ACC/AHA guidelines for the management of patients with acute myocardial infarction: executive summary and recommendations: a report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on Management of Acute Myocardial Infarction). Circulation 1999;100:1016–1030.
3. ACC/AHA guidelines for the management of patients with unstable angina and non–ST–segment elevation myocardial infarction. A report of the American College of Cardiology/American Heart Association Task Force on Pratice Guidelines (Committee on the Management of Patients with Unstable Angina). J Am Coll Cardiol 2000;36:970–1062.
4. Management of acute coronary syndromes: acute coronary syndromes without persistent ST segment elevation. Recommendations of the Task Force of the European Society of Cardiology. Eur Heart J 2000;21:1406–1432.
5. Лечение острого коронарного синдрома без стойких подъемов сегмента ST на ЭКГ. Российские рекомендации. Разработаны Комитетом эксрпертов Всероссийского научного общества кардиологов. М 2001;23.