Аранесп (Aranesp)
Лечение препаратом Аранесп должно проводиться врачами, имеющими опыт назначения по вышеупомянутым показаниям.
Способ применения
Терапия симптоматической анемии в сочетании с хронической почечной недостаточностью (ХПН) у взрослых и детей
Симптомы анемии и последствия могут варьироваться в зависимости от возраста пациентов, их пола и тяжести заболевания; в каждом случае необходим анализ индивидуальных клинических данных пациента лечащим врачом. Аранесп может применяться подкожно или внутривенно для повышения содержания гемоглобина, но не выше 12 г/дл. У пациентов, не находящихся на диализе, подкожный способ введения является предпочтительным, так как позволяет избежать пункций периферических вен. Следует проводить тщательное наблюдение за пациентами для обеспечения адекватной коррекции анемии при сохранении концентрации гемоглобина ниже или на уровне 12 г/дл с применением минимальных одобренных доз препарата Аранесп. Следует с осторожностью повышать дозу препарата Аранесп у пациентов с хронической почечной недостаточностью. У пациентов с недостаточным ответом на Аранесп в отношении содержания гемоглобина следует рассмотреть альтернативные объяснения такого недостаточного ответа (см. разделы «Фармакодинамика» и «Особые указания»). Содержание гемоглобина у пациентов подвержено индивидуальным колебаниям, в том числе иногда выше или ниже желаемых целевых значений. При отклонении содержания гемоглобина за пределы целевых значений проводят модификацию дозы, при этом под целевым значением следует рассматривать интервал от 10 г/дл до 12 г/дл. Следует избегать стойкого повышения содержания гемоглобина выше 12 г/дл, указания по модификации дозы при значениях гемоглобина выше 12 г/дл представлены ниже. Также следует избегать повышения содержания гемоглобина более чем на 2 г/дл за 4-х недельный период. В этом случае также необходима коррекция дозы.
Лечение препаратом Аранесп включает две стадии — фаза коррекции и поддерживающая фаза. Рекомендации по применению и дозированию у взрослых и детей в инструкции приводятся отдельно.
Взрослые пациенты с хронической почечной недостаточностью
Фаза коррекции:
Начальная доза при подкожном или внутривенном введении должна составлять 0,45 мкг/кг массы тела при однократном еженедельном введении. Альтернативно, для пациентов, не получающих диализ, следующие начальные дозы препарата также могут назначаться подкожно: 0,75 мкг/кг массы тела каждые две недели или 1,5 мкг/кг массы тела один раз в месяц. Если увеличение содержания гемоглобина недостаточно (менее 1 г/дл в течение 4 недель), необходимо увеличить дозу препарата примерно на 25%. Повышение дозы препарата не должно осуществляться чаще, чем один раз в четыре недели.
Если увеличение содержания гемоглобина превышает 2 г/дл за 4 недели, дозу препарата следует уменьшить примерно на 25%. В случае, когда содержание гемоглобина превышает 12 г/дл, следует рассмотреть возможность уменьшения дозы препарата. Если содержание гемоглобина продолжает увеличиваться, дозу следует снизить примерно на 25%. Если после снижения дозы гемоглобин продолжает повышаться, необходимо временно прекратить применение препарата до начала снижения содержания гемоглобина, после чего можно возобновить терапию, причем дозу препарата следует уменьшить примерно на 25% от предыдущей дозы.
Содержание гемоглобина следует измерять еженедельно или раз в две недели до его стабилизации. В последующем промежутки между измерениями гемоглобина можно увеличить.
Поддерживающая фаза:
Пациентам, находящимся на диализе, можно продолжить вводить Аранесп один раз в неделю или перейти на введение один раз каждые две недели. При переводе пациентов, находящихся на диализе, с еженедельных инъекций препарата Аранесп на режим введения однократно раз в две недели, исходная доза должна вдвое превышать дозу, вводившуюся один раз в неделю.
Для пациентов, не получающих диализа, можно продолжить вводить Аранесп один раз в неделю или один раз каждые две недели или один раз в месяц. Для пациентов, получающих Аранесп один раз каждые две недели, после достижения требуемой концентрации гемоглобина, подкожное введение препарата Аранесп затем может производиться один раз в месяц с использованием исходной дозы, вдвое превышающей предыдущую дозу, вводившуюся раз в две недели.
Титрование дозы с целью поддержания требуемой концентрации гемоглобина следует производить так часто, как это требуется.
Если необходима корректировка дозы для поддержания требуемой концентрации гемоглобина, рекомендуется изменять дозу примерно на 25%.
Если увеличение содержания гемоглобина превышает 2 г/дл за 4 недели, дозу препарата следует уменьшить приблизительно на 25% в зависимости от степени увеличения содержания гемоглобина. В случае, когда содержание гемоглобина превышает 12 г/дл, следует рассмотреть возможность уменьшения дозы препарата. Если содержание гемоглобина продолжает увеличиваться, дозу следует снизить примерно на 25%. Если после снижения дозы гемоглобин продолжает повышаться, необходимо временно прекратить применение препарата до начала снижения содержания гемоглобина, после чего можно возобновить терапию, причем дозу препарата следует уменьшить примерно на 25% от предыдущей дозы.
После любого изменения дозы или режима введения содержание гемоглобина следует контролировать еженедельно или раз в две недели. Изменение дозы во время поддерживающей фазы должно выполняться не чаще одного раза в две недели.
При изменении пути введения следует использовать ту же дозу препарата и контролировать содержание гемоглобина один раз в 1 или 2 недели, чтобы скорректировать дозу при необходимости с целью поддержания требуемого содержания гемоглобина.
Согласно данным клинических исследований, взрослых пациентов, получающих инъекции рчЭпо один, два или три раза в неделю, можно перевести на режим однократного еженедельного введения препарата Аранесп или его введение один раз в две недели. Исходную еженедельную дозу препарата Аранесп (мкг/неделю) определяют, разделив общую еженедельную дозу рчЭпо (МЕ/неделю) на 200. Исходную дозу препарата Аранесп * (мкг/две недели) при режиме введения один раз в две недели определяют путем деления суммарной кумулятивной дозы рчЭпо, введенного за двухнедельный период, на 200. По причине индивидуальных различий для отдельных пациентов требуется подбор оптимальной терапевтической дозы. При замене рчЭпо на Аранесп содержание гемоглобина следует измерять еженедельно или раз в две недели, а способ введения препарата должен оставаться неизменным.
Дети с хронической почечной недостаточностью
Применение препарата у детей в возрасте до 1 года не изучалось в рандомизированных клинических исследованиях (см. раздел «Фармакодинамика»).
Фаза коррекции:
Для детей в возрасте от 1 года и старше начальная доза при подкожном или внутривенном введении препарата составляет 0,45 мкг/кг веса тела в виде однократной инъекции один раз в неделю. У пациентов, не получающих диализ, может применяться начальная доза, равная 0,75 мкг/кг, подкожно один раз в две недели. Если увеличение содержания гемоглобина недостаточно (менее 1 г/дл в течение 4 недель), необходимо увеличить дозу препарата примерно на 25%. Повышение дозы препарата не должно осуществляться чаще, чем один раз в четыре недели.
Если увеличение содержания гемоглобина превышает 2 г/дл за 4 недели, дозу препарата следует уменьшить примерно на 25% в зависимости от степени увеличения содержания гемоглобина. В случае, когда содержание гемоглобина превышает 12 г/дл, следует рассмотреть возможность уменьшения дозы препарата. Если содержание гемоглобина продолжает увеличиваться, дозу следует снизить примерно на 25%. Если после снижения дозы гемоглобин продолжает повышаться, необходимо временно прекратить применение препарата до начала снижения содержания гемоглобина, после чего можно возобновить терапию, причем дозу препарата следует уменьшить примерно на 25% от предыдущей дозы.
Содержание гемоглобина следует измерять еженедельно или раз в две недели до его стабилизации. В последующем промежутки между измерениями гемоглобина можно увеличить.
Лечение анемии препаратом Аранесп в фазе коррекции у детей в режиме дозирования один раз в месяц не изучено.
Поддерживающая фаза:
У детей от 1 года и старше в поддерживающую фазу терапии введение препарата Аранесп можно продолжать в режиме один раз в неделю или один раз в две недели. Пациентам в возрасте до 6 лет может потребоваться применение более высокой дозы для поддержания содержания гемоглобина, чем у пациентов более старшего возраста. При переводе пациентов, находящихся на диализе, с еженедельных инъекций препарата Аранесп на режим введения однократно раз в две недели, исходная доза должна вдвое превышать дозу, вводившуюся один раз в неделю.
Для пациентов в возрасте 11 лет и старше, не находящихся на диализе, после того как достигнуто целевое содержание гемоглобина в режиме дозирования препарата 1 раз в две недели, Аранесп может назначаться подкожно 1 раз в месяц, при этом начальная дозировка должна составлять удвоенную дозу от той, что использовалась в режиме 1 раз в две недели. Клинические данные показали, что пациенты детского возраста, получающие рчЭпо два или три раза в неделю, могут быть переведены на Аранесп, вводимый 1 раз в неделю, и пациенты получающие рчЭпо один раз в неделю могут быть переведены на режим введения Аранеспа один раз в две недели. Начальная дозировка Аранеспа для детей (мкг/нед), вводимого еженедельно может быть определена путем деления суммарной недельной дозы рчЭпо (МЕ/нед) на 240. Начальная дозировка Аранеспа при введении каждые 2 недели (мкг/каждые 2 недели) может быть определена путем деления суммарной дозы рчЭпо за двухнедельный период на 240. По причине индивидуальных различий для отдельных пациентов требуется подбор оптимальной терапевтической дозы. При замене рчЭпо на Аранесп содержание гемоглобина следует измерять еженедельно или раз в две недели, а способ введения препарата должен оставаться неизменным.
Титрование дозы с целью поддержания требуемой концентрации гемоглобина следует производить так часто, как это требуется.
Если необходима корректировка дозы для поддержания требуемой концентрации гемоглобина, рекомендуется изменять дозу примерно на 25%.
Если увеличение содержания гемоглобина превышает 2 г/дл за 4 недели, дозу препарата следует уменьшить примерно на 25% в зависимости от степени увеличения содержания гемоглобина. В случае, когда содержание гемоглобина превышает 12 г/дл, следует рассмотреть возможность уменьшения дозы препарата. Если содержание гемоглобина продолжает увеличиваться, дозу следует снизить примерно на 25%. Если после снижения дозы гемоглобин продолжает повышаться, необходимо временно прекратить применение препарата до начала снижения содержания гемоглобина, после чего можно возобновить терапию, причем дозу препарата следует уменьшить примерно на 25% от предыдущей дозы.
У пациентов, начинающих диализ на фоне терапии препаратом Аранесп, следует тщательно контролировать содержание гемоглобина.
После любого изменения дозы или режима введения содержание гемоглобина следует контролировать еженедельно или раз в две недеди. Изменение дозы во время поддерживающей фазы должно выполняться не чаще одного раза в две недели.
При изменении пути введения препарата следует использовать ту же дозу препарата и контролировать содержание гемоглобина один раз в 1 или 2 недели, чтобы скорректировать дозу при необходимости с целью поддержания требуемого содержания гемоглобина.
Лечение симптоматической анемии, индуцированной химиотерапией, у пациентов с онкологическими заболеваниями
У пациентов с анемией (например, при концентрации гемоглобина равной или ниже 10 г/дл) Аранесп может применяться подкожно для повышения концентрации гемоглобина до уровня не выше 12 г/дл. Симптомы анемии и последствия могут варьироваться в зависимости от возраста пациентов, их пола и тяжести заболевания; в каждом случае необходим анализ индивидуальных клинических данных пациента лечащим врачом. Содержание гемоглобина у пациентов подвержено индивидуальным колебаниям, в том числе иногда выше или ниже желаемых целевых значений. При отклонении содержания гемоглобина за пределы целевых значений проводят модификацию дозы, при этом под целевым значением следует рассматривать интервал от 10 г/дл до 12 г/дл. Следует избегать повышения содержания гемоглобина более 12 г/дл; ниже представлено руководство по коррекции дозы в случае, если содержание гемоглобина превышает 12 г/дл.
Рекомендованная начальная доза препарата — 500 мкг (6,75 мкг/кг) 1 раз в 3 недели либо по 2,25 мкг/кг 1 раз в неделю. Если клинический ответ (утомляемость, содержание гемоглобина) через девять недель неадекватен, дальнейшая терапия может оказаться неэффективной.
Применение препарата Аранесп прекращают примерно через четыре недели после завершения химиотерапии.
После достижения целевого содержания гемоглобина дозировку препарата следует уменьшить на 25-50%, для адекватного контроля симптоматики анемии с использованием минимальных одобренных доз Аранеспа. Возможно титрование дозы между 500 мкг, 300 мкг и 150 мкг.
Следует производить тщательный мониторинг состояния пациентов. Если содержание гемоглобина у пациента превышает 12 г/дл, дозу препарата следует уменьшить на 25-50%. Если содержание гемоглобина превышает 13 г/дл, следует временно прекратить применение препарата Аранесп. После снижения содержания гемоглобина до 12 г/дл или ниже, терапию можно возобновить, дозировка препарата при этом должна быть примерно на 25% меньше предыдущей.
Если увеличение содержания гемоглобина превышает 2 г/дл за 4 недели, дозу препарата следует уменьшить примерно на 25-50%.
Способ введения
Препарат Аранесп может вводиться подкожно самим пациентом или лицом, осуществляющим уход, после обучения лечащим врачом, медицинской сестрой или провизором.
Препарат Аранесп в дозировке 20 мкг, 30 мкг, 500 мкг в лекарственной Форме раствор для инъекций в предварительно заполненном шприце (ПЗШ)
Аранесп может применяться подкожно или внутривенно, как описано в режиме дозирования.
Необходимо менять места введения препарата и вводить препарат медленно, чтобы избежать возникновения дискомфорта в месте инъекции.
Аранесп поставляется готовым для применения в предварительно заполненных шприцах. Инструкции по применению препарата, обращению с ним и порядку его уничтожения приводятся в разделе «Особые указания».
Фармацевтическая несовместимость
Поскольку исследования совместимости еще не проводились, данный медицинский препарат не следует смешивать или вводить методом инфузии вместе с другими лекарственными препаратами.
ТЕХНИКА ПРОЦЕДУРЫ ИНЪЕКЦИИ ПРЕПАРАТА АРАНЕСП В ПРЕДВАРИТЕЛЬНО ЗАПОЛНЕННЫХ ШПРИЦАХ
Этот раздел описывает процедуру инъекции препарата Аранесп, которую вы можете выполнить самостоятельно. Перед началом применения препарата в предварительно заполненных шприцах, пожалуйста, сначала ознакомьтесь с «Общими рекомендациями», приведенными ниже (раздел 1), а затем, с инструкцией (раздел 2).
Раздел 1. Общие рекомендации
Очень важно, чтобы Вы не делали инъекцию сами, пока ваш лечащий врач, медицинская сестра или провизор не научит вас. Если у Вас будут вопросы, то проконсультируйтесь с Вашим врачом, медицинской сестрой или провизором.
Перед началом инъекции
Внимательно прочитайте все рекомендации перед введением препарата.
Как Вам, или тому кто делает вам эту инъекцию, использовать Аранесп ПЗШ?
Ваш врач назначил Вам Аранесп ПЗШ для подкожных инъекций. Ваш лечащий врач, медицинская сестра или провизор расскажет Вам какое количество препарата Аранесп и как часто необходимо вводить.
Оборудование:
Для самостоятельных инъекций вам потребуется:
— Новый ПЗШ с препаратом Аранесп и
— Смоченные спиртом тампоны или сходные материалы.
Перед проведением инъекции
1. Выньте предварительно заполненный шприц из холодильника. Оставить ПЗШ при комнатной температуре примерно на 30 минут. Это позволит сделать инъекцию более комфортной. Не подогревать предварительно заполненный шприц каким-либо другим способом (например, в горячей воде или в микроволновой печи). Не оставлять предварительно заполненный шприц под прямыми солнечными лучами.
2. Не встряхивать предварительно заполненный шприц.
3. Не удалять серый колпачок предварительно заполненного шприца до тех пор, пока Вы не готовы к инъекции.
4. Вы используете тот препарат и дозу, которые Вам назначил лечащий врач.
5. Срок годности на этикетке предварительно заполненного шприца (ГОДЕН ДО). Не использовать ПЗШ, если истек последний день указанного месяца.
6. Описание препарата Аранесп. Раствор должен быть прозрачным, бесцветным или светло-желтым. Если раствор мутный или содержит частицы, препарат использовать нельзя.
7. Тщательно вымыть руки.
8. Выбрать комфортное, хорошо освещенное место и чистую поверхность, удобно расположить все необходимые материалы.
Как выбрать место инъекции?
Лучше всего делать инъекции в верхнюю часть бедра и в живот. Если инъекции Вам делает кто-то другой, можно использовать наружную поверхность плеча.
Если область, куда Вы собрались делать инъекцию, покраснела или отекла, можно выбрать другое место инъекции.
Раздел 2. Рекомендации по введению препарата Аранесп в предварительно заполненном шприце
Как подготовиться к инъекции препаратом Аранесп?
Перед инъекцией препаратом Аранесп Вы должны сделать следующее:
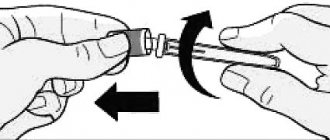
1. Во избежание загиба иглы, осторожно потянуть колпачок с иглы сразу, без скручивания, как показано на рисунках 1 и 2.
2. Не дотрагиваться до иглы и не нажимать на поршень.
3. Вы можете заметить маленькие пузырьки воздуха в предварительно заполненном шприце. Вам не нужно удалять пузырьки воздуха перед инъекцией. Введение раствора с пузырьками воздуха является безопасным.
4. Теперь Вы можете использовать предварительно заполненный шприц.
Как вводить препарат?
1. Продезинфицировать место инъекции с помощью смоченного в спирте тампона, и зажать кожу (не сдавливая) большим и указательным пальцами.
2. Ввести иглу в кожу полностью так, как показывал врач, медицинская сестра или провизор.
3. Ввести назначенную дозу подкожно, как показывал Ваш врач, медицинская сестра или провизор.
4. Медленно и непрерывно надавливать на поршень, при этом сжимать кожную складку и не отпускать ее, пока шприц не опустеет.
5. Извлечь иглу и отпустить складку кожи.
6. Если выступит кровь, аккуратно вытереть ее ватным шариком либо тканью. Не растирать место инъекции. При необходимости, можно заклеить его пластырем.
7. Один предварительно заполненный шприц предназначен для однократного применения. Не использовать оставшийся в шприце препарат Аранесп.
Помните
: При возникновении сложностей, обратитесь за помощью или советом к лечащему врачу или медицинской сестре.
Аранесп
Аранесп
РЛС > Лекарства и субстанции > Аранесп Аранесп (Aranesp) Последняя актуализация описания производителем 12.10.2012 Аранесп 12.10.2012 Действующее вещество: Дарбэпоэтин альфа* (Darbepoetin alfa*) Содержание АТХ B03XA02 Дарбэпоэтин альфа Фармакологическая группа Нозологическая классификация (МКБ-10) Состав Раствор для инъекций 1 предварительно заполненный шприц активное вещество: дарбэпоэтин альфа (рекомбинантный) — 10 мкг (25 мкг/мл); 15 мкг (40 мкг/мл); 20 мкг (40 мкг/мл); 30 мкг (100 мкг/мл); 40 мкг (100 мкг/мл); 50 мкг (100 мкг/мл); 60 мкг (200 мкг/мл); 80 мкг (200 мкг/мл); 100 мкг (200 мкг/мл); 150 мкг (500 мкг/мл); 300 мкг (500 мкг/мл); 500 мкг (500 мкг/мл) вспомогательные вещества в 1 мл раствора: натрия дигидрофосфата моногидрат — 2,118 мг; натрия гидрофосфат — 0,661 мг; натрия хлорид — 8,182 мг; полисорбат 80 — 0,05 мг; вода для инъекций — до 1 мл Описание лекарственной формы Прозрачная, бесцветная жидкость. Характеристика Дарбэпоэтин альфа производится с использованием генной технологии в клетках яичников китайского хомяка (СНО-К1). Фармакологическое действие Фармакологическое действие — гемопоэтическое. Фармакодинамика Дарбэпоэтин альфа стимулирует эритропоэз по тому же механизму, что и эндогенный эритропоэтин. Дарбэпоэтин альфа содержит 5 N-связанных углеводных цепей, в то время как эндогенный гормон и рекомбинантный человеческий эритропоэтин (рчЭПО) имеют всего три цепи. Дополнительные остатки сахаров, с молекулярной точки зрения, не отличаются от таковых, представленных в эндогенном гормоне. Вследствие повышенного содержания углеводов дарбэпоэтин альфа обладает более длительным периодом полувыведения в сравнении с рчЭПО, а следовательно, и большей активностью in vivo. Несмотря на указанные изменения молекулярной структуры, дарбэпоэтин альфа сохраняет очень узкую специфичность к эритропоэтиновому рецептору. Эритропоэтин — фактор роста, который в основном стимулирует образование эритроцитов. Рецепторы к эритропоэтину могут экспрессироваться на поверхности различных опухолевых клеток. Больные с хронической почечной недостаточностью В 2 клинических исследованиях было выявлено, что у пациентов с ХПН риск летального исхода и серьезных сердечно-сосудистых нежелательных явлений выше при применении стимуляторов эритропоэза до более высоких целевых уровней гемоглобина при сравнении с более низкими — 135 г/л (8,4 ммоль/л) против 113 г/л (7,1 ммоль/л); 140 г/л (8,7 ммоль/л) против 100 г/л (6,2 ммоль/л). В рандомизированном, двойном слепом плацебо-контролируемом исследовании (TREAT), 4038 пациентов с ХПН, диабетом типа 2 и уровнем гемоглобина ≤110 г/л, не находящихся на диализе, получали дарбэпоэтин альфа с целью достижения уровня гемоглобина 130 г/л или плацебо (с назначением дарбэпоэтина альфа при снижении уровня гемоглобина ниже 90 г/л). Исследование не достигло основной цели, заключающейся в снижении риска смертности по любым причинам или по сердечно-сосудистой заболеваемости (дарбэпоэтин альфа vs плацебо; соотношение рисков 1,05; 95% ДИ (0,94; 1,17), равно как и цели заключающейся в снижении смертности по любым причинам и прогрессирования до терминальной стадии почечной недостаточности (ТСПН) (дарбэпоэтин альфа vs плацебо; соотношение рисков 1,06; 95% ДИ (0,95; 1,19). Анализ индивидуальных компонентов композитных конечных точек показал следующее соотношение рисков (95% ДИ): летальный исход 1,05 (0,92; 1,21), хроническая сердечная недостаточность (ХСН) 0,89 (0,74; 1,08), инфаркт миокарда (ИМ) 0,96 (0,75; 1,23), инсульт 1,92 (1,38; 2,68), госпитализация в связи с ишемией миокарда 0,84 (0,55; 1,27), ТСПН 1,02 (0,87; 1,18). Онкологические больные, получающие химиотерапию Выживаемость и прогрессирование опухоли были изучены в общей сложности у 2833 пациентов в рамках пяти крупных контролируемых исследований. Из них четыре были двойными слепыми и плацебо-контролируемыми, а одно — открытым. В двух исследованиях включались больные, которым уже было проведено химиотерапевтическое лечение. В двух исследованиях целевой уровень гемоглобина устанавливался равным и выше 130 г/л, а в трех других — в интервале от 120 до 140 г/л. В открытом исследовании не получено различий в показателях общей выживаемости между группой, получавшей лечение рчЭПО, и контрольной. В четырех плацебо-контролируемых исследованиях показатели риска были в пользу группы контроля и находились в пределах от 1,25 до 2,47. В этих четырех исследованиях был выявлен необъяснимый статистически достоверный прирост смертности по сравнению с контролем у больных с типичными видами рака и анемией, лечение которой проводилось рчЭПО. Сравнение частоты тромбозов и других осложнений в группах, получавших лечение рчЭПО, и контрольной, не дает удовлетворительного объяснения причин этого прироста. Также был проведен систематический анализ 57 исследований, включавших суммарно более 9000 онкологических пациентов. При мета-анализе общей выживаемости показатель риска равнялся 1,08 в пользу контроля (ДИ 95%: 0,99–1,18; 8167 пациентов в 42 исследованиях). У пациентов, получавших лечение рчЭПО, отмечалось повышение относительного риска развития тромбоэмболических событий (ОР=1,67; ДИ 95%: 1,35–2,06; 6769 пациентов в 35 исследованиях). Таким образом, существует достаточный объем данных, свидетельствующих о возможности возникновения значительного вреда при лечении онкологических больных рчЭПО. Неясно, до какой степени это применимо к случаям назначения рекомбинантных человеческих эритропоэтинов для достижения целевого уровня гемоглобина менее 130 г/л у пациентов с онкологическими заболеваниями, которые получают химиотерапию, поскольку в проанализированных данных имелось незначительное число пациентов с такими характеристиками. Также был проведен анализ данных более чем у 13900 пациентов со злокачественными заболеваниями (химиотерапия, лучевая терапия, химиотерапия и лучевая терапия или отсутствие терапии), включенных в 53 контролируемых клинических исследования нескольких эпоэтинов. Мета-анализ данных по общей выживаемости выявил соотношение рисков 1,06 в пользу контрольной группы (95% ДИ: 1; 1,12; 53 исследования и 13933 пациента), и для пациентов со злокачественными заболеваниями, получающими химиотерапию, соотношение рисков общей выживаемости составило 1 ,04 (95% ДИ: 0,97; 1,11; 38 исследований и 10441 пациент). Мета-анализ также указывает на значительное повышение относительного риска тромбоэмболических событий у пациентов со злокачественными образованиями, получающих рекомбинантный человеческий эритропоэтин (см. раздел «Особые указания»). Доклинические данные по безопасности Во всех исследованиях на крысах и собаках при применении дарбэпоэтина альфа значимо возрастала концентрация гемоглобина, гематокрита, эритроцитов и ретикулоцитов, что соответствует ожидаемому фармакологическому эффекту. Нежелательные явления при введении очень высоких доз препарата рассматривались как следствие усиленного фармакологического действия (снижение тканевого кровотока вследствие увеличения вязкости крови). Сюда же были отнесены миелофиброзы и гипертрофия селезенки, а также расширение комплекса QRS на ЭКГ у собак, без нарушения сердечного ритма и влияния на интервал QT. Дарбэпоэтин альфа не обладал каким-либо генотоксическим потенциалом и не оказывал влияния на пролиферацию клеток негематологического ряда ни in vitro, ни in vivo. В исследованиях по хронической токсичности не наблюдалось туморогенного или неожиданного митогенного ответа ни в одном изученном типе тканей. В продолжительных исследованиях на животных оценка канцерогенного потенциала дарбэпоэтина альфа не выполнялась. В испытаниях, проводившихся на крысах и кроликах, не наблюдалось клинически значимого влияния на беременность, эмбриональное/фетальное развитие, роды или постнатальное развитие. Уровень проникновения препарата через плаценту был минимальным. Изменений фертильности не отмечалось. Фармакокинетика В связи с повышенным содержанием углеводов концентрация циркулирующего в крови дарбэпоэтина альфа превышает минимальную концентрацию, необходимую для стимуляции эритропоэза в течение более продолжительного времени, в сравнении с эквивалентными дозами рчЭПО, что позволяет снизить частоту введения дарбэпоэтина альфа с сохранением эквивалентного уровня биологического ответа. Больные с хронической почечной недостаточностью Фармакокинетика дарбэпоэтина альфа была изучена у больных с хронической почечной недостаточностью при в/в и п/к введении препарата. Его период полувыведения составлял 21 ч (стандартное отклонение (СО 7,5) при в/в введении. Клиренс дарбэпоэтина альфа составил 1,9 мл/ч/кг (СО 0,56), а объем распределения (Орс) был приблизительно эквивалентен объему плазмы (50 мл/кг). При п/к введении препарата его биодоступность соответствовала 37%. При ежемесячном п/к введении дарбэпоэтина альфа в дозе от 0,6 до 2,1 мкг/кг его период полувыведения составлял 73 ч (СО 24). Более продолжительный период полувыведения дарбэпоэтина альфа при п/к введении, по сравнению с в/в, обусловлен кинетикой абсорбции. В ходе клинических исследований минимальное накопление препарата наблюдалось при любом способе введения. В доклинических исследованиях было продемонстрировано, что почечный клиренс дарбэпоэтина минимален (до 2% общего клиренса) и не оказывает влияния на период полувыведения препарата из сыворотки. Фармакокинетика дарбэпоэтина альфа изучалась у детей (3–16 лет) с ХПН, находящихся или не находящихся на диализе, при этом забор образцов проводился от момента однократного п/к или в/в введения препарата до одной недели (168 ч) после введения. Периоды забора образцов были такой же продолжительности, как и у взрослых с хронической почечной недостаточностью, и сравнение показало, что фармакокинетика дарбэпоэтина альфа у взрослых и детей с хронической почечной недостаточностью похожа. После в/в введения препарата отмечалось приблизительно 25% различие между взрослыми и детьми в отношении площади под фармакокинетической кривой «концентрация-время» от нулевой отметки времени до бесконечности (AUC0-∞); тем не менее, указанное различие для детей составило менее двухкратного диапазона AUC0-∞. После п/к введения препарата величина AUC0-∞ у взрослых и детей была аналогичной. Как после в/в, так и после п/к введения препарата, период полувыведения препарата у детей и взрослых с ХПН был сходен. Онкологические больные, получающие химиотерапию После п/к введения препарата в дозе 2,25 мкг/кг взрослым онкологическим больным средние максимальные концентрации (Cmax) дарбэпоэтина альфа, составляющие 10,6 нг/мл (СО 5,9), устанавливалась в среднем, в течение 91 ч (СО 19,7). Эти параметры соответствовали линейной фармакокинетике в широком диапазоне значений (от 0,5 до 8 мкг/кг при еженедельном введении и от 3 до 9 мкг/кг при введении 1 раз в 2 нед). Фармакокинетические параметры не изменялись при многократном дозировании в течение 12 нед (еженедельное введение или введение раз в две недели). Отмечалось ожидаемое умеренное повышение (<2-кратного) сывороточной концентрации препарата при достижении равновесного состояния, но не было выявлено признаков его накопления при повторном назначении. Исследования фармакокинетики были выполнены с привлечением пациентов с индуцированной во время химиотерапии анемией, которые в комбинации с химиотерапией п/к получали инъекции дарбэпоэтина альфа в дозе 6,75 мкг/кг раз в три недели. В данном исследовании среднее значение (СО) периода полувыведения составляло 74 (СО 27) ч. Данное видео представляет препарат Аранесп. Показания препарата Аранесп лечение симптоматической анемии у взрослых и детей, страдающих хронической почечной недостаточностью (ХПН) ; терапия симптоматической анемии у взрослых онкологических больных с немиелоидными злокачественными новообразованиями, получающих химиотерапию.