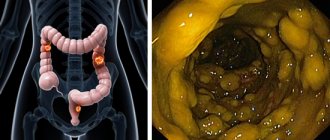
Аутоиммунный гепатит (АИГ) — это хроническое воспалительное заболевание печени, характеризующееся утратой иммунологической толерантности организма к тканевым антигенам [1, 2].
Впервые сведения о тяжелом поражении печени с выраженной желтухой и гиперпротеинемией появились в 30–40‑х гг. XX века. В 1950 г. шведский врач Ян Вальденстрем (Jan Waldenström) наблюдал у 6 молодых женщин хронический гепатит с желтухой, телеангиоэктазиями, повышением СОЭ, гипергаммаглобулинемией. Гепатит хорошо отвечал на лечение кортикотропином [3]. Из-за сходства лабораторных изменений с картиной системной красной волчанки (наличие антинуклеарных антител в сыворотке, положительные результаты LE-теста) одним из названий патологии стал «люпоидный гепатит».
В настоящее время аутоиммунный гепатит определяют как хронический, преимущественно перипортальный гепатит с лимфоцитарно-плазмоцитарной инфильтрацией и ступенчатыми некрозами (рис. 1). Характерные проявления: гипергаммаглобулинемия, появление аутоантител в крови.
Классификация
В зависимости от вида аутоантител выделяют три типа заболевания:
- АИГ 1 типа встречается наиболее часто и характеризуется появлением в крови антинуклеарных антител (АНА, antinuclear antibodies, ANA) и/или антител к гладким мышцам (АГМА, smooth muscle antibodies, SMA).
- При АИГ 2 типа образуются аутоантитела к микросомальным антигенам печени и почек (anti-liver kidney microsomal type-1 antibodies, anti-LKM-1).
- АИГ 3 типа связан с образованием аутоантител к растворимому печеночному антигену, ткани печени и поджелудочной железы (anti-soluble liver antigen/liver-pancreas antibodies, anti-SLA/LP).
- Некоторые авторы объединяют АИГ 1 и АИГ 3 в силу сходства клинико-эпидемиологических особенностей [4].Существуют также перекрестные формы (overlap syndrome) различных аутоиммунных патологий печени, включающие в себя АИГ: АИГ+ПБЦ (первичный билиарный цирроз), АИГ+ПСХ (первичный склерозирующий холангит). Пока не вполне ясно, следует ли считать эти заболевания параллельно текущими самостоятельными нозологиями или частями непрерывного патологического процесса.
В качестве отдельной нозологии рассматривается АИГ, развившийся de novo после трансплантации печени, выполненной по поводу печеночной недостаточности, связанной с другими заболеваниями [1, 5].
Аутоиммунный гепатит встречается повсеместно. Распространенность АИГ в европейских странах — около 170 случаев на 1 млн населения. При этом до 80 % всех случаев составляет АИГ 1 типа. АИГ 2 типа распространен неравномерно — до 4 % в США и до 20 % в Европе.
Болеют преимущественно женщины (соотношение полов среди пациентов в странах Европы составляет 3–4:1). Возраст заболевших — от 1 года до 80 лет, средний возраст — около 40 лет [6].
Причины
Причина возникновения аутоиммунного гепатита (иначе говоря, причина, по которой иммунная система атакует и разрушает здоровые клетки печени) до сих пор не выяснена. Есть предположение, что воспалительно-некротическое поражение печени может быть связано как с дисбалансом эффекторных и регуляторных T-клеток (клеток иммунной системы), так и может возникать в результате неблагоприятного воздействия окружающей среды или из-за генетической предрасположенности.
Без соответствующего лечения заболевание прогрессирует, могут развиваться следующие осложнения: асцит (скопление жидкости в брюшной полости), желудочно-кишечное кровотечение из-за нарушения кровотока в пищеводе и желудке, цирроз печени (и рак печени из-за повышенного риска, связанного с циррозом), почечная недостаточность.
Этиопатогенез
Этиология АИГ неизвестна, однако считается, что на развитие заболевания влияют как генетические факторы, так и факторы окружения.
Важным звеном патогенеза могут быть определенные аллели генов HLA II (человеческий лейкоцитарный антиген типа II, Human leucocyte antigen II) и генов, связанных с регуляцией деятельности иммунной системы [7, 8].
Отдельно стоит сказать об АИГ, входящем в клиническую картину аутоиммунного полиэндокринного синдрома (autoimmune polyendocrine syndrome, autoimmune polyendocrinopathy-candidiasis-ectodermal dystrophy, APECED). Это моногенное заболевание с аутосомно-рецессивным наследованием, связанное с мутацией в гене AIRE1. Таким образом, в данном случае генетическая детерминированность является доказанным фактом [4, 9].
Аутоиммунный процесс при АИГ представляет собой Т-клеточный иммунный ответ, сопровождающийся образованием антител к аутоантигенам и воспалительным повреждением тканей.
Факторы патогенеза АИГ:
- провоспалительные факторы (цитокины), продуцируемые клетками в ходе иммунного ответа. Косвенным подтверждением может служить то, что аутоиммунные заболевания часто бывают сопряжены с бактериальными или вирусными инфекциями;
- угнетение активности регуляторных Т-клеток, играющих важнейшую роль в поддержании толерантности к аутоантигенам;
- нарушение регуляции апоптоза, в норме — механизма, контролирующего иммунный ответ и его «правильность»;
- молекулярная мимикрия — явление, когда иммунный ответ против внешних патогенов может затрагивать и структурно схожие с ними собственные компоненты. Важную роль в этом могут играть вирусные агенты. Так, в нескольких исследованиях было показано наличие пула циркулирующих аутоантител (ANA, SMA, anti-LKM-1) у пациентов, страдающих вирусными гепатитами В и С [2,4];
- фактор токсического лекарственного воздействия на печень. Некоторые исследователи связывают манифестацию АИГ с употреблением противогрибковых препаратов, нестероидных противовоспалительных средств.
Клиника
Примерно у четверти больных АИГ начинается остро, описаны даже редкие случаи развития острой печеночной недостаточности. Острый гепатит с желтухой чаще встречается у детей и молодых людей, у этой же группы чаще отмечается фульминантное течение заболевания [6].
Следует отметить, что у некоторых пациентов с явлениями острого АИГ в отсутствие лечения может наблюдаться спонтанное улучшение состояния и нормализация лабораторных показателей. Однако через несколько месяцев обычно наступает повторный эпизод АИГ. Гистологически также определяется персистирующий воспалительный процесс в печени [6].
Чаще клиника АИГ соответствует клинике хронического гепатита и включает в себя такие симптомы, как астения, тошнота, рвота, боли или дискомфорт в правом верхнем квадранте живота, желтуха, порой сопровождающаяся кожным зудом, артралгии, реже — пальмарная эритема, телеангиэктазии, гепатомегалия [2, 6]. При развившемся циррозе печени могут превалировать симптомы портальной гипертензии, явления энцефалопатии.
АИГ может быть сопряжен с аутоиммунными заболеваниями различных профилей:
- гематологического (тромбоцитопеническая пурпура, аутоиммунная гемолитическая анемия);
- гастроэнтерологического (воспалительные заболевания кишечника);
- ревматологического (ревматоидный артрит, синдром Шегрена, системная склеродермия);
- эндокринного (аутоиммунный тиреоидит, сахарный диабет);
и других профилей (узловая эритема, пролиферативный гломерулонефрит) [1, 2].
Диагностика АИГ
Диагностика аутоиммунного гепатита основывается на:
- результатах исследований: клинического, серологического и иммунологического;
- исключении других заболеваний печени, протекающих с аутоиммунным компонентом или без оного (хронический вирусный гепатит, токсический гепатит, неалкогольный стеатоз, болезнь Вильсона, гемохроматоз, а также криптогенный гепатит).
АИГ 1 и 3 типа схожи по демографическим характеристикам заболевших, профилю HLA, активности воспалительного процесса и ответу на терапию. Существенные отличия имеет АИГ 2 типа, поражающий чаще детей и подростков и обычно имеющий острое начало и более тяжелое течение.
Необходимо помнить о вероятном АИГ у пациентов с повышением уровня печеночных ферментов, а также у пациентов с циррозом печени. При наличии признаков холестаза в круг патологий для проведения дифференциального диагноза следует включить первичный билиарный цирроз и первичный склерозирующий холангит.
Клинический поиск включает в себя определение таких лабораторных показателей, как активность аланинаминотрансферазы и аспартатаминотрансферазы (АЛТ и АСТ), щелочной фосфатазы (ЩФ), уровень альбумина, гамма-глобулина, IgG, билирубина (связанного и несвязанного). Необходимо также определение уровня аутоантител в сыворотке крови и получение данных гистологического исследования [9].
Для больных, у которых в течение 4 лет не удалось достичь ремиссии и приостановить развитие цирроза, метод выбора — трансплантация печени. 10‑летняя выживаемость у пациентов, перенесших эту операцию, достаточно высока (75–85 %), однако и доля рецидивов достигает 11–41 %. Сохранение аутоантител в крови не является признаком рецидива АИГ и не позволяет предсказать его развитие.
Методы визуальной диагностики (УЗИ, КТ, МРТ) не имеют решающего вклада в диагностику АИГ, однако позволяют установить факт прогрессии АИГ и исход в цирроз печени, а также исключить наличие очаговой патологии.В целом диагностика базируется на 4 пунктах [10]:
- Гипергаммаглобулинемия — один из наиболее доступных тестов. Показательно повышение уровня IgG при нормальном уровне IgA и IgM. Однако существуют трудности при работе с пациентами с исходно низким уровнем IgG, а также с пациентами (5–10 %) с нормальным уровнем IgG при АИГ. В целом этот тест считается полезным при мониторинге активности заболевания на фоне лечения [6].
- Наличие аутоантител. При этом антитела типов ANA и SMA не являются специфическим признаком аутоиммунного гепатита, также как и антитела anti-LKM-1, встречающиеся у 1/3 детей и малой части взрослых, страдающих АИГ. Только антитела anti-SLA/LP специфичны для АИГ. Также у пациентов могут определяться антитела к двухцепочечной ДНК.
- Гистологические изменения, оцениваются в комплексе с предыдущими показателями. Не существует строго патогномоничных признаков АИГ, но многие изменения являются весьма типичными. Портальные поля инфильтрированы в разной степени Т-лимфоцитами и плазмоцитами. Воспалительные инфильтраты способны «отсекать» и разрушать отдельные гепатоциты, проникая в паренхиму печени, — данное явление описано как ступенчатый (мелкоочаговый некроз), пограничный гепатит (interface hepatitis). Внутри долек возникает баллонная дегенерация гепатоцитов с их отеком, образованием розеток и некрозом отдельных гепатоцитов — рис. 2. Для фульминантного течения часто характерны центролобулярные некрозы. Также могут наблюдаться мостовидные некрозы, соединяющие соседние перипортальные поля [2, 6].
- Отсутствие маркеров вирусного гепатита.
- Международной группой по исследованию АИГ разработана балльная система для оценки достоверности диагноза — табл. 1.
Лечение аутоиммунного гепатита
АИГ относится к заболеваниям, при которых лечение позволяет существенно повысить выживаемость больных.
Показаниями для начала лечения служат:
- повышение активности АСТ в сыворотке крови в 10 раз по сравнению с нормой или в 5 раз, но в сочетании с двукратным повышением уровня гамма-глобулина;
- наличие мостовидных или мультилобулярных некрозов при гистологическом исследовании;
- выраженная клиника — общие симптомы и симптомы поражения печени.
Менее выраженные отклонения в лабораторных показателях в сочетании с менее выраженной клиникой являются относительным показанием к лечению. При неактивном циррозе печени, наличии признаков портальной гипертензии в отсутствие признаков активного гепатита, при «мягком» гепатите со ступенчатыми некрозами и без клинических проявлений лечение не показано [1, 9].
Общая концепция терапии при АИГ предполагает достижение и поддержание ремиссии. Базовой является иммуносупрессивная терапия — глюкокортикостероиды (преднизолон) в качестве монотерапии или в сочетании с азатиоприном [2, 6, 9, 11]. Терапия продолжается до достижения ремиссии, причем важно достичь именно гистологически подтвержденной ремиссии, которая может отставать от нормализации лабораторных показателей на 6–12 мес. Лабораторная же ремиссия описывается как нормализация уровня АСТ, АЛТ, гамма-глобулина, IgG [2].
Поддерживающую терапию более низкими дозами иммуносупрессантов для снижения вероятности рецидива после достижения ремиссии проводят по крайней мере в течение 2 лет.
Кроме того, обсуждается возможность применения препаратов урсодезоксихолевой кислоты (УДХК)при аутоиммунном гепатите в качестве сопутствующей терапии или даже монотерапии [11]. АИГ у пациентов, получавших препараты УДХК при моно- и комбинированной терапии, характеризовался более мягким течением и ускоренной нормализацией лабораторных показателей.
Симптомы
Симптомы аутоиммунного гепатита различаются от человека к человеку, на ранней стадии могут быть незначительными или возникнуть внезапно.
К симптомам АИГ относятся:
- повышенная утомляемость, усталость;
- дискомфорт и боль в животе;
- кожная сыпь, зуд, образование паутинчатых ангиом;
- желтушность кожных покровов и видимых слизистых оболочек (желтуха);
- боль в суставах;
- моча темного цвета;
- аменорея (прекращение менструаций);
- гепатомегалия;
- спленомегалия.
Ответ на лечение
Результаты лечения преднизолоном и азатиоприном при АИГ могут быть следующими:
- Полный ответ — нормализация лабораторных показателей, которая сохраняется в течение года на фоне поддерживающей терапии. При этом нормализуется и гистологическая картина (за исключением небольших остаточных изменений). О полной эффективности лечения говорят и в тех случаях, когда достоверно уменьшается выраженность клинических маркеров аутоиммунного гепатита, и в течение первых месяцев терапии лабораторные показатели улучшаются по крайней мере на 50 % (а в последующие 6 месяцев не превышают нормальный уровень более чем в 2 раза).
- Частичный ответ — отмечается улучшение клинических симптомов и в течение первых 2 месяцев наблюдается улучшение лабораторных показателей на 50 %. В последующем положительная динамика сохраняется, однако полной или практически полной нормализации лабораторных показателей в течение года не происходит.
- Отсутствие терапевтического эффекта (неэффективность лечения) — улучшение лабораторных показателей менее чем на 50 % в первые 4 недели лечения, причем дальнейшего их снижения (вне зависимости от клинического или гистологического улучшения) не происходит.
- Неблагоприятный исход терапии характеризуется дальнейшим ухудшением течения заболевания (хотя в некоторых случаях и отмечается улучшение лабораторных показателей).
О рецидиве заболевания говорят, когда после достижения полного ответа вновь появляются клинические симптомы и ухудшаются лабораторные показатели.
Обычно терапия дает хороший эффект, однако у 10–15 % больных она не приводит к улучшению, хотя и хорошо переносится. Причинами неэффективности терапии могут служить [6]:
- отсутствие ответа на препарат;
- отсутствие комплаенса и приверженности терапии;
- непереносимость препаратов;
- наличие перекрестных синдромов;
- гепатоцеллюлярная карцинома.
В качестве альтернативных препаратов для лечения аутоиммунного гепатита используют и другие иммуносупрессоры: будесонид, циклоспорин, циклофосфамид, микофенолата мофетил, такролимус, метотрексат [1, 2, 6, 11].
Клинический случай
Девочка восьми лет наблюдалась по поводу кожных высыпаний (эритематозные и нодулярные элементы без какого‑либо отделяемого на нижних конечностях), беспокоящих ее в течение 5–6 мес. Два месяца использовала местные средства от экземы, улучшения не было. Позднее возникли дискомфорт в эпигастральной области, слабость, периодически — тошнота и рвота.
Высыпания локализовались на ногах. При гистологическом исследовании кожного биоптата выявлена инфильтрация подкожной жировой клетчатки лимфоцитами без признаков васкулита. Данные явления были расценены как узловатая эритема.При осмотре выявлена невыраженная гепатоспленомегалия, в остальном соматический статус — без выраженных особенностей, состояние стабильное.
По результатам лабораторных исследований:
- ОАК: лейкоциты — 4,5×109/л; нейтрофилов 39 %, лимфоцитов 55 %; признаки гипохромной микроцитарной анемии (гемоглобин 103 г/л); тромбоциты — 174,000/мкл, СОЭ — 24 мм/ч;
- биохимический анализ крови: креатинин — 0,9 мг/дл (норма 0,3–0,7 мг/дл); билирубин общий — 1,6 мг/дл (норма 0,2–1,2 мг/дл), билирубин прямой – 0,4 мг/дл (норма 0,05–0,2 мг/дл); АСТ — 348 Ед/л (норма — до 40 Ед/л), АЛТ — 555 Ед/л (норма — до 40 Ед/л); щелочная фосфатаза — 395 Ед/л (норма — до 664 Ед/л), лактатдегидрогеназа — 612 Ед/л (норма — до 576 Ед/л).
Показатели системы гемостаза (протромбиновое время, международное нормализованное отношение), уровень общего белка, сывороточного альбумина, гамма-глобулина, уровень ферритина, церулоплазмина, альфа-антитрипсина, гамма-глутамилтранспептидазы — в пределах референсных значений.
В сыворотке крови не выявлены HBs-антиген, антитела к HBs, HBc, антитела к вирусу гепатита А и С. Также отрицательными были тесты на цитомегаловирус, вирус Эпштейна — Барр, токсоплазму, бруцеллу. Титр АСЛ-О в пределах нормы.Данных за сахарный диабет, тиреоидит, болезнь Грейвса, пролиферативный гломерулонефрит — не выявлено.
При УЗИ органов брюшной полости визуализировалась увеличенная печень с измененной эхоструктурой, без признаков портальной гипертензии и асцита. Офтальмологический осмотр не выявил наличия кольца Кайзера — Флейшера.
Титр антител anti-SMA — 1:160, ANA, AMA, anti-LKM-1 антитела не выявлены. Пациентка позитивна по гаплотипам HLA DR3, HLA DR4.
При гистологическом исследовании биоптата печени зафиксированы фиброз, лимфоцитарная инфильтрация, образование розеток гепатоцитов и другие признаки хронического аутоиммунного гепатита.
Пациентке выставлен диагноз «аутоиммунный гепатит 1 типа, ассоциированный с узловатой эритемой», начата терапия преднизолоном и азатиоприном. Счет по шкале IAIHG составлял 19 баллов до начала лечения, что характеризуется как «достоверный АИГ».
Через 4 недели терапии отмечалось купирование общеклинической симптоматики, нормализация лабораторных показателей. Через 3 месяца терапии кожные высыпания полностью регрессировали. Через 6 месяцев после окончания терапии состояние пациентки было удовлетворительным, лабораторные показатели — в пределах референсных значений.
Адаптировано из Kavehmanesh Z. et al. Pediatric Autoimmune Hepatitis in a Patient Who Presented With Erythema Nodosum: A Case Report. Hepatitis monthly, 2012. V. 12. — N. 1. — P. 42–45.
Таким образом, АИГ — это достаточно редкое и относительно хорошо поддающееся лечению заболевание. На фоне внедрения современных протоколов иммуносупрессивной терапии 10‑летняя выживаемость больных достигает 90 %. Менее благоприятен прогноз у больных с аутоиммунным гепатитом 2 типа, особенно у детей и подростков, у которых АИГ прогрессирует гораздо быстрее, а эффективность терапии в целом ниже. Следует помнить и о риске развития гепатоцеллюлярной карциномы (4–7 % в течение 5 лет после установления диагноза цирроза печени).
Список источников
- Вирусные гепатиты и холестатические заболевания / Юджин Р. Шифф, Майкл Ф. Соррел, Уиллис С. Мэддрей; пер. с англ. В. Ю. Халатова; под ред. В. Т. Ивашкина, Е. А. Климовой, И. Г. Никитина, Е. Н. Широковой. — М.: ГЭОТАР-Медиа, 2010.
- Kriese S., Heneghan M. A. Autoimmune hepatitis. Medicine, 2011. V. 39. — N. 10. — P. 580–584.
- Аутоиммунный гепатит и его вариантные формы: классификация, диагностика, клинические проявления и новые возможности лечения: пособие для врачей. Т. Н. Лопаткина. — М. 4ТЕ Арт, 2011.
- Longhia M. S. et al. Aethiopathogenesis of autoimmune hepatitis. Journal of Autoimmunity, 2010. N. 34. — P. 7–14.
- Muratori L. et al. Current topics in autoimmune hepatitis. Digestive and Liver Disease, 2010. N. 42. — P. 757–764.
- Lohse A. W., Mieli-Vergani G. Autoimmune hepatitis. Journal of Hepatology, 2011. V. 55. — N. 1. — P. 171–182.
- Oliveira L. C. et al. Autoimmune hepatitis, HLA and extended haplotypes. Autoimmunity Reviews, 2011. V. 10. — N. 4. — P. 189–193.
- Agarwal, K. et al. Cytotoxic T lymphocyte antigen-4 (CTLA-4) gene polymorphisms and susceptibility to type 1 autoimmunehepatitis. Hepatology, 2000. V. 31. — N. 1. — P. 49–53.
- Manns M. P. et al. Diagnosis and Management of Autoimmune Hepatitis. Hepatology, 2010. V. 51. — N. 6. — P. 2193–2213.
- Lohse A. W., Wiegard C. Diagnostic criteria for autoimmune hepatitis. Best Practice & Research Clinical Gastroenterology, 2011. V. 25. — N. 6. — P. 665–671.
- Strassburg C. P., Manns M. P. Therapy of autoimmune hepatitis. Best Practice & Research Clinical Gastroenterology, 2011. V. 25. — N. 6. — P. 673–687.
- Ohira H., Takahashi A. Current trends in the diagnosis and treatment of autoimmune hepatitis in Japan. Hepatology Research, 2012. V. 42. — N. 2. — P. 131–138.
Возможности эхографии в диагностике аутоиммунного гепатита у детей
УЗИ сканер RS80
Эталон новых стандартов!
Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
Введение
В настоящее время в связи с развитием высокоразрешающей ультразвуковой диагностической аппаратуры значительно повышается интерес к возможностям эхографии в дифференциальной диагностике диффузных болезней печени. В работах ряда авторов [l,2] представлены эхо- и доплерографические критерии оценки печени при вирусных гепатитах и циррозах печени. Однако в России в структуре хронических гепатитов у детей 2% приходится на долю аутоиммунного гепатита, что составляет значительную величину и привлекает активное внимание гепатологов [3].
Аутоиммунный гепатит — прогрессирующее гепатоцеллюлярное воспаление неясной этиологии, характеризующееся наличием перипортального гепатита, гипергаммаглобулинемии, печеночноассоциированных сывороточных аутоантител и положительным ответом на иммуносупрессивную терапию [4]. Девочки и женщины составляют 75% больных [5]. Этиология аутоиммунного гепатита неизвестна, а патогенез изучен недостаточно. В качестве возможных пусковых факторов возникновения заболевания обсуждается роль вирусов Эпштейна-Барр, гепатитов А и С, а также лекарств. Не исключается возможность возникновения аутоиммунного гепатита вследствие первично обусловленного нарушения иммунного ответа, когда появление «запрещенных клонов» аутореактивных клеток происходит без воздействия триггерных факторов [6]. Обязательным для постановки диагноза аутоиммунного гепатита является наличие аутоантител в сыворотке крови: антинуклеарных (ANA), и/или антигладкомышечных (SМА) антител при аутоиммунном гепатите I типа; аутоантител к микросомам печени и почек (anti-LKM I) при аутоиммунном гепатите II типа, гипергаммаглобулинемии, а также отсутствие признаков вирусных и метаболических болезней печени [7]. В исходе аутоиммунного гепатита не редко формируется цирроз печени в относительно короткие сроки после первой манифестации процесса. У детей цирроз печени встречается в 74% при аутоиммунном гепатите I типа и в 44% случаев при аутоиммунном гепатите II типа [5]. У взрослых ситуация об ратная: при аутоиммунном гепатите II типа чаще развивается цирроз печени, чем при аутоиммунном гепатите I типа (82% против 43%, со ответственно) [6].
Учитывая актуальность проблемы и отсутствие в доступной литературе данных о возможностях ультразвуковой диагностики в распознавании аутоиммунного гепатита, целью работы явилось определение эхографических изменений печени при аутоиммунном гепатите у детей.
Материалы и методы
Наблюдались 36 детей (31 девочка и 5 мальчиков) в возрасте от 7 до 15 лет с диагнозом аутоиммунный гепатит. Средняя продолжительность наблюдения 31,4±19,8 месяцев. К моменту поступления продолжительность заболевания была от 1 месяца до 8 лет.
Всем детям проводили лабораторное об следование, включающее общий анализ крови, биохимический анализ крови, определение содержания иммуноглобулинов (Ig) классов А, М, G, маркеров вирусных гепатитов А, В, С (anti-HAV IgM, HbsAg, anti-HBc, anti-HBe, anti-HBs, anti-HCV) методом ИФА, ДНК вируса гепатита В и РНК вируса гепатита С методом полимеразной цепной реакции (ПЦР). Были выявлены нарушения пигментного обмена, признаки цитолиза и изменений иммунологической активности. У 33 пациентов (91,7%) диагностирован аутоиммунный гепатит I типа, характеризующийся наличием ANA и SMA, но отсутствием anti-LKM I в сыворотке крови и у 3 (8,3%) детей — аутоиммунный гепатит II типа.
Пункционная биопсия печени проведена у 27 из 36 больных. Морфологическое исследование ткани печени свидетельствовало о наличии хронического гепатита у 8 больных; признаки цирроза печени были выявлены у 19 больных. У 9 больных в связи с отказом от проведения пункционной биопсии печени формирование цирроза печени было установлено на основании клинико-лабораторных данных. Таким образом, у 28 из 36 детей с аутоиммунным гепатитом был цирроз печени. Эндоскопическое исследование при поступлении в клинику выявило варикозное расширение вен пищевода 12 степени у 19 пациентов с циррозом печени и еще у 6 больных через 1-1,5 года с момента начала наблюдения.
Контрольную группу составили 25 здоровых сверстников. В качестве группы сравнения обследовано 56 детей с вирусным гепатитом В и 42 ребенка с вирусным гепатитом С в возрасте от 7 до 15 лет. Всем проводили ультразвуковое исследование органов брюшной полости и забрюшинного пространства. Использовались датчики частотой 3,5-5,0 МГц. Выполнялась обще принятая методика эхографической оценки печени и кровотока в цветовом и импульсном режимах. Исследование печени включало измерение левой доли (переднезадний, медиально-латеральный и верхненижний размеры), правой доли (верхненижний размер).
Доплерографическое исследование сосудов портальной системы и чревного ствола проводилось по воротной вене — в области ствола, по печеночным и селезеночным артериям — в месте их выхода из чревного ствола, по селезеночной вене — в области ворот селезенки, по средней печеночной вене — отступая 2-3 см от места ее впадения в нижнюю полую вену. Основными критериями оценки кровотока являлись показатели объемного кровотока, индекса резистентности по артериям и пульсового индекса по печеночной вене. Полученные результаты обрабатывались статистически по общепринятым методикам вариационнй статистики. Достоверность различий изучаемых показателей определяли по критерию Стьюдента.
Результаты исследований
У всех детей с аутоиммунным гепатитом на стадии хронического гепатита наблюдалось диффузное увеличение печени. Четкой зависимости от активности процесса или давности заболевания не прослеживалось. Увеличение правой доли составило в среднем 20%, а левой доли — 8% по верхненижнему и 20% по медиально-латеральному размерам по сравнению с нормальными возрастными показателями. Контур печени был ровный, но с выраженной дольчатостью. Углы долей соответствовали нормальному контуру печени. Отмечалась гиперэхогенность паренхимы. Неоднородность ее была обусловлена гипер- и гипоэхогенными участками сред них размеров (3-5 мм), гиперэхогенной тяжистостью по ходу ветвей воротной вены, что создавало впечатление сетчатости печеночного рисунка (рис. 1 а). Визуализировались единичные печеночные вены с небольшой протяженностью от места впадения в нижнюю подую вену, тонкие, горизонтально направленные, с ровным контуром (косой срез печени). Ослабления ультразвука не наблюдалось, и паренхима печени хорошо прослеживалась до заднего контура. Диаметр ствола воротной вены оставался в пределах допустимых значений. Имела место гиперэхогенность стенок как ствола, так и мелких ветвей воротной вены. У одного ребенка определялось не большое раскрытие пупочной вены (до 2 мм) без признаков кровотока в ней.
Рис. 1.
Эхограммы печени при аутоиммунном гепатите на разных стадиях.
а)
При хроническом гепатите.
б)
При циррозе печени.
в)
При вирусном гепатите С.
Изменений размеров селезенки, ее паренхимы и ствола селезеночной вены не наблюдалось. Эхографических признаков портальной гипертензии в этой группе больных выявлено не было.
По данным доплерографии (таблица 1) отмечалось увеличение объемного кровотока по воротной вене за счет повышения его скорости. Диаметр сосуда был в пределах нор мы. Определялся двухфазный кровоток по средней печеночной вене в отличие от трех фазного у здоровых детей. У 2-х пациентов имел место линейный характер доплеровской кривой. Наблюдалась тенденция к увеличению индекса резистентности кровотока по печеночной артерии. Кровоток по сосудам селезенки практически не отличался от такового у детей из контрольной группы.
Таблица 1.
Показатели гемодинамики портального кровотока у детей с аутоиммунным гепатитом (М±m).
| Сосуд | Контрольная группа (n = 25) | Аутоиммунный гепатит | ||||
Хронический гепатит (n =  | Цирроз печени (n = 28) | |||||
| Q | IR | Q | IR | Q | IR | |
| Воротная вена | 0,47±0,02 | 0,59±0,03* | 0,76±0,05* | |||
| Печеночная артерия | 0,73±0,03 | 0,78±0,04 | 0,81±0,06* | |||
| Селезеночная вена | 0,39±0,02 | 0,41±0,05 | 0,50±0,02* | |||
| Селезеночная артерия | 0,59±0,02 | 0,70±0,04 | 0,75±0,04* | |||
Q — объемный кровоток в л/мин; IR — индекс резистентности. * Достоверные различия по сравнению с контрольной группой (р
При УЗИ пациентов с циррозом печени в исходе аутоиммунного гепатита было выявлено увеличение правой доли на 30-40%, левой доли на 10-20% по верхненижнему и на 40% по медиально-латеральному размерам по сравнению с возрастной нормой, и оставалось таковым до появления признаков декомпенсации процесса. У поло вины детей контур печени был неровный или явно бугристый; углы закруглены. Отмечалось повышение эхогенности паренхимы. Эхоструктура печени была неоднородной за счет узлов различных размеров и количеств, с четким контуром, однородных по структуре, чаще изоэхогенных, реже — умеренно гипоэхогенных без четкой локализации. Так же наблюдались так называемые «радиальные расщелины», которые визуализировались как гипоэхогенные тяжи по всей паренхиме печени, вертикально направленные с неровным контуром (рис. 1б). У 18% больных отмечалось ослабление ультразвука на 1/4-1/3 по переднезаднему размеру. Сосудистый рисунок был обеднен. Визуализировались единичные печеночные вены, вертикально направленные, с извитым контуром. На первый план выступали ультразвуковые признаки портальной гипертензии. Ствол воротной вены был расширен до 10-14 мм. Отмечались гиперэхогенные тяжи по ходу ствола воротной вены и ее расширенных ветвей, а также по ходу межсегментарных перегородок. Имелись множественные дополни тельные ветви воротной вены, реканализация пупочной вены с кровотоком по ней. Селезенка была значительно увеличена: у 13 детей на 15%, у 10 детей на 20-25% и 5 детей на 30-40% по сравнению с возрастной нормой. Паренхима ее была неоднородной, гиперэхогенной со множеством внутриорганных ветвей и анастомозов между селезеночной артерией и веной в области ворот. Ствол селезеночной вены был расширен до 8-14 мм и извит.
При доплерографическом исследовании отмечалось снижение скорости кровотока по воротной и селезеночной венам. Однако за счет значительного расширения диаметра этих сосудов объемный кровоток был увеличен. Индекс резистентности по печеночной и селезеночной артериям повышался (см. табл.). У всех больных с циррозом печени определялся линейный характер кровотока по средней печеночной вене.
У больных с аутоиммунным гепатитом с одинаковой частотой как при хроническом гепатите, так и при циррозе печени выявлялись различные деформации желчного пузыря (перегибы в области дна или тела) и увеличение его размеров. Уплотнение или небольшое утолщение стенок пузыря (до 2 мм) было характерно для пациентов с хроническим гепатитом, тогда как при циррозе печени чаще имело место более значительное их утолщение до (2-4 мм). У 9 детей определялся варикоз сосудов стенок желчного пузыря (один из признаков портальной гипертензии), что сочеталось с варикозным расширением вен пищевода и васкулопатией слизистой желудка по данным эндоскопического исследования.
Изменения поджелудочной железы чаще носили характер реактивных изменений, что проявлялось либо диффузным увеличением всей железы, либо увеличением какого-либо ее отдела (головки или хвоста), без изменений паренхимы. При этом отмечались множественные линейные параллельные гиперэхогенные сигналы, чаще в области хвоста или головки железы, что расценивалось как уплотнение стенок сосудов. Вирсунгов проток визуализировался в основном в области тела железы и был в пределах нормальных возрастных значений (1-2 мм). У 8 детей (28%) с циррозом печени диффузное увеличение поджелудочной железы сочеталось со снижением эхогенности ее паренхимы, то есть имели место ультразвуковые признаки панкреатита.
При поступлении в клинику всем детям назначали иммуносупрессивную терапию (преднизолон и азатиоприн). Повторные УЗИ показали, что в основном на фоне терапии отмечалось небольшое уменьшение размеров как печени, так и селезенки, а также диаметров стволов воротной и селезеночной вен. Структура и эхогенность паренхимы печени не менялись. Наблюдалась тенденция к снижению объемного кровотока по воротной вене и уменьшению индекса резистентности по печеночной артерии.
У 9 детей с циррозом печени в исходе аутоиммунного гепатита выявлялись признаки декомпенсации процесса (выраженная портальная гипертензия, угроза кровотечения из варикозно расширенных вен пищевода, печеночная энцефалопатия), что обусловило необходимость постановки вопроса о проведении у них операции ортотопической трансплантации печени.
Обсуждение
С УЗИ часто начинается обследование ребенка при подозрении на заболевание печени, поэтому встает вопрос о первичной дифференциальной диагностике болезней печени. Гиперэхогенность и неоднородность ее паренхимы при отсутствии признаков портальной гипертензии выстраивают дифференциальный ряд, на первом месте в котором стоят вирусные и затем метаболические болезни печени.
Эхографическая картина паренхимы печени у больных с аутоиммунным гепатитом на стадии хронического гепатита характеризовалась неоднородностью за счет гипер- и гипоэхогенных участков средних размеров, гиперэхогенной тяжистостью по ходу ветвей воротной вены и обеднением сосудистого рисунка. Такая картина отличалась от мелкодиффузной неоднородной паренхимы печени, наблюдаемой при гепатитах В и С в группе сравнения. Различия выявлялись также в характеристике сосудистого русла: обилие печеночных вен с ровным контуром, горизонтально направленных, прослеживающихся по всему срезу паренхимы печени. Не было ярко выраженной гиперэхогенной тяжистости по ходу ветвей воротной вены (рис. 1в), Иногда отмечались параллельные линейные средней эхогенности сигналы по ходу мелких ветвей воротной вены, но, как правило, это сочеталось с увеличением желчного пузыря, его деформациями и снижением сократительной функции. Совокупность этих признаков расценивалась как дискинезия желчевыводящих путей с явлениями холестаза.
В области ворот печени у 80% пациентов с вирусным гепатитом В и С визуализировались один или два лимфоузла овальной формы с четким, ровным контуром, гипоэхогенные и однородные по структуре. Раз мер их был в пределах 8 х 5 — 10 х 5 мм. Данный признак ни разу не был зафиксирован при аутоиммунном гепатите.
Каких-либо достоверных различий в показателях гемодинамики портального кровотока у пациентов с вирусным гепатитом и аутоиммунным гепатитом выявлено не было. Отмечалась лишь тенденция к увеличению индекса резистентности по печеночной артерии у детей с аутоиммунным гепатитом.
Таким образом, при комплексном УЗИ печени у детей с аутоиммунным гепатитом выявляются характерные диагностические признаки, которые мо гут быть использованы в дифференциальной диагностике с другими диффузными заболеваниями печени.
Литература
- Аббас Н.М. Состояние центральной и периферической гемодинамики у детей с хроническими заболеваниями печени: Дис. …канд. мед. наук. М., 1996. 160 с.
- Митьков В.В. Количественная ультразвуковая оценка чревной гемодинамики при неопухолевых заболеваниях гепатобилипанкреатической зоны: Дис. … д-ра мед. наук. M., 2001. 278 c.
- Terminology of Chronic Hepatitis. International Working Party Report //Am. J. Gastroenterol. 1995. Vol. 90, N 2. Р. 181-189.
- Нисевич Н.И., Учайкин В.Ф. Эволюция инфекционных болезней детей в XX веке и проблемы ХХI / Медицинский форум. 1999. N 1 (13). C. 17-20.
- Autoimmune hepatitis in childhood: 20-Year Experience / G.V.Gregorio, B. Portmann, F. Reid et al. // Hepatology. 1997. Vol. 25. P. 541547.
- Czaja A.J. Autoimmune hepatitis. Evolving concepts and treatment strategies // Dig. Dis. Sci. 1995. Vol. 40. Р.435-456.
- International Autoimmune Hepatitis Group Report: review of criteria for diagnosis of autoimmune hepatitis // Hepatol. 1999. Vol. 31. P. 929-938.
УЗИ сканер RS80
Эталон новых стандартов!
Беспрецедентная четкость, разрешение, сверхбыстрая обработка данных, а также исчерпывающий набор современных ультразвуковых технологий для решения самых сложных задач диагностики.
« предыдущая статья
следующая статья »