Этанол (этиловый спирт, винный спирт) — органическое соединение, представитель ряда одноатомных спиртов состава С 2 Н5 ОН (сокращенно EtOH). При обычных условиях представляет собой бесцветную, легковоспламеняющейся жидкостью. Согласно Национального стандарта Украины ДСТУ 4221: 2003 этанол — это токсичное вещество наркотическим действием, по степени воздействия на организм человека относится к четвертому классу опасных веществ. Обладает канцерогенными свойствами.
Этанол является главным действующим составляющей спиртных напитков, которые обычно изготавливаются ферментацией углеводов. Для промышленных нужд этиловый спирт часто синтезируют с нефтяной и газовой сырья каталитической гидратацией этилена. Кроме изготовления пищевых продуктов этанол применяется в большом количестве в качестве горючего, растворителя, антисептика и как сырье для получения других промышленно важных веществ.
История
Этанол использовался человечеством еще с древних времен. Он играл роль составной части напитков, лекарств, как успокоительное и афродизиак, а также имел место в проведении религиозных обрядов.
В Древнем Египте его добывали ферментацией растительного сырья. Таким способом получали только разбавленный раствор спирта. С целью увеличения концентрации в Китае изобрели способ перегонки. Как свидетельствуют росписи на китайской керамике, напитки из ферментированной смеси риса, фруктов и меда изготавливали еще 9000 назад. Примерно в это же время на Ближнем Востоке спирт получали из винограда и ячменя, о чем свидетельствуют записи на глиняных табличка в Междуречье.
В Средневековье этиловый спирт играл роль основы для приготовления многочисленных лекарств и настоек. Алхимики всегда использовали этанол в своих работах, дав ему название лат. Aqua vitae, то есть живая вода.
Чистый этанол впервые получил в 1796 году российско-немецкий химик Товий Егорович Ловиц. Согласно описанию ведущего ученого того времени Антуана Лорана Лавуазье, исследуемая соединение состояла из химических элементов углерода, водорода и кислорода. В 1808 году швейцарский биохимик Николя Теодор де Соссюр установил химическую формулу этанола, а пятьдесят лет спустя шотландский химик Арчибальд Скотт Купер предложил его структуру.
Первый синтетический метод получения этилена разработали независимо друг от друга английский химик Генри Геннель и французский фармацевт Жорж-Симон Серюлла в 1826 году. А в 1828 английский физик и химик Майкл Фарадей получил этанол путем каталитической гидратации этен, побочного продукта переработки нефти и газа. Этот способ лег в основу многих методов, которые применяются в производстве этанола и по сей день.
Примеры решения задач
ПРИМЕР 1
| Задание | Определите простейшую формулу соединения калия с марганцем и кислородом, если массовая доля калия равна 24,7%, марганца 34,8%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: ω (Х) = n × Ar (X) / M (HX) × 100%. Вычислим массовую долю кислорода в соединении: ω (P) = 100% — ω(K) — ω(Mn)= 100% — 24,7% — 34,8% = 40,5%. Обозначим количество моль элементов, входящих в состав соединения за «х» (калий), «у» (марганец) и «z» (кислород). Тогда, мольное отношение будет выглядеть следующим образом (значения относительных атомных масс, взятых из Периодической таблицы Д.И. Менделеева, округлим до целых чисел): x:y:z = ω(K)/Ar(K) : ω(Mn)/Ar(Mn) : ω(O)/Ar(O); x:y:z= 24,7/39 : 34,8/55 : 40,5/16; x:y:z= 0,63 : 0,63:2,53 = 1 : 1: 4. Значит формула соединения калия, марганца и кислорода будет иметь вид KMnO4. Это перманганат калия. |
| Ответ | KMnO4 |
ПРИМЕР 2
| Задание | Выведите простейшую формулу соединения, в котором массовая доля фосфора составляет 43,66%, а массовая доля кислорода – 56,34%. |
| Решение | Массовая доля элемента Х в молекуле состава НХ рассчитывается по следующей формуле: ω (Х) = n × Ar (X) / M (HX) × 100%. Обозначим число атомов фосфора в молекуле через «х», а число атомов кислорода через «у» Найдем соответствующие относительные атомные массы элементов фосфора и кислорода (значения относительных атомных масс, взятые из Периодической таблицы Д.И. Менделеева, округлим до целых чисел). Ar(P) = 31; Ar(O) = 16. Процентное содержание элементов разделим на соответствующие относительные атомные массы. Таким образом мы найдем соотношения между числом атомов в молекуле соединения: x:y = ω(P)/Ar(P) : ω (O)/Ar(O); x:y = 43,66/31 : 56,34/16; x:y: = 1,4 : 3,5 = 1 : 2,5 = 2 : 5. Значит простейшая формула соединения фосфора и кислорода имеет вид P2O5. Это оксид фосфора (V). |
| Ответ | P2O5 |
структура
Оба атома углерода в молекуле этанола, в том числе и атом, который связан с гидроксильной группой, находятся в состоянии sp 3 -гибридизации. Расстояние C-C составляет 1,512 ангстрем.
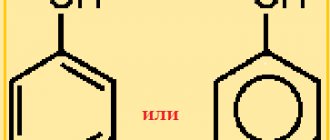
В зависимости от положения гидроксильной группы по отношению к другой части молекулы, различают гош — (фр. Gauche) и транс-формы.Транс-форма характеризуется положением связи O-H гидроксильной группы в одной плоскости со связью C-C и одним из C-H связей. В гош -форме атом водорода в гидроксильной группе обращен в сторону. Дипольный момент для гош-формы составляет 1,68 D, а для транс-формы — 1,44 D.
Этиловый спирт детям
Абсолютных противопоказаний к использованию у детей данного раствора не имеется. Однако будьте внимательны, спирт имеет системное отравляющее действие, особенно ярко проявляющееся у детей. Потому даже при наружном применении не увлекайтесь растирками и примочками.
Есть часть настоек и препаратов, основанных на спирте, которые в некоторых случаях разрешены для приема детям. Будьте внимательны и осторожны, внимательно читайте состав препарата и инструкцию к применению
Обращайте внимание на состояние и поведение своего ребенка. Использование подобных средств, а особенно в повышенной дозировке, могут вызвать серьезные симптомы алкогольного отравления у ребенка
Распространение в природе
Этанол является продуктом жизнедеятельности некоторых грибов. Среди них основными являются рода Saccharomyces, Schizosaccharomyces, а также Kluyveromyces. Одним из наиболее известных представителей этих классов является вид Saccharomyces cerevisiae, который имеет тривиальное название пивные дрожжи. К другим распространенным видам относятся Saccharomyces pastorianus, Saccharomyces anamensis, Schizosaccharomyces pombe, Candida utilis тому подобное. Также этанол образуют некоторые бактерии, например, Zymomonas mobilis.
В 1975 году астрономы сообщили о нахождении значительных скоплений этанола в газо-пылевом облаке Стрелец B2. По подсчетам ученых количество имеющихся там молекул этанола значительно превышает количество спирта, полученного за всю историю человечества. Найденный этанол имел транс-форму молекул, а в 1996 году он был зафиксирован и в гош -форме.
Среди возможных путей образования этанола в межзвездной среде приводится, в частности, его синтез из метана и метил-катиона под действием излучения:
Другим потенциальным способом является взаимодействие метил-катиона с формальдегидом, который также распространен в космосе:
Вред и польза алкоголя
Давайте не будем трогать этот огромный айсберг под названием «пить или не пить». Вспомним слова всеми любимого Семена Семеновича Горбункова о пользе алкоголя. Алкоголь способен незначительно предотвратить формирование тромбов, снизить содержание в крови холестерина, расширить сосуды, что приведет к более интенсивному кровообращению. А лекарство, как известно, любит четкую дозировку, поэтому 50 мл лечит и бодрит. Но польза, которую приносит алкоголь, слишком мала по сравнению с его вредом: алкоголь вносит изменения в генетическую структуру человека, что может привести к отклонениям в умственном развитии потомков, оказывает пагубное действие на нравственное поведение человека. При этом стоит вспомнить, что именно алкоголь побуждает человека совершать необдуманные, глупые и жестокие поступки. Чтобы такого не случилось, следует четко соблюдать норму. Полезным будет и полный отказ от разнообразных алкогольных напитков.
Помните, что если вы превысите норму, то алкоголь станет ядом, который нанесет вред органам и даже целым системам вашего организма.
Собственно на этом и можно закончить рассуждение о том, как отличить метиловый от этилового спирта.
fb.ru
физические свойства
Этанол — бесцветная жидкость со слабым «алкогольным» запахом. Он летучим и легковоспламеняющимся. Смешивается в любых пропорциях с водой, эфирами, ацетоном, бензол. Этиловый спирт является хорошим растворителем для многих органических, а также неорганических веществ.
С водой образует азеотропную смесь: 95,6% спирта и 4,4% воды. Безводный этанол незначительно гигроскопичен: для достижения стабильности он способен поглотить 0,3-0,4% воды.
Вязкость этанола, мПа * с
| -25 °C | 0 °C | 25 °C | 50 °C | 75 °C |
| 3,262 | 1,786 | 1,074 | 0,694 | 0,476 |
Примечания
- Статья «Абсолютный спирт» в БСЭ.
- Фармацевтический справочник Химик.ру
- Большая Советская Энциклопедия, статья «Этиловый спирт»
- БСЭ, статья «Алкоголизм»
- Средства, влияющие на ЦНС
- E1510 — спирт этиловый
- Постановление Правительства Российской Федерации от 29 декабря 2007 г. N 964 г. Москва «Об утверждении списков сильнодействующих и ядовитых веществ для целей статьи 234 и других статей Уголовного кодекса Российской Федерации, а также крупного размера сильнодействующих веществ для целей статьи 234 Уголовного кодекса Российской Федерации»
- Статья 26 Федерального закона от 22.11.1995 N 171-ФЗ (ред. от 05.04.2010) (Консультант+)
получение
гидратация этилена
Для получения этанола из этилена есть два основных пути. Исторически первым стал метод непрямой гидратации, изобретенный в 1930 году . Другой, разработанный в 1970-х годах, был спроектирован как бескислотный метод (отказ от использования серной кислоты).
косвенная гидратация
Получение этанола из этилена с использованием серной кислоты происходит в три стадии. Сначала этилен поглощается концентрированной кислотой, образуя эфиры етилсульфат или диэтил сульфат:
Поглощение проводится 95-98% раствором кислоты при температуре 80 ° C и давлении 1,3-1,5 МПа. Данное взаимодействие экзотермической, поэтому стенки реактора должны иметь охлаждения. Присутствие в растворе кислоты етилсульфату позволяет существенно увеличить скорость поглощения, поскольку растворимость этилена в етилсульфати значительно выше, чем в чистой кислоте.
На второй стадии полученные продукты реакции испытывают гидролиза и разлагаются с образованием спирта и кислоты. Однако выключенной является взаимодействие двух базовых эфиров, которая ведет к образованию третьего, диэтилового:
После обработки серной кислоты с абсорбированы этил- и диэтилсульфат в достаточном количестве воды, раствор приобретает концентрации около 50-60%. Продукты гидролиза направляются на колонны для разделения: разведенная кислота оставаться внизу резервуара, а газовать спиртово-Этерна смесь — наверху. Целевую смесь промывают водой или разбавленным раствором гидроксида натрия, а затем очищают перегонкой.
Заключительным этапом является восстановление концентрации разбавленной кислоты. Этот этап является одним из самых дорогостоящих во всем синтезе. С помощью системы кислотных испарителей удается поднять концентрацию кислоты до 90%. Увеличение этого показателя до необходимых 98% проводится смешиванием с олеумом (концентрации 103%).
Серьезной проблемой для метода непрямой гидратации является образование в кислоте углеродистых веществ, которые оказывают существенное влияние на ее концентрацию. Использование концентрированной кислоты также вызывает появление коррозии на оборудовании, поэтому некоторые части оборудования производятся из кремния, сплавов тантала, свинца и т.
прямая гидратация
Синтез по схеме прямой гидратации проводится с использованием катализаторов. Здесь существует две формы взаимодействия:
- с твердым или жидким катализатором контактируют газообразные реагенты (газофазной процесс)
- с твердым или жидким катализатором контактируют как жидкие, так и газообразные реагенты (змишанофазний процесс).
Этанол синтезируют преимущественно за газофазным процессом. Выходной этилен и воду пропускают над угольным катализатором, насыщенный ортофосфорная кислота:
При обычных температурах лишь незначительное количество этанола может находиться в газовой фазе, а увеличение температуры приведет к уменьшению его концентрации. Выровнять равновесие реакции можно, применив принцип Ле Шателье — Брауна, — увеличив давление в реакционной смеси и уменьшив количество молекул в системе. Оптимальными условиями для проведения взаимодействия является темепратура 250-300 ° C и давление 6,1-7,1 МПа.
Продукт реакции может подвергаться межмолекулярного дегидратации, что ведет к образованию диэтилового эфира:
В случае, если в углеводном сырье содержится примесь ацетилена, она гидратируется к этаналя:
Присутствие этаналя нежелательна, поскольку из него образуется кротоновой альдегид, который негативно влияет на качество этанола, даже в количестве миллионных частей:
получение ферментацией
Добыча этанола путем ферментации (брожения) сахаристых веществ является старейшим. Для его производства может применяться любой продукт, содержащий сахар или вещества, из которых его можно получить (например, крахмал). В качестве сахаросодержащих продуктов используют фруктовый и тростниковый сахар, сахарную свеклу, патоку, а крахмалосодержащие является картофель, зерна пшеницы, ржи, кукурузы. Также используется в качестве сырья целлюлоза (из отходов сельского хозяйства, целлюлозно-бумажной промышленности и т.п.).
Извлечения из крахмала и сахара
Для превращения крахмала в сахаристые вещества его сначала подвергают гидролизу. С этой целью сырье (растертую картофель или муку) заваривают горячей водой, чтобы ускорить набухание крахмала. Также к сырью добавляют фермент, под воздействием которого происходит оцукровування крахмала, то есть превращение его в глюкозу.
В качестве фермента используют диастаза, содержащаяся в проросших зернах, или другие амилазы грибкового происхождения.
Вторая стадия, которое аналогична и для получения спирта из сахаров, заключается в анаэробном брожении, то есть превращении в спирт и диоксид углерода:
Здесь реакция происходит под действием микроорганизмов: грибов (дрожжей) или бактерий.
Сравнение характеристик некоторых представителей бактерий и дрожжей
| характеристика | Zymomonas mobilis | Saccharomyces carlsbergensis |
| Время удвоения количества, ч | 2,51 | 5,64 |
| Производство этанола, г / (г · ч) | 5,44 | 0,82 |
| Выход продукта, г / г | 0,465 | 0,460 |
Среди применяемых в процессе дрожжей действующее место занимают Saccharomyces cerevisiae (так называемые пивные дрожжи). При их использования важное значение имеют кислотность среды и температура — они влияют на рост дрожжей, выход этанола, формирование побочных продуктов и загрязнения бактериями. Обычно такое брожение в промышленном производстве проводится по pH 4-6. При значении pH менее 5 рост бактерий в среде сильно подавлен; для роста дрожжей Saccharomyces cerevisiae кислотность должна поддерживаться в промежутке 2,4-8,6 с оптимальным значением 4,5, а процесс брожения имеет большую интенсивность в диапазоне 3,5-6.
Большинство дрожжей, используемых в производстве этанола, имеют оптимальную температуру для роста около 39-40 ° C, а максимальное значение наблюдается в виду Kluyveromyces marxianus — 49 ° C. Поскольку процесс брожения является экзотермическим (с 1 г поглощенной глюкозы выделяется 586 Дж тепла), использование дрожжей с высшим оптимальной температурой роста позволяет сэкономить средства на охлаждении реакционной системы. Важным моментом является подача незначительных количеств кислорода для синтеза дрожжами ненасыщенных жирных кислот и эргостерола, которые способствуют их росту и хорошей проницаемости клеток. При отсутствии кислорода нехватка кислот и стерола повлечет изменения в физиологии дрожжей уже через несколько поколений.
Также в синтезе этанола применяют бактерии, в частности, распространенный вид Zymomonas mobilis, которые имеют большую скорость роста, высокий выход конечного продукта и не зависят от подачи кислорода.
Извлечения из целлюлозы
Как целлюлоза, так и крахмал является полисахаридами, полимерами углеводов, но синтез этанола из целлюлозы значительно тяжелее из-за ее малую склонность к гидролизу. Ее структура более подобна кристаллической, что усложняет разрыв связей внутри полимера, а в растениях ее защищает от гидролитического распада слой лигнина (после обработки целлюлозы кислотой гидролизуется лишь 15% всей массы). В отходах сырья также содержится гемицеллюлоза, которая состоит в основном из пентоз.
Предоперационная обработка включает в себя размола, замачивания исходного сырья для набухания. Впоследствии ее нагревают в автоклавах с 0,3-0,5% -ной кислотой под давлением 7-10 атм. В качестве кислоты чаще всего используется серная, реже — соляная. По окончании процесса кислоту концентрируют в отдельном резервуаре и снова пускают в производство, а лигнин отфильтровывают и очищают промывкой.
Полученный таким способом этиловый спирт называют гидролизным. Его применяют только для технических целей, потому что в нем содержится целый ряд вредных примесей, в том числе метиловый спирт, ацетон и др.
Также, в отличие от кислотной гидролиза, применяется энзиматический метод. Здесь гидролиз происходит под действием грибов вроде Trichoderma viride. Предварительная обработка включает в себя устранение лигнинового оболочки действием растворителе кадоксену (раствор с 5-7% содержанием оксида кадмия и 28% Этилендиамин) и обработку жидким аммиаком под высоким давлением, который будоражит волокна в целлюлозе, облегчая проникновение энзимов. В некоторых случаях удается достичь стопроцентной переработки целлюлозы.
другие способы
Гидролиз галогенпроизводных углеводородов
Этанол образуется при гидролизе галогенозамищеного этана. Его проводят в воде или в водном растворе щелочей. В первом случае реакция является обратной, а во втором может происходить элиминирования (отщепления) гидрогенгалогениду:
Конверсия синтез-газа
Добыча этанола из синтез-газа аналогичен методу получения метанола за процессом Фишера — Тропша:
Реакция происходит при температуре 125-175 ° C и давлении 1,42 МПа, используя катализатор типа порошкообразного железа.
Восстановление органических соединений
Восстановление альдегидов и кислот является довольно распространенным методом получения спиртов, в том числе и этанола:
Каталитическое восстановление зазвичать проводят над никелем Ренея, платиной; в лабораторных условиях застосовуетьcя алюмогидрид лития и борогидрид натрия.
очистка этанола
Синтезированный этанол обычно водно-спиртовой смесью. Его очистки и обезвоживания начинается с перегонки (ректификации), которой можно достичь концентрации 95,6% об. Образована смесь является азеотропной и не может быть очищена последующей перегонкой. Для дополнительной дегидратации используют бензол, циклогексан или гептан. Их присутствие создает новые азеотропные смеси с низкой температурой кипения, что позволяет получить безводный этанол.
В промышленных масштабах для обезвоживания могут использоваться молекулярные сита, чьи поры проницаемы для молекул воды, но не для этанола. Такие сита могут быть искусственными или цеолитов природного происхождения (например, клиноптилолита). 75% адсорбированных молекул является водой, остальные 25% — этанол, который затем снова возвращается в перегонных систему.
Также применяется мембранный метод, который заключается в разделении подогретой до 60 ° C водно-спиртовой смеси полупроницаемой мембраной, которая не пропускает этанол. Данная операция выполняется под действием давления менее 1 кПа. В результате разделения образуется этанол с концентрацией 99,85% и раствор, прошедший через мембрану, с концентрацией 23%. Конденсированный мембранный раствор может быть снова ректификованный.
Можно ли пить
Единственный спирт из упомянутой категории, который «с натяжкой» можно пить – этиловый первого сорта (медицинский), да и то – изредка, в небольших количествах и обязательно разведенным с водой. Ожог слизистой ЖКТ грозит гастритом, язвой, онкологией. Не забываем, что этот продукт пусть условно, но относится к категории пищевых.
Использовать технические спирты для употребления внутрь нельзя категорически. Это грозит тяжелым отравлением вплоть до смерти. Можно навсегда остаться инвалидом, потерять зрение, заработать цирроз или рак печени, поджелудочной железы.
Метиловый спирт — ужасная гадость. Случайно выпитый, буквально «разъедает» изнутри, и скорая даже не успевает доехать. Метанол разрушает зрительную, сосудистую и нервную системы. Чтобы отравиться, достаточно выпить 5-10 мл, летальный исход наступает от 30 мл.
Осторожно. Иногда «ветераны» вспоминают, что пили денатурат в 70-х – 80-х, и ничего.
Возможно, так и было
Но сегодня новые стандарты и то, что добавляют к денатурату, по настоящему опасно. К тому же, добавляемые ингредиенты невозможно химически разделить. Поэтому даже пробовать не советуем!
Возможно, так и было. Но сегодня новые стандарты и то, что добавляют к денатурату, по настоящему опасно. К тому же, добавляемые ингредиенты невозможно химически разделить. Поэтому даже пробовать не советуем!
Классификация этанола
Получаемый спирт по своему составу условно разделяют на четыре класса:
- промышленный этанол (96,5% об.) — продукт для промышленного и технического использования: в качестве растворителя, топливо и т. Для предотвращения его применению обычно в него добавляют вещества с неприятным запахом, например, пиридин в количестве 0,5-1% (проводят денатурацию). Также для более легкого определения ему могут оказывать слабого окраска метиловым фиолетовым;
- денатурированный спирт — технический продукт с концентрацией этанола 88% об., что значительное количество примесей. Он денатурируется и окрашивается соответствующим образом. Используется в освещении и обогреве;
- качественный алкоголь (96,0-96,5% об.) — очищенный этанол, применяется для нужд фармацевтики, в изготовлении косметических средств для пищевого потребления;
- абсолютный этанол (99,7-99,8% об.) — очень чистый этанол, применяется в фармацевтике, изготовлении аэрозолей.
В Украине марки получаемого ректификованного этанола регламентируются стандартом ДСТУ 4221: 2003 «Спирт этиловый ректификованный». В зависимости от степени очистки выделяется четыре сорта: «Пшеничная слеза», «Люкс», «Экстра» и «Высшей очистки».
Нормы для сортов спирта по ГОСТ 4221: 2003
| показатель | «Пшеничная слеза» | «Люкс» | «Экстра» | «Высшей очистки» |
| Объемная доля этилового спирта, при температуре 20 ° C,%, не менее | 96,3 | 96,3 | 96,3 | 96,0 |
| Массовая концентрация альдегидов, пересчете на уксусный альдегид в безводном спирте, мг / дм³, не более | 2,0 | 2,0 | 2,0 | 2,0 |
| Массовая концентрация сивушного масла: пропиловый, изопропиловый, бутиловый, изобутиловый и изоамиловый спирты в пересчете на смесь пропилового, изобутилового и изоамилового спиртов (3: 1: 1) в безводном спирте, мг / дм³, не более | 2,0 | 2,0 | 2,0 | 2,0 |
| Массовая концентрация сивушного масла в пересчете на смесь изобутилового и изоамилового спиртов (1: 1) в безводном спирте, мг / дм³, не более | 2,0 | 2,0 | 2,0 | 2,0 |
| Массовая концентрация эфиров, в пересчете на уксусноэтиловый эфир в безводном спирте, мг / дм³, не более | 1,5 | 2,0 | 3,0 | 5,0 |
| Объемная доля метилового спирта в пересчете на безводный спирт,%, не более | 0,005 | 0,01 | 0,02 | 0,03 |
| Массовая концентрация свободных кислот (без СО2), в пересчете на уксусную кислоту в безводном спирте, мг / дм³, не более | 8,0 | 8,0 | 12,0 | 15,0 |
Содержание
- 1 Этимология названий
- 2 Получение 2.1 Брожение 2.1.1 Промышленное производство спирта из биологического сырья
- 2.1.2 Гидролизное производство
- 3.1 Физические свойства
- 4.1 Топливо
- 5.1 Автомобильный парк, работающий на этаноле
- 6.1 Токсикология этанола
химические свойства
Этанол является одноатомный первичным спиртом и гидроксильная группа приводит большинство его химических свойств. Так, этанол может брать часть в реакциях дегидратации — как внитришньомолекулярнои, так и межмолекулярного:
При взаимодействии с другими спиртами образуется смесь трех эфиров:
С карбоновыми кислотами этанол в присутствии концентрированной серной кислоты образует эфиры:
В результате присоединения этанола до ацетилена синтезируется винилетиловий эфир:
Проявляя свои кислотные свойства, этанол реагирует с щелочными металлами (например, натрием) и щелочами с образованием этоксид:
Эта реакция проводится в безводной среде, поскольку гидроксид образуется быстрее, чем этоксид.
Менее активные металлы — алюминий и магний — также взаимодействуют с этанолом, но только в присутствии катализатора ртути:
Имеющаяся в молекуле гидроксильная группа может замещаться галогенидных кислотами с образованием галогенпроизводных этана:
Этанол окисляется до этаналя, а затем — в уксусной кислоты результатом полного окисления (например, сжигание этанола) является диоксид углерода и вода:
Обрабатывая этанол аммиаком при 300 ° C в кислой среде, образуются замещены амины: первичные, вторичные, третичные или даже четвертичные аммониевые соли (в зависимости от соотношения реагентов):
Этанол является сырьем для синтеза бутадиена. Реакция проводится при температуре 370-390 ° C и в присутствии катализаторов — MgO-SiO 2 или Al 2 O 3 -SiO 2 (с селективностью 70%):
Этиловый спирт по ГОСТ
ГОСТ – это прежде всего документ, регламентирующий какими качествами должны обладать товары, продаваемые на территории определенной страны. Существует несколько ГОСТов на этанол, которые описывают предназначение, условия хранения, транспортировки и многое другое.
Но такой сложный вопрос, как употребление алкогольных напитков, может породить многочасовые дебаты. Да и не в этом дело, ведь каждый человек должен сам для себя решать вопросы подобного уровня. Но давайте обратимся к ГОСТу 1972 года: «Этиловый спирт – легковоспламеняющаяся, бесцветная жидкость с характерным запахом. Относится к сильнодействующим наркотикам, которые вызывают сначала возбуждение, а затем — паралич нервной системы».
Теперь читаем ГОСТ 1982 года: «Этиловый спирт – легковоспламеняющаяся, бесцветная жидкость с характерным запахом, относящаяся к сильнодействующим наркотикам». И, наконец, 2000 год: «Этиловый спирт – это бесцветная, легковоспламеняющаяся жидкость с характерным запахом». Эти же самые нормативные документы и регламентируют такое вещество, как спирт этиловый технический.
биологическое действие
метаболизм
Почти весь потребленный спирт (90-98%) метаболизируется организмом и лишь небольшая его часть (2-10%) выводится в неизмененном виде: с мочой, воздухом, потом, слюной. Потребление этанола приводит к чрезмерному мочеиспускания: каждые 10 г алкоголя способствуют потере организмом 100 мл жидкости, не способствует удалению спирта из организма. Основная часть этанола, поступившей в организм, попадает в печень, где в микросомах испытывает биологического преобразования.
На первой стадии метаболизма из этанола образуется ацетальдегид. Это происходит под действием алкогольдегидрогеназы (АДГ) — фермента, кофактором которого является никотинамид (НАД). Впоследствии ацетальдегид, образующийся из этанола, окисляется в ацетат в митохондриях ферментом альдегиддегидрогеназа, которая как кофермент использует НАД, который, присоединяя протон, восстанавливается до НАД · Н. На этой стадии взаимодействие происходит гораздо быстрее, чем на предыдущей. Ацетат поступает в цикл Кребса, где разрушается до СО 2 и Н 2 О. Альдегиддегидрогеназу обнаруживают не только в печени, но и в других органах, включая головной мозг. У взрослого, здорового человека АДГ разрушает около 10 г спирта в час.
Кроме основного метаболического процесса, этанол окисляется также и двумя другими путями. Один из них происходит с участием микросомальное оксидазы в сочетании с восстановленным никотинамидадениндинуклеотидфосфат (НАДФ), в то время как другой — с участием каталазы в сочетании с пероксидом водорода. Оба пути ведут к образованию токсичного альдегида, который обладает канцерогенными свойствами и в десятки раз токсичнее по сравнению с этанолом.
Воздействие на организм
Симптомы в зависимости от полученной дозы спирта
| симптом | Содержание этанола в крови,% |
| растерянность | 0,06—0,08 |
| замедление мышления | 0,10 |
| ступор | 0,11—0,15 |
| опьянения | 0,16 |
| значительное отравления | 0,2—0,4 |
| смерть | 0,4—0,5 |
Попадая в тело человека через пищевод, этанол быстро всасывается. В желудке поглощается 20% первоначального этанола, а в тонком кишечнике — 80%. После поглощения он попадает в кровь уже через 5 минут, распространяясь с кровотоком по всему организму.
Центральная нервная система. Этанол угнетает функции ЦНС подобно другим анестезирующих веществ. Несмотря на распространенное мнение, этанол не стимулирует действие нервной системы: если возбуждение и возникают, то их появление обусловлено противодействием тормозным процессам. В обычных дозах этанол действует в основном на активирующее функцию ретикулярной формации стволовой части мозга и только большие дозы непосредственно подавляют функцию коры головного мозга.
Хроническое употребление этанола вызывает дефицит серотонина. Функциональное снижение активности этой системы препятствует развитию толерантности и, наоборот, увеличение ее активности, повышение уровня серотонина ускоряют развитие толерантности к алкоголю. Под действием этанола нарушается обмен дофамина, который участвует в синтезе норадреналина и координирует движения, эмоциональный и психический состояния. Также этанол оказывает отрицательное влияние на физические и психические возможности: он снижает остроту зрения и слуха, нарушает мышечную координацию и устойчивость, замедляет время реакции на раздражение.
Дыхательная система. Этанол имеет ярко выраженное токсическое действие на органы дыхания. Поражение легких сказывается развитием бронхолегочной инфекции вследствие уменьшения защитных функций организма. Негативное воздействие алкоголя связано с угнетением фагоцитоза и образования антител, содействием проникновению бактерий в дыхательные пути и тому подобное. Бронхолегочные патологии могут перерасти в появлении острой пневмонии, которая имеет значительный процент летальных случаев.
Сердечно-сосудистая система. Под действием этанола растворяются липиды клеточных мембран, в частности, клеток миокарда. В результате увеличивается проницаемость мембран и нарушается обмен ионов натрия, калия, магния и кальция. Это ослабляет сократительную способность сердечной мышцы.
Пищеварительная система. Однократный прием приводит острый геморрагический эрозивный гастрит; аналогичная действие этанола и на слизистую оболочку двенадцатиперстной кишки. Уже через минуту после попадания в желудок крыс этанол вызывал диффузную гиперемию слизистой желудка.
Печень. Степень повреждения печени этанолом напрямую зависит от количества употребленного алкоголя. В результате его действия могут появляться стеатоз, фиброз, алкогольный гепатит и цирроз, нередко заканчивается развитием гепатоклеточная карциномы. Так, по данным Международного агентства по исследованию рака этанол обладает канцерогенным действием.
Одним из результатов длительного воздействия на организм этанола является увеличение объема эритроцитов — макроцитоз, вызванный токсическим действием ацетальдегида, дефицитом фолиевой кислоты и гиперлипидемией.
алкоголизм
Этанол является основой спиртных напитков. Их длительное применение вызывает появление алкоголизма.
Алкоголизм представляет собой совокупность явлений, характеризующих клиническую картину зависимости от алкоголя (то есть этанолсодержащими продуктов). Среди симптомов и проявлений такой зависимости стостеригаються: толерантность организма к алкоголю, физическая зависимость, синдром отмены при прекращении или уменьшении потребления, неконтролируемое и время чрезмерное потребление.
Выделяют три стадии прогресса алкоголизма:
- у человека отсутствует влечение к алкоголю, наблюдается потеря контроля при потреблении, переход к систематическому потреблению, увеличение толерантности к алкоголю, присутствуют начальные расстройства в психической сфере;
- имеется физическая зависимость с потерей меры, формирования психопатоподобной синдрома, нарушения деятельности систем организма (сердечно-сосудистой, мочеполовой, дыхательной) и органов (появление гастрита, гепатита)
- зависимость от алкоголя является психической, присутствует сильное физическое влечение как проявление синдрома отмены, появление галлюцинаций, необратимые повреждения внутренних органов (цирроз печени, сердечные болезни, энцефалопатия и т.д.).
Влияние на беременность
Риск возникновения отклонений в развитии плода является прямо пропорциональна количеству потребленного во время беременности алкоголя.
Этанол легко проникает через плаценту, поэтому его содержание в крови матери и плода быстро достигает одинакового уровня. Он накапливается в тканях плода, богатых фосфолипиды, в головном мозге, а также эритроцитах. Выведения алкоголя из организма осуществляется с помощью ферментов печени, а у будущего ребенка она формируется только во второй половине беременности матери. Вредное воздействие этанола на плод связан с незрелостью защитного механизма и повышенной проницаемостью сосудов и тому подобное. Особое значение имеют критические периоды эмбрионального развития, когда чувствительность эмбриона и плода к чужеродным веществам достигает максимального уровня. Токсическое действие этанола является причиной замедления развития или даже гибели эмбриона.
Потребление матерью этанола во время беременности связано с появлением фетальных (плодотворных) тератогенных эффектов. Влияние алкоголя проявляется в нарушении общего развития плода, рождении ребенка с меньшими, чем в норме, массой тела и ростом, психической неполноценностью. В частности, пораженные тератогенным действием этанола дети имеют видоизмененные черты лица: узкие глазные щели, тонкую верхнюю губу, появление микроцефалии и ретрогнатия, отсутствие фильтруют и различные ушные аномалии. Физические видоизменения дополняются недоразвитостью головного мозга, склонностью к судорожным припадкам, отеков головного мозга, плохой координацией движений, снижением интеллекта и врожденными пороками сердца. Такое действие этанола назван фетальный алкогольный синдром, ФАС (или алкогольный синдром плода).
Взаимодействие с медицинскими препаратами
Этанол обладает способностью усиливать действие антибиотиков, антигистаминных препаратов, барбитуратов, миорелаксантов, а также вызвать негативную реакцию организма.
Взаимодействие медицинских препаратов с этанолом
| класс препаратов | препарат | Тип взаимодействия с этанолом, последствия |
| анальгетики | аспирин Ацетаминофен | Аспирин увеличивает опорожнения желудка, что ведет к быстрой сорбции спирта в тонком кишечнике, может замедлять в желудке действие алкогольдегидрогеназы. Этанол усиливает метаболизм ацетаминофена, продуктом которого является токсичные вещества, которые повреждают печень. Возможно появление усиленного сердцебиения, болей в животе, язв желудка, |
| антибиотики | Эритромицин Изониазид Кетоконазол метронидазол | Эритромицин увеличивает опорожнения желудка, что ведет к быстрой сорбции спирта в тонком кишечнике; совместно с изониазидом алкоголь повышает риск появления болезней печени. Сопровождается головными болями, тошнотой, резкими изменениями артериального давления |
| антигистаминные препараты | Димедрол Клемастин Прометазин | Этанол усиливает влияние препаратов на ЦНС, вызывая появление вялости, снижение моторики совместное действие сильнее сказывается на пожилых людях. |
| барбитураты | фенобарбитал | Слабость организма, головокружение, риск судорожного приступа. Хроническое употребление алкоголя повышает уровень метаболизма барбитуратов цитохрома Р-450 |
| Снотворные средства (бензодиазепины) | Диазепам лоразепам Оксазепам | Этанол усиливает влияние препаратов на ЦНС, вызывая появление проблем с памятью, вялости, снижение моторики, замедление или затруднение дыхания; |
| противовоспалительные препараты | Диклофенак Ибупрофен Напроксен | Потребление этанола увеличивает риск появления желудочного кровотечения, пептических язв |
| Блокаторы H2-рецепторов | Низатидин Ранитидин Циметидин | Препараты подавляют действие алкогольдегидрогеназы и способствуют випирожненню желудка, приводящее к повышенному содержанию этанола в крови. |
Сферы использования спирта
Пользователи нашли еще массу способов применения недорогого технического спирта в быту:
- очищение красок и пятен с разных материалов;
- растворяет практически все химические вещества;
- хорошо очищает обогреватели из керосина;
- может служить наполнителем лекарственных препаратов;
- во флексографической печати;
- спиртом пользуются, как заменителем биотоплива.
Продается технический спирт в любых магазинах Москвы, специализирующихся на химических соединениях. Цена зависит от упаковки и производителя, и может колебаться от 47 рублей за литр и выше.
На всех выставленных на продажу упаковках, обязательно должна быть надпись о том, что этот продукт опасен для человеческого организма, потому что служит причиной не только отравления, но и причиной летального исхода. Применять его внутрь строго запрещено, этот спирт используется только для технических работ. Все входящие в состав технического спирта вещества очень опасны для человеческого организма. Его можно применять только для научных опытов и дезинфекции изделий.
Использование технического спирта на предприятиях в настоящее время очень распространено. Это эксплуатация, механическое обслуживание машин, оснащение, выполнение научных опытов.
У каждого продукта — есть свое значение. Так, технический спирт нужен для производства лакокрасочной продукции, моющих средств, добавок к топливу. Принимать его вовнутрь строго запрещается. У тех людей, которые употребляют разбавленный спирт, чтобы получить удовольствие от опьянения, есть заболевания, связанные с психикой. Эти люди должны обратиться за помощью к медицинскому специалисту, а именно к наркологу. Потому что также есть огромная вероятность того, что у них есть зависимость от алкоголя. Стоимость технического спирта намного меньше, чем у спиртных напитков в магазине. Алкоголики больше всего хотят сэкономить на пагубной привычке, чтобы заплатить меньше, а получить больше наслаждения.
Так, почему нельзя употреблять технический спирт? Его никогда не используют для приема вовнутрь, потому что в его составе есть такие токсичные вещества, которые опасны для человеческого организма. Алкогольная интоксикация является одной из самых страшных последствий приема технического спирта, как напитка. Но что еще хуже, это летальный исход. Даже маленькая доза просто-напросто может убить взрослого человека.
применение
Этанол имеет широкий спектр применений, среди которых наиболее значимыми являются производство спиртных напитков, использование в качестве растворителя, топлива, а также синтез других химических веществ.
топливо
Первый автомобиль, который был способен ездить на этаноле, спроектировал Генри Форд в 1920 году — модель Ford T. Однако тогда эта инновация это не получила необходимого развития через технические и экономические проблемы: производство чистого этанола было слишком дорогим, а использование недоочищенных спирта в смеси с углеводородным топливом было в определенной степени ограниченным — при низких температурах нерастворимая в бензине вода замерзала, закорковуючы топливный бак.
Сейчас, имея технологии для производства дешевого этанола, замена традиционного бензинового или дизельного топлива этанолом, или использование его в качестве добавки, приобрела в мире широкое распространение. Мировое производство этанола для нужд топливной промышленности в 2014 году составил 24750000000. Галлонов.
растворитель
Этанол является наиболее важным растворителем после воды. Его основной применением является производство косметики, парфюмерии, поверхностно-активных веществ и дезинфектантов, фармацевтических препаратов, различных покрытий. Для этих целей применяется этанол как синтетического, так и ферментативного происхождения.
антисептик
Этанол является древнейшим антисептиком, известным человечеству. Его способность обеззараживать ранения была отмечена древнегреческим врачом Клавдием Галеном, а позднее и средневековым французским хирургом Ги де Шолиак.
Этанол проявляет бактерицидные действия при концентрации 30% и выше, в зависимости от типа бактерий, содержания воды и времени действия. Согласно исследованиям наиболее эффективна действие этанола при его концентрации 60-70% — как в присутствии воды, так и при ее отсутствии. Именно такое содержание этанола имеют бытовые антисептики для рук. Использование высокой концентрации (например, 90% раствора) для дезинфекции кожи нецелесообразно, поскольку при таких концентрациях этанол проявляет свои дубильные свойства, в то время как антисептические свойства падают.
Принцип действия этанола на микроорганизмы, вероятно, заключается в воздействии на их мембраны и быстрой денатурации белков, что приводит к нарушению метаболизма бактерий и дальнейшего разрушения клеток. Этанол демонстрирует высокую биоцидную действие против вегетативных бактерий (включая микобактериями), вирусов, грибов, но не спор.
Из-за отсутствия спороцидные действия этанол не может быть использован для стерилизации, однако его свойств достаточно для профилактического обеззараживания поверхностей, обработки кожи и тому подобное.
Преципитация нуклеиновых кислот
Этанол широко применяется в молекулярной биологии для осаждения и концентрирования ДНК и РНК. Его используют совместно с буферными растворами солей, содержащих простые однозарядные катионы (например, катионы натрия). Типичным является использование буфера ацетата натрия концентрации 0,3 моль / л с pH 5,2 (при 4 ° C) и этанола — абсолютного и 70-процентного (при -20 ° C).
Для осаждения нуклеиновых кислот их образец смешивают с буферным раствором и абсолютным этанолом и охлаждают при -20 ° C в течение часа, после чего центрифугируют. Отделив пипеткой лишнюю жидкость с поверхности, добавляют 70% раствор этанола и повторяют центрифугирования и отделения жидкости. Остаток выпаривают при температуре 37 ° C на водяной бане и таким образом получают сконцентрирована вещество.
антидот
Благодаря своей способности образовывать эфиры при взаимодействии со спиртами, этанол используется как доступный антидот при отравлениях метанолом, этиленгликолем и диэтиленгликоля. В организм этанол вводят внутрь или внутривенно, а доза для введения рассчитывается из соображений, что в сыворотке крови его концентрация должна достигать 10-15 мг / л.
Риск в применении этанола заключается в угнетении деятельности центральной нервной системы, появлению гипогликемии (из-за снижения глюконеогенеза) и тошноты. При введении внутривенно возможно появление флебита, гипертонии, гипонатриемии. Применение такого антидота требует постоянного мониторинга содержания этанола в сыворотке и уровня глюкозы в венозной крови.
Синтез других веществ
В промышленности этанол используют для получения этаналя, бутадиена, диэтилового эфира, этилацетата, этиламина и тому подобное.
Польза или вред
Нельзя сказать однозначно, пользу или вред приносит этиловый спирт. Сегодня трудно отыскать область жизнедеятельности человека, где бы он не применялся.
Он приносит неоценимую пользу в медицине в качестве дезинфицирующего средства. С его помощью поддерживается стерильная чистота в операционных. Незаменим он в приготовлении различных видов лекарств.
Для человека прием малых доз спиртосодержащих напитков также очень полезен. При попадании в организм человека, они помогает расширить сосуды, разжижить кровь, улучшив тем самым кровообращение.
Бывает, что только благодаря психотропному действию спиртного человеку удается приглушить сильную боль.
Ярко выраженные антисептические свойства спиртовых растворов давно оценены косметологами. На их основе делаются большинство очищающих лосьонов.
С точки зрения вреда организму человека спиртное является наиболее опасным наркотиком. Частое его употребление может вызвать сильнейшую психологическую и физическую зависимость, недаром алкоголизм давно уже считается болезнью.
Уже доказано, что алкоголь пагубно действует на мозг, печень, почки, сердце и все системы организма. А ведь алкогольные напитки производятся из пищевого спирта.