Этанол или этиловый спирт относится к группе антисептических средств. Его используют наружно для обработки кожных поверхностей перед проведением различных медицинских манипуляций. На базе средства изготавливают различные лекарственные формы. Чаще всего, они предназначены для наружного применения. Внутрь медикаментозные препараты на базе этанола применяют в соответствии с инструкцией и только при наличии врачебных рекомендаций.
Содержание
- 1 Этимология названий
- 2 Получение 2.1 Брожение 2.1.1 Промышленное производство спирта из биологического сырья
- 2.1.2 Гидролизное производство
- 3.1 Физические свойства
- 4.1 Топливо
- 5.1 Автомобильный парк, работающий на этаноле
- 6.1 Токсикология этанола
Получение
Существует 2 основных способа получения этанола — микробиологический (спиртовое брожение) и синтетический (гидратация этилена):
Брожение
Известный с давних времён способ получения этанола — спиртовое брожение органических продуктов, содержащих углеводы (виноград, плоды и т. п.) под действием ферментов дрожжей и бактерий. Аналогично выглядит переработка крахмала, картофеля, риса, кукурузы, источником получения топливного спирта является вырабатываемый из тростника сахар-сырец и проч.
Раствор, получаемый в результате брожения, содержит не более 15 % этанола, так как в более концентрированных растворах дрожжи нежизнеспособны. Полученный таким образом этанол нуждается в очистке и концентрировании, обычно путем дистилляции.
Промышленное производство спирта из биологического сырья
Современная промышленная технология получения этилового спирта из пищевого сырья включает следующие стадии:
- Подготовка и измельчение крахмалистого сырья — зерна (прежде всего — ржи, пшеницы), картофеля, кукурузы и т. п.
- Ферментация. На этой стадии происходит ферментативное расщепление крахмала до сбраживаемых сахаров. Для этих целей применяются рекомбинантные препараты альфа-амилазы, полученные биоинженерным путём — глюкамилаза, амилосубтилин.
- Брожение. Благодаря сбраживанию дрожжами сахаров происходит накопление в бражке спирта.
- Брагоректификация. Осуществляется на разгонных колоннах.
Отходами бродильного производства являются углекислый газ, барда, эфиро-альдегидная фракция, сивушный спирт и сивушные масла.
Спирт, поступающий из брагоректификационной установки (БРУ) не является безводным, содержание этанола в нём до 95,6 %. В зависимости от содержания в нём посторонних примесей, его разделяют на следующие категории:
- 1 сорт
- высшей очистки
- базис
- Экстра
- Люкс
- Альфа
Производительность современного спиртового завода около 30 000—100 000 литров спирта в сутки.
Гидролизное производство
В промышленных масштабах этиловый спирт получают из сырья, содержащего целлюлозу (древесина, солома), которую предварительно гидролизуют. Образовавшуюся при этом смесь пентоз и гексоз подвергают спиртовому брожению. В странах Западной Европы и Америки эта технология не получила распространения, но в СССР существовала развитая промышленность кормовых гидролизных дрожжей и гидролизного этанола.
Гидратация этилена
- В промышленности, наряду с первым способом, используют гидратацию этилена. Гидратацию можно вести по двум схемам: прямая гидратация при температуре 300 °C, давлении 7 МПа, в качестве катализатора применяют ортофосфорную кислоту, нанесённую на силикагель, активированный уголь или асбест.
- гидратация через стадию промежуточного эфира серной кислоты, с последующим его гидролизом (при температуре 80—90 °С и давлении 3,5 МПа).
Эта реакция осложняется образованием диэтилового эфира.
Очистка этанола
Этанол, полученный путём гидратации этилена или брожением, представляет собой водно-спиртовую смесь, содержащую примеси. Для его промышленного, пищевого и фармакопейного применения необходима очистка. Фракционная перегонка позволяет получить этанол с концентрацией около 95,6 % (мас.); эта неразделимая перегонкой азеотропная смесь содержит 4,4 % воды (мас.) и имеет температуру кипения 78,15 °C.
Перегонка освобождает этанол как от легколетучих, так и от тяжёлых фракций органических веществ (кубовый остаток).
Абсолютный спирт
Абсолютный спирт — этиловый спирт, практически не содержащий воды. Он кипит при температуре 78,39 °C, в то время как спирт-ректификат, содержащий не менее 4,43 % воды, кипит при 78,15 °C. Получают перегонкой водного спирта, содержащего бензол, и другими способами.[1]
История
Этанол естественным образом образуется при ферментации сахаристых фруктов. Человек издревле использовал это природное вещество для опьянения и одурманивания. Пиво, а позднее и вина были впервые произведены с помощью природных дрожжей. Содержание спирта в таких напитках было ниже, чем сегодня, потому что природные дрожжи прекращают превращать сахар в этанол при достижении определенной концентрации. Современные культивированные дрожжи позволяют достичь более высоких концентраций.
В 1796 году Иоганн Тобиас Лоуиц впервые получил чистый этанол путем фильтрации дистиллированного спирта через активированный уголь. Антуан Лавуазье впервые описал этанол как соединение углерода, водорода и кислорода. В 1808 году Николя-Теодор де Соссюр определил химический состав. Пятьдесят лет спустя Арчибальд Скотт Купер опубликовал структурную формулу. Синтетически спирт был впервые произведен в 1826 году Генри Хеннелем и Джорджем Саймоном Серуллой в Соединенном Королевстве Великобритании.
Сегодня этанол в основном получают путем ферментации из биомассы. В контексте производства биотоплива его называют биоэтанолом. Сельскохозяйственный спирт — это этанол из сельскохозяйственного сырья.
Свойства
Физические свойства
Внешний вид: в обычных условиях представляет собой бесцветную летучую жидкость с характерным запахом. Следует избегать популярной ошибки: часто смешивают свойства 95,57 % спирта и абсолютизированного. Их свойства почти одинаковы, но величины начинают различаться, начиная с 3 — 4-й значащей цифры.
Свойства этанола
| Температура плавления | −114,15 °C |
| Температура кипения | 78,15 °C |
| Растворимость | смешивается с бензолом, водой, глицерином, диэтиловым эфиром, ацетоном, метанолом, уксусной кислотой, хлороформом |
Смесь 95,57 % этанола + 4,43 % воды является азеотропной, т. е. не разделяется при перегонке.
Химические свойства
Взаимодействует со щелочными металлами с образованием этилатов (или в общем случае — алкоголятов) и водорода.
Наркотические свойства
Существует разница между химико-фармакологическим и юридическим определениями наркотических свойств этанола. С химико-фармацевтической точки зрения этанол обладает наркотическими свойствами, в то время как с юридической точки зрения этанол наркотиком не признаётся, хотя указание на наркотические свойства в некоторой технико-юридической документации также присутствует.
Указание на наркотические свойства этанола присутствуют в ряде учебников по фармакологии, в специализированных фармацевтических и химических словарях[2], в энциклопедиях.[3] Так, химико-фармакологическое определение, взятое из Учебника фармакологии» под ред. С. В. Аничкова, М. Л. Беленького, гласит:
Этиловый алкоголь — винный спирт, Spiritus Vini (C2H5OH) по своим фармакологическим свойствам относится к наркотическим веществам жирного ряда.
Наркотические свойства этанола проявляются также в характерном алкогольном возбуждении, за которым следует угнетение функций центральной нервной системы, включая блокирование работы центров торможения.
Наркотический характер воздействия этанола также подтверждается тем фактом, что алкоголизм, являющийся формой зависимости от этанола, рассматривается как форма наркомании[4].
Зерновой дистиллят по ГОСТ
В настоящее время на территории РФ действует ГОСТ Р 55799-2013 «Дистиллят зерновой. Технические условия».
В таблице 3 представлены органолептические показатели для зерновых дистиллятов.
Таблица 3
| Наименование показателя | Характеристика |
| Внешний вид | Прозрачная жидкость без осадка и посторонних включений |
| Цвет | Бесцветная жидкость или от светло-золотистого до янтарного |
| Аромат и вкус | Характерные для дистиллята, выработанного из соответствующего зернового сырья, без постороннего привкуса и запаха |
По физико-химическим свойствам зерновые дистилляты должны соответствовать значениям, указанным в таблице 4.
Применение
Топливо
Этанол может использоваться как топливо, в т. ч. для ракетных двигателей, двигателей внутреннего сгорания в чистом виде. Ограничено в силу своей гигроскопичности (отслаивается) используется в смеси с классическими нефтяными жидкими топливами. Применяется для выработки высококачественного топлива и компонента бензинов — Этил-трет-бутилового эфира, более независимого от ископаемой органики, чем МТБЭ.
Химическая промышленность
- Служит сырьём для получения многих химических веществ, таких, как ацетальдегид, диэтиловый эфир, тетраэтилсвинец, уксусная кислота, хлороформ, этилацетат, этилен и др.;
- Широко применяется как растворитель (в лакокрасочной промышленности, в производстве товаров бытовой химии и многих других областях);
- Является компонентом антифризов и стеклоомывателей.
- В бытовой химии этанол применяется в чистящих и моющих средствах, в особенности для ухода за стеклом и сантехникой. Является растворителем для репеллентов.
Медицина
В медицине этиловый спирт в первую очередь используется как растворитель, экстрагент и антисептик.
- по своему действию этиловый спирт можно отнести к антисептикам;
- как обеззараживающее и подсушивающее средство, наружно;
- подсушивающие и дубящие свойства 96%-го этилового спирта используются для обработки операционного поля или в некоторых методиках обработки рук хирурга;
- растворитель для лекарственных средств, для приготовления настоек, экстрактов из растительного сырья и др.;
- консервант настоек и экстрактов (минимальная концентрация 18 %);
- пеногаситель при подаче кислорода, искусственной вентиляции легких;
- в согревающих компрессах;
- для физического охлаждения при лихорадке (для растирания)[5];
- возможно применение как компонента парентерального питания (в виде 5 % раствора) у ослабленных больных с учётом высокой энергетической ценности вещества
- компонент общей анестезии в ситуации дефицита медикаментозных средств
- Как пеногаситель при отеке легких в виде ингаляции 33 % раствора.
- Этанол является противоядием при отравлении некоторыми токсичными спиртами, такими как метанол и этиленгликоль. Его действие обусловлено тем, что фермент алкогольдегидрогеназа, при наличии нескольких субстратов (например, метанол и этанол) осуществляет лишь конкурентное окисление, благодаря чему после своевременного
(почти немедленного, вслед за метанолом/этиленгликолем) приёма этанола уменьшается текущая концентрация токсичных метаболитов (для метанола — формальдегида и муравьиной кислоты, для этиленгликоля — щавелевой кислоты).
Парфюмерия и косметика
Является универсальным растворителем различных веществ и основным компонентом духов, одеколонов, аэрозолей и т. п. Входит в состав разнообразных средств, включая даже такие как зубные пасты, шампуни, средства для душа, и т. д.
Пищевая промышленность
Наряду с водой, является необходимым компонентом спиртных напитков (водка, виски, джин и др.). Также в небольших количествах содержится в ряде напитков, получаемых брожением, но не причисляемых к алкогольным (кефир, квас, кумыс, безалкогольное пиво и др.). Содержание этанола в свежем кефире ничтожно (0,12 %), но в долго стоявшем, особенно в тёплом месте, может достичь 1 %. В кумысе содержится 1—3 % этанола (в крепком до 4,5 %), в квасе — от 0,6 до 2,2 %.
Растворитель для пищевых ароматизаторов. Может быть использован как консервант для хлебобулочных изделий, а также в кондитерской промышленности.
Зарегистрирован в качестве пищевой добавки E1510
[6].
Энергетическая ценность этанола — 7,1 ккал/г.
Описание
Этанол (C2 H5 OH) относится к линейным алканолам. «Алкоголь или спирт» является устоявшимся разговорным обращением. Термин «спирты» обозначает группу органических химических соединений, которые, в дополнение к углеводородному скелету, имеют по меньшей мере одну гидроксильную группу в качестве дополнительной функциональной группы. При этом у атома углерода, содержащего гидроксильную группу, отсутствует заместитель более высокого порядка.
Спирт является естественным продуктом алкогольного брожения в зрелых фруктах и соках. Многие продукты содержат небольшое количество этанола. Например, безалкогольное пиво содержит до 0,5%. Фруктовые соки могут иметь содержание спирта около 0,38%. Исключением является виноградный сок, который может содержать до 1% этанола, также как спелый банан и кефир. Физиологическое содержание спирта в крови человека составляет от 0,02 до 0,03%.
Применение этанола в качестве автомобильного топлива
В разных странах действуют разные государственные программы применения этанола на транспорте:
| Страна | Требования |
| США | производит ежегодно 28 млрд литров этанола к 2012 году, 85%-я смесь этанол/бензин (E85) |
| Евросоюз | 2 % в 2005, 5,75 % биотоплив к 2010 году (этанол + биодизель) |
| Китай | производить ежегодно 3 млн тонн к 2010 году |
| Таиланд | В Бангкоке 10%-я смесь, 5%-я смесь по всей стране с 2007 года |
В США «Энергетический билль», подписанный президентом Бушем в августе 2005 года, предусматривает производство к 2012 году ежегодно 30 миллиардов литров этанола из зерна и 3,8 миллиардов литров из целлюлозы (стебли кукурузы, рисовая солома, отходы лесной промышленности).
Этанол хорошо смешивается с водой, в отличие от бензина. Проблема расслаивания смеси бензина и этанола на данный момент не решена.
Автомобильный парк, работающий на этаноле
Смесь этанола с бензином обозначается буквой Е. Цифрой у буквы Е обозначается процентное содержание этанола. Е85 — означает смесь из 85 % этанола и 15 % бензина.
Смеси до 20 % содержания этанола могут применяться на любом автомобиле. Однако некоторые производители автомобилей ограничивают гарантию при использовании смеси с содержанием более 10 % этанола. Смеси, содержащие более 20 % этанола, во многих случаях требуют внесения изменения в систему зажигания автомобиля.
Автопроизводители выпускают автомобили, способные работать и на бензине, и на Е85. Такие автомобили называются «Flex-Fuel». В Бразилии такие автомобили называют «гибридными». В русском языке названия нет. Большинство современных автомобилей либо изначально поддерживают использование такого топлива, либо опционально, по соответствующему запросу.
В 2005 году в США более 5 млн автомобилей имели Flex-Fuel двигатели. В конце 2006 г. в США эксплуатировалось 6 млн автомобилей с Flex-Fuel двигателями. Общий автопарк составляет 230 млн автомобилей.
1200 заправочных станций продают Е85 (май 2007). Всего в США автомобильное топливо продают около 170 000 заправочных станций.
В Бразилии около 29 000 заправочных станций продают этанол.
Экономичность
Себестоимость бразильского этанола (около 0,19 долларов США за литр в 2006 г.) делает его использование экономически выгодным.
Экологические аспекты
Биоэтанол как топливо нейтрален в качестве источника парниковых газов. Он обладает нулевым балансом диоксида углерода, поскольку при его производстве путём брожения и последующем сгорании выделяется столько же CO2, сколько до этого было взято из атмосферы использованными для его производства растениями.
В 2006 году применение этанола в США позволило сократить выбросы около 8 млн тонн парниковых газов (в СО2 эквиваленте), что примерно равно годовым выхлопам 1,21 млн автомобилей.
Безопасность и регулирование
Денатурат
- Этанол — горючее вещество, смесь его паров с воздухом взрывоопасна.
- Спирт этиловый синтетический, технический и пищевой, непригодный для производства алкогольной продукции, входит в список ядовитых веществ для целей статьи 234 и других статей Уголовного кодекса Российской Федерации[7]
- С 2005 года розничная продажа спирта в России запрещена (за исключением районов Крайнего Севера) [8]
Токсикология этанола
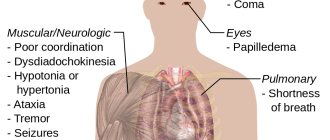
В зависимости от дозы, концентрации, пути попадания в организм и длительности воздействия этанол может обладать наркотическим, наркозным и токсическим действием. В определённых дозах к массе тела и концентрациях приводит к острому отравлению и смерти (смертельная разовая доза — 4-12 граммов этанола на килограмм веса). Однако этанол является естественным метаболитом человеческого организма, и в определённых дозах используется в медицине как самостоятельное лекарственное средство, а также как растворитель фармацевтических препаратов, экстрактов и настоек.
Длительное употребление этанола может вызвать такие заболевания, как гастрит, язва желудка, рак желудка и рак пищевода.
Употребление этанола может вызвать оксидативное повреждение нейронов головного мозга.
Злоупотребление алкогольными напитками может привести к алкоголизму.
Влияние на здоровье
Этанол всасывается по всему пищеварительному тракту. Первый этап в небольшой степени начинается уже в слизистой оболочке полости рта. Поглощенный там спирт поступает непосредственно в кровь и, таким образом, распределяется по всему телу, включая мозг. Около 20% всасывается в желудке, остальное в тонкой кишке.
Этанол, абсорбированный в желудке и кишечнике, сначала попадает в печень вместе с кровью, где он частично разлагается. Всасывание спирта увеличивается за счет различных факторов, таких как тепло (ирландский кофе, грог), сахар (ликер) и углекислый газ (игристое вино).
Приблизительно 2-10% выпитого спирта выделяется с мочой, потом и выдыхаемым воздухом.
В печени, основная часть этанола (как и другие растворимые в воде токсины) с помощью ферментов алкогольдегидрогеназы (АДГ) деградируют спирт до уксусной кислоты. Уксусная кислота затем превращается в CO2 через цикл Кребса. Промежуточный этанал отвечает за так называемые симптомы «похмелья» — головная боль, тошнота и рвота. Разложение этана сдерживается сахаром, поэтому похмелье бывает особенно интенсивно при употреблении сладких алкогольных напитков, особенно ликера и некоторых сортов шампанского.
Скорость деградации алкогольдегидрогеназой является постоянной в определенных пределах. У мужчин это около 0,1 г в час и кг массы тела, у женщин 0,085
Примечания
- Статья «Абсолютный спирт» в БСЭ.
- Фармацевтический справочник Химик.ру
- Большая Советская Энциклопедия, статья «Этиловый спирт»
- БСЭ, статья «Алкоголизм»
- Средства, влияющие на ЦНС
- E1510 — спирт этиловый
- Постановление Правительства Российской Федерации от 29 декабря 2007 г. N 964 г. Москва «Об утверждении списков сильнодействующих и ядовитых веществ для целей статьи 234 и других статей Уголовного кодекса Российской Федерации, а также крупного размера сильнодействующих веществ для целей статьи 234 Уголовного кодекса Российской Федерации»
- Статья 26 Федерального закона от 22.11.1995 N 171-ФЗ (ред. от 05.04.2010) (Консультант+)