Нарушение метаболизма кальция вследствие отклонений в функциональности эндокринных желез моет привести к серьезным осложнениям. Кальция является минералом, необходимым организму для формирования и сохранения полноценного состояния костной ткани. В организме этот минерала содержится в количестве 1,5 кг.
Кальций поступает в организм с продуктами питания, а так же вырабатывается паращитовидными железами. Эндокринная система регулирует обменные процессы между кальцием и фосфором. При гормональном дефиците происходит повышение фосфатов в крови с сопутствующим снижением показателей уровня кальция. Нарушение функций железы моет привести и к обратному процессу, когда показатели кальция увеличены. Оба вида отклонений не считаются нормой и вызывают развитие патологических процессов.
Характерные особенности
В организме человека нарушение кальциевого метаболизма провоцирует развитие различных заболеваний. Кальций считается важным элементом в процессе регулирования нервной возбудимости мышечных тканей, процессе гемостаза, в стабилизации клеточной ткани мембран, в трансдукции внутриклеточного сигнала.
В медицине выделяют две формы нарушения минерального метаболизма в эндокринной системе:
- гипокальциемия (гипопаратиреоз);
- гиперкальциемия (гиперпаратиреоз).
Второй тип заболевания опаснее и требует более сложного лечения. В большинстве случаев, если патология запущена, врачи прибегают к хирургическому вмешательству.
Для того чтобы понять, что могло спровоцировать изменение в выработке паращитовидными железами кальция в кровь, как бороться с этим нарушением и какие могут быть последствия, следует рассматривать каждую патологию отдельно.
Обмен кальция и фосфора в организме и его нарушения
Метаболизм кальция
К функциям кальция в организме относятся:
· структурная (кости, зубы);
· сигнальная (внутриклеточный вторичный мессенджер-посредник);
· ферментативная (кофермент факторов свертывания крови);
· нейромышечная (контроль возбудимости, выделение нейротрансмиттеров, инициация мышечного сокращения).
Главная роль в метаболизме кальция в организме человека принадлежит костной ткани. В костях кальций представлен фосфатами — Са3(РО4)2 (85%), карбонатами — СаСО3 (10%), солями органических кислот — лимонной и молочной (около 5%). Вне скелета кальций содержится во внеклеточной жидкости и практически отсутствует в клетках. В состав плотного матрикса кости, наряду с коллагеном, входит фосфат кальция — кристаллическое минеральное соединение, близкое к гидроксилапатиту Са10(РО4)6(ОН)2. Часть ионов Са2+ замещена ионами Mg2+, незначительная часть ионов ОН– — ионами фтора, которые повышают прочность кости. Минеральные компоненты костной ткани находятся в состоянии химического равновесия с ионами кальция и фосфата сыворотки крови. Клетки костной ткани могут ускорять отложение или, наоборот, растворение минеральных компонентов при локальных изменениях рН, концентрации ионов Са2+, НРО42-, хелатообразующих соединений (Д. Мецлер, 1980). В организме взрослого человека содержится 1-2 кг кальция, 98% которого находится в составе скелета (А. Уайт и соавт., 1981). Он составляет около 2% массы тела (примерно 30 моль). В крови уровень кальция — 9-11 мг/100 мл (2,2-2,8 ммоль/л), во внеклеточной жидкости — около 20 мг/100 мл. Регуляция обмена кальция между вне- и внутриклеточной жидкостью осуществляется паратгормоном, кальцитонином, 1,25-диоксихолекальциферолом. При уменьшении концентрации ионов кальция возрастает секреция паратиреотропного гормона (ПТГ), и остеокласты увеличивают растворение содержащихся в костях минеральных соединений. ПТГ увеличивает одновременно реабсорбцию ионов Са2+ в почечных канальцах. В итоге повышается уровень кальция в сыворотке крови. При увеличении содержания ионов кальция секретируется кальцитонин, который снижает концентрацию ионов Са2+ за счет отложения кальция в результате деятельности остеобластов. В процессе регуляции участвует витамин D, он требуется для синтеза кальцийсвязывающих белков, необходимых для всасывания ионов Са2+ в кишечнике, реабсорбции его в почках. Постоянное поступление витамина D необходимо для нормального течения процессов кальцификации. Изменение уровня кальция в крови могут вызывать тироксин, андрогены, которые повышают содержание ионов Са2+, и глюкокортикоиды, снижающие его. Ионы Са2+ связывают многие белки, в том числе некоторые белки системы свертывания крови. В белках системы свертывания содержатся кальций-связывающие участки, образование которых зависит от витамина К.
В пищевых продуктах кальций содержится в основном в виде фосфата кальция, который и поступает в организм. В природе кальций встречается в виде карбоната, оксалата, тартрата, фитиновой кислоты (в составе злаков).
Дефицит кальция в организме часто связан с малой растворимостью большинства его солей.
С плохой растворимостью солей кальция авторы связывают кальцификацию стенок артерий, образование камней в желчном пузыре, почечных лоханках и канальцах.
Фосфаты кальция легко растворяются в желудочном содержимом. Максимальное всасывание кальция происходит в проксимальных отделах тонкого кишечника и уменьшается в дистальных отделах.
Доля усвоения кальция более значительна у детей (по сравнению со взрослыми), у беременных и кормящих. Усвоение кальция снижается с возрастом человека, при дефиците витамина D.
В плазме крови содержатся фракции связанного с белком (недиффундирующего) кальция (0,9 ммоль/л) и диффундирующего: ионизированного (1,1-1,4 ммоль/л) и неионизированного (0,35 ммоль/л). Биологически активным является ионизированный кальций, он проникает в клетки через мембраны, неионизированная форма связана с белками (альбумином), углеводами и другими соединениями. Внутри клеток концентрация свободного кальция низкая. Так, общая концентрация ионов Са2+ в цитоплазме эритроцитов составляет около 3 мкМ, из них на свободные ионы приходится менее 1 мкМ. Градиент концентрации ионов кальция по разные стороны от мембраны (от 102 до 105) поддерживается при помощи кальциевого насоса. Очень медленная обратная диффузия ионов внутрь клетки противостоит работе насоса. Са2+ относится к вторичным месенджерам — внутриклеточным веществам, концентрация которых контролируется гормонами, нейромедиаторами, внеклеточными сигналами. Низкий уровень кальция в клетках поддерживается кальциевыми насосами (кальциевыми АТФ-азами) и натрийкальциевыми обменниками. Высокая активация Mg2+-, Са2+-АТФ-азы связана с конформационными изменениями кальциевого насоса, приводящими к переносу Са2+. Резкое увеличение содержания кальция в клетке происходит при открытии кальциевых каналов или внутриклеточных кальциевых депо (концентрация повышается до 500-1000 нМ при 10-100 нМ в нестимулированной клетке). Открытие каналов может быть вызвано деполяризацией мембран, действием сигнальных веществ, нейромедиаторов (глутамат, АТФ), вторичных мессенджеров (инозит-1,4,5-трифосфат, цАМФ) (Я. Кольман, К. Г. Рем, 2000). Уровень кальция в клетках повышается (в 5-10 раз) в виде кратковременных флюктуаций (высокие концентрации кальция оказывают цитотоксическое действие). В клеточных органеллах и цитоплазме клеток имеется большое количество белков, способных связывать кальций и выполнять роль буфера. Действие кальция опосредовано «кальциевыми сенсорами» — специальными кальцийсвязывающими белками — аннексином, кальмодулином, тропонином. Кальмодулин имеется во всех клетках и при связывании четырех ионов кальция переходит в активную форму, которая может взаимодействовать с белками. С2+ оказывает влияние на активность ферментов, ионных насосов, компонентов цитоскелета за счет активации кальмодулина.
Гипоальбуминемия не влияет на уровень ионизированного кальция, который варьирует в узком диапазоне и тем самым обеспечивает нормальное функционирование нервно-мышечного аппарата. С увеличением рН доля связанного кальция возрастает. При алкалозе ионы водорода диссоциируют из молекулы альбумина, что приводит к снижению концентрации ионов кальция. Это может вызвать клинические симптомы гипокальциемии, несмотря на то, что концентрация общего кальция в плазме не изменена. Обратная картина (увеличение концентрации ионов кальция в плазме) отмечается при остром ацидозе. Глобулины также связывают кальций, хотя и в меньшей степени, чем альбумин.
Составные компоненты регуляции содержания кальция в плазме крови включают:
· скелет (резервуар кальция);
· почки;
· экскрецию кальция через кишечник с желчью;
· паратгормон, кальцитонин (их секреция определяется уровнем кальция в плазме);
· 1,25-диоксихолекальциферол.
Внеклеточный пул кальция в течение суток обновляется приблизительно 33 раза (В. Дж. Маршалл, 2002), проходя через почки, кишечник и кости. И даже небольшое изменение любого из этих потоков оказывает существенное влияние на концентрацию кальция во внеклеточной жидкости, включая плазму крови. Кальций, входящий в состав секретов пищеварительного тракта, частично реабсорбируется вместе с пищевым кальцием.
Нарушения обмена кальция сопровождаются нарушениями обмена фосфатов и клинически проявляются в изменениях костного скелета и нервно-мышечной возбудимости.
Наблюдается обратная зависимость между содержанием кальция и фосфора в сыворотке крови (одновременное повышение наблюдается при гиперпаратиреоидизме, снижение — при рахите у детей). При повышенном содержании фосфора в пище в желудочно-кишечном тракте образуется невсасывающийся трехосновной фосфорнокислый кальций. Суточная потребность в кальции взрослого человека составляет 20-37,5 ммоль (0,8-1,5 г), у беременных и кормящих в два раза выше (М. А. Базарнова и соавт., 1986). В пищевой канал ежедневно поступает 35 ммоль кальция, но всасывается только половина, в 50 раз медленнее, чем натрий, но интенсивнее, чем железо, цинк, марганец. Всасывание происходит в тонком кишечнике (максимально в 12-перстной кишке). Лучше всего всасывается глюконат и лактат кальция. Оптимум всасывания наблюдается при рН=3,0. Кальций соединяется с жирными и желчными кислотами и через воротную вену поступает в печень. Транспорту через мембрану энтероцита в кровь способствует витамин D. Всасывание снижается при недостатке фосфатов (важное значение имеет соотношение кальций/фосфор). На всасывание влияет концентрация Nа+, активность щелочной фосфатазы, Mg2+-, Са2+-АТФ-азы, содержание кальций-связывающего белка. Из организма в норме кальций выводится через кишечник. Ежедневно в пищевой канал секретируется слюнными, желудочными и поджелудочными железами и выводится около 25 ммоль Са2+ (М. А. Базарнова и соавт., 1986). Выведение кальция с калом сохраняется даже при бескальциевой диете (в составе желчи). В почках за сутки фильтруется около 270 ммоль Са2+. 90% кальция, фильтруемого в почках, реабсорбируется, поэтому в целом с мочой его выделяется мало (выделение возрастает при увеличении концентрации кальция в крови и ведет к образованию камней в почках). Суточная экскреция колеблется от 1,5 до 15 ммоль и зависит от суточного ритма (максимум в утренние часы), уровня гормонов, кислотно-основного состояния, характера пищи (углеводы усиливают выведение кальция). При рассасывании минерального остова костей, реабсорбция кальция снижается. Кости являются резервуаром кальция: при гипокальциемии кальций поступает из костей и, наоборот, при гиперкальциемии он откладывается в скелете.
Ионы кальция важны для течения многих процессов:
· нервно-мышечного возбуждения;
· мышечного сокращения;
· свертывания крови;
· проницаемости клеточных мембран;
· активности многих ферментов и перекисного окисления липидов.
Основные источники кальция — молоко, молочные продукты (творог, твердые сыры), рыба, яйца. Он содержится также в зеленых овощах, орехах. Одним из источников кальция является питьевая вода (в 1 литре до 350-500 мг). С питьевой водой поступает 10-30% кальция (В. И. Смоляр, 1991). Биодоступность кальция улучшают кисломолочные продукты, животные белки, снижают ее — пищевые волокна, алкоголь, кофеин, избыток жиров (образуются нерастворимые соединения), фосфаты, оксалаты. Повышенное содержание в пище магния и калия тормозит всасывание кальция: они конкурируют с кальцием за желчные кислоты. Препараты витамина D способствуют всасыванию кальция. При лечении остеопороза одновременно с назначением препаратов кальция необходимо восполнение дефицита белков, кальциферола, витаминов.
Гиперкальциемия — результат повышенного поступления кальция во внеклеточную жидкость из резорбируемой костной ткани или из пищи в условиях снижения почечной реабсорбции. Наиболее частой причиной гиперкальциемии (90% случаев) являются первичный гиперпаратиреоз, злокачественные новообразования. Часто гиперкальциемия клинически не проявляется. К редким причинам гиперкальциемии относят (У. Клаттер, 1995) гранулематозные заболевания (в том числе саркоидоз), гипервитаминоз D, тиреотоксикоз, применение тиазидных диуретиков, препаратов лития, молочно-щелочной синдром, длительную обездвиженность, наследственную гипокальциурическую гиперкальциемию, почечную недостаточность. К клиническим симптомам гиперкальциемии относятся:
· отсутствие аппетита, тошнота, рвота, боли в животе (развивается язва желудка и 12-перстной кишки, панкреатит), запоры;
· слабость, утомляемость, снижение массы тела, мышечная слабость;
· изменения личности, ухудшение концентрации внимания, сонливость, кома;
· аритмии, укорочение интервала Q-T на ЭКГ;
· нефрокальциноз, почечные конкременты, кальциноз сосудов, роговицы;
· полиурия, дегидратация, почечная недостаточность.
Наиболее частой причиной снижения общей концентрации кальция в сыворотке является гипоальбуминемия.
Обмен кальция в организме не нарушается, если содержание свободного кальция находится в пределах нормы. Концентрация свободного кальция в сыворотке снижается при гипопаратиреозе, резистентности к паратиреоидному гормону (псевдогипопаратиреозе), авитаминозе D, почечной недостаточности, выраженной гипомагниемии, гипермагниемии, остром панкреатите, некрозе скелетных мышц (рабдомиолизе), распаде опухолей, многократном переливании цитратной крови. К клиническим проявлениям гипокальциемии относятся: парестезии, чувство онемения, судороги мышц, спазм гортани, отклонения в поведении, ступор, положительные симптомы Хвостека и Труссо, удлинение интервала Q-T на ЭКГ, катаракта. Умеренная гипокальциемия может быть бессимптомной.
Гиперкальциурия развивается при повышенном потреблении кальция с пищей, передозировке витамина D (усиливается резорбция в кишечнике), канальцевых расстройствах (идиопатическая гиперкальциурия, почечные тубулярные ацидозы), при повышенном распаде костной ткани (миеломная болезнь, опухоли костной ткани, фосфатный диабет, остеопороз, гиперпаратиреоз).
Гипокальциурия наблюдается при гипопаратиреозе, гиповитаминозе D, гипокальциемии, снижении клубочковой фильтрации.
Роль фосфора в организме человека
В организме взрослого человека содержится около 670 г фосфора (1% массы тела), который необходим для образования костей и клеточного энергетического обмена. 90% фосфора, подобно кальцию, находится в скелете — костях и зубах (М.А. Базарнова и соавт., 1986). Вместе с кальцием они составляют основу твердого вещества кости. В костях фосфор представлен трудно растворимым фосфатом кальция (2/3) и растворимыми соединениями (1/3). Большая часть остального количества фосфора находится внутри клеток, 1% — во внеклеточной жидкости. Поэтому уровень фосфора в сыворотке крови не позволяет судить об общем его содержания в организме.
Фосфаты являются структурными элементами костной ткани, участвуют в переносе энергии в виде макроэргических связей (АТФ, АДФ, креатинфосфат, гуанинфосфат и других). Фосфор и сера — два элемента в организме человека, которые входят в состав различных макроэргических соединений. С участием фосфорной кислоты осуществляется гликолиз, гликогенез, обмен жиров. Фосфор входит в структуру ДНК, РНК, обеспечивающих синтез белка. Он участвует в окислительном фосфорилировании, в результате которого образуется АТФ, фосфорилировании некоторых витаминов (тиамина, пиридоксина и других). Фосфор важен также для функционирования мышечной ткани (скелетной мускулатуры и сердечной мышцы). Неорганические фосфаты входят в состав буферных систем плазмы и тканевой жидкости. Фосфор активирует всасывание ионов кальция в кишечнике. Суточная потребность в фосфоре составляет 30 ммоль (900 мг), у беременных она возрастает на 30-40%, в период лактации — в два раза (М. А. Базарнова и соавт, 1986). По данным В. И. Смоляра (1991), потребность в фосфоре у взрослых — 1600 мг в сутки, у детей — 1500-1800 мг в сутки.
В организм человека фосфор поступает с растительной и животной пищей в виде фосфолипидов, фосфопротеинов и фосфатов.
В растительных продуктах (в частности, в бобовых) содержится много фосфора, однако усвояемость его низкая. Важным источником его является мясо и рыба. В желудке и кишечнике фосфорная кислота отщепляется от органических соединений. Всасывание 70-90% фосфора происходит в тонком кишечнике. Оно зависит от концентрации фосфора в просвете кишки, активности щелочной фосфатазы (угнетение ее снижает всасывание фосфора). Активность щелочной фосфатазы повышает витамин D, а всасывание фосфатов — паратиреоидный гормон. Всосавшийся фосфор поступает в печень, участвует в процессах фосфорилирования, частично откладывается в виде минеральных солей, которые затем переходят в кровь и используются костной и мышечной тканью (синтезируется креатинфосфат). От обмена фосфатов между кровью и костной тканью зависит нормальное течение процессов окостенения, поддержания нормальной костной структуры.
В крови фосфор находится в виде четырех соединений: неорганического фосфата, органических фосфорных эфиров, фосфолипидов и свободных нуклеотидов. В плазме крови неорганический фосфор присутствует в виде ортофосфатов, но его концентрацию в сыворотке оценивают непосредственно (1 мг% фосфора=0,32 ммоль/л фосфата). Он проникает через полунепроницаемые мембраны, фильтруется в почечных клубочках. Концентрация неорганического пирофосфата в плазме крови составляет 1-10 мкмоль/л. Содержание неорганического фосфора в плазме крови взрослых людей — 3,5-4 мг фосфора/100 мл, несколько выше оно у детей (4-5 мг/100мл) и у женщин после менопаузы. В плазме также содержатся гексозофосфаты, триозофосфаты и другие. Скелет является резервуаром неорганического фосфора: при снижении его содержания в плазме он поступает из скелета и, наоборот, откладывается в скелете при повышении его концентрации в плазме. Концентрацию фосфора в сыворотке крови рекомендуется определять натощак: богатая фосфором пища повышает его, а углеводы, инфузия глюкозы — снижают. Фосфор выводится из организма через кишечник и почки в виде фосфата кальция. С мочой выделяется 2/3 растворимых одно- и двузамещенных фосфатов натрия и калия и 1/3 фосфатов кальция и магния. В почках за сутки фильтруется около 208 ммоль фосфата, экскретируется 16-26 ммоль. Соотношение одно- и двузамещенных солей фосфора зависит от кислотно-основного состояния. При ацидозе однозамещенных фосфатов выводится в 50 раз больше, чем двузамещенных. При алкалозе усиленно образуются и выделяются двузамещенные соли фосфатов.
Паратиреоидный гормон снижает уровень фосфора в сыворотке крови, угнетая реабсорбцию его в проксимальных и дистальных канальцах, усиливая выведение с мочой. Кальцитонин оказывает гипофосфатемическое действие, уменьшая реабсорцию и усиливая экскрецию. 1,25(ОН)2Д3, усиливая всасывание фосфата в кишечнике, повышает его уровень в крови, способствует фиксации фосфорно-кальциевых солей костной тканью. Инсулин стимулирует поступление фосфата в клетки и тем самым снижает его содержание в сыворотке крови. Гормон роста увеличивает реабсорбцию фосфатов, вазопрессин — экскрецию.
Обмен фосфора и кальция тесно взаимосвязаны. Считается (В. И. Смоляр, 1991), что оптимальным для совместного усвоения из пищи является соотношение между фосфором и кальцием равное 1:1-1,5. Гиперкальциемия, снижая секрецию паратиреоидного гормона, стимулирует реабсорбцию фосфатов. Фосфат может соединяться с кальцием и приводить к отложению кальция в тканях и гипокальциемии.
При нарушении обмена фосфора обнаруживаются повышение и снижение его в крови. Гиперфосфатемия часто наблюдается при почечной недостаточности, встречается при гипопаратиреозе, псевдогипопаратиреозе, рабдомиолизе, распаде опухолей, метаболическом и респираторном ацидозе. Гиперфосфатемия подавляет гидроксилирование 25-гидроксикальциферола в почках. Умеренная гипофосфатемия не сопровождается существенными последствиями. Тяжелая гипофосфатемия (менее 0,3 ммоль/л (1 мг%) сопровождается нарушением функции эритроцитов, лейкоцитов, мышечной слабостью (нарушается образование АТФ, 2,3-дифосфоглицерата). Она наблюдается при злоупотреблении алкоголем и абстиненции, респираторном алкалозе, нарушении всасывания в кишечнике, приеме средств, связывающих фосфат, возобновлении приема пищи после голодания, при переедании, тяжелых ожогах, лечении диабетического кетоацидоза (У. Клаттер, 1995). При диабетическом кетоацидозе гипофосфатемия не является признаком истощения запасов фосфата. Умеренная гипофосфатемия (1,0-2,5 мг%) может наблюдаться при инфузии глюкозы, дефиците витамина D в пище или снижении его всасывания в кишечнике, при гиперпаратиреозе, остром тубулярном некрозе, после пересадки почек, при наследственной гипофосфатемии, синдроме Фанкони, паранеопластической остеомаляции, увеличении объема внеклеточной жидкости. Респираторный алкалоз может вызвать гипофосфатемию, стимулируя активность фосфофруктокиназы и образование фосфорилированных промежуточных продуктов гликолиза. Хроническая гипофосфатемия приводит к рахиту и остеомаляции.
Гипофосфатемия проявляется потерей аппетита, недомоганием, слабостью, парестезиями в конечностях, болью в костях. Гипофосфатурия наблюдается при остеопорозе, гипофосфатемическом почечном рахите, инфекционных заболеваниях, острой желтой атрофии печени, снижении клубочковой фильтрации, повышенной реабсорбции фосфора (при гипосекреции ПТГ).
Гиперфосфатурия наблюдается при повышенной фильтрации и сниженной реабсорбции фосфора (рахит, гиперпаратиреоз, тубулярный ацидоз, фосфатный диабет), гипертиреозе, лейкозах, отравлениях солями тяжелых металлов, бензолом, фенолом.
Гомеостаз кальция и фосфата
Гипокальциемия стимулирует секрецию паратиреоидного гормона и тем самым увеличивает продукцию кальцитриола. В результате увеличивается мобилизация кальция и фосфатов из костей, их поступление из кишечника. Избыток фосфатов экскретируется с мочой (ПТГ оказывает фосфатурическое действие), а реабсорбция кальция в почечных канальцах возрастает, и концентрация его в крови нормализуется. Гипофосфатемия сопровождается усилением секреции только кальцитриола. Увеличение под действием кальцитриола его концентрации в плазме приводит к снижению секреции паратиреоидного гормона. Гипофосфатемия приводит к стимуляции абсорбции фосфата и кальция в кишечнике. Избыток кальция выводится с мочой, так как кальцитриол усиливает реабсорбцию кальция в незначительной мере (по сравнению с ПТГ). В результате описанных процессов нормальная концентрация фосфата в плазме крови восстанавливается независимо от концентрации кальция.
Причины гипокальциемии
Эндокринные органы чувствительны к воздействию на них, поэтому кальциевый метаболизм может нарушаться по разным причинам.
Понижение содержания Ca в плазме может произойти по следующим причинам:
- травматизация шеи с кровотечением;
- осложнение после проведенные операции на щитовидной железе;
- воспалительные процессы;
- ионизирующее излучение;
- метастазирование в эндокринных органах;
- недостаточность надпочечников;
- аутоиммунные заболевания;
- болезни системного типа.
Выявление причин считается основой лечения, поскольку при продолжении влияния негативных факторов терапия окажется не эффективной.
Причины гиперкальциемии
Избыточное количество Ca в плазме может быть спровоцировано несколькими факторами. Не редко, нарушение кальциевого метаболизма возникает по причине развития злокачественных образований или доброкачественных опухолей.
У 80% больных гиперкальциемия развивается из-за нарушений, возникающих в результате формирования на гипофизе аденомы солитарной. Аденома в свою очередь образуется по причине стрессов, пониженного давления, приема гормонов и др.
В 12% случаев причиной становится первичная форма гиперплазии. У 2% пациентов диагностируется рак железы паращитовидной. Около 6 % больных имеют множественную аденому.
К причинам так же можно отнести:
- дефицит в рационе продуктов, содержащих кальций;
- нарушение мальабсорбционных функций кишечника;
- почечная недостаточность в хронической форме.
Лечение в данном случае предполагает устранение причины. Если после этого показатели не изменяются, проводится направленная терапия, или даже хирургическое вмешательство.
Патологии кальциевого обмена
Патогенетические механизмы нарушения обмена кальция можно условно разделить на две группы: эндокринные и энергозависимые. К первой группе относятся состояния, обусловленные нарушением функции паращитовидных желез, играющих роль в регуляции уровня кальция во внеклеточной жидкости. Для паратгормона органами-мишенями являются костная ткань и почки. Вторым важнейшим регулятором обмена кальция является гормон щитовидной железы кальцитонин, поддерживающий внутриклеточный гомеостаз кальция3. Но самое непосредственное участие в обмене кальция в клетках кожи принимают эстрогены и витамин Д. Со снижением выработки эстрогенов у женщин после менопаузы быстро стареет кожа и возникают серьезные проблемы с обменом кальция в костях. С другой стороны, ограничение воздействия УФ лучей на кожу с возрастом снижает накопление в коже витамина Д, который образуется путем фото- биогенеза, происходящего в коже под влиянием УФ лучей. Витамин Д, кроме того обеспечивает устойчивость кожи к УФ лучам. Гормональная форма витамина Д — 1.25 дигидроксихолекальциферол (кальцитриол) стимулирует всасывание кальция и фосфатов в кишечнике и реабсорбцию их в почках, стимулирует ремоделирование костной ткани, транспорт кальция через мембраны клеток, дифференцировку клеток, развитие иммунной системы. Помимо гормонов, регулирующих обмен кальция (I группа факторов), большое значение в его регуляции имеет вторая группа факторов, вырабатываемых в клетках в результате трансформации АТФ. К этой группе факторов относятся неорганические поли- и бисфосфаты, являющиеся продуктами нормального энергетического обмена в клетках. С возрастом значительно падает продукция АТФ и, как следствие, снижается образование поли- и бисфосфатов, что приводит к нарушениям кальциевого обмена4.
Немного подробнее о симптоматике
Клиническая картина в обоих случаях — выраженная. Основной областью поражения становится костная система, которая содержит более 90% кальция от общего его содержания в организме.
Симптоматика гиперкальциемии, относительно костной ткани:
- псевдо- и простая форма подагры;
- деформация;
- болевые ощущения;
- мышечная слабость и атрофия;
- переломы даже при простых ушибах;
- кистозные образования костей.
При тяжелой стадии возникает ощущение «мурашек», онемение и жжение на отдельных участках тела, может наблюдаться временная парализация тазовых мышц.
Гипокальциемия характеризуется судорожными приступами, которые могут затрагивать не только конечности, но и мышцы грудной клетки. Опасность предоставляет гипокальциемический криз, который вызывает серьезные осложнения.
Введение
Во второй половине нашего столетия были сделаны существенные открытия в области минерального обмена и его эндокринной регуляции. Полученные новые знания о регуляции и нарушениях обмена кальция позволили понять патогенез различных клинических синдромов, обусловленных этими нарушениями. К таким синдромам относятся рахит, остеохондроз, остеопороз, особенно постменопаузальный с высоким риском переломов позвонков, висцеральные и скелетные формы гиперпаратиреоза, остеодистрофии, мочекаменная болезнь, атеросклероз, болезнь Фара с отложением кальция в мозгу, кальциноз, дерматомиозит и другие.
Кальций по природе является фосфатофилом и содержится в разных тканях, в частности в митохондриях клеток в виде фосфатных солей (гидроксиапатит кальция). Если апатиты являются наиболее малорастворимыми солями кальция, то соединения с неорганическими бисфосфатами (пирофосфатами) могут становиться в зависимости от условий нерастворимыми (в костях) или растворимыми (в мягких тканях), т.е. неорганические бисфосфаты являются естественными регуляторами обмена кальция в организме. При постепенном снижении активности многочисленных регуляторных механизмов с возрастом обмен кальция нарушается и нерастворимые соли кальция откладываются в мягких тканях. Возникает вопрос, является ли кожа исключением? Для ответа на этот вопрос было проведено исследование изменения содержания кальция в клетках различных слоев кожи в зависимости от возраста.
Гиперкальциемический криз
Редким, но опасным осложнением является гиперкальциемический криз. В остром состоянии у больного нарушается работа всей нервной системы и ускоряется свертываемость крови. Повышенная густота крови, предполагает повышенные риски для жизни больного, поскольку это может привести к формированию тромбов или полной остановке сердечной мышцы.
Криз гиперкальциемический имеет симптоматику:
- сохранение температуры более 40°C;
- внутренние кровотечения;
- признаки лихорадки;
- сильный зуд кожи.
Нарушения ЦНС приводят и к возникновению психоза, а в дальнейшем шока. Состояние больного приводит к тому, что он не понимает того, что происходит. Если медицинская помощь не оказывается своевременно, начинается паралич органов дыхания с последующей остановкой сердца и летальным исходом.
Физиологические эффекты кальция[править | править код]
Нервы и мышцы[править | править код]
Умеренное повышение концентрации кальция во внеклеточной жидкости может и не сопровождаться клиническими признаками нарушения функции нервной и мышечной систем. Однако при выраженной гиперкальциемии возбудимость нервов и мышц снижается, что приводит к развитию мышечной слабости, сонливости и даже к коме. Напротив, умеренное снижение концентрации кальция повышает возбудимость, приводя к появлению симптомов Хвостека и Труссо,тетанических судорог и ларингоспазма. Считается, что поступление Са в клетки осуществляется: 1) путем облегченной диффузии (с помощью переносчика), 2) за счет Na+/CaJ+-o6MeHa, 3) через каналы. Проницаемость последних регулируется гормонами и медиаторами, а во многих клетках эти каналы являются потенциалзависимыми. В печени и скелетных мышцах внутриклеточный кальций обратимо поглощается соответственно эндоплазматическим и саркоплазматическим ретикулумом.
Ионы кальция играют важную роль в электромеханическом сопряжении. Потенциал действия вызывает высвобождение кальция из саркоплазматического ретикулума мышечной клетки. Освобожденный кальций связывается с тропонином, снимая блокирующее влияние тропомиозина на взаимодействие актина с миозином, и тем самым активирует процесс сокращения. Когда кальций вновь поглощается саркоплазматическим ретикулумом, восстанавливается блокирующее действие тропомиозина и мышца расслабляется.
Ионы кальция необходимы и для экзоцитоза, поэтому они играют важную роль в сопряжении стимуляции с секрецией в большинстве экзокринных и эндокринных желез. Секреция катехоламинов мозговым веществом надпочечников, выделение медиаторов в синапсах и высвобождение некоторых других биологически активных веществ (например, гистамина тучными клетками) — все эти процессы требуют присутствия кальция. Сердечно-сосудистая система. Ионы кальция играют важнейшую роль в электромеханическом сопряжении в сердечной мышце, а также в проведении электрических импульсов по определенным участкам сердца, в частности в АВ-узле. Деполяризация волокон сердечной мышцы открывает потенциалзависимые кальциевые каналы (так называемые медленные кальциевые каналы), через которые во время плато потенциала действия кальций поступает внутрь клетки. Локальное повышение концентрации кальция вызывает открывание кальциевых каналов саркоплазматического ретикулума, что еще больше увеличивает концентрацию кальция в цитоплазме и приводит к сокращению. В некоторых клетках, например в клетках АВ-узла, потенциал действия почти полностью обеспечивается за счет поступления кальция через медленные кальциевые каналы.
В гладких мышцах, в том числе в гладких мышцах сосудов, кальций обеспечивает сокращение и часто создает существенную часть деполяризующего тока. Поэтому антагонисты кальция оказывают сильное влияние на сократимость миокарда и гладких мышц сосудов, равно как и на проведение импульсов в сердце. Эти препараты занимают важное место среди антиангинальных, антиаритмических и гипотензивных средств. Прочие эффекты. Ионы кальция поддерживают целость слизистых, участвуют в адгезии клеток и обеспечивают функции клеточных мембран. Кальций играет важную роль в механизмах свертывания крови, хотя и не применяется в качестве лечебного средства при нарушениях свертывания. Кальция хлорид оказывает закисляющее действие на мочу (хотя соли аммония в этом отношении гораздо эффективнее) и способствует диурезу.
Гипокальциемический криз
Обострение при кальциевом дефиците характеризуется снижением минеральных веществ в плазме менее 2,25 ммоль/л. Криз гипокальциемический так же опасен.
Приступ может наступить внезапно, но, как правило, ему предшествует ряд симптомов:
- ощущение «мурашек»;
- чувство покалывания по всему телу;
- конечности и часть лица немеют;
- сильная слабость мышц;
- внезапные мышечные боли;
- депрессивное состояние;
- изменение цвета кожного покрова.
Постепенно потерю чувствительности и другие признаки сменяют подергивания мышц. Первоначально больной ощущает лишь легкие и единичные спазмы, но достаточно быстро состояние переходит в припадки сильных судорог.
Тонус мышц выражается характерными проявлениями:
- «рука акушера»;
- «конская стопа»;
- «рыбий рот»;
- и другие.
Опасность возникает, когда спазмы затрагивают мышечные ткани внутренних органов: почечные/печеночные колики, ларингоспазм или бронхоспазм. Нарушение дыхания может спровоцировать асфиксию.
Больной в момент криза ощущает нестерпимые боли, от которых теряет сознание и способность разумно воспринимать происходящее.
Кальций[править | править код]
Кальций — основной внеклеточный двухвалентный катион. В организме здоровых мужчин и женщин содержится соответственно около 1300 и 1000 г кальция, из которых более 99% — в костях. Небольшие количества кальция присутствуют в плазме и межклеточной жидкости и еще меньшие — в клетках, где в покое концентрация ионизированного кальция составляет примерно 0,1 мкмоль/л. Под влиянием химических, электрических или механических стимулов кальций входит в клетки, и его внутриклеточная концентрация достигает 1 мкмоль/л. При этом он взаимодействует со специфическими кальцийсвязывающими белками, которые активируют множество внутриклеточных процессов. Главный кальцийсвязываюший белок — кальмодулин. Это высококонсервативный белок, каждый моль которого связывает 4 моля кальция. Ионы кальция необходимы для возбуждения нейронов, выделения медиаторов, мышечного сокращения, поддержания структуры мембран, свертывания крови и многих других физиологических реакций. Кроме того, кальций выполняет роль второго посредника многих гормонов, медиаторов и пр.
Осуществление всех этих разнообразных функций возможно лишь при определенной концентрации ионизированного кальция. В плазме человека концентрация кальция составляет 8,5—10,4 мг% (2,1—2,6 ммоль/л). Примерно 45% этого количества связано с белками (главным образом с альбумином) и 10% образует комплексы с анионами буферных систем (цитратом и фосфатами). Остальное приходится на долю ионизированного кальция, который и обладает физиологической активностью. Именно уменьшение концентрации ионизированного кальция вызывает симптомы гипокальциемии. Для того чтобы по общей концентрации кальция в плазме судить о концентрации ионизированного кальция, необходимо знать концентрацию белка. Здесь помогает следующее приблизительное правило: отклонение концентрации альбумина в плазме на 1 г% (норма — 4 г%) должно сопровождаться изменением общей концентрации кальция на 0,8 мг%.
Концентрация кальция в крови находится под строгим гормональным контролем. Гормоны влияют на его всасывание в кишечнике и выделение почками, а также регулируют поступление в кровь кальция, запасенного в костях. Запасы кальция. Более 99% всего кальция в организме содержится в костях в кристаллической форме, напоминающей минерал гидроксиапатит Са|0(РО4)6(ОН)2. Минеральное вещество костей содержит и другие ионы, в том числе натрий, калий, магний и фтор. Количество кальция в костях зависит от соотношения между резорбцией и остеогенезом — двух сопряженных процессов постоянного обновления костной ткани (см. ниже). Кроме того, в костях имеется лабильная фракция кальция, из которой он легко выходит в межклеточную жидкость костей, а из нее — в кровь. На скорость всех этих процессов влияют лекарственные средства, гормоны, витамины и другие факторы.
Всасывание и экскреция кальция[править | править код]
Жители США примерно 75% кальция, поступающего с пищей, получают с молоком и молочными продуктами. Суточная потребность в кальции у подростков составляет 1300 мг, у лиц до 24 лет — 1000 мг, у мужчин и женщин старше 50 лет — 1200мг(см. часть XIII, «Введение») (Institute of Medicine, 1997). В то же время медиана потребления кальция мальчиками и девочками в возрасте 9 лет и старше составляет соответственно 865 и 625 мг/сут, а у женщин после 50 лет она постепенно снижается до 517 мг/сут (Institute of Medicine, 1997).
На рис. 62.1
Рисунок 62.1. Обмен кальция. Приведены приблизительные величины суточных потоков кальция.
приведена схема обмена кальция. Кальций поступает в организм только из кишечника. В ЖКТ он усваивается лишь частично. Всасывание кальция обеспечивается двумя механизмами. В проксимальном отделе двенадцатиперстной кишки происходит активный витамин-Э-зависимый транспорт кальция. Кроме того, большое количество кальция всасывается путем облегченной диффузии по всей длине тонкой кишки. Обязательные потери кальция через кишечник составляют примерно 150 мг/сут; это количество содержится в секрете слизистой, желчи и слущивающихся клетках кишечника.
Усвояемость кальция обратно пропорциональна его потреблению: при низком содержании в пище доля всасываемого кальция возрастает, отчасти вследствие усиления активации витамина D. С возрастом эта компенсаторная реакция существенно ослабевает. Некоторые лекарственные средства (например, глюкокортикоиды и фенитоин) угнетают всасывание кальция. Определенные присутствующие в пище соединения (например, фитиновая и щавелевая кислоты) препятствуют всасыванию кальция, образуя с ним нерастворимые комплексы. Усвояемость кальция падает и при заболеваниях, сопровождающихся стеатореей, поносом или хроническим нарушением всасывания.
Экскреция кальция с мочой зависит от соотношения его клубочковой фильтрации и канальцевой реабсорбции. В сутки фильтруется примерно 9 г кальция, и более 98% этого количества реабсорбируется. Реабсорбция кальция регулируется ПТГ, но на нее влияют также количество фильтруемого натрия, присутствие нереабсорби-руемых анионов и диуретики. Экскреция кальция с мочой непосредственно связана с потреблением (а, соответственно, и с экскрецией) натрия. Петлевые диуретики увеличивают экскрецию кальция. Напротив, тиазидные диуретики обладают уникальной способностью нарушать связь между экскрецией натрия и кальция, приводя к снижению экскреции кальция (Lemann et al., 1985). Потребление белка также влияет на экскрецию кальция с мочой, что связано, вероятно, с действием серосодержащих аминокислот на функцию почечных канальцев. У здоровых людей содержание кальция в моче лишь в слабой степени зависит от его количества в пище. Во время лактации значительные количества кальция экскре-тируются с молоком. Небольшое количество этого элемента теряется с потом.
Обновление костной ткани[править | править код]
Сразу же после образования костной ткани в ней начинается непрерывный процесс обновления (резорбции и остеогенеза), который продолжается в течение всей жизни. После прекращения линейного роста, когда масса костной ткани достигает максимума, дальнейшие ее изменения в конечном счете определяются именно динамикой процессов обновления. Эти процессы независимо протекают в огромном количестве отдельных участков — единиц костного обновления (рис. 62.2)
Рисунок 62.2. Цикл обновления костной ткани.
. Обновление происходит на костной поверхности, примерно 90% которой в норме неактивно и покрыто тонкой клеточной выстилкой. В ответ на физические или биохимические сигналы костномозговые клетки-предшественники перемещаются к поверхности кости и, сливаясь друг с другом, превращаются в характерные многоядерные остеокласты; последние резорбируют расположенный под ними костный слой, образуя в нем углубления.
Образование остеокластов регулируется цитокинами (например, М-КСФ, ИЛ-1, ИЛ-6, фактором дифференцировки остеокластов), которые вырабатываются остеобластами. Недавние исследования проливают свет на механизмы этого процесса (Suda et al., 1999). Белок, продукция которого необходима для образования активных остеокластов, получил название RANK (Receptor for Activating NFkB“- рецептор, активирующий фактор транскрипции NFkB). Естественным лигандом этого рецептора служит фактор дифференцировки остеокластов (называемый также RANK-лигандом), расположенный на мембране остеобластов. Взаимодействуя с белком RANK, фактор дифференцировки остеокластов индуцирует созревание остеокластов. Действительно, антитела к этому фактору предотвращают усиливающее резорбцию действие многих регуляторов обновления костной ткани (Yasuda et al., 1998). Фактор дифференцировки остеокластов не только запускает дифференцировку предшественников остеокластов, но и активирует зрелые остеокласты (Jimi et al., 1999). Ц Остеобласты вырабатывают также растворимый ингибитор, называемый остеопротегерином, который выступает в роли ложного рецептора для фактора дифференцировки остеокластов. В условиях, способствующих усилению резорбции костной ткани (например, при дефиците эстрогенов), выработка остеопротегерина угнетается, фактор дифференцировки остеокластов свободно взаимодействует с белком RANK и образование остеокластов усиливается. При восстановлении уровня эстрогенов выработка остеопротегерина увеличивается и он препятствует связыванию фактора дифференцировки остеокластов с рецептором.
В результате резорбции в компактном веществе кости образуются туннели в каналах остеонов, а в губчатом веществе — неровные участки поверхности, носящие название резорбцион-ных (гаушиповых) лакун. По окончании резорбции остается полость глубиной около 60 мкм, граничащая в своей самой глубокой части с линией склеивания (областью рыхло организованных коллагеновых волокон). По завершении стадии резорбции на дно полости поступают преостеобласты, образующиеся из клеток стромы костного мозга. Преостеобласты приобретают характерные черты остеобластов и начинают восстанавливать резорбированную кость, образуя новые компоненты органического матриксаколлаген, остеокальцин и другие белки. Как только слой новообразованного органического матрикса достигает примерно 20 мкм, начинается его минерализация. Весь цикл обновления в норме занимает около 6 мес.
Если остеогенез количественно соответствует резорбции то обновление не приводит к изменению массы ткани. Однако в силу недостаточной эффективности обновления после каждого его цикла сохраняется небольшой дефицит массы. С годами такой дефицит увеличивается, чем и объясняется известное уменьшение массы костной ткани, начинающееся вскоре после прекращения роста. Изменение скорости обновления — это общий конечный механизм влияния различных стимулов (недостаточного питания, гормонов, лекарственных средств и т. п.) на состояние костей. Общая скорость обновления костной ткани зависит от динамики отдельных составляющих этого процесса. Гормональные изменения часто приводят к активации обновления костной ткани или увеличению количества единиц костного обновления. Это происходит, например, при тиреотоксикозе, гиперпаратиреозе и гипервитаминозе D. Другие факторы в частности высокие дозы глюкокортикоидов и этанол, нарушают функцию остеобластов. Наконец, дефицит эстрогенов, по-видимому, усиливает активность остеокластов (Marcus 1987; Dempster, 1992).
В каждый момент времени существует некоторый дефицит массы костной ткани, который определяется еще не заполненными очагами резорбции. В ответ на любой стимул, изменяющий скорость появления новых единиц костного обновления, этот дефицит увеличивается или уменьшается, пока не установится новое равновесие между резорбцией и остеогенезом.
Читайте основную статью:
Физиология восстановления костной ткани
Диагностика
Нарушение метаболизма кальция определяется путем лабораторных анализов. Для определения причины патологии требуются более обширные исследования, поэтому специалисты назначают аппаратные исследования. Дополнительно может быть проведена дифференциальная диагностика.
Методы обследования:
- анализ мочи (общий) — при повышенных показателях Ca в биоматериале будет присутствовать минерал и щелочная реакция будет выраженной;
- анализ крови (биохимический) — в плазме выявляется значительное превышение/понижение ионизированного, а так же общего кальция;
- ультразвуковое исследование — обследуется вся эндокринная система на наличие новообразований, увеличение тканей и другие отклонения;
- рентгенография — используется для обследования костей с целью определения возможного развития остеопороза, переломов, кистозных образований и других патологических процессов;
- денситометрия — применяется для точного определения плотности тканей костей;
- рентгенография (с контрастным веществом) — помогает выявлению язвенного поражения ЖКТ и паратиреоаденому в загрудинном пространстве;
- компьютерная — томография — исследуется мочевыделительная система и почки на наличие камней;
- магниторезонансная томография — позволяет получить максимально точные данные об опухолевых образованиях желез щитовидки;
- спинтиграфия — исследование с применением радиоактивных изотопов, с помощью которого удается визуализировать исследуемую область.
Диагностика позволяет получить максимальное количество информации для выявления провоцирующих факторов, особенностей заболевания и возможных осложнений. Лечение может начинаться только после получения результатов обследования.
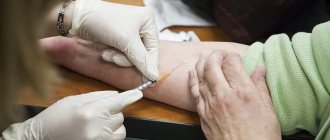
![Таблица 1. Биоусвояемость (абсорбция) различных органических форм кальция в течение 2 ч после перорального приема в эксперименте [22]](https://laram-halal.ru/wp-content/uploads/tablica-1-biousvoyaemost-absorbciya-razlichnyh-organicheskih-form-kalciya-v-techenie-330x140.jpg)