Нейромидин – это особый препарат, который не относится ни к миорелаксантам, ни к обезболивающим, ни к противовоспалительным средствам. Его нет ни в одном международном и отечественном протоколе лечения острой боли в спине, и тем более – когда боль вызвана дискогенными осложнениями остеохондроза (протрузиями и грыжами). Стоимость Нейромидина достаточно высока, и превышает 1000 рублей. Разберемся: применение Нейромидина при грыже позвоночника действительно помогает, или же это просто трата денег впустую?
Вопрос этот далеко не праздный. Межпозвонковые протрузии и грыжи имеют все признаки «удобных» заболеваний для знахарей и шарлатанов. Вот эти признаки:
- непосредственной угрозы жизни или инвалидизации нет;
- межпозвонковых дисков много, и беспокоят боли часто;
- острая, дискогенная боль в спине течет долгие годы, со сменой обострений и ремиссий, и пациента можно «пользовать» много лет, поскольку боль проходит и так, а применяя какое – либо сомнительное средство, можно внушить пациенту, что помогло именно оно;
- выраженность боли – высокая, а при люмбаго пациент несколько дней не может повернуться и рассмеяться, так как воспаленные корешки нервов тут же отдаются «прострелом», и в это время пациент готов на все.
Таким образом, вариантов консервативно «полечить» грыжу есть множество: мази, кремы, кинезиотерапия и краниосакральное воздействие, массаж и физиотерапия, мануальные техники и блокады. Следует помнить одно: все эти методы лечения не имеют отношения к грыже, как к дефекту межпозвонкового диска. Они помогают устранить неприятные симптомы, которые вызвала грыжа, «натирая» нервные корешки, связки и мышцы.
Все без исключения консервативные способы лечения помогают только лишь снять боль и увеличить объем движений в спине, но при этом — это не свидетельство радикального излечения. Это результат уменьшения воспаления, боли и отека, улучшения кровоснабжения окружающих тканей и снижения мышечного тонуса. Грыжа вновь проявит себя, возможно, она увеличится, и эти методы консервативного лечения перестанут помогать. Тогда спасет только операция.
Современная спинальная нейрохирургия
Лишь современное малоинвазивное оперативное вмешательство (например, видеоэндоскопическая микродискэктомия, или лазерная вапоризация и нуклеопластика) может удалить сам грыжевой дефект, или воспрепятствовать его появлению в случае наличия протрузии. Однако, российский пациент прекрасно знает, что такое операция. Это больно. Это надолго выводит из нормальной жизни. Это может быть опасно. Таких «но» набирается так много, что операцию считают последним видом лечения, когда перестают помогать массажисты, сеансы карбокситерапии, «мануальщики» и кинезитерапевты.
К счастью, в странах Европы, Израиле, США – подход совсем другой. Если есть показания, то пациент оперируется без боли, и зачастую в тот же день, или на следующий, покидает стационар на собственных ногах. Качество жизни у него сохраняется. Ему не запрещается сидеть в течение многих дней, и он не вынужден справлять большую нужду стоя. Поэтому там современную операцию считают лучшим, быстрейшим и эффективным средством радикального лечения. Кстати, врачи многих страны Восточной Европы, например, Чехии, показывают отличные результаты лечения грыж оперативным путем при довольно скромных затратах.
В России же предпочитают не удалять сразу грыжевое выпячивание, а многие годы бороться с его последствиями и осложнениями – периодически лечить воспаление, боли и отек корешков, которые упорно возникают снова и снова. И в этом отношении отечественный пациент напоминает несчастного водителя, который вместо того, чтобы, наконец, поменять проколотое колесо, вынужден накачивать его через каждые полчаса езды. Только в отличие от водителя, пациент, длительно «лечащий» грыжу, подчас тратит в несколько раз больше денег, чем стоила бы операция.
Грыжа шейного отдела на МРТ.
Но даже в ряду лекарств для снятия отека, боли в спине, избыточного мышечного напряжения Нейромидин не «числится». Однако, его иногда назначают при грыжах, и совершенно неоправданно. Ситуация усугубляется невообразимо большим количеством сайтов, которые написаны с потрясающей медицинской безграмотностью. Ибо если есть запрос «Нейромидин при грыжах как принимать», то тут же появится услужливая, но безграмотная статья, которая даже может нанести вред здоровью. Как принимать Нейромидин при грыжах? Никак не принимать. Но обо всем по порядку….
Механизм действия препарата
Известно, что от нервов приказ мышцам на сокращение отдает ацетилхолин, который выбрасывается в синаптическую щель – место связи нерва с мышцей. Ацетилхолин, если его не убрать вовремя, будет держать мышцу в длительном сокращении. Поэтому «очистка» синаптической щели от ацетилхолина очень важна, и им занимается фермент ацетилхолинэстераза. Так вот, Нейромидин ее угнетает, и ацетилхолин дольше циркулирует в синаптической щели, и импульс становится ярче, продолжительнее, активнее. Он влияет на уровне каналов калия. В итоге улучшается нейромышечная передача, сократимость гладкой мускулатуры.
Показания к применению: можно ли применять при грыжах?
Поэтому применять Нейромидин следует там, где есть дефект нейромышечной передачи (например, слабость и вялость мышц, когда есть наследственный дефицит ацетилхолина). Это миастения и различные мистеноподобные синдромы.
Второе показание – это собственно плохие нервы, по которым импульс проводится плохо, с потерями. Это полинейропатия, например, при сахарном диабете, или алкогольная полинейропатия. В последнем случае многолетнее употребление алкоголя привело к разрушению нервов, а в первом случае – высокий уровень сахара. Сюда же примыкают и демиелинизирующие заболевания, например, рассеянный склероз, когда миелиновая оболочка нервов дефектная, и часто возникает «короткое замыкание» и нарушение передачи импульса вследствие плохой изоляции.
Обширная группа показаний – это различные параличи и парезы, когда нейроны очень плохо генерируют импульс, и тогда нужно на периферии, в месте подхода аксона нерва к мышце хоть как-то его усилить. Это бульбарные параличи, парезы с двигательным дефицитом.
Наконец, вследствие влияния на гладкую мускулатуру Нейромидин показан при низком тонусе кишечника и для лечения атонических запоров.
Нужна ли улучшенная нейромышечная передача при грыжах?
Конечно, нет. Вспомним, что:
- двигательные нейроны, которые «приказывают» сокращаться мышцам спины, лежат в передних рогах спинного мозга, и весьма далеко от грыжи, которая никакого влияния на них не оказывает;
- улучшение нейромышечной передачи приводит к усилению импульса и долгому времени действия. При грыжах, напротив, мышцы излишне спазмированы, и их, напротив, нужно ослаблять, снимая с них излишний потенциал действия.
И, наконец, «вишенка на торте»: ацетилхолин – это медиатор парасимпатической нервной системы, и он не имеет ну никакого отношения к мышцам туловища или поясничного отдела. Нейромидин стимулирует такие эффекты, как:
- замедление сердечных сокращений и расширение сосудов на периферии;
- снижение артериального давления;
- усиление перистальтики кишечника;
- сокращение мышц желчного пузыря, бронхов и матки;
- улучшенная секреция пищеварительного сока;
- стимуляция работы слезных и потовых желез, а также уменьшение зрачков, в связи с влиянием на парасимпатическую часть глазодвигательного нерва.
Кроме этого, ацетилхолин является нервным медиатором внутри центральной нервной системы, и циркулирует внутри головного мозга. Его дефицит может вызвать болезнь Альцгеймера, и поэтому Нейромидин может ещё применяться, как препарат, помогающий замедлить прогрессирование симптомов этого заболевания.
Как видно, никакого отношения к грыже межпозвонковых дисков это средство не имеет, и иметь не может. Его механизм действия лежит вне влияния на воспаление, боль, отек и мышечный спазм, который и имеет место при протрузиях и грыжах.
Побочные эффекты и противопоказания
Нейромидин — это серьезный препарат. Если его применять в высоких дозах, то может быть боль за грудиной, рвота, головокружение, головная боль. У женщин может повышаться тонус матки. Поскольку стимулируются мускариновые холинорецепторы, то в качестве симптомов передозировки у пациентов может быть диарея, потливость, сердцебиение, появится избыточное отхождение мокроты, вплоть до признаков бронхоспазма, могут возникать даже и судороги.
Перечень противопоказаний для приёма Нейромидина также достаточно внушительный. Это беременность, период грудного вскармливания, а также детский и подростковый возраст, включая 18 лет. Препарат категорически запрещен у пациентов с:
- эпилепсией;
- головокружениями и вестибулопатиями;
- с синдром слабости синусового узла и редкими сердечными сокращениями, при наличии брадикардии;
- при бронхиальной астме и стенокардии;
- при непроходимости кишечника, или обструкции мочевыводящих путей;
- препарат категорически запрещен у пациентов с наличием язвенной болезни желудка и двенадцатиперстной кишки и особенно — в стадии обострения.
Существует и перечень заболеваний, когда Нейромидин применять по показаниям можно, но с большой осторожностью. Это различные обструктивные заболевания легких, бронхит и, тиреотоксикоз, болезни сердечно-сосудистой системы, при наличии панических атак, и кардионевроза, поскольку препарат может снижать порог судорожной готовности.
Категорически запрещается употреблять в процессе лечения алкоголь, поскольку количество побочных эффектов препарата совместно с этиловым спиртом усиливается. На фоне лечения Нейромидином пациент не должен водить автотранспорт, а также работать на производстве при наличии факторов риска, поскольку препарат не может гарантировать быстроту психомоторных реакций и хорошей концентрации внимания
Роль нейромидина в реабилитации больных вестибулярной дисфункцией
Реабилитация больных вестибулярной дисфункцией остается одним из актуальных и приоритетных направлений в современной оториноларингологической практике. Медицинская и социальная значимость проблемы определяется высоким уровнем заболеваемости, стойкой утратой трудоспособности вследствие тяжелого вегетосоматического симптомокомплекса и развития тугоухости, сопровождающих течение болезни [3, 4, 10, 14, 15, 16]. Ограничение возможности полноценного общения, обусловленное в том числе и нарушением слуховой рецепции, приводит к существенному снижению качества жизни больных вестибулярной дисфункцией [2].
Лечебная тактика традиционно основывается на знаниях об этиологии и патогенезе вестибулярных расстройств. Однако отсутствие единой концепции развития нарушений в функциональной системе равновесия [1, 4, 10, 16] приводит к многообразию методов консервативного лечения заболевания, большинство из которых эмпиричны, а наблюдаемый клинический эффект порой трудно объясним [9]. Понижение слуха связывают с нарушением гемо- и ликвородинамики, обменных процессов рецепторных клеток, ионного состава жидкостей внутреннего уха. Немаловажную роль в ухудшении слухового восприятия отводят изменениям холинергической медиации [6, 7, 8]. В связи с этим в схемы лечения больных включают вещества антихолинэстеразного действия, применяемые курсами в межприступном периоде. Новым препаратом этого ряда является ипидакрин (нейромидин).
Механизм фармакологической активности препарата основан на блокаде калиевой проницаемости клеточной мембраны и обратимом ингибировании холинэстеразы, способствующих повышению активности пресинаптического аксона и стимуляции нейромышечной проводимости.
Нами проведена оценка эффективности реабилитации больных вестибулярной дисфункцией периферического уровня при дополнении комплексного лечения ипидакрином (нейромидином). Обследовано 64 больных находившихся на стационарном лечении в клинике болезней уха, носа и горла СамГМУ. Среди обследованных 21 мужчина (32,8%), 43 женщины (67,2%), средний возраст больных — 48,8±0,5 лет. В 85,9% наблюдениях диагностировано одностороннее поражение, в 14,1% случаев заболевание носило двусторонний характер. Средняя давность вестибулярной дисфункции составила 14,8±0,3 года. Развитие вестибулярных расстройств у всех пациентов предшествовало появлению нарушений слуховой функции. Основной жалобой являлись приступы системного головокружения, сопровождающиеся нарушением походки и расстройством равновесия, понижение слуха флюктуирующего характера, у 24 человек (37,5%) страдала разборчивость речи, шум в ушах беспокоил 31 больного (48,4%).
Основную группу составили 30 пациентов с вестибулярной дисфункцией периферического уровня, из них 11 мужчин (36,7%), 19 женщин (63,3%); средний возраст больных в группе 49,2±0,4 года. В контрольную группу вошли 34 пациента: 10 мужчин (29,4%), 24 женщины (70,6%); средний возраст 48,4±0,5 лет. Всем больным до начала лечения и после его завершения проведена акуметрия, вестибулометрия, оценка качества жизни по опроснику SF-36.
Комплексная схема лечения включала использование медикаментозных средств, улучшающих гемомикроциркуляцию и обменные процессы мозга, меатотимпанальные, внутриносовые блокады по Агеевой–Майковой, занятия лечебной физкультурой. Пациенты основной группы дополнительно получали ипидакрин (нейромидин) в таблетках по 20 мг 3 раза в сутки после еды в течение 21 дня. Критерием ограничения использования препарата в основной группе больных вестибулярной дисфункции периферического уровня стало наличие нарушений сердечного ритма и тяжелых форм стенокардии. Использование в комплексной схеме лечения ипидакрина (нейромидина) ни у одного пациента основной группы не вызвало ухудшения вестибулярной симптоматики.
Для характеристики выраженности жалоб и субъективных ощущений больного вестибулярной дисфункцией периферического уровня нами использована оценочная шкала в баллах. У пациентов основной группы положительная динамика состояния слуховой функции и уменьшение интенсивности ушного шума отмечены уже на 6–7-е сутки лечения, аналогичные изменения у больных контрольной группы наблюдались на 10-й день.
Анализ динамики порогов тонального слуха при воздушном (ВП) и костном проведении (КП) был выполнен с учетом степени потери слуха. Для оценки влияния препарата у пациентов с начальными потерями слуха выделяли 0 степень тугоухости, соответствующую понижению слуховой чувствительности на тоны в зоне речевых частот до 10 дБ. I степень понижения слуха характеризовалась повышением порогов слуха в указанном диапазоне на 11–40 дБ, II степень — на 41–60 дБ, III степень — на 61–80 дБ.
У всех обследованных основной и контрольной группы после проведенного курса лечения определялась положительная тенденция динамики порогов тонального слуха. Изменение слуховой чувствительности оказались наиболее показательными при 0 и I степени понижения слуха.
Пороги тонального слуха при ВП у больных основной группы с 0 степенью тугоухости снизились с 10,0±0,01 дБ, при I степени — на 1,7±0,3 дБ, при II степени — на 5,0±0,01 дБ. Пороги тонального слуха при КП также имели тенденцию к улучшению: при 0 степени — на 2,5±0,9 дБ, при I степени — на 3,3±2,1 дБ. У больных со II степенью тугоухости по КП и III степени понижения слуха по ВП и КП динамики не наблюдалось. На частотах 4000–8000 Гц существенной динамики слуховой чувствительности не выявлено. Незначительное улучшение тонального слуха по КП определялось у лиц со II степенью тугоухости, по ВП у больных с III степенью понижения слуха.
В контрольной группе пороги тонального слуха при воздушном проведении у больных с 0 степенью тугоухости не изменились, при I степени снизились на 2,5±7,5 дБ, при II степени снизились на 5,0±0,01 дБ. Пороги тонального слуха при костной проводимости также имели тенденцию к улучшению при 0 степени на 2,5±2,5 дБ, при I степени на 2,9±0,6 дБ. При II степени по КП и III степени тугоухости по ВП и КП изменений не выявлено. На частотах 4000–8000 Гц наблюдалось незначительное улучшение тонального слуха по КП у лиц с 0 степенью тугоухости и по ВП у больных с I степенью понижения слуха.
Сравнительная оценка динамики слуховой чувствительности на тоны речевого и высокочастотного диапазона свидетельствовала о больших положительных сдвигах у больных, получающих в комплексном лечении ипидакрин (нейромидин).
Достоверных изменений дифференциального порога восприятия силы звука (ДПВСЗ) на частотах 500, 1000, 2000, 4000 Гц у больных основной и контрольной групп нами не выявлено (p > 0,05). Изменение порогов 50% и 100% разборчивости речи у пациентов обеих групп характеризовалось тенденцией к улучшению. Выявлена прямая корреляционная взаимосвязь (r = 0,31, p < 0,05) результата лечения по слуховой функции от давности заболевания.
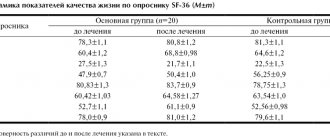
Для оценки показателя качества жизни больных вестибулярной дисфункцией периферического уровня нами использовался неспецифический опросник SF-36, позволяющий определить физический и психологический компоненты здоровья больного. Согласно проведенному анализу у больных основной группы отмечено улучшение общего состояния здоровья и перспектив лечения с 42,5±3,7 до 56,4±6,2 балла. Психологический компонент здоровья возрос за счет повышения степени социальной активности (SF) на 9,26±2,3 балла, жизненной активности больного (VT) на 5,4±1,9 балла и его эмоционального состояния.
В контрольной группе аналогичные изменения качества жизни как основного критерия эффективности проводимых реабилитационных мероприятий характеризовались меньшими значениями и наблюдались у меньшего количества больных.
Таким образом, включение ипидакрина (нейромидина) в комплексную схему лечения больных вестибулярной дисфункцией периферического уровня позволило добиться большего улучшения слуховой функции и показателей качества жизни. Результаты комплексной акуметрии обосновывают необходимость возможно раннего назначения препарата уже при начальных степенях нарушения слуха. Использование ипидакрина (нейромидина) в комплексной программе реабилитации при вестибулярной дисфункции периферического уровня в межприступном периоде не привело к появлению вестибулярной симптоматики.
Литература
- Аськова Л. Н. Болезнь Меньера. Издат. Саратов. Универ., Самарский филиал, 1991. 254 с.
- Бабияк В. И., Митрофанов В. В. Некоторые психолого-философские аспекты проблемы «качество жизни человека»//Сб. тр. Всероссийской конференции. Проблема реабилитации в оториноларингологии. Самара, 2003. С. 36-40.
- Бабияк В. И., Ланцов А. А., Базаров В. Г. СПб.: Гиппократ, 1996. С. 130-143.
- Гофман В. Р. История развития вестибулологии на кафедре оториноларингологии Военно-медицинской академии//Теоретические и практические проблемы современной вестибулологии: Тез. докл. Всероссийской научной конференции 29-30 октября 1996. СПб., 1996. С. 15-24.
- Еремина Н. В. Медицинский аспект реабилитации больных с вестибулярными нарушениями: Автореф. дис. … д-ра мед. наук. Самара, 2000. 508 с.
- Нехамкина Г. С., Храппо Н. С., Миркина А. Я. К изучению состояния холинергической системы при отосклерозе и болезни Меньера//Негнойные заболевания уха: Тр. Куйбыш. мед. ин-та им. Д. И. Ульянова. Куйбышев, 1975. Т. 95. С.125-129.
- Пальчун В. Т., Буяновская О. Я., Алмазова В. И. Роль осмолярности сыворотки крови в патогенезе болезни Меньера//Вестн. оториноларингологии. 1983. № 3. С. 3-7.
- Плужников М. С., Комарович Г. М., Янтарева Л. И. О содержании свободного ацетилхолина в перилимфе человека//Вестн. оториноларингологии. 1972. № 5. С. 28-32
- Сагалович Б. М., Пальчун В. Т. Болезнь Меньера. М.: МИА, 1999. С. 433-435.
- Солдатов И. Б. Физиология и патология вестибулярного аппарата//Восьмой съезд оториноларингологов СССР: Тезисы докладов. Суздаль, 1982. С. 177-184.
- Солдатов И. Б., Храппо Н. С. Острая вестибулярная дисфункция и ее лечение: Методическое письмо для врачей оториноларингологов. Куйбышев, 1975. 13 с.
- Солдатов И. Б., Храппо Н. С. Медикаментозное лечение болезни Меньера//Патология органа слуха: Сб. тр. Моск. НИИ уха, горла и носа. М., 1984. С. 50-57.
- Солдатов И. Б., Сущева Г. П., Храппо Н. С. Вестибулярная дисфункция. М.: Медицина, 1980. С. 182-188.
- Руководство по оториноларингологии/Под ред. И. Б. Солдатова. М.: Медицина. 1997. 608 с.
- Шварцман Н. А. Некоторые вопросы патогенеза лабиринтных дисфункций /Журнал ушных, носовых и горловых болезней. 1984. № 2. С. 48-55.
- Янов Ю. К., Новиков В. С., Герасимов К. В. Начала системного анализа в клинической и экспериментальной вестибулологии. СПб.: Наука, 1997. 240 с.
Н. В. Еремина, доктор медицинских наук, профессор Т. Ю. Владимирова Самарский государственный медицинский университет, Самара
Взаимодействия с другими лекарствами
Также Нейромидин может взаимодействовать с другими лекарственными средствами. Он усиливает свой седативный эффект, если вы применять с препаратами, угнетающими центральную нервную систему, например со снотворными препаратами, транквилизаторами из группы бензодиазепинов или совместно с барбитуратами. Напомним, что известный представитель барбитуратов — фенобарбитал входит в состав Валокордина и Корвалола, которые продаются без рецепта. Если сочетать прием Нейромидина с бета-адреноблокаторами, которые уменьшают частоту сердечных сокращений и работу сердца, то возникает риск брадикардии, коллаптоидного и обморочного состояния.
Нейромидин
Препарат нейромидин — это м-, н-холиномиметик, относящийся к группе антихолинэстеразных средств и используемый в лечении заболеваний периферической и центральной нервной системы, а также атонии кишечника (в данном случае — только таблетки). Долгие годы в практике врача-невролога использовался (и используется до сих пор) препарат прозерин, обладающий мощным действием на постганглионарные холинэргические синапсы. Сегодня в целом ряде случаев клиницисты предпочитают лекарственное средство нейромидин, как препарат, несомненно, более широкого диапазона фармакологической активности, который с успехом может применяться не только при заболеваниях периферической нервной системы, но и в случаях органических поражений центральной нервной системы. Достоинством нейромидина является его хорошая переносимость и наличествующий минимум негативных побочных эффектов, что открывает дополнительные возможности для его использования у пациентов пожилого возраста, страдающих множеством коморбидностей. О том, как действует данный препарат, о его преимуществах и особенностях применения можно будет узнать из настоящей статьи.
Нейромидин стимулирует проведение волн возбуждения по нервным волокнам и синапсам центральной и периферической нервной системы. Его действие развивается по двум направлениям: блокада калиевых каналов в мембранах нейронов и миоцитов и временное подавление активности фермента холинэстеразы в межнейрональных и нервно-мышечных синапсах. При этом нейромидин потенцирует действие не только ацетилхолина но и других медиаторов, включая серотонин и гистамин.
В результате этого помимо оптимизации проводимости нервных импульсов и нервно-мышечной передачи препарат усиливает сократительные способности гладкомышечных клеток, а также улучшает память. Начальный эффект инъекционного введения нейромидина отмечается, в среднем, через 15–20 минут и длится еще 3–5 часов, что обусловлено продолжительной блокадой калиевых каналов (в то время как эффект прозерина сходит на нет спустя 2–3 часа после однократной инъекции). Нейромидин, отличие от прозерина, в большинстве случаев хорошо переносится пациентами: побочные эффекты если и возникают, то слабовыраженные, не требующие прекращения фармакотерапии. При приеме препарата следует воздержаться от потребления алкоголя, в противном случае можно собственными руками «сотворить» для себя целый «букет» негативных побочных реакций.
Нейромидин выпускается в двух лекарственных формах: раствор для внутримышечного или подкожного введения и таблетки. Что касается доз и продолжительности использования препарата, то здесь все очень индивидуально: врач оценивает степень тяжести заболевания еще целый ряд факторов, прежде чем определиться с тактикой лечения. При передозировке нейромидина следуют известному в народе принципу «клин клином вышибают»: в преломлении на биохимические реалии он будет заключаться в приеме препаратов группы м-холиноблокаторов (атропин, циклодол и т.д.).
Формы выпуска и аналоги
Нейромидин содержит действующее вещество — ипидакрин, выпускается он в виде таблеток, а также раствора для инъекций. Таблетки продаются в упаковке по 20 мг № 50, а раствор для инъекций – в виде двух дозировок. Первая — 5 мг на миллилитр, а вторая втрое более концентрированная: 15 мг на миллилитр ипидакрина. В одной упаковке находятся 10 ампул.
Применять Нейромидин при полинейропатии желательно, в среднем, по одной таблетке от одного до 3 раз в день, курс лечения — от одного до 2 месяцев. В случае тяжелых миастенических кризов вводят внутривенно Нейромидин по одному или два мл, то есть до 30 мг раствора 1,5%, а затем переходят на таблетированную форму.
При тяжелых параличах пациенту назначают по 1 таблетке 3 раза в сутки длительным курсом, до 6 месяцев. При наличии атонии кишечника дозировка такая же, одна таблетка 2-3 раза в сутки, но курс короткий — не более 2 недель. Максимальная суточная доза не должна составлять более 10 таблеток, Или 200 мг.
Сам Нейромидин стоит недешево: одна упаковка таблеток, которую хватит на две недели применения (1 таблетка 3 раза в день) стоит, в среднем 1350 руб. Производит Нейромидин латвийская компания Олайнфарм.
Аналогом является словацкий (НВМ-фарма) препарат Ипигрикс (1100 рубля за такую же упаковку), а также отечественный Аксамон. Выпускает его Пик – фарма, по средней цене 1263 руб. за упаковку в 50 табл.
Сенсоневральная тугоухость (СНТ) наблюдается почти у 3/4 больных, страдающих расстройством слуха, и относится к заболеваниям, проблема диагностики и лечения которых не теряет своей актуальности в течение многих десятилетий. Сенсоневральная (перцептивная) тугоухость — это поражение различных отделов слухового анализатора — от волосковых клеток улитки (в большинстве случаев) до слуховой зоны коры головного мозга.
В последнее время увеличивается количество пациентов с сенсоневральной тугоухостью в возрасте 20-40 лет, впервые обратившихся за помощью к врачу сурдологу-оториноларингологу. Такие пациенты предъявляют жалобы на снижение слуха, шум в ушах, нередко причиняющий дискомфорта больше, чем при нарушении слуха [1-3].
Широкая распространенность поражений органа слуха в современных условиях обусловлена большим количеством неблагоприятных факторов, приводящих к возникновению тугоухости и глухоты. При всем многообразии причин возникновения СНТ, в ее патогенезе ведущую роль играют нарушения микроциркуляции вплоть до капиллярного стаза, что приводит к ишемии волосковых клеток улитки [4].
В клинической картине острой СНТ ведущее место занимают жалобы на внезапное ухудшение слуха, ощущение заложенности уха, ушной шум и нередко головокружение [5, 6]. Современный подход к диагностике поражений органа слуха диктует необходимость проведения многопланового обследования больного, включающего исследование функции звукопроводящей и звуковоспринимающей систем, вестибулярного анализатора, изучение показателей свертывающей системы крови и функции печени, оценку состояния сердечно-сосудистой, выделительной и эндокринной систем, что дает возможность установить причину заболевания и выбрать наиболее эффективную лечебную тактику.
Лечение пациентов с СНТ остается актуальной проблемой современного здравоохранения. Это определяется ростом числа слабослышащих лиц в индустриально развитых странах, возрастающей социальной значимостью дефектов слуха, малой результативностью лечения [7].
Особое внимание следует обратить на то, что только максимально рано начатое лечение будет эффективным. С учетом особенностей заболевания используются медикаментозные препараты, улучшающие кровоснабжение, в том числе внутреннего уха, церебральную гемодинамику и реологические свойства крови, антихолинэстеразные средства, ноотропные препараты, витамины группы В, лекарственные препараты, обладающие антиоксидантной направленностью и т.д. [1, 4, 5, 8]. Следует отметить, что при использовании комплекной терапии с прозерином в 45% случаев положительной динамики не наблюдалось.
Для улучшения проводимости нервных импульсов от рецептора до коры полушарий мозга, усиления холинергической медиации при лечении СНТ различной этиологии с успехом применяют антихолинэстеразный препарат нейромидин — оригинальный модулятор нейропластичности, выпускаемый в таблетированной и инъекционной формах [9-11]. В отличие от других препаратов этой группы, временно инактивирующих фермент ацетилхолинэстеразу в синапсах, нейромидин дополнительно вызывает блокаду калиевой проницаемости мембраны. Это приводит к продлению реполяризационной фазы потенциала действия и повышению активности пресинаптической мембраны, последующему увеличению входа ионов кальция в пресинаптическую терминаль и, как следствие, усилению выброса медиатора в синаптическую щель во всех синапсах.
Цель работы — оценка эффективности применения нейромидина для лечения СНТ различной этиологии.
Пациенты и методы
За последние 3 года в сурдологическом отделении ГБУЗ «Самарская областная клиническая больница
им. М.И. Калинина» проводилось наблюдение за 230 пациентами с СНТ. Из них 32 пациента с острой СНТ.
К возрастной группе от 40 до 60 лет относятся 168 пациентов. Основной причиной СНТ в этой группе были сосудистые расстройства — гипертоническая болезнь, атеросклероз сосудов головного мозга, транзиторные ишемические атаки. У 24 пациентов в группе от 20 до 40 лет причиной СНТ явились острые вирусные инфекции, у 6 — акустические и баротравмы, у 21 — сосудистые нарушения (вегетососудистая дистония), у 5 — интоксикации, у 6 — черепно-мозговые травмы. Среди пациентов с диагнозом СНТ женщины составляли 65%. Критериями исключения из исследования являлись наличие у пациентов выраженных стенокардии и брадикардии, беременность или период лактации, эпилепсия, механическая непроходимость кишечника и мочевыводящих путей.
Пациенты 1-й группы (100 человек) получали традиционные методы лечения — прозерин по 1 мл 0,05% раствора внутримышечно в течение 10 дней, трентал внутривенно с глюкозой в течение 10 дней, пирацетам — 20% раствор по 2-6 г/сут в 0,9% растворе хлорида натрия внутривенно капельно ежедневно, всего 5 инъекций, никотиновая кислота — 0,1% раствор, начиная с 1 мл, увеличивая дозу до 5 мл, затем снижая ее до 1 мл внутримышечно или внутривенно; стугерон (циннаризин) по 0,05 г 2-3 раза в сутки внутрь во время еды. При острой СНТ к терапии добавлялись глюкокортикоиды — дексаметазон (4 мг/сут), преднизолон (30-60 мг/сут) внутримышечно или внутривенно.
Пациентам 2-й группы (130 человек) в вышеуказанной комплексной терапии вместо прозерина назначали внутримышечно препарат нейромидин по 1 мл 1,5% раствора для инъекций (15 мг/сут) в течение 10 дней и далее в таблетках по 20 мг 3 раза в день в течение месяца. Оценку эффективности до и после лечения проводили с помощью клинико-аудиометрического исследования и реоэнцефалографии (РЭГ).
Результаты и обсуждение
У большей части пациентов отмечено улучшение слуха и разборчивости речи, а при острой СНТ в ряде случаев полное восстановление слуха. Эффективность терапии напрямую зависела от сроков начала лечения. Улучшение и полное восстановление отмечали у пациентов, обратившихся в срок до 10 дней с момента потери слуха.
Субъективно отметили улучшение слуха и разборчивости обращенной к ним речи 28,5% пациентов 1-й группы и 54,3% пациентов 2-й группы. Уменьшение субъективного ушного шума отметили 25,7 и 47,1% больных соответственно. Понижение порогов слуховой чувствительности на частотах 500-2000 Гц при воздушном звукопроведении зарегистрировано у 28,6 и 54,3% пациентов, при костном — в 30,6 и 54,3% наблюдений. Аналогичные изменения были отмечены на частоте 4000 Гц: у 28,6% в 1-й группе и у 47,1% во 2-й группе, причем чаще у лиц с нарушением слуха шумового генеза. Улучшение показателей церебральной гемодинамики наблюдалось у 28,6 и 54,3% пациентов соответственно. Это проявлялось увеличением объемного кровенаполнения, уменьшением межполушарной асимметрии кровенаполнения, улучшением венозного кровотока.
Обращают на себя внимание результаты лечения больных, которые, наряду с базисной терапией, принимали нейромидин: возросло число случаев полного выздоровления и резко снизилось число случаев без динамики в отличие от группы лиц, не принимавших препарат. Кроме того, субъективно пациенты отмечали уменьшение шума в ушах.
Побочных эффектов во время приема нейромидина выявлено не было.
Выводы
Таким образом, применение препарата нейромидин внутримышечно по 1 мл 1,5% раствора для инъекций (15 мг/сут) в течение 10 дней и далее в таблетках по 20 мг 3 раза в день в течение месяца обосновано и необходимо в лечении сенсоневральной тугоухости, в том числе острой формы. Нейромидин обладает высокой клинической эффективностью, хорошей переносимостью, не оказывает серьезных побочных эффектов даже при длительном применении, что позволяет повысить эффективность терапии и улучшить качество жизни пациентов.