Альтевир (Интерферон альфа-2b) раствор для инъекций, 5млн МЕ/мл амп 1мл N5
Владелец регистрационного удостоверения
ФАРМАПАРК (Россия)
Лекарственная форма
Лекарственный препарат — Альтевир® (Altevir)
Описание
Раствор для инъекций
прозрачный, бесцветный.
1 мл
человеческий рекомбинантный интерферон альфа-2b 3 млн.МЕ
Вспомогательные вещества
: натрия ацетат, натрия хлорид, этилендиаминтетрауксусной кислоты динатриевая соль, твин-80, декстран 40, вода д/и.
1 мл — ампулы (5) — упаковки ячейковые контурные (1) — пачки картонные. 1 мл — ампулы (5) — упаковки ячейковые контурные (2) — пачки картонные. 1 мл — флаконы (1) — пачки картонные. 1 мл — флаконы (5) — упаковки ячейковые контурные (1) — пачки картонные. 1 мл — шприцы стеклянные (1) — упаковки ячейковые контурные (1) — пачки картонные. 1 мл — шприцы стеклянные (1) — упаковки ячейковые контурные (3) — пачки картонные. 1 мл — шприцы стеклянные (3) — упаковки ячейковые контурные (1) — пачки картонные. 1 мл — шприцы стеклянные (3) — упаковки ячейковые контурные (3) — пачки картонные.
Показания
В составе комплексной терапии у взрослых:
- при хроническом вирусном гепатите В без признаков цирроза печени;
- при хроническом вирусном гепатите С в отсутствии симптомов печеночной недостаточности (монотерапия или комбинированная терапия с рибавирином);
- при папилломатозе гортани;
- при остроконечных кондиломах;
- при волосатоклеточном лейкозе, хроническом миелолейкозе, неходжкинской лимфоме, меланоме, множественной миеломе, саркоме Капоши на фоне СПИД, прогрессирующем раке почки.
Противопоказания к применению
- тяжелые сердечно-сосудистые заболевания в анамнезе (неконтролируемая хроническая сердечная недостаточность, недавно перенесенный инфаркт миокарда, выраженные нарушения сердечного ритма);
- тяжелая почечная и/или печеночная недостаточность (в т.ч. вызванная наличием метастазов);
- эпилепсия, а также тяжелые нарушения функций ЦНС, особенно выражающиеся депрессией, суицидальными мыслями и попытками (в т.ч. в анамнезе);
- хронический гепатит с декомпенсированным циррозом печени и у больных, получающих или получавших недавно лечение иммунодепрессантами (за исключением завершенного кратковременного курса лечения ГКС);
- аутоиммунный гепатит или иное аутоиммунное заболевание;
- лечение иммунодепрессантами после трансплантации;
- заболевание щитовидной железы, не поддающееся контролю общепринятыми терапевтическими методами;
- декомпенсированные заболевания легких (в т.ч. ХОБЛ);
- декомпенсированный сахарный диабет;
- гиперкоагуляция (в т.ч. тромбофлебит, тромбоэмболия легочной артерии);
- выраженная миелодепрессия;
- беременность;
- период лактации (грудного вскармливания);
- повышенная чувствительность к компонентам препарата.
Фармакологическое действие
Интерферон. Альтевир® оказывает противовирусное, иммуномодулирующее антипролиферативное и противоопухолевое действие.
Интерферон альфа-2b, взаимодействуя со специфическими рецепторами на поверхности клетки, инициирует сложную цепь изменений внутри клетки, включающую в себя индукцию синтеза ряда специфических цитокинов и ферментов, нарушает синтез вирусной РНК и белков вируса в клетке. Результатом этих изменений является неспецифическая противовирусная и антипролиферативная активность, связанная с предотвращением репликации вируса в клетке, торможением пролиферации клеток и иммуномодулирующим действием интерферона. Интерферон альфа-2b стимулирует процесс презентации антигена иммунокомпетентным клеткам, обладает способностью стимулировать фагоцитарную активность макрофагов, а также цитотоксическую активность Т-клеток и «натуральных киллеров», участвующих в противовирусном иммунитете.
Предотвращает пролиферацию клеток, особенно опухолевых. Оказывает угнетающее влияние на синтез некоторых онкогенов, приводящее к ингибированию опухолевого роста.
Лекарственное взаимодействие
Лекарственное взаимодействие между Альтевиром и другими лекарственными средствами полностью не изучено. С осторожностью следует применять Альтевир® одновременно со снотворными и седативными средствами, наркотическими анальгетиками и препаратами, потенциально оказывающими миелодепрессивный эффект.
При одновременном назначении Альтевира и теофиллина следует контролировать концентрацию последнего в сыворотке крови и при необходимости изменять режим его дозирования.
При применении Альтевира в комбинации с химиотерапевтическими препаратами (цитарабин, циклофосфамид, доксорубицин, тенипозид) повышается риск развития токсических эффектов.
Режим дозирования
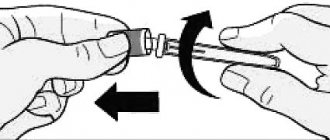
Применяют п/к, в/м и в/в. Лечение должно быть начато врачом. Далее с разрешения врача пациент может вводить себе поддерживающую дозу самостоятельно (в случаях, когда препарат назначен п/к или в/м).
Хронический гепатит В:
Альтевир® вводят п/к или в/м в дозе 5-10 млн. ME 3 раза в неделю в течение 16-24 недель. Лечение прекращают после 3-4 месяцев применения при отсутствии положительной динамики (по данным исследования ДНК вируса гепатита В).
Хронический гепатит С:
Альтевир® вводят п/к или в/м в дозе 3 млн. ME 3 раза в неделю в течение 24-48 недель. У пациентов с рецидивирующим течением заболевания и больных, ранее не получавших лечение интерфероном альфа-2b, эффективность лечения увеличивается при комбинированной терапии с рибавирином. Продолжительность комбинированной терапии составляет не менее 24 недель. Терапию Альтевиром следует проводить 48 недель больным хроническим гепатитом С и 1-м генотипом вируса с высокой вирусной нагрузкой, у которых к концу первых 24 недель лечения в сыворотке крови не определяется РНК вируса гепатита С.
Папилломатоз гортани:
Альтевир® вводят п/к в дозе 3 млн. МЕ/м2 3 раза в неделю. Лечение начинают после хирургического (или лазерного) удаления опухолевой ткани. Дозу подбирают с учетом переносимости препарата. Достижение положительного ответа может потребовать проведения лечения в течение 6 месяцев.
Волосатоклеточный лейкоз:
рекомендуемая доза Альтевира для п/к введения пациентам после спленэктомии или без нее составляет 2 млн. МЕ/м2 3 раза в неделю. В большинстве случаев нормализация одного и более гематологических показателей наступает через 1-2 месяца лечения, возможно увеличение сроков лечения до 6 месяцев. Этого режима дозирования следует придерживаться постоянно, если при этом не происходит быстрого прогрессирования заболевания или возникновения симптомов тяжелой непереносимости препарата.
Хронический миелолейкоз:
рекомендуемая доза Альтевира в качестве монотерапии — 4-5 млн. МЕ/м2 в день п/к ежедневно. Для поддержания числа лейкоцитов может потребоваться применение в дозе 0.5-10 млн. МЕ/м2. Если лечение позволяет добиться контроля числа лейкоцитов, то для поддержания гематологической ремиссии препарат следует применять в максимальной переносимой дозе (4-10 млн. МЕ/м2 ежедневно). Препарат необходимо отменить через 8-12 недель, если терапия не привела к частичной гематологической ремиссии или клинически значимому снижению числа лейкоцитов.
Неходжкинская лимфома:
Альтевир® применяют в качестве адъювантной терапии в комбинации со стандартными схемами химиотерапии. Препарат вводят п/к в дозе 5 млн. МЕ/м2 3 раза в неделю в течение 2-3 месяцев. Дозу необходимо корректировать в зависимости от переносимости препарата.
Меланома:
Альтевир® применяют в качестве адъювантной терапии при имеющемся высоком риске рецидива у взрослых после удаления опухоли. Альтевир® вводят в/в в дозе 15 млн. МЕ/м2 5 раз в неделю в течение 4 недель, затем п/к в дозе 10 млн. МЕ/м2 3 раза в неделю в течение 48 недель. Дозу необходимо корректировать в зависимости от переносимости препарата.
Множественная миелома
: Альтевир® назначают в период достижения устойчивой ремиссии в дозе 3 млн. МЕ/м2 3 раза в неделю п/к.
Саркома Капоши на фоне СПИД:
оптимальная доза не установлена. Препарат можно применять в дозах 10-12 млн. МЕ/м2/сут п/к или в/м. В случае стабилизации заболевания или ответа на лечение, терапию продолжают до тех пор, пока не произойдет регресс опухоли или не потребуется отмена препарата.
Рак почки:
оптимальная доза и схема применения не установлены. Рекомендуется применять препарат п/к в дозах от 3 до 10 млн. МЕ/м2 3 раза в неделю.
Приготовление раствора для в/в введения
Набирают объем раствора Альтевира, необходимый для приготовления требуемой дозы, добавляют к 100 мл стерильного 0.9% раствора натрия хлорида и вводят в течение 20 мин.
Передозировка
Данные по передозировке препарата Альтевир® не предоставлены.
Побочное действие
Общие реакции:
очень часто — лихорадка, слабость (являются дозозависимыми и обратимыми реакциями, исчезают в течение 72 ч после перерыва в лечении или его прекращения), озноб; менее часто — недомогание.
Со стороны ЦНС:
очень часто — головная боль; менее часто — астения, сонливость, головокружение, раздражительность, бессонница, депрессия, суицидальные мысли и попытки; редко — нервозность, тревожность.
Со стороны костно-мышечной системы:
очень часто — миалгия; менее часто — артралгия.
Со стороны пищеварительной системы:
очень часто — снижение аппетита, тошнота; менее часто — рвота, диарея, сухость во рту, изменение вкуса; редко — боль в животе, диспепсия; возможно обратимое повышение активности печеночных ферментов.
Со стороны сердечно-сосудистой системы:
часто — снижение АД; редко — тахикардия.
Дерматологические реакции:
менее часто — алопеция, повышенное потоотделение; редко — кожная сыпь, кожный зуд.
Со стороны системы кроветворения
: возможны обратимые лейкопения, гранулоцитопения, снижение уровня гемоглобина, тромбоцитопения.
Прочие:
редко — снижение массы тела, аутоиммунный тиреоидит.
Особые указания
До лечения Альтевиром хронического вирусного гепатита В и С рекомендуется провести биопсию печени, чтобы оценить степень повреждения печени (признаки активного воспалительного процесса и/или фиброза). Эффективность лечения хронического гепатита С увеличивается при комбинированной терапии Альтевиром и рибавирином. Применение Альтевира не эффективно при развитии декомпенсированного цирроза печени или печеночной комы.
В случае возникновения побочных эффектов во время лечения Альтевиром дозу препарата следует снизить на 50% или временно отменить препарат до их исчезновения. Если побочные эффекты сохраняются или возникают вновь после снижения дозы, или наблюдается прогрессирование заболевания, то лечение Альтевиром следует прекратить.
При снижении уровня тромбоцитов ниже 50×109/л или уровня гранулоцитов ниже 0.75×109/л рекомендуется уменьшение дозы Альтевира в 2 раза с контролем анализа крови через 1 неделю. Если указанные изменения сохраняются, то препарат следует отменить.
При снижении уровня тромбоцитов ниже 25×109/л или уровня гранулоцитов ниже 0.5 х109/л рекомендуется отмена препарата Альтевир® с контролем анализа крови через 1 неделю.
У пациентов, получающих препараты интерферона альфа-2b, в сыворотке крови могут определяться антитела, нейтрализующие его противовирусную активность. Практически во всех случаях титры антител невысоки, их появление не приводит к снижению эффективности лечения или возникновению других аутоиммунных нарушений.
Условия хранения
Препарат следует хранить в недоступном для детей месте, в соответствии с СП 3.3.2-1248-03 при температуре от 2° до 8°С; не замораживать.
Срок годности
Срок годности — 18 месяцев.
Транспортировать при температуре от 2° до 8°С; не замораживать.
Применение при беременности и кормлении грудью
Ограничения при беременности — Противопоказано. Ограничения при кормлении грудью — Противопоказано.
Препарат противопоказан при беременности и в период лактации (грудного вскармливания).
Применение при нарушениях функции почек
Ограничения при нарушениях функции почек — С осторожностью.
Препарат противопоказан при тяжелой почечной и/или печеночной недостаточности (в т.ч. вызванными наличием метастазов).
Применение при нарушениях функции печени
Ограничения при нарушениях функции печени — С осторожностью.
Препарат противопоказан при тяжелой почечной и/или печеночной недостаточности (в т.ч. вызванными наличием метастазов).
Условия реализации
Препарат отпускается по рецепту.
Контакты для обращений
ФАРМСТАНДАРТ АО (Россия)
141701 Московская обл. г. Долгопрудный, Лихачевский пр-д, д. 5Б Тел./факс E-mail
ПИТРС I линии. Пегилированный интерферон бета-1a
Пегилированный интерферон бета-1a представляет собой человеческий интерферон бета-1a, который химически связан с производным полиэтиленгликоля (отсюда сокращенное название пэгинтерферон). Такое изменение естественной структуры белковой молекулы интерферона повышает стабильность вещества, снижает ответную реакцию иммунной системы и позволяет пролонгировать действие препарата.
Препараты из группы интерферонов бета обладают доказанной эффективностью и безопасностью применения при рецидивирующем рассеянном склерозе. Интерфероны бета успешно применяются для лечения пациентов. Тем не менее у таких препаратов имеются некоторые недостатки – необходимость частого проведения инъекций и потеря терапевтической эффективности в результате образования антител. Для улучшения фармакологических свойств были предприняты попытки химически модифицировать природную структуру молекул интерферона. Одной из таких модификаций стало пегилирование – присоединение молекулы метоксиполиэтиленгликоля к молекуле интерферона бета-1a [1, 2].
Пегилированный интерферон бета-1a:
- модулирует иммунную систему и подавляет воспалительный процесс;
- снижает число обострений рассеянного склероза;
- замедляет прогрессирование инвалидизации;
- требует меньшее количество инъекций за счет пролонгированного действия;
- не вызывает иммунный ответ со стороны организма (частота образования нейтрализующих антител составляет менее 1%) в отличие от остальных препаратов интерферона.
Пегилированный интерферон бета-1a назначается для лечения ремиттирующего рассеянного склероза. Дозировка препарата определяется врачом индивидуально.
Препарат представляет собой раствор для подкожного введения. Инъекции можно проводить дома самостоятельно, но в начале лечения рекомендуется контроль со стороны медицинского работника [3].
У пэгинтерферона есть некоторые противопоказания к применению:
- повышенная чувствительность к интерферону бета или пэгинтерферону;
- беременность;
- тяжелая форма депрессии;
- возраст до 18 лет;
- с осторожностью применять у пациентов с нарушениями функций почек или печени, эпилепсией.
Наиболее распространенные побочные эффекты пегилированного интерферона бета-1a – гриппоподобный синдром (головная боль, повышение температуры, озноб) и постинъекционные реакции (зуд, боль, раздражение кожи). Неприятные симптомы сильнее всего проявляются во время первых недель лечения и проходят по мере продолжения терапии. Тем не менее обо всех изменениях в состоянии здоровья необходимо сообщить лечащему врачу для назначения дополнительных препаратов, уменьшающих неприятные ощущения. В некоторых случаях при появлении тяжелых побочных реакций врач может принять решение о замене препарата [3].
История применения лекарственных средств насчитывает, вероятно, столько же времени, сколько существует человеческая цивилизация. От периода наскальной живописи первобытных людей до настоящего времени человеческий интеллект настойчиво демонстрирует осознанную необходимость вмешательства в болезнь посредством применения лекарственных средств, арсенал которых составляют уже не только травы и минералы, но и антибиотики, противоопухолевые препараты, белки, цитокины, требующие высочайших интеллектуальных и материальных затрат на свое производство. И какое бы средство не применялось для лечения того или иного заболевания, логично стремление врача и пациента к максимальной эффективности используемого препарата и минимизации его побочных эффектов. Пути повышения клинической эффективности лекарственного вещества могут быть различными: это изменение его химической структуры, соединение с другими препаратами, способными усилить или, наоборот, ослабить действие основного препарата. Особую проблему в этом смысле составляют препараты белковой или пептидной структуры (интерфероны, гормоны, факторы роста, цитокины, тромболитики), поскольку принципиальное изменение структуры их молекулы как химического понятия либо нивелирует их биологические свойства, либо влечет возрастание числа побочных эффектов, связанных с их применением. В то же время лечение нативными препаратами белковой или пептидной природы имеет ряд существенных недостатков: они быстро гидролизуются в пищеварительном тракте и поэтому используются, как правило, парентерально. Относительно короткий период «естественной» полужизни таких препаратов в организме пациента предполагает их многократное использование для достижения требуемого терапевтического воздействия. Еще одним серьезным негативным фактором, ограничивающим применение нативных или рекомбинантных пептидно-белковых препаратов, является их высокая иммуногенность и связанные с ней реакции гиперчувствительности.
Один из путей повышения эффективности лекарственных средств белковой структуры – это химическая модификация их молекулы, состоящая не в собственно изменении ее структуры, а в физико-химической трансформации, достигаемой соединением нативной молекулы с полиэтиленгликолем (ПЭГ). Процесс соединения нативной молекулы лекарственного препарата с ПЭГ получил название «пегилирование». Такая химическая модификация фармацевтических препаратов белковой структуры адресно направлена на улучшение их переносимости, снижение иммуногенности, повышение периода их полужизни и, в конечном итоге, на повышение качества жизни больного в процессе проведения лечения.
ПЭГ в качестве потенциального модификатора веществ белковой и пептидной природы привлек внимание исследователей еще в начале 70-х годов прошлого века. В настоящее время ПЭГ одобрен Обществом по питанию и лекарственным препаратам США (FDA) в качестве субстанции, разрешенной к использованию в медицине (производство лекарственных препаратов), продуктах питания и косметологии. Молекулы ПЭГ – это водорастворимые полимеры окиси этилена с двумя терминальными гидроксильными группами. Они могут иметь различную молекулярную массу и стереохимическую структуру. Масса молекул ПЭГ может колебаться в пределах 300-4000 Дальтон, а выстроенные в цепи макромолекулы ПЭГ могут формировать как разветвленную, так и линейную стереохимию. Именно масса ПЭГ и его стереохимическая структура обычно определяют принципиальные свойства будущего модифицированого пептидного субстрата.
ПЭГ может быть связан с протеином в нескольких позициях, но некоторые из них являются премироваными. Так, например, наиболее часто ковалентное соединение с белком происходит в месте атома азота E-аминогруппы лизина (интерферон-альфа 2а) или в месте имидазольной группы гистидина (интерферон-альфа 2b). Такие связи позволяют активировать гидроксильные группы ПЭГ и выстроить молекулу, в которой целевые места имеют ковалентные связи. Кроме того, прямые ковалентные связи ПЭГ в месте положения лизина и аргинина (карбоксильные концы) напрямую препятствуют расщеплению модифицированных молекул трипсином.
Еще одной из важнейших особенностей модифиицрованных ПЭГ-молекул является их высокая гидрофильность, формирующая принципиально новые физико-химические свойства измененного пептида. Высокое содержание атомов водорода даже в одной молекуле ПЭГ позволяет ей связываться с 2-3 молекулами воды. Подобный эффект влечет за собой формирование «водного облака» вокруг модифицированной молекулы «ПЭГ-белок», за счет чего значительно повышается ее гидродинамический радиус. Этот своеобразный «щит» воды вокруг модифицированной молекулы, с одной стороны, значительно повышает растворимость и биодоступность препарата, а с другой, – защищает молекулу от других белков (нейтрализующие антитела, комплемент). Таким образом ПЭГ-модифицированные белки и пептиды значительно более защищены от опсонизации и активного фаго- и эндоцитоза клеточных структур макроорганизма. Наиболее часто для связи пептидных молекул используется монометоксиПЭГ; его молекула имеет одну гидроксильную группу, с которой и происходит связывание пептида, другие концы молекулы содержат нереактогенные метильные группы. Примеры формирования возможных связей ПЭГ с молекулами пептидной структуры представлены на рисунке 1.
Изменения фармакокинетических и фармакодинамических свойств ПЭГ-модифицированных пептидов зависят как от массы молекулы ПЭГ, так и от специфических мест связывания. Так, например, продемонстрирована прямая корреляция между массой молекулы ПЭГ и периодом полужизни собственно пептида. В таблице 1 приведены сравнительные данные о периодах полужизни некоторых биологически активных нативных белков, пептидов и их ПЭГ-конъюгатов. Обычно более длинные цепи ПЭГ ассоциируются с большей продолжительностью периода полужизни конъюгата «ПЭГ-пептид» и его фармакологической стабильностью. Еще одним важным фактором, влияющим на фармакодинамику и фармакокинетику ПЭГ-модифицированных пептидов, является структура ПЭГ-цепочек: разветвленная молекула ПЭГ замедляет активный метаболизм препарата, что так же влечет за собой удлинение времени его активной циркуляции. С разветвленной структурой цепочек ПЭГ связана и значительно меньшая иммуногенность модифицированных препаратов при сохранении их основных фармакологических свойств. Подобные эффекты могут быть достигнуты и другим путем – например, связыванием пептида не одной, а несколькими молекулами ПЭГ с линейной структурой цепочек. Примером может являться интерлейкина-2 (ИЛ-2). Так как молекула ИЛ-2 очень мала, она свободно фильтруется через почки и имеет очень короткий период полужизни. Соединение ИЛ-2 с ПЭГ, имеющим молекулярную массу менее 20 kDa, практически никак не влияет на его фармакодинамику, но повышение молекулярной массы ПЭГ до 60-70 kDA значительно замедляет фильтрацию коньюгата ПЭГ-ИЛ-2 и увеличивает время его полужизни и биодоступность. Говоря о специфических местах связывания ПЭГ с пептидом, следует подчеркнуть, что наиболее прочные связи по отношению к возможному протеолизу (чаще всего трипсином) формируются, если связывание пептида с ПЭГ происходит в месте гистидина.
В таблице 2 приведены данные о ПЭГ-модифицированных соединениях белковой или пептидной природы, разрешенных FDA к медицинскому применению или находящихся на различных стадиях преклинических и клинических испытаний. Из представленных в ней данных следует, что современные технологии пегилирования биологически активных белковых и пептидных молекул привели к значительному расширению области их настоящего и будущего практического применения. Появление ПЭГ-конъюгатов белков и пептидов позволило наблюдать целый ряд принципиально новых фармакодинамических и фармакокинетических эффектов известных соединений. Ярким примером тому могут служить результаты уже проведенных клинических испытаний ПЭГ-эритроцитов, ПЭГ-интерферона-альфа 2b, ПЭГ-аденозиндеаминазы, ПЭГ-растворимого рецептора некротизирующего фактора опухолей-альфа.
В настоящем сообщении рассматриваются особенности структуры, фармакодинамики и клинической эффективности недавно появивишихся пегилированных аналогов альфа-интерферона – ПЭГ-интерферона-альфа 2b (Пегинтрон; Shering Plough) и ПЭГ-интерферона-альфа 2а (Пегасис; Hoffmann La Roche). Следует подчеркнуть, что профиль безопасности, фармакодинамика, фармакокинетика и клиническая эффективность упомянутых препаратов были наиболее детально изучены на примере пациентов с хроническим гепатитом С. Данное обстоятельство чрезвычайно важно, так как при хроническом гепатите С, в отличие, например, от хронического гепатита В, в ближайшей перспективе не будет серьезной альтернативы интерферону-альфа, как средству базисного лечения. К сожалению, результаты терапии хронического гепатита С нативным («коротким») интерфероном-альфа нельзя считать удовлетворительными: частота доказанного ответа на лечение в общей популяции больных с этим заболеванием не превышала 20-22%, а у пациентов с 1b генотипом HCV и/или циррозом печени – 8-10%. Одна из основных причин столь неутешительных результатов – короткий период полужизни молекулы нативного альфа-интерферона, в результате чего не обеспечивается надежный контроль кинетики вируса гепатита С. Однако короткий период полужизни нативного альфа-интерферона – не единственная причина его низкой эффективности при лечении хронического гепатита С. Подтверждением этому является отсутствие достоверного улучшения результатов лечения при использовании ежедневных или высокодозных режимов монотерапии нативными альфа-интерферонами. По-видимому, не меньшую роль, чем короткий период полужизни, в неэффективности этих препаратов играют такие факторы, как индукция образования антител, иммуногенные свойства молекулы альфа-интерферона, особенности его метаболизма и некоторые другие моменты.
ПЭГ-интерферон-альфа 2b (ПЕГИНТРОН)
Противовирусная терапия – одна из основных областей перспективного использования пегилированных препаратов пептидной структуры. В настоящее время для лечения хронических вирусных гепатитов В и С широко используется непегилированный интерферон-альфа 2b (Интрон-А), способный подавлять репликацию вирусных ДНК или РНК. При традиционном режиме его применения (3 млн. МЕ 3 раза в неделю) максимальная концентрация препарата после подкожного введения определяется в пределах 8-12 часов, а период его полужизни в среднем составляет 6 часов. Из этого со всей очевидностью следует, что наряду с периодами стабильной концентрации препарата существуют и периоды, когда его уровень в сыворотке крови и тканях организма может снижаться практически до неопределяемых значений. Логично предположить, что для достижения приемлемого терапевтического уровня интерферона-альфа, вводимого извне, необходимо существенное изменение параметров его фармакокинетики и фармакодинамики. Такая постановка вопроса предопределила создание принципиально новой лекарственной формы интерферона-альфа 2b, конъюгированного с ПЭГ. Этот препарат уже прошел все необходимые клинические испытания и зарегистрирован к применению во всех ведущих европейских странах и США под торговым названием Пегинтрон. На рисунке 2 представлены основные параметры фармакокинетики нативного интерферна-альфа 2b и Пегинтрона. Очевидно, что Пегинтрон имеет значительно лучший фармакологический профиль, чем нативный интерферон-альфа 2b, что выражается в значительном увеличении периода полужизни и ослаблении иммуногенных свойств. В процессе работы по созданию Пегинтрона было показано, что его антивирусная активность in vitro составляет приблизительно 35-40% от таковой нативного интерферона-альфа 2b. В то же время присоединение относительно небольшой молекулы ПЭГ с молекулярной массой 12 kDa к нативному интерферону приводит к тому, что in vivo максимальная концентрация последнего достигается, как и при применении непегилированного препарата, через 8 – 12 часов, но стабильная концентрация поддерживается в течение 48-72 часов. Таким образом, период «эффективной» полужизни препарата составляет в среднем около 40 часов. Данный фармакологический профиль обеспечивается введением препарата 1 раз в неделю, что благоприятно сказываться и на качестве жизни пациента, получающего противовирусное лечение. Еще одно принципиально важное преимущество Пегинтрона перед нативным интерфероном-альфа 2b состоит в том, что он может использоваться при циррозах печени. Ранее пациенты с хроническим гепатитом С на стадии морфологического цирроза были, как правило, лишены возможности получения полноценной противовирусной терапии, поскольку введение непегилированного интерферона-альфа могло значительно ухудшить их состояние. Особенности строения молекулы Пегинтрона (относительно небольшой размер и линейность) позволяют применять его у этой категории больных, так как препарат не требует для полноценного выведения высокосохранной почечной гемоперфузии. Проведенные клинические испытания Пегинтрона продемонстрировали его очевидные преимущества перед нативным интерфероном-альфа при лечении хронического гепатита С как при использовании в качестве монотерапии, так и в комбинации с рибавирином.
ПЭГ-интерферон-альфа 2а (ПЕГАСИС)
Еще одним представителем группы пегелированных интерфернов-альфа является аналог интерферона-альфа 2а, выпускаемый под торговым названием Пегасис. Он отличается от Пегинтрона несколько более сложной химической структурой – интерферон соединен с разветвленной цепью ПЭГ, имеющей более высокую молекулярную массу – 40 kDa (общая молекулярная масса Пегасиса около 60 kDa), при конъюгации использована амидная химическая связь в положении аминогруппы лизина, являющаяся наиболее прочной. Это и предопределило особенности фармакодинамики и клинической эффективности Пегасиса у пациентов с хроническим гепатитом С. Результаты исследований позволяют рассматривать этот препарат как наиболее эффективный среди интерферонов-альфа, особенно у так называемой сложной категории пациентов с 1b генотипом HCV и/или высокой вирусной нагрузкой, с циррозом печени.
Хотя специальные исследования по сравнению эффективности Пегинтрона и Пегасиса у пациентов с хроническим гепатитом С не проводились, имеющиеся на сегодня данные клинических испытаний этих препаратов позволяют говорить об определенном преимуществе Пегасиса как с точки зрения противовирусного эффекта, так и влияния на качество жизни больных.
Использование Пегасиса в режиме монотерапии у пациентов с хроническим гепатитом С в среднем позволяет добиться стойкого терапевтического ответа в 39% случаев, тогда как при применении Пегинтрона – только в 25% (рис. 3). Еще более успешной монотерапия Пегасисом была у «трудной» категории больных: лечение было эффективным почти у трети пациентов. Пегинтрон при назначении в аналогичном режиме был эффективен только в 14% случаев (рис. 4).
Интересными представляются результаты исследований эффективности пегилированных интерферонов-альфа, применявшихся в сочетании с рибавирином, представленные Di Bisciegli (2000). Как оказалось, у пациентов с иным, чем 1b, генотипом HCV эффективность лечения при использовании Пегинтрона и Пегасиса была одинаковой (стойкий ответ в 75% и 76% случаев соответственно), но в группе больных с 1b генотипом HCV Пегасис существенно превосходил Пегинтрон –стойкий ответ был получен в 41% и 30% случаев соответственно (рис. 5). Таким образом, у этой категории больных при проведении комбинированной терапии хронического гепатита С предпочтение следует отдавать Пегасису. У пациентов с циррозом печени использование Пегасиса в режиме комбинированного лечения также позволило добиться значительного повышения частоты стойкого терапевтического ответа (до 43%; рис. 6).
Анализируя частоту побочных эффектов (рис. 7) пегилированных интерферонов-альфа по данным литературы, можно констатировать, что реже они наблюдались при применении Пегасиса.
Обращает на себя внимание существенное улучшение качества жизни больных, которым назначался Пегасис, по сравнению с теми, кому вводился нативный интерферон-альфа 2а (рис. 8). Это обусловлено хорошей переносимостью и удобством применения Пегасиса. При его использовании не требуется подбор дозы в зависимости от массы тела пациента (в отличие от Пегинтрона), препарат вводится один раз в неделю и выпускается в виде готовой жидкой лекарственной формы, не требующей предварительных манипуляций при применении (в отличие от Пегинтрона).
Таким образом, разработка и внедрение пегилированных препаратов интерферона-альфа в практику комбинированной терапии хронического гепатита С позволяют говорить о новом «золотом стандарте» лечения этого заболевания, причем результаты их использования вселяют определенный оптимизм. Чрезвычайно важное значение приобретает вопрос правильного отбора больных для проведения такой терапии, от которого во многом зависят результаты лечения и качество жизни пациента.