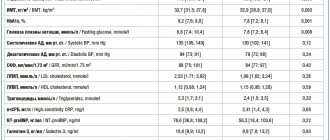
Пембролизумаб (Кейтруда, Китруда, MK-3475) — инновационный препарат, который был одобрен FDA (Американским управлением по надзору за качеством пищевых продуктов и медикаментов) в сентябре 2014 года, и в настоящее время уже достаточно широко применяется для лечения меланомы на поздних стадиях.
В 2014 году Кейтруда получила статус «приоритетное рассмотрение» и «прорыв в медицине». Это означает, что Пембролизумаб был включен в группу лекарственных средств, способных повысить эффективность и безопасность лечения редких и серьезных заболеваний. Именно поэтому препарат был так быстро одобрен и внедрен в клиническую практику -обычно это происходит намного дольше.
Как действует Пембролизумаб?
Препараты для иммунотерапии меланомы и других злокачественных опухолей существуют уже достаточно давно. Но они всегда имели низкую эффективность, и до недавнего времени ученые не знали, как справиться с этой проблемой.
Задача иммунотерапии — активировать иммунную систему больного, заставить её атаковать и уничтожать раковые клетки. Долгое время препятствием для достижения этой цели становился белок PD-1.
Белок PD-1 блокирует работу иммунной системы. Он не дает Т-лимфоцитам распознавать и уничтожать раковые клетки. Кейтруда содержит моноклональные антитела, которые блокируют PD-1. Препарат помогает убрать «тормоз», благодаря чему лимфоциты приобретают способность атаковать опухолевую ткань.
Форма выпуска
Концентрат для приготовления раствора для инфузий. Прозрачный или опалесцирующий от бесцветного до светло-желтого цвета раствор.
В 1 флаконе содержится:
действующее вещество: пембролизумаб 100,0 мг;
вспомогательные вещества: L-гистидин 1,2 мг; L-гистидина гидрохлорида моногидрат 6,8 мг; полисорбат – 80 0,8 мг; сахароза 280 мг; вода для инъекций до 4,0 мл.
По 4 мл препарата во флаконе из бесцветного стекла типа I (Евр. Фарм., Фарм. США), укупоренный пробкой из хлорбутилового каучука, обжатый алюминиевым колпачком и защищенный пластиковой крышкой.
Насколько эффективен Пембролизумаб?
В Калифорнийском Университете в Лос-Анджелесе было проведено исследование, в котором приняли участие 173 человека с диагностированной прогрессирующей меланомой. Их разделили на две группы. В одной из них пациенты получали стандартную дозу препарата 2 мг на килограмм массы тела через каждые 3 недели. Во второй группе доза была увеличена в 5 раз (10 мг/кг).
У 24% пациентов, получавших препарат в дозе 2 мг/кг, опухоль уменьшилась более чем на треть. Повторный рост меланомы не отмечался, а эффект препарата сохранялся от 1,4 до 8,5 месяцев (в отдельных случаях — дольше).
Компания MSD сообщила, что пембролизумаб в комбинации с химиотерапией (ХТ) продемонстрировал улучшение общей выживаемости (ОВ), выживаемости без прогрессирования (ВБП) и частоты объективных ответов (ЧОО) у пациентов с распространенным немелкоклеточным раком легкого (НМРЛ) без экспрессии PD-L1 в опухоли (TPS <� 1 %) при применении в первой линии терапии.
По данным объединенного анализа исследований KEYNOTE-189, KEYNOTE-407 и KEYNOTE-021 (Когорта G), пембролизумаб в комбинации с ХТ обеспечивает снижение риска смерти на 44 % (ОР = 0,56), по сравнению с химиотерапией. В группе пембролизумаб+ХТ ЧОО составила 46,9 %, по сравнению с 28,6 % в группе ХТ. Профиль безопасности пембролизумаба соответствовал данным предшествующих клинических исследования среди больных распространенным НМРЛ.
«Целью нашей программы клинических исследований по раку легкого является поиск возможностей увеличения выживаемости пациентов, у которых было выявлено данное заболевание», сообщил доктор Jonathan Cheng [Джонатан Ченг], вице-президент научно-исследовательского подразделения MSD по клиническим исследованиям в онкологии. «Проведенный анализ подтверждает эффективность пембролизумаба в комбинации с ХТ у пациентов с НМРЛ, у которых отсутствует экспрессия PD-L1 в опухоли (TPS<1%).»
«На основании данных о преимуществе в общей выживаемости, которое было продемонстрировано в клинических исследованиях, пембролизумаб в комбинации с химиотерапией стал стандартом терапии первой линии для пациентов с распространенным немелкоклеточным раком легкого в отсутствии активирующих мутаций», сообщил доктор Hossein Borghaei [Хоссейн Боргхеи], руководитель торакального отделения онкологического .
Дополнительные данные объединенного подгруппового анализа исследований KEYNOTE-189, KEYNOTE-407 и KEYNOTE-021 (Когорта G)
Данные представленные во время Всемирной конференции по раку легкого, получены в результате объединенного подгруппового анализа 428 пациентов, ранее не получавших лечение, без экспрессии PD-L1 в опухоли (TPS <� 1 %), которые принимали участие в исследованиях KEYNOTE-189 (неплоскоклеточный НМРЛ; n = 190), KEYNOTE-407 (плоскоклеточный НМРЛ; n = 194) и KEYNOTE-021 (неплоскоклеточный НМРЛ; n = 44 [Когорта G]). Пациенты были рандомизированы в группы лечения пембролизумабом в дозе 200 мг каждые 3 недели в комбинации с химиотерапией (n = 243) или химиотерапии (n = 185). Больные неплоскоклеточным НМРЛ получали лечение пеметрекседом в комбинации с препаратом платины, больные плоскоклеточным НМРЛ получали карбоплатин в комбинации с паклитакселом или наб-паклитакселом. Больные с генетическими аберрациями EGFR или ALK к участию в исследованиях не допускались. Ключевые цели по оценке эффективности включали ОВ, ВБП и ЧОО.
На фоне терапии пембролизумабом в комбинации с химиотерапией при медиане наблюдения 10,2 мес отмечено снижение риска смерти на 44 % (ОР = 0,56 [95 % ДИ; 0,43–0,73]), по сравнению с химиотерапией. Расчетные показатели общей выживаемости через 12 месяцев в группе комбинации пембролизумаба с химиотерапией составили 66 %, по сравнению с 47 % в группе химиотерапии; показатели общей выживаемости через 18 месяцев составили 52 % и 29 %, соответственно. Медиана ОВ в группе комбинации пембролизумаба с химиотерапией составила 19,0 месяцев (95 % ДИ; 15,2–24,0), по сравнению с 11,0 месяцами (95 % ДИ; 9,2–13,5) в группе химиотерапии.
На фоне комбинации пембролизумаба с химиотерапией также отмечено снижение риска прогрессирования заболевания или смерти на 33 % (ОР = 0,67 [95 % ДИ; 0,54–0,84]), по сравнению с химиотерапией. Расчетные показатели выживаемости без прогрессирования через 12 месяцев в группе комбинации пембролизумаба с химиотерапией составили 29 %, по сравнению с 17 % в группе химиотерапии; показатели выживаемости без прогрессирования через 18 месяцев составили 22 % и 9 %, соответственно. Медиана ВБП в группе комбинации пембролизумаба с химиотерапией составила 6,5 месяцев (95 % ДИ; 6,2–8,5), по сравнению с 5,4 месяцами (95 % ДИ; 4,7–6,2) в группе химиотерапии.
ЧОО в группе комбинации пембролизумаба с химиотерапией составила 46,9 % (n = 114), а в группе химиотерапии этот показатель составил 28,6 % (n = 53). Медиана длительности ответа в группе комбинации пембролизумаба с химиотерапией составила 7,9 месяцев (диапазон, от 1,1+ до 28,4+), а в группе химиотерапии этот показатель составил 6,7 месяцев (диапазон, от 1,4+ до 30,1+). У 42,4 % пациентов в группе комбинации пембролизумаба с химиотерапией продолжительность ответа на терапию составила 12 месяцев и более, по сравнению с 35,3 % в группе химиотерапии.
Среди пациентов в группе комбинации пембролизумаба с химиотерапией частота нежелательных явлений (НЯ) 3–5 степени тяжести составила 68 % (n = 165), по сравнению с 72 % (n = 131) в группе химиотерапии. Частота НЯ 3–5 степени тяжести, которые привели к смерти, в группе комбинации пембролизумаба с химиотерапией составила 9 % (n = 23) и 6 % (n = 11) в группе химиотерапии. Частота иммуноопосредованных НЯ 3–5 степени тяжести и инфузионных реакций в группе комбинации пембролизумаба с химиотерапией составила 11 % (n = 27), по сравнению с 3 % (n = 5) в группе химиотерапии. Летальные исходы вследствие иммуноопосредованных НЯ и инфузионных реакций в группе комбинации пембролизумаба с химиотерапией были отмечены в 1 % случаев (n = 2), тогда как в группе химиотерапии летальных исходов не было.
О пембролизумабе
Пембролизумаб представляет собой гуманизированное моноклональное антитело, которое селективно блокирует взаимодействие между рецептором PD-1 на Т-лимфоцитах иммунной системы и лигандами PD-L1 и PD-L2 на опухолевой клетке.
Пембролизумаб был впервые зарегистрирован в 2014 году в США для терапии пациентов с неоперабельной и метастатической меланомой, у которых выявлено прогрессирование заболевания после предшествующей терапии. Позже препарат был одобрен для терапии пациентов по 14 показаниям.
Пембролизумаб был впервые зарегистрирован в России в ноябре 2016 года. В настоящее время препарат одобрен к применению по девяти показаниям для лечения пациентов:
Меланома
— для лечения взрослых пациентов с неоперабельной или метастатической меланомой;
— в качестве адъювантной терапии у пациентов с меланомой с поражением лимфатических узлов после хирургического лечения.
Немелкоклеточный рак легкого
— в комбинации с химиотерапией, включающей препарат платины и пеметрексед в качестве 1-ой линии терапии у пациентов с метастатическим неплоскоклеточным немелкоклеточным раком легкого при отсутствии мутаций в генах эпидермального фактора роста (EGFR) или киназы анапластической лимфомы (ALK);
— в комбинации с карбоплатином и паклитакселом или альбумин-стабилизированным нанодисперсным паклитакселом в качестве 1-ой линии терапии у пациентов с метастатическим плоскоклеточным немелкоклеточным раком легкого;
— в качестве монотерапии 1-ой линии у пациентов с местнораспространенным или метастатическим немелкоклеточным раком легкого с экспрессией PD-L1≥ 1% опухолевыми клетками, определяемой валидированным тестом, при отсутствии мутаций в генах EGFR или ALK;
— в качестве монотерапии для лечения пациентов с распространенным немелкоклеточным раком легкого с экспрессией PD-L1≥ 1% опухолевыми клетками, определяемой валидированным тестом, которые ранее получали терапию, включающую препараты платины. При наличии мутаций в генах EGFR или ALK пациенты должны получить соответствующую специфическую терапию прежде, чем им будет назначено лечение препаратом.
Рак головы и шеи
— для лечения пациентов с рецидивирующим или метастатическим плоскоклеточным раком головы и шеи с прогрессированием заболевания во время или после химиотерапии, включающей препараты платины.
Классическая лимфома Ходжкина (кЛХ)
— для лечения взрослых и детей с рефрактерной классической лимфомой Ходжкина или с рецидивом заболевания после трех и более предшествующих линий терапии.
Уротелиальная карцинома
— для лечения пациентов с местнораспространенной или метастатической уротелиальной карциномой, у которых невозможно проведение химиотерапии, включающей цисплатин, с экспрессией PD-L1 (комбинированный показатель позитивности (combined positive score, CPS≥ 10) по данным валидированного теста, а также у пациентов, которым невозможно проведение химиотерапии любыми препаратами платины, независимо от экспрессии PD-L1;
— для лечения пациентов с местнораспространенной или метастатической уротелиальной карциномой, которые ранее получали химиотерапию, включающую препараты платины
Рак желудка
— для лечения пациентов с рецидивирующей местнораспространенной или метастатической аденокарциномой желудка или пищеводно желудочного перехода с экспрессией PD-L1 (комбинированный показатель позитивности (combined positive score, CPS≥ 1) по данным валидированного теста. У больных должно быть зарегистрировано прогрессирование заболевания на фоне или после проведения двух и более линий предшествующей терапии, включая химиотерапию фторпиримидинами и препаратами платины, а также, при необходимости, таргетную терапию препаратами анти-НЕR2/nеu.
Злокачественные новообразования с высоким уровнем микросателлитной нестабильности
— для лечения пациентов с распространенными злокачественными новообразованиями с высоким уровнем микросателлитной нестабильности (МSI-H), включая нарушения системы репарации ДНК (dMМR), которые ранее получали терапию
Гепатоцеллюлярная карцинома
— для лечения пациентов с гепатоцеллюлярной карциномой (ГЦК), которые ранее получали анти-ангиогенную терапию ингибиторами тирозинкиназ (ИТК).
Рак шейки матки
— для лечения пациентов с рецидивирующим или метастатическим раком шейки матки с экспрессией PD-L1 (CPS≥ 1) по данным валидированного теста при прогрессировании заболевания на фоне или после проведения химиотерапии.
Об иммуноонкологии
Последние открытия в области иммуноонкологии открывают для пациентов со злокачественными новообразованиями новые возможности в лечении их заболеваний и увеличении продолжительности жизни. Иммуноонкологические препараты усиливают естественную способность иммунной системы бороться с опухолью. В отличие от химиотерапии (которая ингибирует клеточное деление быстрорастущих опухолевых клеток) и таргетной терапии (воздействующей на различные молекулярные мишени на опухолевых клетках) иммуноонкологические препараты воздействуют на различные компоненты иммунной системы, в том числе точки иммунного контроля, в норме отвечающие за регулирование работы иммунной системы.
О компании MSD
На протяжении более 125 лет MSD является одной из ведущих международных компаний в области здравоохранения. MSD – это фирменное наименование компании Merck & Co. Inc., штаб-квартира которой находится в Кенилворте, штат Нью-Джерси, США.
Мы создаем, разрабатываем и производим инновационные рецептурные лекарственные препараты, включая биологические лекарственные средства и вакцины, которые помогают сохранять и улучшать здоровье людей. В портфеле MSD представлены лекарственные препараты для профилактики и лечения онкологических заболеваний, сахарного диабета, гепатита C, ВИЧ-инфекций, аутоиммунных воспалительных и респираторных заболеваний, болезней системы кровообращения и других нозологий.
Мы реализуем и поддерживаем программы и партнерские проекты, которые способствуют повышению качества медицинской помощи.
В России компания MSD работает с 1991 года, концентрируя внимание на обеспечении доступности инновационных лекарств и вакцин, партнерстве с локальными производителями и ведущими медицинскими учреждениями, а также поддержке медицинского образования. Мы применяем богатый международный опыт, чтобы внести вклад в развитие здравоохранения и фармацевтической промышленности России.
Безопасна ли Китруда?
Второе исследование было проведено с участием 411 пациентов, которые имели прогрессирующую меланому и принимали Кейтруду. При этом тяжелые побочные эффекты со стороны кишечника, легких и печени отмечались редко.
Чаще всего у больных возникали такие побочные эффекты, как повышенная утомляемость, кашель, тошнота, сыпь, кожный зуд, снижение аппетита, запор, диарея, боли в суставах (источник).
Информация носит справочный характер. «Евроонко» сотрудничает с израильскими, европейскими и американскими врачами, которые накопили значительный опыт работы с препаратом Кейтруда.
Запись на консультацию круглосуточно
+7+7+78
Исследование KEYNOTE-185
В исследовании KEYNOTE-185 (3 фаза) оценивалась эффективность и безопасность леналидомида в комбинации с низкой дозой дексаметазона с или без пембролизумаба у больных множественной миеломой, у которых невозможна трансплантация аутологичных стволовых клеток.
- Из 301 рандомизированного пациента, 19 умерли в группе пембролизумаба, по сравнению с 9 пациентами из группы контроля (коэффициент рисков, 2.06 (95% CI: 0.93-4.55)).
- Отмечено 22% повышение риска тяжелой токсичности (степень 3-5) в группе пембролизумаба, а также более высокая частота серьезных нежелательных явлений (54% vs. 39%).
- Причинами смерти у больных из группы пембролизумаба, не ассоциированными с прогрессией заболевания, являлись, легочная эмболия, кишечная ишемия, миокардит, сердечная недостаточность, внезапная смерть, пневмония.
Источник:
FDA. Drug Safety and Availability. 31August 2017
Взаимодействие с другими лекарственными препаратами
Специальных исследований фармакокинетического взаимодействия препарата Кейтруда с другими лекарственными препаратами не проводили. Поскольку пембролизумаб выводится из кровообращения за счет катаболизма, то не следует ожидать метаболических лекарственных взаимодействий.
Следует избегать применения системных кортикостероидов или иммуносупрессантов до начала терапии препаратом Кейтруда, учитывая их возможное влияние на фармакодинамическую активность и эффективность препарата Кейтруда. Тем не менее, системные кортикостероиды или другие иммуносупрессанты можно использовать после начала лечения пембролизумабом для терапии иммуноопосредованных нежелательных реакций (см. «Особые указания»).