Виды
В зависимости от причины развития выделяют первичный идиопатический нефротический синдром и вторичные гломерулопатии. Различают следующие виды первичного идиопатического нефротического синдрома:
- болезнь минимальных изменений;
- мембранозная гломерулопатия;
- фокально-сегментарный гломерулосклероз;
- мембрано-пролиферативный (мезангиокапиллярный) гломерулонефрит;
- другие пролиферативные гломерулонефриты.
Вторичный нефротический синдром протекает в рамках следующей патологии:
- Инфекций (инфекционного эндокардита, сифилиса, лепры, гепатитов В и С, мононуклеоза, цитомегаловирусной инфекции, ветряной оспы, ВИЧ, малярии, токсоплазмоза, шистосомиаза);
- Применения медикаментов и наркотических средств (препаратов золота, пеницилламина, препаратов висмута, лития, пробенецида, высоких доз каптоприла, параметадона, героина);
- Системных заболеваний (системной красной волчанки, синдрома Шарпа, ревматоидного артрита, дерматомиозита, пурпуры Шенлейн-Геноха, первичного и вторичного амилоидоза, полиартериита, синдрома Такаясу, синдрома Гудпасчера, герпетиформного дерматита, синдрома Шегрена, саркоидоза, криоглобулинемии, язвенного колита;
- Нарушений обмена веществ (сахарного диабета, гипотиреоза, семейной средиземноморской лихорадки);
- Злокачественных новообразований (болезни Ходжкина, неходжкинской лимфомы, хронического лимфолейкоза, множественной миеломы, злокачественной меланомы, карциномы легких, толстой кишки, желудка, молочных желез, шейки матки, яичников, щитовидной железы и почек);
- Аллергических реакций (укуса насекомых, поллиноза, сывороточной болезни);
- Врождённых заболеваний (синдрома Альпорта, болезни Фабри, серповидно-клеточной анемии, дефицита альфа1-антитрипсина).
Нефротический синдром иногда может развиваться у пациентов, страдающих преэклампсией, IgА-нефропатией, стенозом почечной артерии.
Морфологическая классификация нефротического синдрома по МКБ включает следующие формы патологии почек:
- незначительные гломерулярные нарушения;
- очаговые и сегментарные гломерулярные повреждения;
- мембранозный гломерулонефрит;
- мезангиальный пролиферативный гломерулонефрит;
- диффузный эндокапиллярный пролиферативный гломерулонефрит;
- диффузный мезангиокапиллярный (мембранопролиферативный) гломерулонефрит;
- болезнь плотного осадка;
- диффузный серповидный гломерулонефрит;
- амилоидоз почек.
По активности процесса выделяют полную, частичную ремиссию и рецидив – вновь возникшую протеинурию после полной ремиссии или нарастание после частичной ремиссии.
Определение состояния функции почек при нефротическом синдроме основано на 2 показателях: скорости клубочковой фильтрации и признаках почечного повреждения. Повреждение почек – это структурные и функциональные изменения почек, которые выявляют в анализах крови, мочи или при визуальных обследованиях.
3.Симптомы и диагностика
В нефрологии употребляется аббревиатура МИНС, означающая «минимальные изменения при нефротическом синдроме».
Однако уже на этом этапе наблюдаются характерные отеки, особенно под глазами, в поясничной и генитальной зонах.
С утяжелением патологии отечность распространяется на всю жировую подкожную клетчатку (такое состояние носит название «анасарка»). Прогрессирующие нарушения гидробаланса в организме, которые поначалу сказываются локальными отеками, нарастающим ухудшением состояния волос и кожи (иссушение, растрескивание, затем мокнутие трещин), со временем могут приводить к очень серьезным осложнениям, таким как:
- гиповолемия (резкое сокращение объема крови в организме);
- дистрофия печени и других органов;
- асцит, гидроторакс, гидроперикард (скопление больших объемов жидкости, соотв., в брюшной полости, плевральном пространстве, сердечной сумке);
- инфаркт вследствие тромбоза;
- отеки мозга, легких.
Со стороны мочевыводящей системы наблюдается сокращение суточного объема мочи с повышением ее плотности и специфическим изменением состава.
Нефротический синдром может быть предположен уже при внешнем осмотре больного, сборе жалоб и анамнеза. Одним из наиболее доказательных подтверждений служит характерная картина лабораторных аналитических результатов: резкое повышение белка в моче с появлением аномальных цилиндрических микросгустков из клубочковой системы (протеинурия, цилиндрурия); снижение белка в крови (гипопротеинемия, гипоальбуминемия) с одновременным повышением кровяной концентрации жирных соединений (прежде всего, холестерина). В диагностическом плане информативны также различные модификации УЗИ почек, сердца и сосудов, нефросцинтиграфия, а также гистологическое исследование почечной ткани (биопсия).
О нашей клинике м. Чистые пруды Страница Мединтерком!
Причины
Некоторые люди подменяют понятия нефротический и нефритический синдром. В медицине данные понятия разделяют. Так, нефротический синдром характеризуется поражением почек. При нефритическом синдроме развивается воспалительный процесс и другие сопутствующие признаки.
Развитие нефритического синдрома связано с проникновением антигенов из крови в почечные структуры. После их проникновения в почки активизируются иммунные механизмы, происходит иммунный ответ на чужеродное тело. Нефритический синдром может развиваться вследствие следующих причин:
- вирусная или бактериальная инфекция;
- аутоиммунные заболевания;
- действие радиационного излучения;
- после введения вакцины или сыворотки;
- развития опухоли;
- токсическое воздействие после употребления алкоголя или приема наркотических веществ;
- поражение сосудов вследствие диабета;
- интоксикация организма химическими веществами различных классов;
- хронические патологии мочевыводящих путей;
- повышенная физическая активность;
- резкие изменения температуры воздуха.
Нефритический синдром может развиваться как на фоне воспалительного процесса, так и неинфекционных нарушений – в зависимости от этого разрабатывается тактика лечения. В многопрофильной Юсуповской больнице работают опытные специалисты, которые сопровождают пациента в процессе лечения. Так, при аутоиммунной природе данного синдрома необходима консультация врача-ревматолога.
Записаться на приём
Симптомы
При нефритическом синдроме в Юсуповскую больницу обращаются пациенты с типичными жалобами. Признаками нефритического синдрома являются:
- появление в моче крови;
- изменение цвета мочи – он приобретает багровый оттенок;
- образование отеков, наиболее выраженной является отечность лица, век, ног в вечернее время;
- чувство жажды и медленное образование мочи.
- Патологический процесс в почках может вызывать у больных следующие симптомы:
- слабость, тошнота;
- боли в области поясницы, появляющиеся в ночное время;
- головные боли, появляющиеся при ослаблении организма;
- признаки инфекционных заболеваний дыхательных путей;
- температура тела повышается крайне редко.
Острый нефритический синдром развивается через 7-10 дней после воздействия на организм провоцирующего фактора или инфицирования. При появлении первых признаков патологической работы почек следует воспользоваться услугами специалистов Юсуповской больницы и посетить диагностический class=»aligncenter» width=»1024″ height=»682″[/img]
Диагностика
Во время амбулаторного обследования пациентов с нефротическим синдромом врачи Юсуповской больницы проводят следующие основные диагностические мероприятия:
- клинический анализ крови;
- общий анализ мочи;
- биохимический анализ крови (общий белок, альбумин, мочевина, креатинин, К, Na, Ca, уровень глюкозы и холестерина в сыворотке крови);
- расчет скорости клубочковой фильтрации по формуле Кокрофта-Голта;
- иммуноферментный анализ на вирусный гепатит В и С;
- анализ крови на ВИЧ;
- ультразвуковое исследование почек и органов брюшной полости.
К дополнительным диагностическим обследованиям, которые проводятся на амбулаторном уровне, относится суточная протеинурия или протеин/креатининовый, альбумин/креатининовый коэффициенты, иммунологические методы исследования сыворотки крови, определение концентрации уровня Циклоспорина-А в сыворотке крови. По необходимости может быть выполнена компьютерная томография.
При поступлении пациента в клинику терапии нефрологи Юсуповской больницы назначают следующие обязательные диагностические обследования:
- биопсию почки;
- общий анализ крови (до и после биопсии почки);
- общий анализ мочи (до и после биопсии почки);
- суточную протеинурию или протеин/креатининовый, альбумин/креатининовый коэффициенты;
- ультразвуковое исследование почек (после биопсии);
- коагулограмму;
- морфологическую диагностику биоптата ткани почки;
- иммуногистохимию.
Сложные исследования пациенты имеют возможность пройти в клиниках-партнерах, расположенных в Москве. К дополнительным диагностическим обследованиям, которые проводятся на стационарном уровне, относится электронная микроскопия биоптата ткани почки, определение криоглобулинов в сыворотке крови, электрофорез белков мочи, иммунофиксация белков крови на парапротеины, определение концентрации уровня Циклоспорина-А в сыворотке крови. При необходимости может быть выполнена стернальная пункция, фиброэндогастроскопия, колоноскопия, рентгенография плоских костей черепа.
По показаниям выполняют компьютерную томографию, ультразвуковое допплеровское сканирование сосудов почек, определяют уровень онкомаркеров в биологических жидкостях. При подозрении на токсическое происхождение нефротического синдрома определяют наличие и концентрацию висмута, лития, параметадона, героина в крови.
Пациента консультируют профильные специалисты в зависимости от предполагаемой причины нефротического синдрома:
- онколог – при подозрении на паранеопластическую нефропатию;
- фтизиатр – при подозрении на специфический процесс;
- ревматолог – при подозрении на системное заболевание.
Офтальмолог производит осмотр глазного дна. Хирурга приглашают на консультацию при нефротических кризах для исключения острой хирургической патологии. Консультация невролога назначается при подозрении на нейролюпус, системный васкулит. Гематолог проводит осмотр пациентов при подозрении на миеломную болезнь, болезнь легких цепей. Если у пациента с нефротическим синдромом длительная лихорадка, его консультирует инфекционист. Дифференциальный диагноз нефротического синдрома проводят с заболеваниями, которые протекают с выраженным отечным синдром: циррозом печени, застойной хронической сердечной недостаточностью.
Нефротический синдром
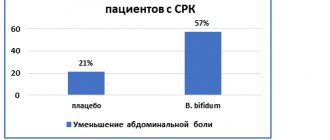
Диагностика основывается на выявленных изменениях в анализах крови и мочи (протеинурия, гиперлипидемия, гипопротеинемия), на клинических данных. Клиника МИНС развертывается постепенно, причем преобладают экстраренальные симптомы, особенно отечный: появляются нарастающие отеки, вначале век, лица, поясничной области (в дальнейшем могут достигать степени анасарки — распространенный отек подкожной клетчатки), половых органов, асцит, гидроторакс, реже — гидроперикард. Характерна значительная гепатомегалия вследствие дистрофии печени. Кожа становится бледной (“перламутровая” бледность) при отсутствии анемии, сухой, появляются признаки гиповитаминозов А, С, В1, В2, дистрофические изменения. Могут наблюдаться ломкость и потускнение волос, на коже — трещины, из которых вытекает жидкость, striae distensae. Ребенок вялый, плохо ест, развивается одышка, тахикардия, систолический шум на верхушке (“гипопротеинемическая кардиопатия”). Тяжелым осложнением у больных анасаркой, т. е. выраженной гипопротеинемией, может быть гиповолемический шок, которому предшествуют анорексия, рвота, резкие боли в животе. В наблюдениях Н. Д. Савенковой и А. В. Папаяна (1997) абдоминальный болевой синдром развивается у 23,5 % детей с гипоальбуминемией менее 15 г/л, а мигрирующие рожеподобные эритемы у 33,3 %, тромботические эпизоды у 12,5 %, ОПН у 3,3% детей с той же выраженностью гипоальбуминемии, тогда как нефротический гиповолемический шок отмечен лишь при уровне белка в сыворотке менее 10 г/л (у 5%). По мере схождения отеков становится все заметнее уменьшение массы скелетных мышц. Артериальное кровяное давление обычно нормальное, лишь у до10% детей может быть кратковременная артериальная гипертензия. Уровень альбумина в сыворотке крови у таких детей менее 10 г/л.
Содержание общего белка в плазме (сыворотке) крови снижено иногда до 40 г/л. Особенно резко снижена концентрация альбуминов и g-глобулина, тогда как уровень a2-глобулинов повышен, т. е. наблюдается резкая диспротеинемия. Сыворотка крови имеет молочный цвет, в ней находят высокий уровень липидов, холестерина, фибриногена. Уровень азотистых шлаков крови, как правило, нормальный, а содержание калия и натрия снижено. СОЭ резко увеличена (до 50–70 мм/час). Ренальная симптоматика — олигурия с высокой относительной плотностью (1,026–1,030) мочи и выраженная протеинурия. При исследовании клубочковой фильтрации по эндогенному креатинину получают нормальные и даже повышенные показатели, но это ложное впечатление. Если учесть степень протеинурии, то клубочковая фильтрация при МИНС всегда снижена.
Клиническая картина, течение и исход нефротического синдрома, осложнившего диффузный гломерулонефрит, отличаются от клиники МИНС. Мочевой синдром при МИНС слагается из следующих симптомов: 1. протеинурия, 2. олигурия с высокой относительной плотностью мочи, 3. цилиндрурия.
Протеинурия при МИНС, как правило, селективная, т. е. в моче находят белки плазмы крови с молекулярной массой менее 85 000 (альбумин и его полимеры, преальбумины, сидерофилин, гаптоглобин, трансферрин, a1- и b-глобулины, a1- и a2-гликопротеины и др.). В большинстве случаев у детей с селективной протеинурией прогноз лучше, и они чувствительны к терапии глюкокортикоидами. В генезе протеинурии имеет значение и нарушение реабсорбции белка в почечных канальцах. Неселективная протеинурия, когда в моче есть много крупномолекулярных белков, как правило, следствие фибропластического процесса, склероза, т. е. для МИНС нехарактерна. Напомним, что у здорового ребенка старше 4 лет в суточной моче может быть до 100–150 мг белка. Олигурия связана с гиповолемией, гиперальдостеронизмом, поражением канальцев. Из-за протеинурии относительная плотность мочи увеличена, достигает 1,040. Высока активность в крови больных и АДГ.
Иногда при нефротическом синдроме отмечается массивная лейкоцитурия, обусловленная иммунопатологическим процессом в почках. Лейкоцитурия чаще кратковременная и не связана с бактериальной инфекцией, т. е. пиелонефритом. Частота выявления лейкоцитурий и эритроцитурий при МИНС по данным разных авторов не превышает 10%.
При большом количестве белка в моче он может свернуться еще в канальцах, принимая их форму; на этот слепок наслаивается жироперерожденный почечный эпителий — так образуются гиалиновые, зернистые и восковые цилиндры.
Отеки. Массивная и длительная альбуминурия у больного с нефротическим синдромом в конце концов неизбежно вызывает гипопротеинемию, так как потери белка превышают интенсивность его синтеза. Гипопротеинемия ведет к нарушению старлингова равновесия между гидродинамическим, фильтрационным и коллоидно-осмотическим давлением. Это приводит к преобладанию оттока жидкости из артериального русла над притоком. Отеки начинают появляться, когда уровень альбумина снижается ниже 27 г/л плазмы и развиваются всегда, если гипоальбуминемия достигает 18 г/л. В патогенезе отеков важную роль играет и вторичный гиперальдостеронизм, типичный для нефротического синдрома. В результате его в организме задерживается натрий, а следовательно, и вода, хотя в крови имеется гипонатриемия.
Гипопротеинемия. Основной причиной гипопротеинемии у больных с нефротическим синдромом являются большие потери альбуминов с мочой и перемещение их в ткани. Кроме того, имеют значение повышенный катаболизм альбуминов, нарушение белоксинтезирующей функции печени. Уменьшение содержания g-глобулинов в крови больных прежде всего с нарушением их синтеза. Гипоальбуминемия и гиповолемия, дефицит антикоагулянтов — антитромбина III и протеинов С и S, гиперфибриногенемия, гиперлипидемия создают угрозу для тромботических нарушений у больных МИНС.
Гиперлипидемия. Некоторые авторы связывают увеличение уровня липопротеинов низкой и очень низкой плотности, холестерина и липидов (свободные жирные кислоты, триглицериды, фосфолипиды и др.) при нефротическом синдроме с нарушением функции печени, другие объясняют это явление понижением функции щитовидной железы. В связи с тем, что внутривенное введение раствора альбумина препятствует нарастанию гиперхолестеринемии, предполагают, что увеличение уровня холестерина в крови происходит компенсаторно вследствие уменьшения содержания альбуминов. Поскольку липидемию в эксперименте можно получить после перевязки мочеточников, высказывают мысль о том, что гиперхолестеринемия и липидемия при МИНС имеют почечное происхождение и зависят от повреждения интермедиарного обмена в ферментной системе канальцев. В генезе гиперлипидемии имеет значение также низкий уровень в крови лецитин-холестеринацетилтрансферазы, в больших количествах выделяющейся с мочой, и низкая активность липопротеидлипазы. При МИНС обычно диагностируют IIа и IIб типы гиперлипидемий.
Нарушения фосфорно-кальциевого обмена (гипокальциемия, остеопороз, остеомаляция) обусловлены нарушением функции почек, а также метаболизма витамина D.
Нарушения обмена железа и микроэлементов с низкими уровнями в крови как железа, так и цинка, меди, кобальта определяют в значительной степени склонность таких больных к анемиям, трофическим расстройствам кожи, задержке роста, а возможно — иммунодефицитам.
Вязкость крови при МИНС повышена за счет гиперлипидемии, повышенной адгезивности тромбоцитов. В то же время уровни факторов свертывания крови (прокоагулянтов) и антисвертывания (антитромбин III, протеины С и S) снижены, что и объясняет сравнительно низкую частоту декомпенсированного ДВС-синдрома при МИНС.
Инфекции — прежде одно из очень частых осложнений МИНС. Особенно часто были перитониты, которые в большинстве случаев вызывались пневмококками, но в 25–50% случаев — кишечной палочкой.
Характерная клинико-лабораторная картина МИНС в подавляющем большинстве случаев (90–95%) у детей 2–7 лет позволяет поставить диагноз без биопсии почек. Хороший и быстрый ответ на терапию глюкокортикоидами подтверждает диагноз. В то же время, целесообразно у любого ребенка с нефротическим синдромом определить уровень IgE, выяснить наличие хронических персистирующих вирусных инфекций (гепатит В, цитомегалия, герпесвирусные инфекции и др.), так как положительные результаты существенно дополняют и модифицируют терапию. О рецидивирующем течении нефротического синдрома свидетельствуют 2 рецидива в год, а о часто рецидивирующем — 3 и более рецидивов в год. Ремиссию констатируют при отсутствии протеинурии или ее значении менее 4 мг/м2 в час и достижении уровня альбумина сыворотки 35 г/л. Биопсия показана детям с нефротическим синдромом в возрасте до года и старше 12 лет, ибо у них очень мала частота МИНС.
Лечение
Лечение нефритического синдрома преследует следующие цели:
- достижение ослабления или исчезновения признаков заболевания;
- ликвидация внепочечных симптомов (артериальной гипертензии, отеков) и осложнений (электролитных нарушений, инфекции, нефротического криза);
- замедление прогрессирования хронической болезни почек и отдаление ее терминальной стадии с помощью диализа, трансплантации почки.
Пациенту в зависимости от тяжести нефротического синдрома рекомендуют свободный или постельный режим (при тяжелом состоянии пациента и наличии осложнений). Физическая активность дозированная – по 30 минут 5 раз в неделю. Пациентам врачи рекомендуют отказаться от курения и употребления алкоголя. Диета сбалансированная, с адекватным количеством белка (1,5-2г/кг), калоражем по возрасту. При наличии артериальной гипертензии и отеков ограничивают употребление поваренной соли (менее 1-2г в сутки).
Патогенетическую терапию после установки морфологического диагноза начинают в клинике терапии и продолжают в амбулаторных условиях. Лечение значительных отеков проводят диуретиками. Мочегонные препараты не назначают при диарее, рвоте, гиповолемии. При длительно сохраняющихся отеках назначают фуросемид внутривенно однократно болюсно или торасемид внутрь. Для лечения пациентов с рефрактерными отеками используют комбинацию петлевых и тиазидоподобных или калийсберегающих диуретиков. При высоком риске развития нефротического криза применяют комбинацию альбумина и диуретиков.
Если у пациента наблюдаются резистентные отеки в сочетании с почечной недостаточностью в остром периоде нефротического синдрома, проводят гемодиализ с ультрафильтрацией до выхода из критического состояния почечной недостаточности и появления диуреза.
Кардиологи Юсуповской больницы дифференцированно подходят к выбору метода терапии у пациентов с нефритическим синдромом. При отсутствии симптомов острого почечного повреждения с антигипертензивной целью назначают ингибиторы АПФ или блокаторы АТ1-рецепторов ангиотензина, но не в комбинации. При сохраняющемся высоком артериальном давлении применяют блокаторы кальциевых каналов. Если у пациента регистрируется частый пульс или присутствуют признаки хронической сердечной недостаточности, дополнительно назначают бета-блокаторы.
Патогенетическая терапия нефритического синдрома зависит от морфологического варианта. Ее назначают только после проведения биопсии почки и уточнения морфологического диагноза.
При терапии болезни проводят также лечение заболевания, которое вызвало нефротический синдром. При обнаружении паразитов, гельминтов назначают антипаразитарные (противогельминтные) препараты. Пациентам с новообразованиями проводят химиотерапию, лучевое лечение, выполняют оперативное вмешательство. При диабетической нефропатии эндокринологи проводят лечение сахарного диабета, нефрологи назначают препараты, оказывающие нефропротекторное действие.
В дебюте нефротического синдрома пациентам назначают метилпреднизолон или преднизолон. По достижению полной или частичной ремиссии постепенно снижают дозы преднизолона.
Пациенты, у которых после приема полной дозы преднизолона в течение 16 недель не наступает полной или частичной ремиссии, определяются как стероид-резистентные. Им проводится комбинированная терапия циклоспорином-А и минимальной дозой преднизолона.
У 50-75% пациентов с нефротическим синдромом, которые ответили на стероидную терапию, встречаются рецидивы. При повторном возникновении нефротического синдрома назначают преднизолон. Если рецидивы наступают три и более раз в течение одного года или имеет место стероид-зависимая форма, используют комбинированную терапию низкими дозами преднизолона в сочетании с одним из препаратов следующих групп:
- алкилирующих агентов;
- ингибиторов кальцинейрина;
- антиметаболитов.
Пациентам с нефротическим синдромом и хронической болезнью почек назначают статины. При резистентном нефротическом синдроме используют ритуксимаб. Лечение нефротического синдрома при системной красной волчанке проводят в зависимости от класса волчаночного нефрита.
Начатое в клинике терапии патогенетическое лечение продолжают в амбулаторных и домашних условиях пациента под ежемесячным контролем результатов лабораторных данных (клинического анализа крови, общего анализа мочи, биохимического анализа крови). Проводят мониторинг уровня протеинурии по тест-полоскам 1 раз в 1-2 недели, пациенты регулярно измеряют артериальное давление. При нарастании количества протеинов в моче определяют протеин/креатининовый коэффициент и проводят коррекцию иммуносупрессивной терапии. Если пациент не отвечает на проводимую иммуносупрессивную терапию, выполняют повторную биопсию почки в условиях клиники терапии.
Если причиной нефротического синдрома являются инфекционные заболевания, проводят антибактериальную терапию. Препараты подбирают каждому пациенту индивидуально в зависимости от вида возбудителя инфекции. При высоком риске артериальных и венозных тромбозов подкожно вводят низкомолекулярные гепарины в течение длительного времени.
4.Лечение
Любая терапевтическая схема лечения нефротического синдрома обязательно включает строгую диету с ограниченным потреблением натрия (в частности, с поваренной солью); акцент в рационе смещается в сторону калийсодержащих и витаминных продуктов. По индивидуальным показаниям, которые могут быть очень разными (или даже противоположными, что делает любые попытки самолечения опасными) назначаются антибиотики, гипотензивные средства, иммуносупрессоры, гормональные препараты, цитостатики, средства нормализации уровня белка в крови.