Что известно об «Ультрикс Квадри»?
Это инактивированная расщепленная вакцина, содержащая антигены вируса гриппа типов A (H1N1 и H3N2) и В (линии Yamagata и Victoria). Таким образом, в отличие от обычного Ультрикса, она является четырехкомпонентной. Вакцины такого типа появились в России 2 года назад, в 2022 году. Они считаются более эффективными (так как защищают от большего количества разновидностей гриппа), но производственных мощностей изначально хватало только для групп риска (людей с тяжелыми хроническими заболеваниями), так что широкому кругу пациентов они стали доступны сравнительно недавно. Сейчас она оценивается как одна из самых надежных прививок от гриппа, доступных россиянам. Вакцина была создана , входящей в государственную корпорацию «Ростех».
Вакцинопрофилактика гриппа. Новая отечественная вакцина Ультрикс®
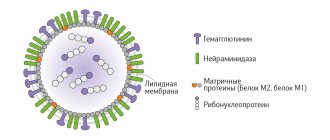
Вирусы гриппа А наиболее контагиозны и вирулентны, в их состав входят 2 типа нейраминидазы (Na1, NA2) и 3 типа гемагглютинина (HA1, HA2, HA3). В состав вируса гриппа В входят 1 тип нейраминидазы и 1 тип гемагглютинина. Вирус С не содержит нейраминидазы, но содержит гемагглютинин, имеет рецептор-разрушающий энзим – нейраминат-0-ацетилэстеразу и не обладает изменчивостью. Изменение NA или HA называют антигенным шифтом. Промежуточными хозяевами и природным резервуаром вируса гриппа А могут быть птицы (птичий грипп). Изменчивость вируса может быть связана с точечными мутациями в геноме и изменением NA или HA (антигенный дрейф). Возможна полная замена HA и NA через механизм реассортации/рекомбинации (антигенный шифт), что происходит 1 раз в 10–12 лет и может приводить к развитию пандемии. К пандемиям гриппа отнесены: «испанка» (H1N1) в 1918 г., азиатский грипп (H2N2) в 1957 г., гонконгский грипп (H3N2) в 1968 г. При антигенном дрейфе заболевают около 10% населения, при антигенном шифте – 40–60%, т. к. отсутствует иммунитет к новому типу вируса [1, 2]. По данным ВОЗ, взрослый человек 3–4 р./год может болеть респираторными инфекциями, посещающие школу дети – 4–5 раз, дошкольники – до 6 раз, дети первого года жизни могут заболевать 2–12 р./год [3]. Последняя эпидемия гриппа наблюдалась в 2009 г., она была вызвана вирусом гриппа А (H1N1) pdm 09. В мире заболели 220 тыс. человек, из них 1900 человек умерли [3, 4]. В эпидемический сезон 2012–2013 гг. вирус гриппа А (H1N1) pdm 09 циркулировал уже как сезонный, вместе с другими вирусами гриппа А (H3N2) и В [3, 16]. В России в эпидсезон 2013–2014 гг. зарегистрировано 138 умерших от гриппа, подтвержденного лабораторно. От 135 умерших выделен вирус гриппа А (H1N1) pdm 09, от 1 человека выделен вирус А (H3N2) и от 1 – вирус гриппа В. У 40,8% умерших диагностирована эндокринная патология, у 24,8% – ожирение и у 37,6% – заболевания сердечно-сосудистой системы [3].
Специфическая вакцинопрофилактика гриппа проводится достаточно эффективно. В таблице 2 перечислены наиболее часто используемые вакцины. Вакцины обладают сходной иммуногенностью, их состав изменяется каждый год, согласно прогнозу ВОЗ. Отечественная вакцина гриппол является тривалентной полимер-субъединичной вакциной, в ее состав входит полиоксидоний, высокомолекулярный адъювант, связанный с антигенами вируса гриппа А (H1N1, H3N2) и В – нейраминидазой и гемагглютинином. Полиоксидоний усиливает формирование протективного иммунитета, несмотря на сниженное содержание в вакцине антигенов вирусов гриппа. Для инактивации вируса используется ультрафиолет, что повышает безопасность вакцины. Гриппол разрешен для применения с 6 мес., включен в национальный календарь прививок, является низкореактогенной и высокоочищенной вакциной, его безопасность контролируется на уровне Государственного института стандартизации и контроля при Роспотребнадзоре РФ. Многочисленные исследования показывают, что после вакцинации заболеваемость гриппом снижается в 3–4 раза по сравнению с контрольной группой, а за счет полиоксидония повышается резистентность к другим респираторным инфекциям. За создание вакцины коллектив авторов был удостоен Государственной премии РФ в 2002 г. [5, 6].
В группах риска (дети, люди старше 50 лет, пациенты с сопутствующими заболеваниями, иммунодефицитами, аллергическими заболеваниями, при которых наблюдаются более тяжелое течение инфекций, развитие осложнений и смертельные исходы), по рекомендациям ВОЗ вакцинация проводится субъединичными вакцинами. У пожилых людей высок риск серьезных осложнений, включая вторичную бактериальную пневмонию, обострения сопутствующих хронических заболеваний, приводящие к госпитализации и повышенной смертности. Инактивированные противогриппозные вакцины применяют более 50 лет, они безопасны, проверены на миллионах людей [7, 8]. Вакцинация уменьшает число смертельных исходов, развитие и тяжесть осложнений [9–11, 13–15]. У детей с аллергическими заболеваниями показана эффективность вакцины инфлювак [12]. Для профилактики эпидемий необходимо вакцинировать наибольшее количество населения. С учетом большого количества вирусов, способных вызывать ОРЗ, заболеваемость гриппом после вакцинации должна быть подтверждена серологически. В рандомизированном контролируемом исследовании (Нидерланды) после вакцинации 1838 человек старше 60 лет случаи гриппа, подтвержденные серологически, составили 58% ОРЗ [7]. По результатам метаанализа показано, что вакцинация против гриппа пожилых людей в различных странах позволяет уменьшить количество случаев госпитализации в среднем на 33%, в т. ч. связанные с пневмонией и гриппом, – на 27–38%, общую смертность – на 50% [11, 13].
Несмотря на успехи профилактики, объем вакцинации остается ограниченным [24, 25]. В США в 1997 г. вакцинированных в возрасте до 65 лет было менее 30%, сейчас, по данным ВОЗ, количество вакцинированных увеличивается. Не всегда наблюдается полное соответствие структуры вакцины циркулирующим штаммам, соответственно, защитный эффект вакцины составляет 70–90% [25], в в группах риска, у лиц преклонного возраста, пациентов с иммунодефицитом эффективность снижается до 30–40% [26, 27].
Меры по предотвращению пандемии необходимо принимать заранее, т. к. в случае ее развития существенно возрастет расход лекарственных препаратов, увеличится потребность в первичных консультациях, число обращений к врачу, случаев госпитализации, осложнений. По прогнозам ВОЗ, при пандемии за короткий срок число посещений в поликлиниках достигнет 233 млн, поступлений в больницу – 5,2 млн, смертей – 7,4 млн человек [28]. Предполагают, что наиболее выраженные проявления пандемии будут отмечаться в слаборазвитых странах вследствие недостаточно организованной работы системы здравоохранения. С другой стороны, будет наблюдаться недостаток вакцины, сотрудников, что повлечет за собой нарушения работы учреждений здравоохранения, общественного транспорта, правоохранительных органов. Без развития пандемии в США ежегодно от гриппа умирает от 10 тыс. до 40 тыс. человек, при этом в последние 60 лет не было отмечено снижения показателей смертности от гриппозной пневмонии [29].
В России ежегодно регистрируется от 27 млн до 41 млн больных ОРЗ, 95% которых вызываются вирусами. В 2002 г. привитые от гриппа в России составляли 10–12%, в эпидсезон 2013–2014 гг. – 27,8% населения [3]. По приказу Министерства здравоохранения РФ № 125н от 21 марта 2014 г. «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям» в группу риска входят: дети с 6 мес.; учащиеся 1–11 классов, обучающиеся в профессиональных образовательных организациях и образовательных организациях высшего образования; взрослые, работающие по отдельным профессиям и должностям (работники медицинских и образовательных организаций, транспорта, коммунальной сферы); беременные женщины; взрослые старше 60 лет; лица, подлежащие призыву на военную службу; лица с хроническими заболеваниями, в т. ч. с заболеваниями легких, сердечно-сосудистыми заболеваниями, метаболическими нарушениями и ожирением [18].
До конца 1970-х гг. в России вакцинацию против гриппа проводили живой ослабленной вакциной. Проведение вакцинации в группе риска живой ослабленной вакциной невозможно, что связано с реактогенностью и возможностью развития гриппа у ослабленного контингента пациентов. В последние годы в практическое здравоохранение активно внедряются вакцины IV поколения, виросомальные вакцины, в которые введены мембранные антигены вируса гриппа, что позволяет повысить их иммуногенность и приводит к активации клеточного иммунитета, повышает титр и увеличивает длительность циркуляции протективных антител [17].
Новая отечественная инактивированная расщепленная вакцина Ультрикс® получена с помощью обработки вирусов гриппа детергентом β-октилгликозидом и в своем составе содержит высокоактивные псевдовирусные частицы в виде виросом, поверхностные и внутренние антигены вирусов гриппа А (H1N1 – 15 мкг, H3N2 – 15 мкг) и В (15 мкг). Введение вакцины не приводит к повышению уровня иммуноглобулина (Ig) E, что указывает на ее безопасность при аллергических заболеваниях [19]. В клинических испытаниях показана безопасность вакцины у детей старше 6 лет, взрослых 18–60 лет и старше 60 лет. Иммуногенность вакцины по уровню сероконверсии антител к вирусу гриппа А (H1N1) – 94%, А (H3N2) – 86%, В – 90%. Состав антигенов вакцины меняется согласно рекомендациям ВОЗ. Через 6 мес. после вакцинации сохранялся защитный титр антител к вирусу гриппа А (H1N1) у 81,3%, А (H3N2) – у 61,5%, В – у 47,3% вакцинированных, при этом не наблюдалось достоверного снижения титра антител. При вакцинации детей не было отмечено выраженной реактогенности, иммуногенность вакцины по уровню сероконверсии антител составляла к вирусу гриппа А (H1N1) 70%, А (H3N2) – 50%, В – 70%. После вакцинации не отмечалось выраженных общих и местных реакций [3]. Эффективность вакцинации оценивали в клиническом исследовании в октябре – ноябре 2013 г. у 5743 жителей 7 регионов РФ, 325 человек из них были старше 60 лет. Местную реакцию наблюдали в единичных случаях, при этом не потребовалось терапевтического вмешательства [3].
Результаты проведенной вакцинации против гриппа в 9 школах г. Подольска Московской области показали хороший эффект, заболеваемость гриппом снизилась в 4,7 раза, другими ОРВИ – в 1,4 раза [20, 21]. По мнению В.К. Таточенко, в цельновирионных и расщепленных вакцинах против гриппа может сохраняться РНК вируса, что может приводить к повышению синтеза интерферона и противовирусной защите против других вирусов. Изучение возможности профилактики других ОРВИ после вакцинации вакциной Ультрикс® проводилось у 594 медицинских работников, 1389 человек из закрытых организованных коллективов в Калужской области, 1000 жителей г. Тимашевска Краснодарского края. Среди непривитых медицинских работников заболеваемость гриппом была в 2,8 раза выше по сравнению с привитыми. В закрытых коллективах заболеваемость гриппом у непривитых была в 47 раз выше по сравнению с привитыми вакциной Ультрикс®. Заболеваемость гриппом у привитых жителей г. Тимашевска была в 2,4 раза ниже, чем в контрольной группе. Осложненное течение ОРВИ у привитых, если пациенты заболевали, зарегистрировано в 9,1% случаев, в контрольной группе – в 36% случаев [3].
И. Фельдблюм и соавт. проведено открытое проспективное рандомизированное исследование с включением 1008 взрослых от 18 до 63 лет, 504 человека из них были вакцинированы вакциной Ультрикс®, 504 человека не были вакцинированы (контрольная группа). В течение 6 мес. осуществляли проспективное наблюдение за группой. Иммуногенность вакцины оценивали по уровню сероконверсии (доля лиц, у которых титр противовирусных антител возрос в 4 раза) и серопротекции (доля лиц, у которых титр антител был больше 1:40). Наблюдение в поствакцинальном периоде выявило слабые местные реакции у 0,8% вакцинированных, слабые общие – у 2,8%, комбинированные – у 0,4% вакцинированных. Наблюдение в течение 6 мес. не выявило значимых изменений биохимических показателей крови и мочи (показатели билирубина, креатинина, мочевины, ферменты печени, в моче не определяли повышения уровня белка и лейкоцитов). Общий IgE на начало исследования составлял 50,14 МЕ/мл, через 180 дней после вакцинации оставался в пределах нормы – 88,3 МЕ/мл (разница достоверна). Повышение уровня IgE может быть связано с усилением экологической и антропогенной нагрузки в условиях крупного города (г. Пермь), преобладанием T-хелперов 2-го типа иммунного ответа. Иммуногенность вакцины по уровню сероконверсии антител к вирусу гриппа А (H1N1) составила 66,7%, А (H3N2) – 53,5%, В – 46,5%. Фактор сероконверсии к вирусу гриппа А (H1N1) был равен 5,18, А (H3N2) – 3,94, В – 3,55. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 98%, А (H3N2) – у 76,8%, В – у 70,7% привитых. После вакцинации у привитых диагностирован 31 случай, в контрольной группе – 32 случая ОРВИ. Показатель заболеваемости у привитых составил 61,5 на 1 тыс. человек, в контрольной группе – 85,3 на 1 тыс. человек (разница достоверна). В группе привитых диагноз гриппа не был подтвержден, в контрольной группе подтвержден у 5 человек (длительность заболевания – 7,6 дня (среднетяжелая форма). Таким образом, коэффициент защищенности составил 100% [22].
И. Никоноровым и соавт. проведено сравнительное исследование вакцины ваксигрип и новой виросомальной вакцины Ультрикс® в течение 2007, 2008 и 2010 гг. на базе Института гриппа и в Пермской государственной медицинской академии им. Е.А. Вагнера в 2011 г. в соответствии с национальным стандартом. В исследование были включены 1286 человек, включая 78 детей, 40 взрослых старше 60 лет и 1208 взрослых до 60 лет. Ультрикс® был использован в 2-х дозировках: 1) 35 мкг – антигены HA вирусов гриппа А (H1N1 – 10 мкг, H3N2 – 10 мкг) и В (15 мкг); 2) 45 мкг – антигены НА вирусов гриппа А (H1N1 – 15 мкг, H3N2 – 15 мкг) и В (15 мкг). Состав вакцины ваксигрип 45 мкг – антигены НА вирусов гриппа А (H1N1 – 15 мкг, H3N2 – 15 мкг) и В (15 мкг). Результаты наблюдения и осмотра пациентов терапевтом, оториноларингологом заносили в индивидуальные регистрационные карты. При вакцинации 150 клинически здоровых добровольцев в возрасте 18–60 лет слабые системные реакции наблюдали у 8% при дозе вакцины Ультрикс® 35 мкг, у 12% – при дозе вакцины Ультрикс® 45 мкг и у 8% – при вакцинации ваксигрипом в дозе 45 мкг. Уровень IgE при первом обследовании до вакцинации превышал показатели нормы в 28% случаев при дозе вакцины Ультрикс® 35 мкг, в 14% случаев – при дозе вакцины Ультрикс® 45 мкг и в 16% случаях – до вакцинации ваксигрипом. У добровольцев не диагностировали аллергических заболеваний. Лица с аллергическими заболеваниями не вакцинировались по критериям исключения. Иммуногенность вакцины Ультрикс® 35 мкг по уровню сероконверсии антител к вирусу гриппа А (H1N1) составила 94%, А (H3N2) – 86%, В – 90%. Фактор сероконверсии к вирусу гриппа А (H1N1) был равен 18, А (H3N2) – 8,6, В – 10,4. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 94%, А (H3N2) – у 90%, В – у 78% привитых [29]. Иммуногенность вакцины Ультрикс® 45 мкг была сходной по уровню сероконверсии антител к вирусу гриппа А (H1N1) – 94%, А (H3N2) – 86%, В – 90%. Фактор сероконверсии к вирусу гриппа А (H1N1) был равен 19,4, А (H3N2) – 9,4, В – 6,9. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 86%, А (H3N2) – у 90%, В – у 78% привитых. Иммуногенность вакцины ваксигрип 45 мкг по уровню сероконверсии антител к вирусу гриппа А (H1N1) составила 98%, А (H3N2) – 94%, В – 88%. Фактор сероконверсии к вирусу гриппа А (H1N1) достиг 26,7, А (H3N2) – 9,7, В – 14,7. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 100%, А (H3N2) – у 94%, В – у 86% привитых [29]. На втором этапе была изучена возможность вакцинации 40 лиц в возрасте старше 60 лет. Данные о возможности вакцинации пожилых людей остаются противоречивыми [30]. 20 человек были вакцинированы вакциной Ультрикс® 45 мкг и 20 человек – ваксигрипом 45 мкг. Слабые системные реакции были отмечены у 15% пациентов в каждой группе. После вакцинации уровень общего IgE оставался в пределах нормы. У пожилых иммуногенность вакцины Ультрикс® 45 мкг была сходной по уровню сероконверсии антител к вирусу гриппа А (H1N1) – 80%, А (H3N2) – 85%, В – 65%. Фактор сероконверсии составил к вирусу гриппа А (H1N1) 9,5, А (H3N2) – 12,1, В – 28,3. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 70%, А (H3N2) – у 90%, В – у 50% привитых. Иммуногенность у пожилых вакцины ваксигрип 45 мкг по уровню сероконверсии антител к вирусу гриппа А (H1N1) была равна 95%, А (H3N2) – 90%, В – 80%. Фактор сероконверсии к вирусу гриппа А (H1N1) достиг 21,9, А (H3N2) – 12,6, В – 7,5. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 95%, А (H3N2) – у 90%, В – у 80% привитых [29]. На следующем этапе были вакцинированы 36 детей в возрасте 12–18 лет, а в 2010–2011 гг. были вакцинированы 42 ребенка в возрасте 6–12 лет. Дети были рандомизированно разделены на группы, получавшие Ультрикс® 45 мкг и ваксигрип 45 мкг. При вакцинации не отмечали повышения общего IgE у детей. Не было зарегистрировано аллергических заболеваний, но у 55% детей в возрасте 6–12 лет уровень IgE был повышен и снижался при наблюдении после вакцинации.
Иммуногенность у детей 12–18 лет вакцины Ультрикс® 45 мкг была по уровню сероконверсии антител к вирусу гриппа А (H1N1) 70%, А (H3N2) – 50%, В – 70%. Фактор сероконверсии составил к вирусу гриппа А (H1N1) 6,5, А (H3N2) – 2,7, В – 4. Серопротекция наблюдалась к вирусу гриппа А (H1N1) у 90%, А (H3N2) – у 80%, В – у 85% привитых. Показатели сопоставимы с результатами вакцинации ваксигрипом 45 мкг [29]. Таким образом, исследования показали хорошую безопасность, иммуногенность и низкую реактогенность новой отечественной гриппозной виросомальной вакцины Ультрикс® у детей старше 6 лет и взрослых, включая лиц старше 60 лет.
Литература 1. Грипп и другие ОРВИ / под ред. проф. В.П. Малого и проф. М.А. Андрейчина М.: ГЭОТАР-Медиа, 2013. 319 с. 2. Гендон Ю.З. Анализ активности гриппа в эпидемический сезон 2003/2004 гг. // Новости вакцинопрофилактики. Вакцинация. 2004. № 3. С. 6. 3. Селькова Е.П., Гренкова Т.А., Гудова Н.В. и др. Эпидемиологическая значимость вакцинопрофилактики гриппа. Отечественная противогриппозная вакцина последнего поколения // Эпидемиол. и инфекционные болезни. Актуальные вопросы. 2014. № 4. С. 43–51. 4. WHO. Guidellnes for pharmacological management of pandemic (H1N1) 2009 influenza and other influenza viruses. Publication date: 20 August 2009. 5. Хаитов Р.М., Некрасов А.В., Бектемиров Т.А. Аллергия, астма и клиническая иммунология. 1999. № 9. С. 7–9. 6. Бектемиров Т.А., Горбунов М.А., Ельшина Г.А. Перспективы применения полиоксидония с вакцинами против вирусных гепатитов и гриппа // Аллергия, астма и клиническая иммунология. 2001. № 1.С. 63–65. 7. World Health Organization. Influenza vaccines // Wkly Epidemiol Rec. 2000. Vol. 75. Р. 281–288. 8. World Health Organization. Influenza vaccines // Wkly Epidemiol Rec. 2002. Vol. 77. Р. 229. 9. Учайкин В.Ф., Шамшева О.В. Вакцинопрофилактика. Настоящее и будущее. М.: ГЭОТАР-Мед, 2001. 399 с. 10. Palach А.M. Tens years experience with a subunit influenza vaccine // Europ.J.of Clin.Research. 1992. Vol. 3. Р. 117–138. 11. Palach А.М., de Bruijn I.A. J. Nauta. Influenza immunization // J. of Clin. Research. 1999. Vol. 2. Р. 111–139. 12. Маркова Т.П., Чувиров Д.Г. Применение вакцины инфлювак для профилактики гриппа у детей с аллергическими заболеваниями // Росс. вестник перинатологии и педиатрии. 2001. № 6. С. 53–54. 13. Nichol K.L. Wuomema J, von Sternberg T. Benefits of influenza vaccination for low-, intermediate-, and high-risk senior citizens // Arch Intern Med. 1998. Vol.158. Р.1769–1776. 14. Uphoff H., Cohen J.M., Fleming D., Noone A. Harmonisation of national influenza surveillance morbidity data from EISS: a simple index // Euro Surveill. 2003 Jul. Vol. 8 (7). Р. 156–164. 15. Aymard M. Hospices Civils de Lyon, France. Presentation at a symposium entitled. Meeting the challenge of influenza., European Respiratory Society 1998 Annual Congress, Geneva, Switzerland. 16. Письмо Роспотребнадзора от 24.06.2013 № 01/7080-13-32 «Об итогах распространения гриппа и ОРВИ в мире и Российской Федерации в эпидсезон 2012-2013 гг. и прогноз на эпидсезон 2013-2014 гг.». 17. Bruljn I.A., Nauta J., Gerez L. Virosomal influenza vaccine: a save and effective influenza vaccine with high efficacy in elderly and subjects with low pre-vaccination titers // Virus Research. 2004. Vol. 103. P. 139–145. 18. Приказ Минздрава России от 21 марта 2014 г. № 125н «Об утверждении национального календаря профилактических прививок и календаря профилактических прививок по эпидемическим показаниям». 19. Зверев В.В., Ерофеева М.К., Максакова М.Л. и др. Разработка и внедрение в практику здравоохранения РФ новой отечественной расщепленной виросомальной вакцины против гриппа // Лечащий врач. 2008. № 9. С. 68–70. 20. Брико Н.И. Вакцинация – решающая мера профилактики гриппа // Лечащий врач. 2011. № 8. С. 90–93. 21. Хаитов Р.М., Некрасов А.В., Лыткина И.Н. и др. О влиянии вакцинопрофилактики на уровень заболеваемости гриппом и ОРВИ // Вакцинопрофилактика гриппа. Вакцинация. 2001. № 5 (7). С. 27–34. 22. Фельдблюм И., Полушкина А., Воробьева И. Иммунизация взрослых 18-60 лет отечественной гриппозной виросомальной вакциной ультрикс // Врач. 2014. № 9. С. 54–56. 23. Никаноров И., Максакова В., Фельдблюм И. и др. Отечественный препарат последнего поколения для профилактики гриппа // Врач. 2014. № 3. С. 1–6. 24. Murphy B.R.,Webster R.G. Orthomyxoviruses. In: Fields B.N. et al. editors. Fields virology, 3rd Edn. Philadelphia, USA: Lippincott–Raven, 1996. Р. 1397–445. 25. Palache A.M. Influenza vaccines. A reappraisal of their use // Drugs. 1997. Vol. 54. Р. 841–856. 26. Arden N.H., Patriarca P.A., Kendal A.P. Experiences in the use and efficacy of inactivated influenza vaccine in nursing homes. In: Kendal A.P., Patriarca P.A., editors. Options for the Control of Influenza. New York; Alan R. Liss Inc., 1986. Р. 155–168. 27. Patriarca P.A.,Weber J.A., Parker R.A. et al. Efficacy of influenza vaccine in nursing homes: reduction in illness and complications during an influenza A (H3N2) epidemic // JAMA. 1985. Vol. 253. Р. 1136–1139. 28. WHO checklist for influenza pandemic preparedness planning. Geneva, World Health Organization, 2005. 29. Center for Disease Control and Prevention (CDC). Prevention and control of influenza: recommendations of the Advisory Committee on Immunization Practices (ACIP) // MMWR. 2000. Vol. 49. Р. 1–38. 30. Lang P., Mendes A., Socquet J. et al. Effectiveness of influenza vaccine in aging and older adults: comprehensive analysis of the evidence // Clin. Interv. Aging. 2012. Vol. 7. P. 55–64.
Что входит в состав вакцины «Ультрикс Квадри»?
Точный состав антигенов, как и у других противогриппозных вакцин, обновляется ежегодно в соответствии с рекомендациями ВОЗ. Дозировка каждого составляет не менее 15 мкг, что рекомендовано ВОЗ. Помимо непосредственно них, в состав препарата входят только 3 компонента: это полисорбат 80, широко использующийся в пищевой промышленности как эмульгатор, октоксинол 10 в качестве стабилизатора и фосфатно-буферный раствор. Ультрикс Квадри не содержит дополнительных усилителей иммунного ответа, за что некоторые другие отечественные препараты неоднократно подвергались критике.
СПОСОБ ПРИМЕНЕНИЯ И ДОЗИРОВКА
Вакцинация проводится ежегодно в осенне-зимний период. Возможна вакцинация в начале эпидемического подъема заболеваемости гриппом.
Вакцину вводят в внутримышечно в дозе 0,5 мл однократно в область дельтовидной мышцы (верхняя треть наружной поверхности плеча).
Не пригоден к применению препарат в шприцах/флаконах с нарушенной целостностью или маркировкой, при изменении физических свойств (цвета, прозрачности), при наличии в растворе посторонних частиц, при истекшем сроке годности, нарушении требований к условиям хранения.
Вскрытие шприцев /флаконов и проведение вакцинации осуществляют при строгом соблюдении правил асептики и антисептики. Препарат во вскрытых шприцах/флаконах хранению не подлежит.
Какие противопоказания существуют у «Ультрикс Квадри»?
Прививку стоит перенести, если ребенок болен в острой стадии, на срок от 2 до 4 недель – о необходимом перерыве лучше проконсультироваться с личным педиатром. При легких респираторных или кишечных инфекциях необходимо дождаться, когда упадет температура, затем, как правило, прививку делать можно. Делать прививку не следует, если у ребенка выявлена сильная реакция при предыдущих вакцинациях от гриппа (все равно, какими вакцинами) или аллергия на какой-либо из компонентов, в том числе куриный белок.
Пациентам переболевшим covid-19, вакцинацию против гриппа можно проводить через 1 месяц после выздоровления.
Источники:
- Инструкция по применению вакцины Ультрикс Квадри
- Вакцина Ростеха от четырех штаммов гриппа «Ультрикс Квадри» одобрена для всех возрастов.//Ростех, 21.09.2021
- Создатель новой российской вакцины от гриппа Антон Катлинский: Мы сделали прививки Сергею Чемезову и Веронике Скворцовой.//Сноб, 15.10.2019
ЗАПИШИТЕСЬ НА ПРИЁМ ЦЕНЫ
МЕРЫ ПРЕДОСТОРОЖНОСТИ
- Не вводить внутривенно.
- Перед прививкой вакцинируемые должны быть осмотрены врачом (фельдшером) с обязательным проведением термометрии. При температуре тела выше 37С вакцинацию не проводят.
- Кабинеты, где проводится вакцинация, должны быть оснащены средствами противошоковой терапии. Вакцинированный должен находиться под наблюдением медработника в течение 30 мин после вакцинации.
Применение при беременности и в период грудного вскармливания
Опыт применения гриппозных инактивированных вакцин показывает, что вакцинация женщин в период грудного вскармливания не оказывает токсического воздействия на ребенка.
Окончательное решение о вакцинации беременных и кормящих грудью женщин должно приниматься врачом индивидуально с учетом риска заражения гриппом и возможных осложнений, вызванных заболеванием гриппом.
Наиболее безопасный период вакцинации беременных женщин — второй и третий триместры беременности.
ВЗАИМОДЕЙСТВИЕ С ДРУГИМИ ЛЕКАРСТВЕННЫМИ ПРЕПАРАТАМИ
Вакцина может применяться одновременно с инактивированными и живыми вакцинами Национального календаря профилактических прививок РФ (за исключением туберкулезных вакцин и инактивированными вакцинами календаря профилактических прививок по эпидемиологическим показаниям (за исключением антирабических). При этом должны учитываться противопоказания к каждой из при меняемых вакцин; препараты следует вводить в разные участки тела разными шприцами.
Вакцина может вводиться на фоне базисной терапии основного заболевания. Вакцинация пациентов, получивших иммуносупрессивнvю терапию (глюкокортикостероиды, цитотоксические препараты, радиотерапия), может быть менее эффективной.