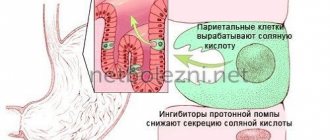
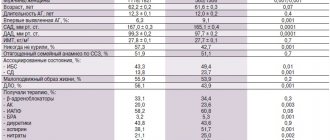
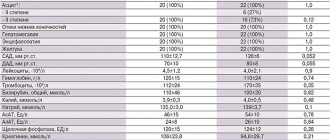
Применение блокаторов ангиотензиновых рецепторов при лечении артериальной гипертензии
В чем преимущество блокаторов ангиотензиновых рецепторов перед другими классами антигипертензивных препаратов, в частности перед ингибиторами АПФ? Какова сравнительная эффективность различных блокаторов ангиотензиновых рецепторов?
На основании репрезентативной выборки (1993) можно утверждать, что распространенность артериальной гипертензии (АГ) в России составляет среди мужчин 39,2%, среди женщин — 41,1%. При этом о наличии заболевания знают только 58,9% женщин и 37,1% мужчин, лечение получают 46,7% и 21,6% (в том числе эффективное — 17,5% и 5,7%) соответственно (первый доклад экспертов Научного общества по изучению артериальной гипертонии, Всероссийского научного общества кардиологов, Межведомственного совета по сердечно-сосудистым заболеваниям, 2000). Тактика ведения больных АГ в настоящее время регламентируется рекомендациями экспертов Всемирной Организации Здравоохранения (ВОЗ) и Международного общества по проблемам артериальной гипертензии (МОГ) (рекомендации ВОЗ-МОГ, 1999) и разработанными на этой основе Национальными рекомендациями по диагностике и лечению артериальной гипертензии (Всероссийское научное общество кардиологов, секция артериальной гипертензии, 2001). Согласно этим рекомендациям, целью лечения АГ является снижение общего риска сердечно-сосудистой заболеваемости и смертности, что предполагает снижение уровня АД до целевого (менее 140/90 мм рт. ст.), а также коррекцию всех выявленных факторов риска (например, адекватное лечение гиперхолестеринемии, сахарного диабета). Поскольку курсовое лечение АГ малоэффективно (в большинстве случаев АГ нельзя вылечить), пациент должен получать индивидуально подобранную гипотензивную терапию постоянно.
Для длительного лечения АГ в настоящее время используют b-адреноблокаторы, диуретики, ингибиторы ангиотензин-превращающего фермента (АПФ), блокаторы ангиотензиновых рецепторов, антагонисты кальция, a-адреноблокаторы. Как известно, в патогенезе артериальной гипертензии важнейшую роль играет ангиотензин II, обусловливающий вазоконстрикцию, стимуляцию синтеза альдостерона и его освобождение, реабсорбцию натрия в почках, рост сердечной мышцы, пролиферацию гладкомышечных клеток кровеносных сосудов, повышение периферической норадренергической активности и ряд других эффектов. Поэтому наиболее перспективными в медикаментозной коррекции АГ в настоящее время считаются ингибиторы ангиотензин-превращающего фермента (АПФ), препятствующие переходу ангиотензина I в ангиотензин II, и блокаторы ангиотензиновых рецепторов. Широко применяемые ингибиторы АПФ, хотя и высокоэффективны, обладают рядом побочных эффектов (включая кашель, ангиoневротический отек), обусловленных их влиянием на метаболизм брадикинина и субстанции Р [4].
Блокаторы ангиотензиновых рецепторов имеют ряд преимуществ перед ингибиторами АПФ — они более специфично и эффективно подавляют сердечно-сосудистые эффекты активации ренин-ангиотензиновой системы. В настоящее время эта наиболее «молодая» группа гипотензивных средств (первое из них — лосартан, синтезированный в 1988 году) представлена рядом препаратов, несколько отличающихся друг от друга по механизму действия, фармакокинетическим свойствам.
По химической структуре различают бифениловые производные тетразоля (лосартан, ирбесартан, кандесартан), небифениловые нететразоловые соединения (эпросартан, телмисартан) и негетероциклические соединения (вальсартан); в зависимости от наличия активного метаболита — пролекарства (лосартан, кандесартан) и активные лекарственные вещества (вальсартан, ирбесартан, телмисартан, эпросартан); в зависмости от типа антагонизма с ангиотензином II — конкурентные антагонисты (лосартан, эпросартан) и неконкурентные (вальсартан, ирбесартан, кандесартан, телмисартан). Основные характеристики различных блокаторов ангиотензиновых рецепторов приведены в табл. 1.
Гипотензивное действие блокаторов ангиотензиновых рецепторов в первую очередь связано с подавлением сосудосуживающего действия ангиотензина II, реализуемого через рецепторы стенок кровеносных сосудов. Кроме того, блокада рецепторов ангиотензина II приводит к снижению секреции альдостерона, уменьшению реабсорбции натрия и воды в проксимальном сегменте почечных канальцев.
Определенную роль в гипотензивном действии может играть стимуляция рецепторов ангиотензина второго типа при повышенном (вследствие блокады рецепторов первого типа) уровне ангиотензина II. Предполагается, что стимуляция рецепторов ангиотензина II второго типа может приводить к вазодилатации и подавлению пролиферативных процессов.
В то же время электрофизиологические исследования на животных показали, что ангиотензин II, активируя пресинаптические ангиотензиновые рецепторы норадренергических нейронов симпатической нервной системы, увеличивает высвобождение норадреналина. При изучении влияния различных антагонистов ангиотензиновых рецепторов (вальсартана, ирбесартана, лосартана, эпросартана) на симпатический выброс, стимулируемый у децерибрированных нормотензивных крыс раздражением спинного мозга, ингибирующий эффект отмечен только у эпросартана [6]. Таким образом, в клинической практике эпросартан (теветен) представляет собой единственный в своей группе препарат, способный в терапевтических дозах блокировать как пресинаптические рецепторы, так и рецепторы ангиотензина в кровеносных сосудах.
Блокаторы ангиотензиновых рецепторов, применяемые в терапевтических дозах, в среднем снижают систолическое артериальное давление на 10-20 мм рт. ст. и диастолическое — на 10-15 мм рт. ст., что показано в большом количестве исследований. Максимальное снижение АД достигается у большинства больных через 3-4 недели лечения.
В качестве примера приведем несколько клинических исследований, посвященных эффективности эпросартана. 8-недельное двойное слепое, плацебо-контролируемое, рандомизированное, клиническое (243 пациента с артериальной гипертензией легкой и средней тяжести) исследование эпросартана (теветена в дозе 600 мг один раз в сутки) показало, что препарат снижал АД значительно эффективнее, чем плацебо [3]: в группе эпросартана систолическое АД снизилось на 6 мм рт. ст., диастолическое — на 7,5 мм рт. ст.; разница по сравнению с результатами в группе плацебо была статистически достоверной. Терапия считалась эффективной, если диастолическое давление в положении сидя снижалось до 90 мм рт. ст. либо снижение диастолического АД от исходного уровня составляло 10 мм рт. ст. и более. В группе эпросартана терапия оказалась эффективной у 42% пациентов, в группе плацебо — у 21%.
Связь между дозой эпросартана и уровнем снижения АД оценена в многоцентровом, двойном слепом, параллельном, плацебо-контролируемом исследовании, в котором приняли участие 364 пациента с исходным уровнем диастолического АД 95-114 мм рт. ст. Оценивалась эффективность терапии эпросартаном в дозе 400, 600, 800, 1200 мг один раз в сутки по сравнению с плацебо, продолжительность лечения составляла 8 недель. Согласно полученным результатам, оптимальная начальная доза препарата составляла 600 мг в сутки [10].
В ходе 13-недельного двойного слепого, плацебо-контролируемого исследования с параллельными группами [4] 243 пациента получали эпросартан в суточной дозе 400-800 мг один-два раза в день. Доза препарата корригировалась в течение первых 9 недель до достижения оптимального гипотензивного эффекта, после чего терапия препаратом в эффективной дозе продолжалась еще 4 недели. Еще раз подтверждено гипотензивное действие эпросартана (диастолическое АД снизилось в группе лечения в среднем на 9 мм рт. ст. против 4 мм рт. ст. в группе плацебо), причем терапевтический эффект был одинаковым при приеме препарата один или два раза в сутки. Терапия эпросартаном (прием один раз в сутки) оказалась эффективной в 46,8% случаев.
В ряде исследований удалось показать, что по эффективности блокаторы ангиотензиновых рецепторов по меньшей мере не уступают ингибиторам АПФ (табл. 2). Например, проводимая в ходе 26-недельного двойного слепого, клинического (528 пациентов в возрасте 21-78 лет с артериальной гипертензией легкой и средней тяжести) исследования [2] терапия эпросартаном в дозе 400-600 мг в сутки оказалась эффективнее, чем лечение эналаприлом в дозе 5-20 мг в сутки. Пациентов, у которых гипотензивная терапия признана эффективной, оказалось больше в группе эпросартана (81,7%) по сравнению с группой эналаприла (73,4%). При анализе полученных результатов выяснилось, что в подгруппе больных старческого возраста частота случаев «ответа на лечение» оказалась такой же, как и у молодых пациентов [1]. Сходные результаты получены и в ходе другого исследования, посвященного сравнительной оценке гипотензивного действия эпросартана и эналаприла при артериальной гипертензии легкой и средней тяжести [7].
Сравнительная эффективность эпросартана (400-800 мг в сутки в два приема) и эналаприла (10-40 мг в сутки в один прием) при тяжелой артериальной гипертензии изучалась в ходе 10-недельного двойного слепого исследования с участием 118 пациентов (78% из них в возрасте старше 65 лет) [8]. Доза титровалась каждые две недели; при необходимости к терапии добавляли гидрохлоротиазид (гипотиазид по 25 мг в сутки). Терапия эпросартаном привела к более значимому снижению цифр систолического и диастолического АД по сравнению с эналаприлом; дополнительное назначение мочегонных средств потребовалось в обеих группах у почти одинакового числа пациентов (39% больных в группе эпросартана, 37% — в группе эналаприла). Таким образом, по сравнению с эналаприлом эпросартан более эффективно снижает повышенное систолическое АД при тяжелой артериальной гипертензии.
В ряде исследований оценивалась эффективность различных блокаторов ангиотензиновых рецепторов. Например, в 8-недельном исследовании [5] приняли участие 567 пациентов с артериальной гипертензией легкой и средней тяжести (табл 3). Терапия ирбесартаном в дозе 300 мг в сутки оказалась несколько более эффективной, чем лечение лосартаном в дозе 100 мг в сутки; доля пациентов, ответивших на лечение, составила соответственно 52% и 42%. В ходе 4-недельного двойного слепого, рандомизированного, клинического исследования с участием 60 пациентов было выявлено, что эпросартан (600 мг один раз в сутки) действует эффективнее, чем лосартан (50 мг один раз в сутки). Пациенты, у которых терапия была признана эффективной, в группе эпросартана составили 73% и в группе лосартана — 53% [9].
Важнейшим требованием к современным гипотензивным средствам является высокая продолжительность воздействия, позволяющая контролировать АД на протяжении 24 ч. Для оценки выраженности и продолжительности гипотензивного действия пролонгированных препаратов Управление США по контролю за лекарствами и продуктами (Food and Drug Administration — FDA) предложило в 1988-1990 гг. использовать коэффициент «конечный:пиковый» (trough:peak, Т/Р), то есть соотношение между наименьшим снижением систолического или диастолического давления в конце междозового интервала и максимальным его снижением на высоте эффекта препарата. Оптимальной представляется гипотензивная терапия, при которой отсутствуют значительные колебания АД в течение суток, то есть этот коэффициент должен стремиться к единице, или к 100%. По рекомендациям FDA, коэффициент «конечный:пиковый» должен быть не менее 50%; это означает, что современные гипотензивные средства должны обеспечивать снижение АД через 24 часа после приема не менее чем на 50% от снижения показателей в период максимального гипотензивного действия. Это позволяет обеспечить эффективный контроль АД между приемами препарата; невысокие колебания АД способствуют уменьшению повреждения сосудистой стенки, а следовательно, уменьшается частота сердечно-сосудистых осложнений артериальной гипертензии.
Значения коэффициента Т/Р для различных блокаторов ангиотензиновых рецепторов представлены в табл. 4.
С помощью амбулаторного мониторирования АД показано, что однократный прием блокаторов ангиотензиновых рецепторов обеспечивает контроль уровня АД на протяжении суток, в том числе в утренние часы, когда особенно велик риск развития сосудистых катастроф (инфарктов миокарда и инсультов); лишь лосартан в некоторых случаях приходится применять два раза в сутки. Наибольшие значения коэффициента Т/Р (т. е. наибольшая продолжительность эффективного гипотензивного действия) выявлены при использовании эпросартана, ирбесартана и кандесартана.
Высокая эффективность блокаторов ангиотензиновых рецепторов сочетается с хорошей переносимостью. Согласно данным, полученным в ходе плацебо-контролируемых клинических исследований, частота побочных эффектов на фоне терапии препаратами этой группы не отличается от этого показателя в группе плацебо. В частности, частота побочных эффектов на фоне терапии лосартаном составляет 15,3% против 15,5% в группе плацебо, на фоне терапии вальсартаном — 15,7% против 14,5%; частота побочных эффектов на фоне терапии эпросартаном приведена в табл. 5. Очень важно, что препараты этой группы в отличие от ингибиторов АПФ не вызывают и не усиливают кашель. Таким образом, блокаторы ангиотензиновых рецепторов достаточно безопасны; противопоказаниями к их применению являются только беременность, гиперкалиемия и двусторонний стеноз почечных артерий.
Согласно Национальным рекомендациям по диагностике и лечению артериальной гипертензии (2001), абсолютным показанием к применению блокаторов ангиотензиновых рецепторов является непереносимость ингибиторов АПФ (кашель при их применении), относительным показанием — застойная сердечная недостаточность. Последняя рекомендация связана с тем, что, как показали Pitt B. и соавт. (1997), лосартан способен увеличивать продолжительность жизни у больных хронической сердечной недостаточностью.
Следует, однако, отметить, что угнетение эпросартаном и симпатоадреналовой, и ангиотензин-альдостероновой систем приводит к существенному снижению систолического АД, поэтому применение этого препарата перспективно при изолированной систолической гипертензии, артериальной гипертензии после инсульта, ожирении, стресс-индуцированной, метаболической, алкогольной гипертензии (Кобалава Ж. Д., Моисеев В. С., 2000).
Литература
- Argenziano L., Trimarco B. Effect of eprosartan and enalapril in the treatment of elderly hypertensive patients: subgroup analysis of a 26-week, double-blind, multicentre study. Eprosartan Multinational Study Group. Curr Med Res Opin, 1999; 15(1):9-14.
- Gavras I., Gavras H. Effects of eprosartan versus enalapril in hypertensive patients on the renin-angiotensin-aldosterone system and safety parameters: results from a 26-week, double-blind, multicentre study. Eprosartan Multinational Study Group. Curr Med Res Opin, 1999; 15(1):15-24.
- Gradman A. H., Gray J., Maggiacomo F., Punzi H., White W. B. Assessment of once-daily eprosartan, an angiotensin II antagonist, in patients with systemic hypertension. Eprosartan Study Group. Clin Ther, 1999; 21(3):442-453.
- Hedner T., Himmelmann A., for the Eprosartan Multinational Study Group. The efficacy and tolerance of once and twice daily doses of eprosartan in essential hypertension. J. Hypertens, 1999; 17:129-136.
- Kassler-Taub K., Littlejohn T., Elliot W. et al., for the Irbesartan Study Investigators. Сomparative efficacy of two angiotensin II receptor antagonists, irbesartan and losartan, in mild to moderate hypertension. Am J Hypertens. 1998; 11:445-53.
- Ohlstein E. H., Brooks D. P., Feuerstein G. Z., Ruffolo R. R. Inhibition of sympathetic outflow by the angiotensin II receptor antagonist, eprosartan, but not by losartan, valsartan or irbesartan: relationship to differences in prejunctional angiotensin II receptor blockade. Pharmacology, 1997; 55(5):244-51.
- Oparil S. Eprosartan versus enalapril in hypertensive patients with angiotensin-converting enzyme inhibitor cough. Curr Ther Res, 1999; 60(1):1-14.
- Ponticelli C., for the Eprosartan Study Group. Comparison of the efficacy of eprosartan and enalapril in patients with severe hypertension. Am J Hypertens, 1997; 10:128A.
- Puig J. G., Mateos F., Buno A., Ortega R., Rodriguez F., Dal-Re. R. Effect of eprosartan and losartan on uric acid metabolism in patients with essential hypertension. J. Hypertens, 1999; 17(7):1033-1039.
- Weber M. Clinical efficacy of eprosartan. Pharmacotherapy. 1999; 19(4, part 2):95–101.
- Zanchetti A., Omboni S., Di Biago C. Candesartan cilexetil and enalapril are of equivalent efficacy in patients with mild to moderate hypertension. J Hum Hypertens, 1997; 11 (suppl 2):57-9.
Блокаторы РААС и COVID-19
Ренин-ангиотензин-альдостероновая система (РААС) — это элегантный каскад вазоактивных пептидов, организующий ключевые физиологические процессы в теле человека. Коронавирусы тяжелого острого респираторного синдрома SARS-CoV-1 и SARS-CoV-2 стали причиной эпидемии тяжелого острого респираторного синдрома в 2002–2004 годах и текущей пандемии коронавирусной инфекции (COVID-19). Эти вирусы взаимодействуют с РААС через ангиотензин-превращающий фермент 2 (ACE2, АПФ2) — белок, физиологической функцией которого является угнетение активации РААС, но который также служит рецептором для обоих типов вирусов SARS. Эта связь между вирусами SARS и АПФ2 рассматривается как потенциальный фактор инфективности, соответственно, высказываются опасения относительно применения ингибиторов РААС, которые изменяют активность АПФ2, и влияния различий в экспрессии АПФ2 на степень вирулентности вируса в текущей пандемии COVID-19. Действительно, недавно некоторые СМИ и системы здравоохранения призвали к отказу от ингибиторов АПФ и антагонистов рецепторов ангиотензина (АРА) как с профилактической целью, так и в контексте подозрения на COVID-19.
Принимая во внимание обширное применение ингибиторов АПФ и АРА во всем мире, существует срочная потребность в рекомендациях по использованию этих лекарств в терапии пациентов с COVID-19. Здесь мы подчеркиваем, что собранные данные на человеческих выборках весьма скудны и не могут быть применены для подтверждения или опровержения высказываемых гипотез и опасений. В особенности мы обсуждаем неопределенные эффекты блокаторов РААС на уровень и активность АПФ2 у людей и выдвигаем альтернативную гипотезу о том, что изменения АПФ2 могут быть полезны, а не вредны для пациентов с поражениями легких. Также мы недвусмысленно хотим выразить озабоченность касаемо отказа от применения ингибиторов РААС, так как считаем, что это может быть опасным для некоторых пациентов из групп высокого риска с выявленным или подозреваемым COVID-19.
Первые доклады обращали внимание на потенциально высокую встречаемость гипертензии среди пациентов с COVID-19 по сравнению с общей популяцией. В самой большой серии случаев из Китая, собранных во время пандемии, гипертензия была самой часто встречаемой сопутствующей патологией у 1099 пациентов, что составляло примерно 15 % от выборки, однако эти значения оказываются ниже, чем встречаемость гипертензии у пациентов с другими вирусными инфекциям, и ниже, чем частота гипертензии в популяции Китая.
По данным докладов, сопутствующие патологии, включая гипертензию, встречались гораздо чаще у пациентов с тяжелым течением COVID-19, требующих перемещения в отделения интенсивной терапии и назначения ИВЛ, или у погибших пациентов в сравнении с пациентами с более мягким течением. Высказываются опасения, что терапия сопутствующих патологий, в том числе применение ингибиторов РААС, могла внести вклад в исход основного заболевания. Однако эти исходы наблюдались также в тесной связи с пожилым возрастом, который в настоящее время считается самым значимым предиктором COVID-19-ассоциированной смерти. К сожалению, на сегодняшний день в докладах недостаточное внимание уделяется возрасту или иным важным факторам, которые могут выступать в качестве потенциальных предикторов риска. Для других инфекционных заболеваний сопутствующие патологии, такие как гипертензия, являются ключевыми прогностическими факторами, что, скорее всего, верно и в отношении COVID-19.
Важно отметить, что, несмотря на заключения о применении ингибиторов РААС, в этих работах отсутствуют конкретные данные. Согласно популяционным исследованиям, доля получающих антигипертензивную терапию от общего числа больных гипертензией в Китае составляет всего от 30 до 40 %. Ингибиторы РААС как базовую терапию или в составе комбинированной терапии получают только 25–30 %пациентов, проходящих лечение. Представленные данные позволяют оценить, что лишь незначительная часть пациентов с COVID-19 получала терапию ингибиторами РААС, по крайней мере в Китае. Необходимо получить информацию о связи терапии ингибиторами РААС и соответствующими исходами основного заболевания со строгим учетом показаний к терапии и тяжести сопутствующего заболевания у пациентов с COVID-19.
Тканеспецифичные и системные компоненты РААС составляют сложную переплетающуюся сеть активирующих и ингибирующих пептидов (рис. 1). АПФ2 — важнейший ингибирующий белок, ответственный за распад ангиотензина II до ангиотензина-(1–7), который таким образом ослабляет его эффекты на вазоконстрикцию, задержку натрия и процессы фиброзирования. Хотя ангиотензин II и является главным субстратом АПФ2, этот фермент также может превращать ангиотензин I в ангиотензин-(1–9) и участвовать в гидролизе иных пептидов. В исследованиях на людях была показана обширная экспрессия АПФ2 в образцах ткани, полученных из 15 органов, в числе которых были сердце и почки, а также в основных клетках-мишенях SARS-CoV-2 (c манифестными признаками поражения) — альвеолярном эпителии легких. Определенный интерес вызывает низкий уровень растворимых форм АПФ2 в системном кровотоке вместе с относительно низкой функциональной ролью АПФ2 в легочной ткани в нормальных условиях. Однако существуют клинические состояния, способствующие активации этого звена.
Рисунок 1 | Взаимодействие между SARS-CoV-2 и ренин-ангиотензин-альдостероновой системой
Показан процесс проникновения коронавируса тяжелого острого респираторного синдрома 2(SARS-CoV-2) в пневмоциты типа II, после связывания с его функциональным рецептором ангиотензин-превращающим ферментом 2 (АПФ2). После эндоцитоза вирусной частицы происходит подавление экспрессии АПФ2 на поверхности клеточной мембраны, приводящее к неконтролируемому накоплению ангиотензина II. Местная активация ренин-ангиотензин-альдостероновой системы может опосредовать повреждение легочной ткани при вирусной инфекции. АПФ — ангиотензин-превращающий фермент, АРА — антагонист рецепторов ангиотензина.
Можно ожидать, что ингибиторы АПФ и АРА оказывают разное влияние на уровень АПФ2, так как их эффекты на ангиотензин II (основной субстрат АПФ2) различаются. Несмотря на существенную структурную гомологию между АПФ и АПФ2, их активные центры различны. В результате этого ингибиторы АПФ не влияют на активность АПФ2 напрямую. Экспериментальные животные модели позволили обнаружить смешанное воздействие ингибиторов АПФ на уровни АПФ2 и его активность в тканях. Подобные противоречивые результаты в исследованиях на животных моделях наблюдались и в отношении влияния АРА на АПФ2. В одних исследованиях была обнаружена усиленная экспрессия матричной РНК АПФ2 или же увеличенные концентрации самого АПФ2, другие же работы не нашли никаких эффектов.
В отличие от работ на животных моделях, существует мало исследований эффектов ингибиторов РААС на экспрессию АПФ2 на людях. В одной работе описано, что внутривенное введение ингибиторов АПФ пациентам с коронарной недостаточностью никак не повлияло на продукцию ангиотензина-(1–7), что ставит под вопрос влияние ингибиторов АПФ на АПФ2-опосредованный метаболизм ангиотензина II вообще. Аналогично, в другом исследовании среди пациентов с гипертензией уровни ангиотензина-(1–7) остались неизменными после назначения ингибитора АПФ каптоприла. Однако если монотерапия каптоприлом продолжалась 6 месяцев, уровень ангиотензина-(1–7) увеличился. Кроме того, в нескольких исследованиях изучалась активность АПФ2 в плазме или концентрация АПФ2 в моче у пациентов на длительной терапии ингибиторами РААС. В кросс-секционных исследованиях пациентов с сердечной недостаточностью, фибрилляцией предсердий, аортальным стенозом и коронарной недостаточностью, принимающих ингибиторы АПФ или АРА, активность АПФ2 в плазме не отличалась от пациентов с такими же заболеваниями, не получавших терапии. В лонгитюдном когортном исследовании японских пациентов с гипертензией уровень АПФ2 в моче пациентов, получавших длительное лечение АРА олмесартаном, был выше, чем в контрольной группе, не получавшей терапии, но такого эффекта не наблюдалось в отношении ингибитора АПФ эналаприла или других АРА (лозартан, кандесартан, валсартан, и телмисартан). Предшествующая терапия ингибиторами АПФ связывалась с ростом уровня матричной РНК АПФ2 в тканях кишки, но никакой связи между терапией АРА и количеством РНК АПФ2 выявлено не было; влияние ингибиторов РААС на экспрессию АПФ2 в легочной ткани неизвестно.
Эти противоречивые данные указывают на всю сложность устройства ответов РААС на модуляторы и подтверждают предположение о том, что выводы доклинических исследований на модельных организмах нельзя однозначно переносить на человеческую физиологию. Это наводит на мысль, что воздействие ингибиторов РААС на АПФ2 может принимать различные формы в зависимости от конкретного препарата данного класса. Важно отметить, что уровни АПФ2 в плазме могут быть не показательны в отношении полноразмерной мембраносвязанной формы, частично из-за того, что процесс отделения АПФ2 от мембраны отдельно регулируется эндогенным ингибитором. Помимо степени экспрессии, значимость роли АПФ2 может различаться в зависимости от конкретной ткани или клинического состояния. К сожалению, отсутствуют данные о влиянии ингибиторов АПФ, АРА и других ингибиторов РААС на экспрессию АПФ2 в легочной ткани. Более того, даже если ингибиторы РААС и влияют на уровень и/или активность АПФ2 в тканях-мишенях, нет клинических данных о том, что это влияет на процесс связывания и проникновения пепломеров SARS-CoV-2 в клетку. Необходимо дальнейшее изучение взаимного влияния SARS-CoV-2 и РААС на людях.
SARS-CoV-2 не только использует АПФ2 для проникновения в клетку, он также угнетает его дальнейшую экспрессию, что приводит к прекращению его органопротективного действия. В настоящее время предполагается, хоть и без каких-либо доказательств, что непрерывное действие ангиотензина II может частично влиять на степень повреждения органа при COVID-19. Сразу после рецепции и прикрепления пепломера вируса начинается процесс последовательного снижения концентрации АПФ2 на поверхности мембраны. Продолжительно персистирующая вирусная инфекция и репликация вирионов также вносят вклад в снижение экспрессии АПФ2, во всяком случае на клеточных культурах in vitro. Угнетение активности АПФ2 в легких обусловливает первичную инфильтрацию нейтрофилов в ответ на бактериальные эндотоксины и может вести к чрезмерному накоплению освободившегося от ингибирования ангиотензина II и местной активации РААС. Действительно, в экспериментальных моделях на мышах воздействие пепломеров SARS-CoV-1 вызывало острое поражение легких, которое ограничивалось блокадой РААС. В экспериментах с другими мышиными моделями авторы пришли к выводу, что дисрегуляция АПФ2 может способствовать вторичному острому поражению легких при первичном поражении вирулентными штаммами вируса гриппа и респираторно-синцитиального вируса человека. В небольшом исследовании проследили корреляцию между повышенным уровнем плазменного ангиотензина II с общей вирусной нагрузкой и степенью тяжести поражения легких у пациентов с COVID-19. Восстановление уровня АПФ2 посредством введения рекомбинантного препарата АПФ2 позволило обратить разрушительные процессы в легочной ткани на доклинических моделях иных острых вирусных инфекций, а в испытаниях второй фазы у людей с острым респираторным дистресс синдромом безопасно снизить уровень ангиотензина II.
Дисрегуляция АПФ2 при COVID-19 в теории может привести к снижению его кардиопротективного эффекта при вовлечении миокарда и аномальной легочной гемодинамики. Уровни маркеров повреждения миокарда повышались во время развития COVID-19 и продолжали нарастать при ухудшении течения заболевания и перед смертью. Многие вирусы кардиотропны, и многие вирусемии сопровождаются субклиническим вирусным миокардитом. Роль АПФ2 в ответе миокарда на повреждения и его восстановлении хорошо известна. Так, в одном исследовании на животных с нокаутированным геном АПФ2 у них развивались крайне неблагоприятные процессы ремоделирования левого желудочка в ответ на острое повреждение в связи с накоплением ангиотензина II. При аутопсии пациентов, погибших от SARS, в 35 % образов сердец было обнаружено присутствие вирусной РНК, которое, в свою очередь, было ассоциировано со сниженной экспрессией АПФ2. Введение рекомбинантного АПФ2 нормализовало уровень ангиотензина II в изолированных сердцах человека, пораженных дилатационной кардиомиопатией. Данные гипотезы легли в основу испытаний рекомбинантного препарата АПФ2 для восстановления баланса РААС и потенциального предотвращения органного повреждения. В дополнении к этому, на текущий момент проводятся парные исследования лозартана для лечения COVID-19 на пациентах, не получавших ранее терапию блокаторами РААС, которые были госпитализированы, и на пациентах, не имевших госпитализаций в анамнезе.
Несмотря на приведенные теоретические противоречия относительно влияния фармакологический регуляции АПФ2 на инфективность SARS-CoV-2, существует явный риск здоровью при отмене терапии блокаторами РААС у пациентов, которые в остальном находятся в стабильном состоянии. COVID-19 протекает особенно тяжело у пациентов с сопутствующими кардиоваскулярными патологиями, что ведет к активному поражению миокарда, миокардиальному стрессу, и кардиомиопатии. Блокаторы РААС показали клиническую эффективность в отношении протективного действия на сердце и почки, их отмена может привести к клинической декомпенсации у пациентов в группах высокого риска.
Несмотря на то, что данные по сердечной недостаточности нечасто встречаются в эпидемиологических докладах из Китая, встречаемость сердечной недостаточности среди пациентов в критическом состоянии в США может быть велика (> 40 %). В клинических испытаниях квинаприла для лечения сердечной недостаточности было продемонстрировано серьезное прогрессирующее ухудшение состояния пациентов с хронической симптоматической сердечной недостаточностью. В исследовании TRED-HF среди пациентов с асимптоматической сердечной недостаточностью и восстановленной фракции выброса левого желудочка был продемонстрирован стремительный рецидив дилатационной кардиомиопатии сразу после прекращения терапии (в том числе терапии блокаторами РААС). Более того, блокаторы РААС являются базисной терапией после инфаркта миокарда: продолжительная терапия на протяжении нескольких дней или недель после указанного события показала снижение ранней смертности. Инфаркт миокарда, ассоциированный с COVID-19, может быть более опасным среди клинически нестабильных пациентов в случае отмены блокаторов РААС.
Отмена блокаторов РААС, назначенных для контроля гипертензии, может нести меньшие риски, нежели их отмена при состояниях, для которых они показаны множеством клинических рекомендаций как базисный метод терапии, однако в этом случае она может быть сопряжена с иными трудностями. Отмена блокаторов РААС для перехода на другую антигипертензивную терапию у стабильных амбулаторных пациентов должна проводиться осторожно во избежание эффекта рикошета. Более того, подбор эквивалентной дозы иной антигипертензивной терапии может быть проблематичным на практике и зависеть от индивидуальных особенностей каждого пациента. Даже малые и непродолжительные скачки АД после смены терапевтической тактики связаны с избыточным кардиоваскулярным риском. Это может быть особенно важно у пациентов с COVID-19 — инфекцией, влекущей за собой активацию РААС, в странах, где не достигнут адекватный контроль артериального давления в популяции (например, в Китае).
Эффекты при отмене блокаторов РААС или при переходе на другие схемы терапии у пациентов с хронической болезнью почек (ХБП) остаются неопределенными. Хотя в Китае частота встречаемости ХБП, госпитализированных по поводу COVID-19, достаточно низка (1–3 %), в других странах и у пациентов в критическом состоянии встречаемость ХБП может быть выше. Многие пациенты испытывают острую почечную недостаточность разной степени в течении болезни. Для этих групп высокого риска рекомендуется принимать индивидуальные решения по терапевтической тактике в отношении блокаторов РААС, руководствуясь гемодинамическим статусом, функцией почек и клинической стабильностью.
На основе доступных данных мы считаем, что несмотря на теоретические опасения и неопределенность в отношении эффектов блокаторов РААС на АПФ2 и потенциального влияния этих препаратов на течение COVID-19, терапия блокаторами РААС должна быть продолжена у пациентов в стабильном состоянии, имеющих риск заражения или уже болеющих COVID-19 (см. сноску). Данную позицию сейчас поддерживает множество профессиональных ассоциаций (Таблица S2). Несмотря на то, что дополнительные данные могут влиять на принятие решений о терапии пациентов с COVID-19 из групп высокого риска, врачи должны осознавать нежелательные последствия преждевременного прекращения доказанной терапии из-за гипотетических опасений, основанных на неполных экспериментальных данных.
- АПФ2 — фермент, физиологически угнетающий активацию РААС, является функциональным рецептором SARS-CoV-2 — вируса, ответственного за пандемию COVID-19
- Отдельные доклинические исследования показали, что блокаторы РААС могут увеличивать экспрессию АПФ2. Это вызвало озабоченность по поводу безопасности их применения у пациентов с COVID-19
- Существует недостаточно данных, чтобы определить, могут ли эти наблюдения быть перенесены на человеческую физиологию, также отсутствуют работы, в которых бы рассматривались эффекты блокаторов РААС на COVID-19
- Проводятся клинические испытания безопасности и эффективности модуляторов РААС, в числе которых рекомбинантный человеческий АПФ2 и АРА лозартан, в терапии COVID-19
- Резкая отмена блокаторов РААС у пациентов с высоким риском, в том числе у пациентов с сердечной недостаточностью или с историей инфаркта миокарда, может привести к клинической нестабильности и неблагоприятным последствиям для здоровья
- До получения дальнейших данных мы считаем, что блокаторы РААС надлежит продолжать применять в терапии пациентов в стабильном состоянии, которые могут заразиться или уже болеют COVID-19
АНТИГИПЕРТЕНЗИВНЫЕ ЛС И ФАРМГРУППЫ ДЛЯ ВЗАИМОДЕЙСТВИЯ
Преферанский Николай Георгиевич
Руководитель отдела медицинских и фармацевтических информационных систем НП МИАЦ РАМН, проф., д.фарм.н.
Часть IV САРТАНЫ
II.
Блокаторы ангиотензиновых рецепторовI типа(БАТ1)
В зависимости от механизма связывания с ангиотензиновыми рецепторами I типа их различают на средства обратимого конкурентного (Валсартан, Лозартан, Эпросартан) и необратимого неконкурентного (Ирбесартан, Кандесартан) типа действия. Препараты обратимого типа действия имеют период полувыведения: Валсартан Т½ = 6 ч, Лозартан Т½ = 2 ч, Эпросартан Т½ = 5–9 ч и оказывают непродолжительный эффект. Эти препараты связываются прочной ковалентной связью Ирбесартан Т½ = 11–15 ч, Кандесартан Т½ = 9–13 ч, Телмисартан Т½ = 24 ч. Их принимают 1 раз в сутки, т.к. они оказывают длительный эффект.
Классифицируют селективные непептидные блокаторы ангиотензиновых рецепторов I типа по их химической структуре на 3 группы:
1. Бифениловые производные тетразола
(производные бифенилтетразола) —
Лозартан
(Блоктран, Брозаар, Вазотензин, Зисакор, Козаар, Лозап, Лориста, Презартан, Реникард);
Валсартан
(Валз, Валсафорс, Валсакор, Диован);
Ирбесартан
(Апровель);
Кандесартан
(Атаканд).
2. Бифениловые нететразольные соединения
(производные бифенилкарбоновой кислоты) —
Телмисартан
(Микардис, Прайтор); (производные имидазолкарбоновой кислоты)
Олмесартанмедоксомил
(Кардосал 10, Кардосал 20, Кардосал 40).
3. Небифениловые нететразольные соединения
(производное тенилимидазолакриловой кислоты) —
Эпросартан
(Навитен, Теветен).
Табл. Блокаторы ангиотензиновых рецепторов АТ1 с другими группами
| Взаимодействующая группа | Результат взаимодействия | Механизм взаимодействия |
| Альфа–адреноблокаторы | Усиление гипотензивного эффекта | Потенцирование антигипертензивного эффекта |
| Антиаритмический препарат — Пропафенон | Угроза жизни больным при желудочковых тахиаритмиях или тромбоэмболии легочной артерии | |
| Антикоагулянты непрямого действия | Риск развития кровотечений | Угроза жизни больным |
| бета–адреноблокаторы | Усиление гипотензивного эффекта | Синергизм, усиление эффективности |
| Диуретические средства растительного происхождения | Увеличение риска резкого снижения АД | Потенцирование |
| Калийсберегающие диуретики | Увеличение риска развития гиперкалиемии | Уменьшение почечной экскреции калия |
| Комбинированные диуретические средства | Увеличение риска резкого снижения АД | Потенцирование |
| МиМЭ — препараты калия | Увеличение риска развития гиперкалиемии | Синергизм в отношении уровня кальция в крови |
| Нормотимические ЛС (антиманиакальные) | Увеличение концентрации лития и его токсичности | Уменьшение почечной экскреции лития за счет ингибирования его секреции |
| Осмотические диуретики | Увеличение риска резкого снижения АД | Потенцирование |
| Петлевые диуретики | Увеличение риска резкого снижения АД | Потенцирование |
| Разные диуретические средства | Увеличение риска резкого снижения АД | Потенцирование |
| Салуретики, ингибиторы карбоангидразы | Увеличение риска резкого снижения АД | Потенцирование |
| Снотворные средства | Усиление гипотензивного эффекта | Синергизм антигипертензивного действия за счет центрального седативного действия на уровне вазомоторных центров |
| Средства для ингаляционного наркоза | Возможно значительное снижение АД. По возможности, отмена ИАПФ при предстоящем наркозе | Синергизм антигипертензивного действия за счет блокады симпатических ганглиев и расширения кровеносных сосудов кожи и мышц, повышения тонуса блуждающего нерва |
| Фторхинолоны | Резкое снижение АД | Усиление эффективности |
IIа. Взаимодействие наиболее изученных препаратов из группы БАТ1 с другими группами или действующими веществами
| ЛС, снижающие активность РААС | Взаимодействующие группы или действующие вещества | Результат взаимодействия |
| Валсартан | Алкоголь | Усиление гипотензивного эффекта |
| Варфарин | Удлинение протромбинового времени на 12% | |
| Диуретики | Усиление гипотензивного эффекта | |
| НПВС | Снижение гипотензивного эффекта | |
| Ирбесартан | Диуретики | Усиление гипотензивного эффекта |
| Препараты лития | Повышение концентрации лития в крови | |
| Лозартан | Алкоголь | Усиление гипотензивного эффекта |
| Гидрохлортиазид | Синергизм, усиление гипотензивного действия. Рациональная комбинация | |
| Индометацин | Ослабление гипотензивного эффекта | |
| Калийсберегающие диуретики, калийсодержащие препараты | Гиперкалиемия, наблюдение за концентрацией калия в сыворотке крови | |
| Симпатомиметики | Ослабление гипотензивного эффекта | |
| Эстрагены | Ослабление гипотензивного эффекта |
IIб.
Взаимодействие блокаторов ангиотензиновых рецепторов АТ1 с действующими веществами
| Действующее вещество | Результат взаимодействия | Механизм взаимодействия |
| Амиодарон | Резкое снижение артериального давления | Не следует назначать больным в связи с угнетением изоферментов цитохрома Р–450 |
| Кетоконазол | Резкое снижение артериального давления | Угнетением изоферментов цитохрома Р–450 |
| Омепразол | Резкое снижение артериального давления | Угнетением изоферментов цитохрома Р–450 |
| Флуконазол | Резкое снижение артериального давления | Угнетением изоферментов цитохрома Р–450 |
| Циметидин | Резкое снижение артериального давления | Угнетением изоферментов цитохрома Р–450 |
| Циклоспорин А | При одновременном применении циклоспорина с антагонистами рецепторов ангиотензина II возможно развитие выраженной гиперкалиемии |
«Таблетка от давления»: как это работает
Наверное, нет ни одной другой группы лекарств, в которой было бы так много препаратов. К тому же большинство средств имеет добрый десяток аналогов, что сеет среди антигипертензивных хаос, здравому уму малоподвластный. Но ум хорошего кардиолога и профессионального фармацевта может постигнуть и не такой лекарственный ералаш.
«Много» — не значит «хорошо»
Разнообразие антигипертензивных препаратов во многом связано с тем, что сегодня наряду с современными продолжают использоваться средства, которыми лечились наши бабушки. К счастью, применяются они достаточно редко, но, тем не менее, смуту в лечение гипертонии вносят. К тому же следует учитывать, что в российских аптеках до сих пор можно запросто купить любой антигипертензивный препарат без рецепта врача. А это значит, что самолечение гипертонической болезни, которое нельзя назвать иначе, чем «самомучение», продолжает процветать и приносить горькие плоды.
Но неужели есть большая разница, как и чем снижать давление: главное же, чтобы тонометр показывал норму или приближенные к ней цифры? Конечно, есть, и вот почему.
Дело в том, что многие антигипертензивные препараты приводят к резкому снижению давления. Это не лучшим образом сказывается на самочувствии больного, однако есть последствия гораздо более серьезные. Если постоянно принимать эти лекарства, эластичность сосудистой стенки, регулярно напрягающейся и расслабляющейся, снижается. В результате развиваются (или быстро прогрессируют) заболевания сердца и сосудов — наиболее опасные осложнения гипертонии.
К препаратам, обладающим резким сосудорасширяющим эффектом, относятся любимые многими поколениями гипертоников адельфан и клонидин. Менее мощное действие на сосуды оказывают дешевые бендазол и его комбинация с папаверином, метамизолом и фенобарбиталом (андипал). Эти средства уменьшают сердечный выброс и при длительном применении ухудшают показатели ЭКГ.
А растительные гипотензивные препараты, например раунатин, и вовсе рассматривать всерьез не приходится: лекарствам, возраст которых уже перевалил за шестой десяток, уже давно найдена более эффективная и безопасная альтернатива.
Шесть групп
Я перечислила далеко не все гипотензивные препараты, которые продолжают выпускаться и применяться, несмотря на серьезные недостатки и побочные эффекты. Их так много, что я боюсь запутать читателя окончательно. Гораздо проще назвать те средства, которые во всем мире признаны препаратами выбора для лечения гипертонии. Они относятся к шести фармакологическим группам:
- Мочегонные, или диуретики (гидрохлортиазид, индапамид).
- Бета-блокаторы (атенолол, бетаксолол, метопролол, бисопролол, небиволол и др.).
- Блокаторы кальциевых каналов (верапамил, амлодипин, нифедипин, фелодипин и др.).
- Ингибиторы АПФ (каптоприл, эналаприл, лизиноприл, рамиприл, фозиноприл и др.).
- Блокаторы рецепторов ангиотензина II (лозартан, валсартан, кандесартан, ирбесартан, телмисартан и др.).
- Альфа-адреноблокаторы (доксазозин, урапидил и др.).
Механизм действия каждой из этих групп различен и достаточно сложен:
- Мочегонные
препараты (диуретики) увеличивают выведение из организма солей и воды. В результате содержание натрия в стенке сосудов снижается, что препятствует сужению сосудов и повышению артериального давления. - Бета-блокаторы
работают за счет блокирования так называемых β1-адренорецепторов, расположенных в сердце. Это приводит к снижению частоты и силы сердечных сокращений и снижению давления. - Действие блокаторов кальциевых каналов
основано на способности блокировать прохождение ионов кальция внутрь клетки, что позволяет снизить тонус сосудов, расширить их просвет и улучшить кровообращение в них. - Ингибиторы АПФ
блокируют ангиотензинпревращающий фермент, который превращает ангионтензин I в ангиотензин II, оказывающий мощное сосудосуживающее действие. - Блокаторы рецепторов ангиотензина II
действуют на тот же механизм, что и ингибиторы АПФ, но на более поздний его этап. - Альфа-адреноблокаторы
снижают давление, уменьшая спазм сосудов.
Кстати, разницы в эффективности между ними практически нет. Из ряда препаратов выбиваются нифедипин и каптоприл, которые можно принимать как средства скорой помощи для быстрого снижения давления. Кроме того, диуретики, блокаторы кальциевых каналов и ингибиторы АПФ определенно снижают риск развития сердечно-сосудистых катастроф, вероятность которых значительно возрастает при гипертонии.
Антагонисты рецепторов ангиотензина
Большинство врачей для лечения гипертонии порекомендуют сначала попробовать ингибитор АПФ, если он не подойдет, тогда они могут порекомендовать блокаторы (антагонисты) рецепторов ангиотензина (АРА или БРА).
Эта группа препаратов переносится лучше, они не вызывают кашля – что является важнейшим условием повышения приверженности человека к терапии.
Последние открытия позволили расширить применение антагонистов рецепторов ангиотензина, в настоящее время их не только рекомендуют в качестве начальной или дополнительной антигипертензивной терапии, они также показывают преимущества в лечении сердечной недостаточности (СН), диабетической болезни почек, особенно среди пациентов с непереносимостью ингибиторов АПФ и диабетом.
Появились новые показания, как хроническая сердечная недостаточность после перенесенного инфаркта миокарда, фибрилляции предсердий и метаболическом синдроме. Они могут использоваться как в монотерапии, так и в сочетании с другими антигипертензивными препаратами.
На сегодняшний день известно 9 группы. Все они имеют названия, которые заканчиваются на «сартан». Отличаются между собой по способности снижать давление, длительности действия и наличию дополнительных показаний.
На этом преимущества БРА не заканчиваются, среди них легко и просто титровать дозу, не надо так тщательно подбирать из группы, как например, у антагонистов кальция или бета—блокаторов.
Имейте в виду, что сартаны не окажут мгновенного устойчивого гипотензивного действия. Работают они мягко, эффект нарастает постепенно, проявляется на 2–4 неделе и усиливается к 6–8‑й неделе терапии.
Как работают антагонисты рецепторов ангиотензина
Ренин-ангиотензин-альдостероновая система (РААС) представляет собой скоординированный гормональный каскад, который контролирует сердечно-сосудистую, почечную и надпочечниковую функции, регулируя баланс жидкости в организме и электролитов, а также артериальное давление. Он является основным действующим элементом в РААС.
Управлять ренин-ангиотензин-альдостероновой системой могут 4 группы: ингибиторы ангиотензинпревращающего фермента (ИАПФ), блокаторы рецепторов ангиотензина II (БРА), антагонисты альдостерона и прямые ингибиторы ренина. Каждая группа лишь частично подавляет работу РААС. Все они действуют приблизительно одинаково, подавляют выброс гормона, но делают это различными путями.
ИАПФ блокируют фермент, который способствует его образованию, БРА блокируют рецепторы АТ1, через которые реализуется его действие.
Что делает в организме:
- приводит к генерализованному сужению сосудов;
- что повышает периферическое сопротивление;
- увеличивают нагрузку на сердце;
- увеличивает альдостерон, натрий в крови, в результате разрастаются клетки в артериях и сердце (гипертрофия);
- способствует выбросу катехоламинов из надпочечников, вызывая гиперактивность симпатической нервной системы.
Его инактивация, при помощи БРА, способствует регрессу (устранению и повороту вспять) патологических процессов. Люди с высоким ренин-натриевым профилем имеют больший риск инфаркта миокарда, чем люди с нормальным или низким профилем.
Нежелательные явления от этой группы включают головную боль, головокружение, гиперкалиемия, респираторные инфекции, ангионевротический отек и усталость. БРА не следует сочетать с ингибиторами АПФ, поскольку такие комбинации повышают риск гипотонии, гиперкалиемии и почечной недостаточности.
Лозартан
Лекарство проходит преобразование в печени, поэтому активность Лозартана зависит от ее состояния. Начальная доза 50 мг, максимальная— 150 мг, прием 1-2 раза в день.
Эффект Лозартана зависит от объема. Максимальное снижение АД стоит ожидать на 4-6 неделе. Лекарство имеет самые широкие показания: гипертензия, СН, профилактика инсульта при гипетрофии сердца и защита почек при диабете (СД).
Плюсы:
- Лечит гипертоническую болезнь, но слабее действует на АД, чем другие представители
- Защищает почки от повреждений диабетом
- Уменьшает риск инсульта при гипертензии лучше, чем атенолол
- Устраняет гипертрофию сердца
- Влияет уровень мочевой кислоты, чего нет у других БРА, рекомендован при подагре и гипертонии
- Расширяет сосуды
- Выделяется примерно 40% с мочой и 60% с калом
- Хорошо сочетается с диуретиками
- Оказывает антиагрегантное действие путем блокады рецепторов тромбоксана А2
- Недорогой
Минусы:
- Нельзя сочетать с рифампицином, флуконазолом
- Повышает калий в крови
- Имеет короткий период действия, поэтому надо пить несколько раз в день
- Чтобы повысить эффективность, нужно все время повышать количество
- Может вызвать головокружение.
Аналоги:
- Лозаран (Вертекс, Россия) 1000 мг №90 – 400 р.
- Блоктран (Фарм стандарт, Россия) 50 мг№30 — 320 р.
- Козаар (Мерк) 100 мг№28 — 160 р.
- Лозап (Санофи) 100 мг№90 – 531 р.
- Лозартан (Тева) 50 мг №30- 150 р.
- Лориста (КРКА) 100 мг №90- 404 р.
Лозартан в исследованиях продемонстрировал высокую эффективность в снижении риска смерти от инфаркта или инсульта приблизительно на 13% по сравнению с атенололом, особенно у больных с диабетом.
Кандесартан цилексетил
Кандесартан является пролекарством, поэтому требуется активация в печени.
Начальный прием– 4-8 мг, средняя 24 мг, максимальная – 32 мг, прием 1-2 раза в день. Отличный препарат, практически лишен недостатков, заслуживает внимания гипертоников, подходит для длительного пожизненного приема.
Плюсы:
- Расширяет сосуды
- Защищает почечную ткань от повреждений высоким АД и диабетом
- Показан для терапии СН
- Значительно уменьшает риск инсульта, лучше, чем другие БРА
- Отлично переносится
- Не взаимодействует с другими лекарствами, поэтому не мешает их работе.
Минусы:
- Может вызывать головокружение
Аналоги:
- Атаканд (Астра Зенека) Англия- 977 р.
- Гипосард Польфа 16 мг №28- 301 р.
- Кантаб Нобель Турция 8 мг №28- 250 р.
- Кандесар Сунн Индия 8 мг №10- 42 р.
- Касарк (кандесартан + гидрохлортиазид) Эвертоджен Индия – 250 р.
Олмесартан медоксомил
Также является пролекарством, нуждается в преобразовании печенью. Начальное количество 20 мг, максимальная 40 мг, прием 1 раз.
Стоит на втором месте в Европе по популярности, продается под названием «Беникар». Проявляет наибольшую эффективность среди сартанов по контролю повышенного давления.
Плюсы:
- Лечит гипертонию, для лучшего эффекта нужна доза 40 мг
- Начинает работать быстро через 1-2 часа
- Хорошо сочетать с диуретиками
- Рекомендуется детям с 6 лет
- Выводится с калом (60 %) и мочой (40%)
- Длительность действия до 24 часов
- Максимальный антигипертензивный эффект наступает на 8 неделе, результат с АД начинает на 2 неделе
- Пища не влияет на всасывание
- Хорошо переносится, количество побочных эффектов было сравнимо с плацебо.
Минусы:
- Жесткий
- Имеет ряд ограничений со стороны сердца
- Рекомендуется только для лечения гипертонии
- Нельзя при застойной СН
Аналоги:
Кардосал Берлин Хеми (Германия) 10 мг №28 — 468 р.
Азилсартан медоксомил
После активации в печени превращается в активную форму азилсартан. Начальная доза 40-80 мг, максимальная 80 мг. Прием 1 раз.
Плюсы:
- Прочно связывается с рецепторами, чем другие БРА
- Оказывает мощный и продолжительный антигипертензивный эффект
- Повышает чувствительность тканей к инсулину и влияет на массу жировой ткани, перспективен для больных АГ, имеющих метаболические нарушения
- Хорошо сочетается с диуретиками
- Достаточно 2 недель для устойчивой стабилизации АД
- Уменьшает уровень тревоги
- Понижает уровень сахара
- Обладает нефропротективными свойствами.
Минусы:
- Может вызвать головокружение, понос
- Рекомендуется с 18 лет
- Нельзя при тяжелом нарушении функции печени
- Нет аналогов, дорогой.
Аналоги:
- Эдарби Такеда (Япония) 20мг №28 — 377 р., 80 мг №28—830 р.
- Эдарби Кло Такеда (Япония) — Азилсартан 40 мг+ хлорталидон 25 мг №98 шт – 1840 р.
По данным клинических исследований азилсартан в минимальной дозе (40 мг) снижает давление лучше, чем прием максимальных валсартана, олмесартана.
Эпросартан
Не являются пролекарством, поэтому может применяться при патологии печени. Начальный прием — 600 мг, максимальная – 800 мг, прием 1—2 раза в день.
Возглавляет рейтинг популярности в Европе, рекомендован только для терапии гипертонии. Отлично защищает от первичного и повторного инсульта.
Плюсы:
- Лечит гипертоническую болезнь
- Расширяет сосуды
- Оказывает легкое мочегонное действие
- Работает 24 часа
- Максимальный эффект через 2 недели
- Не влияет на частоту пульса
- В основном выводится кишечником (90%)
Минусы:
- Иногда вызывает головную боль и расстройство пищеварения
- Нет аналогов, в продаже только бренд, дорогой
Аналоги:
Теветен (Аббот, Нидерланды) 600 мг №14– 1299 р.
Пациенты, которые принимали телмисартан, эпросартан, ирбесартан реже отказывались от продолжения лечения, чем больные, находившиеся на лозартане.
Ирбесартан
Не является пролекарством, работает сразу, без помощи печени. Ирбесартан обладает одной из самых высоких биодоступностей. Начальная доза 150 мг, максимальная – 300, прием 1 раз. Отличается от аналогов мощным нефропротективным действием.
Плюсы:
- Идеален при гипертонии и поражении почек при сахарном диабете
- Проявляет антиагрегантное действие
- Действует 24 часа
- Превышает эффективность валсартана
- В снижении диастолического АД уступал олмесартану
- Уменьшает частоту случаев застойной СН
- Хорошо сочетается с диуретиками
- Рекомендуется при гипертензии и ожирении
- Защищает почки от повреждения
- Хорошо переносится
Минусы:
- Возможны головокружение
- Повышает уровень калия в крови.
Аналоги:
- Апровель (Санофи Авентис, Франция) 150 мг№14 – 200 р., 300 мг №28- 706 р.
- Ирбесартан Атолл, Россия 300 мг№28 — 559 р.
- Ирбесартан (Канон, Россия) 150мг №28- 391р.
Телмисартан
Телмисартан — самый длительно действующий блокатор рецепторов ангиотензина II, на сегодняшний день — это рекорд для БРА. Обеспечивает гипотензивный эффект до 48 часов.
Сартан второго поколения, является одним из активных метаболитов лозартана, превосходит его по всем параметрам.
Начальная доза 40 мг, максимальная – 80 мг. Прием 1 раз. Телмисартан — препарат выбора у пациентов с ожирением и гипертонией, особенно резистентной к терапии.
Плюсы:
- Не является пролекарством, действует сразу
- Длительность 48 часов
- Имеет быстрое начало действия через 30 минут
- Повышает чувствительность тканей к инсулину и усиливает утилизацию глюкозы в мышцах, тканях
- В терапевтических дозировках действует как сахароснижающий
- Благотворно влияет на углеводный и жировой обмен
- Подходит для пациентов пожилого возраста
- Обладает антиагрегационной активностью тромбоцитов.
- Снижает риск инфаркта и инсульта у диабетиков.
Минусы:
- Совместное введение телмисартана с дигоксином повышает уровень дигоксина в плазме, что может привести к токсичности.
Аналоги:
- Микардис (Берингер Ингельхайм) Германия 40 мг №14 – 335 р.
- Телзап Санофи, Франция 40 мг№90- 703 р.
- Телмиста (КРКА, Словения) 40 мг №84 – 724 р.
- Елмисартан СЗ (Северная звезда, Россия) 40 мг №30— 216 р.
- Телсартан (Доктор Реддис, Индия) 40мг №30 — 230 р.
- Танидол (Гедеон Рихтер, Венгрия) 40 мг №30 – 196 р..
Валсартан
Вальсартан как и лозартан были первыми на рынке. Он не является пролекарством.
Начальная доза — 20- 40 мг или 160 мг, средняя – 254 мг, максимальная 160 мг. Один раз в день.
В Европе на третьем месте по популярности.
Плюсы:
- Лечит гипертоническую болезнь
- Начинает работать через 2 часа
- Показан при хронической СН и после инфаркта
- Падает смертность от сердечно-сосудистых заболеваний при сердечной слабости или после инфаркта миокарда
- Уменьшает риск тромбобразования
- Оказывает сосудорасширяющее действие
- Имеет много аналогов на рынке
- Не влияет на уровень гликемии, не изменяет липидный профиль и уровень триглицеридов.
Минусы:
- Не рекомендуется при тяжелых повреждениях печени и почек
Аналоги:
- Валз (Балканфарма Болгария) 40 мг №30 — 124 р.
- Вальсакор (КРКА, Словения) 80 мг №90 — 682 р.
- Диован (Новартис, Швейцария) 80мг №28 – 1570 р..
- Валсартан (Атолл, Россия) 80 мг №30- 183 р.
- Эксфорж Новартис, Швейцария – это (валсартан / амлодипин) комбинированный —1228 р..
В ряде исследований показано, что валсартан при гипертензии сопоставим с амлодипином в долгосрочной перспективе.
Новости: недавно протестирован новый эффективный комбинированный препарат для лечения недостаточности сердца. В его составе сартан (вальсартан) и новый класс лекарственных средств — ингибиторы неприлизина (сакубитрил).
Называется он «Юперио» (сакубитрил+валсартан). Юперио показал хорошие результаты при хронической СН с гипертензией.
Фимасартан
Еще один новый ингибитор БРА, разработанный корейской компанией. Получен путем преобразования молекулы лозартана, превосходит его и вальсартан в 10 раз.
Применяется только в качестве антигипертензивного средства. Начальная доза – 60 мг, максимальная – 120 мг. Прием раз в сутки.
Плюсы:
- Лечит гипертоническую болезнь
- Может применяться при сердечной недостаточности
- Действует быстро и длительно
- Показывет антигипертензивный эффект в течение 24 часов
- Расширяет сосуды
- Выводится только с калом.
Минусы:
- На рынке представлен одним представителем, дорогой.
Аналоги:
Канарб (Борюнг, Корея) 6 мг №30— 907 р., 120 мг №30 – 1348 р.
Ключевые моменты
Сартаны (БРА) — группа уникальная. Если больной человек хорошо переносит его, у него стабилизировалось давление и удерживается в течение суток, при этом он имеет диабет и повышенный вес, тогда не стоит искать лучшее средство среди других групп лекарств. На нем можно оставаться пожизненно, при необходимости лишь повышать дозу и добавлять диуретик.
Через несколько лет приема увидим положительные сдвиги: размеры сердца и толщина сосудов придут в норму, восстановится работа почек, стабилизируется сахар, уровень холестерина. В перспективе они снизят риск возникновения инфаркта и инсульта.
Также они не допустят появление повторного инфаркта, замедлят прогрессирование почечной недостаточности, снизят риск появления диабета у пациентов из группы риска.
Кроме того, антагонисты рецепторов ангиотензина хорошо переносятся, их следует рассматривать в качестве препаратов первой линии для профилактики и устранении факторов риска ССЗ и других заболеваний.
Добавление сартанов к ингибиторам АПФ или антагонистам альдостерона вряд ли будет целесообразным, этого следует избегать с учетом возникновения гиперкалиемии.
Если у человека, который принимает ингибитор АПФ или сартан, все еще сохраняются симптомы, возможно, добавление антагониста кальция (амлодипина) или бета-блокатора (небиволола) либо попробовать прием ангиотензина/неприлизина (Юперио).
В рейтинге России по рекомендациям врачей лидирует лозартан, на втором месте – валсартан. Объясняется это доступной ценой и хорошей изученностью. Несмотря на то, что другие представители группы мощнее, имеют более продолжительное действие, применяются реже.
Выбор БРА можно считать идеальным, если он рекомендуется с учетом индивидуальных особенностей организма, переносимости и имеющейся патологии.
Как выбрать достойный препарат, чтобы он принес максимальную пользу, при различных состояниях:
- Гипертонческая болезнь – можно любой сартан. Хорошо себя зарекомендовали олмесартан, эпросартан и телмисартан.
- Предупреждение сердечной патологии – лучше телмисартан, можно и лозартан
- Недостаточность сердца (одышка) – лозартан, вальсартан, кандесартан
- Сразу после инфаркта – лучше валсартан, допускается телмисартан
- Инсульт – лозартан либо телмисартан, кандисартан, эпросартан.
- Мерцателная аритмия – телмисартан , на втором месте кандесартан валсартан и лозартан
- Диабет – телмисартан, валсартан. На втором месте – лозартан, ирбисартан и кандисартан. Нежелателен – олмесартан
- Метаблический синдром (ожирение) – телмисартан, втором плане —валсартан
- Подагра – лозартан, нежелателен – кандесартан
- При половой слабости – отдать предпочтение валсартану, лозартану, ирбесартану.
- Когнитивные нарушения – Кандесартан, Ирбесартан, Лозартан, Валсартан, Эпросартан, Телмисартан.
Только правильный подход в выборе лекарства позволит улучшить качество жизни, добиться ее продления и снизить риски фатальных случаев.
Рейтинг
Последние европейские рекомендации 2013 г. по лечению артериальной гипертензии (ESH/ESC Guidelines for the management of arterial hypertension) декларируют, что «…поскольку метаболический синдром часто расценивается как “предиабетическое” состояние, предпочтение отдается блокаторам ренин-ангиотензиновой системы и антагонистам кальция, т. к.
они потенциально могут улучшать или по крайней мере не ухудшать чувствительность к инсулину, в то время как бета-блокаторы (за исключением бета-блокаторов с вазодилатирующими свойствами) и диуретики должны рассматриваться как дополнительные препараты, использовать которые предпочтительно в низких дозах». В рекомендациях в разделе «Препараты, которым отдается предпочтение в определенных ситуациях», указывается также, что ингибиторы ангиотензинпревращающего фермента (иАПФ), блокаторы рецепторов ангиотензина II (БРА) и антагонисты кальция являются препаратами выбора при метаболическом синдроме [1].
Известно, что БРА (сартаны) более полно, чем иАПФ, подавляют активность ренин-ангиотензин-альдостероновой системы и не влияют на систему брадикинина. По антигипертензивной эффективности иАПФ и БРА равнозначны, но последние имеют лучший профиль переносимости, т. к. не вызывают кашель, ангионевротический отек. БРА обеспечивают более высокую приверженность к терапии среди больных АГ из-за лучшего профиля переносимости, отсутствия «ускользания» гипотензивного эффекта.
БРА обладают выраженными кардио- и нефропротективными действиями: предотвращают гипертрофию левого желудочка, увеличивают продолжительность периода удержания синусового ритма при пароксизмальной форме фибрилляции предсердий, уменьшают степень микроальбуминурии и протеинурии, замедляют прогрессирование сердечной и почечной недостаточности. При длительном приеме БРА уменьшают толщину интимы-медиа сонных артерий и объем крупных атеросклеротических бляшек (исследование МORE с телмизартаном).
Значимое снижение риска развития сахарного диабета при терапии БРА установлено также в исследованиях LIVE, VALUE, CHARM, ALPIN.
В исследовании LIFE снижение относительного риска развития новых случаев сахарного диабета на фоне приема лозартана составило 25 %, в SCOPE при терапии эпрозартаном – 20 % и в CHARM при терапии кандесартаном – 22 %. По данным мета-анализа было также показано, что терапия БРА сопровождается снижением развития новых случаев сахарного диабета [2].
При этом отмечено значимое снижение частоты развития сердечно-сосудистых осложнений при лечении БРА больных АГ с сахарным диабетом (LIFE, IDNT, RENAAL).
Важное преимущество терапии БРА в свете эпидемии метаболического синдрома состоит в том, что число АТ1-рецепторов и их чувствительность к ангиотензину II резко возрастают при ожирении, гиперинсулинемии и дислипидемии.
Важным механизмом действия БРА является модуляция активности PPARγ-рецепторов, ответственных за гомеостаз глюкозы, метаболизм липидов и регулирование уровня АД. Этот эффект обеспечивает не только снижение АД, но и нормализацию уровней глюкозы, инсулина и триглицеридов. Причем результаты ряда исследований свидетельствуют об уменьшении инсулинорезистентности тканей за счет стимуляции ядерных PPARγ-рецепторов клеток жировой, мышечной тканей, гепатоцитов и этот эффект сопоставим с действием пероральных гипогликемических препаратов.
Таким образом, существуют убедительные предпосылки к широкому использованию класса БРА при метаболическом синдроме. В то же время перед практическим врачом встает проблема дифференцированного выбора конкретного препарата для конкретного пациента. В связи с этим целесообразно рассмотреть клинико-фармакологические особенности представителей БРА. Тем более что существенные внутриклассовые различия между ними находят новые подтверждения [3]. Так, в клиническом исследовании сравнивали два препарата группы БРА (телмисартан и лозартан), в ходе которого было установлено, что телмисартан в отличие от лозартана уменьшает концентрацию свободной глюкозы крови, несвязанного инсулина и HbA1c, тем самым выявляя основные внутриклассовые различия между препаратами по потенциальному улучшению метаболических нарушений у больных метаболическим синдромом [4].
Лозартан
В течение последнего десятилетия появились многочисленные и убедительные данные о тесной взаимосвязи между повышением уровня мочевой кислоты и увеличением риска сердечно-сосудистых осложнений при артериальной гипертензии, метаболическом синдроме, сахарном диабете 2 типа. При этом доказана связь меду нарушением обмена мочевой кислоты и эндотелиальной дисфункцией [5]. По данным PIUMA Study, наличие гиперурикемии повышает риск кардиоваскулярных осложнений в 1,73, а риск смертности – в 1,96.
Распространенность гиперурикемии при сочетании артериальной гипертензии и метаболического синдрома составляет 37,8 %, а в его отсутствие – 22 % [6]. При этом длительность заболеваний не влияет на частоту гиперурикемии. Авторы исследования показали, что у пациентов с уровнем мочевой кислоты свыше 300 мкмоль/л более выражены метаболические факторы риска, которые находятся в прямой зависимости от степени повышения мочевой кислоты. Лозартан блокирует две основные транспортные системы эпителиоцитов дистальных канальцев, участвующих в реабсорбции уратов (урат/лактат и урат/хлорид) и защищает структуры почечного тубулоинтерстиция от повреждающего действия уратов. При применении лозартана экскреторный пул мочевой кислоты увеличивается только за счет торможения реабсорбции уратов без увеличения фильтрации, что принципиально отличает его от классических урикозурических средств, при применении которых фильтрация уратов возрастает и повышается риск развития нефролитиаза. Показано, что урикозурической активностью обладает сам лозартан, а не его активный метаболит E-3174 [7]. Следовательно, эта активность обусловлена особенностями молекулы, а не блокадой АТ1-рецептора, что принципиально важно при анализе класс-специфических эффектов этой группы антигипертензивных средств. Исследование LIFE, которое оценивало влияние лозартана и атенолола на сердечно-сосудистые осложнения и смертность среди больных артериальной гипертензией с высоким риском и гипертрофией левого желудочка, также позволило изучить связь исходного уровня мочевой кислоты с другими факторами риска и прогнозом заболевания, стало первым крупномасштабным исследованием, продемонстрировавшим, что снижение уровня мочевой кислоты при терапии лозартаном связано с положительным влиянием на частоту осложнений при лечении артериальной гипертензии.
Валсартан
В исследовании NAVIGATOR study показано, что у пациентов с нарушением толерантности к глюкозе и факторами риска терапия валсартаном приводит к относительному снижению на 14 % и абсолютному снижению на 3,8 % частоты новых случаев сахарного диабета [8].
Отличительной чертой валсартана является его положительное влияние на сексуальную функцию у мужчин и женщин [9, 10]. Это обусловлено его способностью оказывать прямой вазодилатирующий эффект, улучшать эндотелиальную функцию и микроциркуляцию, снижать объем соединительной ткани в кавернозных телах, повышать уровень тестостерона у мужчин и опосредованно через метаболиты ангиотензина II (ангиотензин IV) влиять на дофаминергическую систему, участвующую в регуляции полового поведения.
Кандесартан
Метаболические эффекты длительной гипотензивной терапии кандесартаном изучались в исследовании ALPINE [11]. При сравнении с гидрохлоротиазидом в группе кандесартана было выявлено снижение уровня инсулина, глюкозы в крови, триглицеридов и повышение ЛПВП. В группе гидрохлоротиазида по сравнению с группой кандесартана также отмечено повышение соотношений холестерина липопротеидов высокой и низкой плотности и аполипопротеин В/аполипопротеин АI, что указывает на ухудшение липидного профиля. На фоне этих изменений сахарный диабет был диагностирован у 4,1 % больных группы гидрохлортиазида и лишь у 0,5 % больных группы кандесартана, а метаболический синдром был диагностирован у 18 больных в группе гидрохлоротиазида и лишь у 5 больных группы кандесартана. Отличительной чертой препарата является наличие доказательной базы эффективного применения при хронической сердечной недостаточности, в т. ч. в подгруппе пациентов с нарушением углеводного обмена.
Ирбесартан
Нефропротективный эффект и способность препарата уменьшать альбуминурию доказаны в крупных исследованиях (IRMA, IDNT). Но важной особенностью ирбесартана является его способность обеспечивать 70 % пациентов достижение целевого АД при метаболическом синдроме. При этом у всех отмечено уменьшение окружности талии, снижение исходно повышенных уровней инсулина, глюкозы и липидов крови. Причем необходимо отметить, что оно наиболее выраженно при сочетании артериальной гипертензии и метаболического синдрома [12]. Схожие результаты были получены и в другом исследовании [13]. Кроме того, недавние исследования показали, что ирбесартан и телмисартан действуют как частичные агонисты γ-рецептора активатора пролиферации пероксисом (PPARγ) в концентрациях, достигаемых при пероральном приеме, и дозах, рекомендуемых в качестве лечения артериальной гипертензии, что делает возможным их использование для повышения чувствительности к инсулину [14].
Телмисартан
Телмисартан проявляет максимальную активность в отношении PPAR по сравнению с другими БРА и обладает максимальной липофильностью. PPARγ играют ключевую роль в метаболизме и энергообмене жировой ткани – создании запаса липидов в белой жировой ткани и усилении расхода энергии в буром жире. PPARγ участвует также в дифференцировке адипоцитов и регуляции метаболизма глюкозы посредством улучшения чувствительности к инсулину, являясь связующим звеном между метаболизмом липидов и углеводов. Применение телмисартана может предотвращать развитие атеросклероза путем снижения содержания висцерального жира, подавления воспаления сосудов и повышения уровня адипонектина, особенно у пациентов с метаболическим синдромом.
В недавно опубликованном мета-анализе 10 рандомизированных исследований с участием 546 пациентов с метаболическим синдромом было показано, что телмисартан достоверно снижает уровень глюкозы натощак, гиперинсулинемию, гликированный гемоглобин, повышает чувствительность к инсулину и уровень адипонектина [15].
Важно отметить, что такое же положительное влияние на все указанные показатели, а также липиды и резистин телмисартан оказывает и на фоне терапии розиглитазоном [16]. Кроме этого только телмисартан в сочетании с розувастатином уменьшает инсулинорезистентность и уровень С-реактивного белка в отличие от комбинации этого статина с ирбесартаном и олмесартаном [17].
Таким образом, анализ доказательной базы применения БРА при метаболическом синдроме, особенности их клинической фармакологии и опыта практического применения позволяют предложить практическому врачу простой алгоритм их дифференцированного применения при этом состоянии (см. рисунок).