Фурагин
Противомикробное средство широкого спектра действия, относится к группе нитрофуранов. Под влиянием нитрофуранов происходит подавление дыхательной цепочки и цикла трикарбоновых кислот (цикла Кребса), а также угнетение других биохимических процессов микроорганизмов, в результате этого происходит разрушение их оболочки или цитоплазматической мембраны.
Активен в отношении грамположительных кокков: Streptococcus spp., Staphylococcus spp.; грамотрицательных палочек: Escherichia coli, Salmonella spp., Shigella spp., Proteus spp., Klebsiella spp., Enterobacter spp.; простейших: Lamblia intestinalis и других микроорганизмов, резистентных к антибиотикам.
В отношении Staphylococcus spp., Escherichia coli, Aerobacter aerogenes, Bacterium citrovorum, Proteus mirabilis, Proteus morganii фуразидин, по сравнению с другими нитрофуранами, более активен.
В отношении большей части бактерий бактериостатическая концентрация составляет от 1:100 000 до 1:200 000. Бактерицидная концентрация примерно в 2 раза больше.
В результате действия нитрофуранов микроорганизмы выделяют меньше токсинов, в связи с этим улучшение общего состояния пациента возможно еще до выраженного подавления роста микрофлоры. Нитрофураны активизируют иммунную систему организма: повышают титр комплемента и способность лейкоцитов фагоцитировать микроорганизмы. Фуразидин в терапевтических дозах стимулирует лейкопоэз.
Резистентность к фуразидину развивается медленно и не достигает высокой степени.
Фармакокинетика
После приема внутрь фуразидин абсорбируется из тонком отделе кишечника путем пассивной диффузии. Всасывание нитрофуранов из дистального сегмента тонкого кишечника превышает всасывание из проксимального и медиального сегментов соответственно в 2 и 4 раза (следует учитывать при одновременном лечении урогенитальных инфекций и заболеваний ЖКТ, в частности хронических энтеритов). Нитрофураны плохо всасываются из толстой кишки.
Cmax в плазме крови сохраняется от 3 до 7 или 8 ч, в моче фуразидин обнаруживается через 3-4 ч.
В организме фуразидин распределяется равномерно. Клинически важно высокое содержание препарата в лимфе (задерживает распространение инфекции по лимфатическим путям). В желчи концентрация его в несколько раз выше, чем в сыворотке, а в ликворе — в несколько раз ниже, чем в сыворотке. В слюне содержание фуразидина составляет 30% от его концентрации в сыворотке. Концентрация фуразидина в крови и тканях сравнительно небольшая, что связано с быстрым его выделением, при этом концентрация в моче значительно выше, чем в крови.
Метаболизируется в незначительной степени (<10%).
Выводится почками путем клубочковой фильтрации и канальцевой секреции (85%), частично подвергается обратной реабсорбции в канальцах. При низких концентрациях фуразидина в моче преобладает процесс фильтрации и секреции, при высоких концентрациях уменьшается секреция и увеличивается реабсорбция. Фуразидин, являясь слабой кислотой в кислой моче не диссоциирует, подвергается интенсивной реабсорбции, что может усилить развитие системных побочных эффектов. При щелочной реакции мочи выведение фуразидина усиливается.
При снижении выделительной функции почек интенсивность метаболизма возрастает.
Инструкция по применению ФУРАГИН (FURAGIN)
Обычно препарат переносится хорошо, но возможны побочные действия.
Частота случаев побочных реакций лекарственного средства — это выраженное в процентах соотношение количества пациентов, у которых в определенное время возникла побочная реакция при применении лекарственного средства к общему количеству пациентов, которые в определенное время применяли это лекарственное средство.
Побочные реакции указаны в соответствии с системными классами органов, в порядке убывания частоты. Критерии частоты развития побочных реакций:
- свыше 10% — очень частые;
- 1-10% — частые;
- 0.1-1% — нечастые;
- 0.01-0.1% — редкие;
- меньше 0.01% — очень редкие.
Нарушения со стороны крови и лимфатической системы:
очень редкие — нарушения кроветворения (агранулоцитоз, тромбоцитопения, апластическая анемия).
Нарушения со стороны нервной системы:
нечастые — головокружение, сонливость, нарушение зрения;
- редкие — периферическая невропатия;
- очень редкие — легкая интракраниальпая гипертензия.
- редкие — рвота, понос;
- очень редкие — панкреатит (воспаление поджелудочной железы).
- очень редкие — ангионевротический отек, крапивница, дерматит, Erythemamultiforme.
Нарушения со стороны дыхательной системы, органов грудной клетки и средостения:
редкие — острые и хронические легочные реакции. Острая легочная реакция развивается стремительно. Она проявляется тяжелой одышкой, лихорадкой, болью в грудной клетке, кашлем с мокротой или без, эозинофилией (повышение числа эозинофильных гранулоцитов в крови). Имеются сведения об одновременном с острой легочной реакцией появлении высыпаний на коже, зуде, крапивнице, миалгии (мышечная боль), ангионевротическом отеке (отек лица, шеи, тканей полости рта и гортани). В основе острой легочной реакции лежит реакция повышенной чувствительности, которая может развиваться в течение нескольких часов, реже — в течение минут. Острая легочная реакция обладает возвратным характером, она исчезает при прекращении применения препарата. Хроническая легочная реакция может развиваться через длительный промежуток времени после прекращения лечения нитрофуранами (в т. ч. фурагином). Характерно постепенное нарастание одышки, учащенное дыхание, нестабильная лихорадка, эозинофилия, прогрессирующий кашель и интерстициальный пневмонит и/или фиброз легких.
Нарушения со стороны ЖКТ:
нечастые — снижение аппетита, тошнота;
Нарушения со стороны кожи и подкожных тканей:
редкие — папулезная сыпь, зуд, преходящее выпадение волос;
Нарушения со стороны скелетно-мышечной и соединительной ткани:
очень редкие — артралгия (боль в суставах).
Общие нарушения:
редкие — слабость, повышение температуры тела.
Нарушения со стороны печени и желчевыводящих путей:
очень редкие — холестатическая желтуха, гепатит.
Фурагин окрашивает мочу в коричневый цвет.
Побочные действия уменьшаются, если препарат принимают после еды, запивая большим количеством жидкости.
В случае развития побочных действий следует уменьшить дозу или прекратить прием препарата.
Современные подходы к лечению пиелонефрита у детей
Какая диета рекомендована при пиелонефрите? На чем основывается выбор антибиотика и какова длительность его применения? В каких случаях отдается предпочтение комбинированной антибактериальной терапии?
Комплексное лечение пиелонефрита предусматривает организацию и проведение мероприятий, направленных на ликвидацию микробно-воспалительного процесса в почечной ткани, восстановление функционального состояния почек, уродинамики, иммунных нарушений. Выбор терапевтических мероприятий определяется состоянием макроорганизма, формой пиелонефрита (обструктивный, необструктивный), фазой заболевания (активная фаза, ремиссия), биологическими свойствами самого возбудителя.
На период выраженной активности микробно-воспалительного процесса рекомендуется постельный или полупостельный режим. Расширяют режим начиная со второй недели заболевания, после исчезновения экстраренальных проявлений. Диета строится в зависимости от активности заболевания, функционального состояния почек, а также от наличия или отсутствия метаболических нарушений. В период активной фазы пиелонефрита рекомендуется ограничение поступления продуктов, содержащих избыток белка и экстрактивных веществ, исключение или ограничение продуктов, для метаболизма которых требуются большие энергетические затраты, а также ограничение потребления продуктов, содержащих избыток натрия. При остром пиелонефрите на 7—10 дней назначается молочно-растительная диета с умеренным ограничением белка (1,5–2,0/кг), соли (до 2–3 г в сутки). При отсутствии обструкции мочевой системы рекомендуется достаточное питье (на 50% больше возрастной нормы) в виде «некрепкого» чая, компотов, соков. Лечебное питание при хроническом пиелонефрите должно быть максимально щадящим для тубулярного аппарата почек. Рекомендуется прием слабощелочных минеральных вод (типа Славяновской, Смирновской) из расчета 2–3 мл/кг массы на прием в течение 20 дней, 2 курса в год.
Больные пиелонефритом должны соблюдать режим «регулярных» мочеиспусканий — мочиться каждые 2—3 часа в зависимости от возраста. Необходимо следить за регулярным опорожнением кишечника, туалетом наружных половых органов. Показаны ежедневные гигиенические мероприятия — душ, ванна, обтирание в зависимости от состояния ребенка. Лечебная физкультура проводится лежа или сидя, опять-таки в зависимости от состояния ребенка.
На протяжении многих лет основной этиологически значимой микрофлорой мочи при пиелонефрите у детей и взрослых является E. coli, обладающая большим набором факторов вирулентности. В 2000 — 2001 годах в 8 лечебно-профилактических учреждениях 7 городов России было проведено научное исследование АРМИД, которое координировали Л. С. Страчунский и Н. А. Коровина. Обследованы 607 детей в возрасте от 1 месяца до 18 лет с внебольничными инфекциями верхних и нижних отделов мочевой системы, у которых при бактериологическом исследовании мочи был выделен возбудитель в диагностическом титре (>=105 КОЕ/мл). Проведено определение чувствительности выделенных микроорганизмов к антимикробным препаратам основных групп. В результате проведенного исследования было показано, что инфекция мочевой системы (ИМС) в подавляющем большинстве случаев вызывается одним видом микроорганизма, при выявлении же в исследуемых образцах нескольких видов бактерий нужно исключить нарушения техники сбора и транспортировки материала. В то же время микробные ассоциации могут определяться и при хроническом течении уроренальной инфекции.
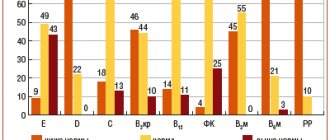
Согласно полученным данным, основными возбудителями внебольничных ИМС в России являются представители семейства Enterobacteriaceae (80,6%), главным образом E. coli, которая обнаруживалась в 53,0% случаев (с колебаниями от 41,3 до 83,3% в различных центрах). Другие уропатогены выделялись значительно реже. Так, Proteus spp. был обнаружен у 8,5%, Enterococcus spp. — у 8,5%, Klebsiella pneumoniae — у 8,0%, Enterobacter spp. — у 5,7%, Pseudomonas spp. — у 5,4%, Staphylococcus aureus — у 3,7% детей. Следует отметить, что у 7,2% больных выявлялись следующие микроорганизмы, которые обычно редко встречаются в клинической практике: Morganella morganii — 2,0%, Klebsiella oxytoca — 1,7%, Citrobacter freundii — 1,1%, Serratia marcescens — 0,8%, Acinetobacter lwoffii — 0,5%, Acinetobacter baumannii — 0,3%, Citrobacter diversus — 0,2%, Streptococcus pyogenes — 0,2%, Flavobacter spp. — 0,2%, Candida kruzei — 0,2%. Структура уропатогенов в разных регионах России была различной. Более высокая частота выделения K. pneumoniae наблюдалась в Санкт-Петербурге (12,3%); Enterococcus spp. — в Иркутске и Казани (соответственно 22,9 и 13,5%). Полученные данные указывают на необходимость проведения регулярного микробиологического мониторинга в различных регионах страны.
У большинства больных с острым течением пиелонефрита до выделения возбудителя «стартовая» антибактериальная терапия назначается эмпирически, то есть с учетом знаний об этиологической характеристике наиболее вероятных возбудителей и их потенциальной чувствительности к данному препарату, поскольку посев мочи и определение чувствительности требуют времени, а начало терапии откладывать недопустимо. При отсутствии клинического и лабораторного (анализ мочи) эффекта через три дня эмпирической терапии проводится ее коррекция со сменой антибиотика с учетом полученных данных о характере микробной флоры и чувствительности к ней препарата. При тяжелом течении инфекции успех терапии во многом определяется своевременным бактериологическим исследованием мочи.
При легком течении пиелонефрита может применяться пероральный путь введения антибиотика — существуют специальные детские формы антибиотиков (сироп, суспензия), которые отличаются хорошей всасываемостью из желудочно-кишечного тракта, приятными вкусовыми качествами. Парентеральный путь введения антибиотика используется при тяжелом и среднетяжелом течении пиелонефрита и предусматривает последующий переход на пероральный путь — «ступенчатая» терапия. При выборе препарата предпочтение следует отдавать бактерицидным антибиотикам. Длительность антибактериальной терапии должна быть оптимальной, до полного подавления активности возбудителя (при остром пиелонефрите и обострении хронического в условиях стационара антибактериальные препараты обычно назначаются непрерывно, в течение 3 недель, со сменой препарата каждые 7 — 10 — 14 дней). Потенцируют действие антибиотиков лизоцим, препараты рекомбинантного интерферона (виферон), фитотерапия.
При тяжелом течении пиелонефрита практикуют комбинированную антибактериальную терапию либо введение препаратов второго ряда.
Комбинированная антибактериальная терапия в нефрологии используется по следующим показаниям:
- тяжелое септическое течение микробно-воспалительного процесса в почечной ткани (с целью использования синергизма действия антибактериальных препаратов);
- тяжелое течение пиелонефрита, обусловленного микробными ассоциациями;
- с целью преодоления полирезистентности микроорганизмов к антибиотикам (особенно при терапии «проблемных» инфекций, вызванных протеем, синегнойной палочкой, цитробактером, клебсиеллой и др.);
- для воздействия на внутриклеточно расположенные микроорганизмы (хламидии, микоплазмы, уреаплазмы).
| Структура возбудителей внебольничных ИМС у детей в России |
При тяжелом течении пиелонефритического процесса чаще всего комбинация антибиотиков применяется для расширения спектра антимикробного действия, что особенно важно при отсутствии данных о возбудителе. При комбинации двух препаратов необходимо учитывать их механизм действия, фармакокинетические и фармакодинамические особенности, то есть одновременно использовать бактерицидные и бактерицидные антибиотики, а препараты бактериостатического действия комбинировать с аналогичными. У больных с тяжелым течением пиелонефрита непрерывная антибактериальная терапия проводится до полного подавления возбудителя со сменой антибиотика в случае эффективности каждые 10—14 дней. На фоне максимальной активности пиелонефрита, сопровождающейся синдромом эндогенной интоксикации, показана инфузионно-корригирующая терапия. Состав и объем инфузионной терапии зависят от состояния больного, показателей гомеостаза, диуреза и других функций почек. При тяжелом, гнойном пиелонефрите урологом устанавливается нефростома и уретральный катетер.
После получения результатов бактериологического исследования мочи в случае отсутствия эффекта от эмпирической терапии проводится этиотропная терапия в соответствии с характером высеваемой микрофлоры мочи и чувствительностью.
В ряде случаев при обострении хронического пиелонефрита дети старшего возраста могут лечиться амбулаторно с организацией «стационара на дому». В качестве антибактериальной терапии применяются «защищенные» пенициллины, цефалоспорины III поколения. Аминогликозиды в амбулаторной практике использовать не следует. В поликлинике под наблюдением нефролога и участкового педиатра после курса непрерывной антибактериальной терапии при наличии обструкции проводится противорецидивное лечение в течение 4—6 недель и более, в зависимости от характера уродинамических нарушений.
Рекомендуются следующие варианты противорецидивной терапии:
- фурагин из расчета 6-8 мг/кг массы (полная доза) в течение 2-3 недель; далее при нормализации анализов мочи и крови переходят на 1/2-1/3-1/4 от максимальной лечебной дозы в течение 2-4-8 и более недель, в зависимости от характера выявленных уродинамических изменений;
- ко-тримоксазол (бисептол) из расчета 2 мг по триметоприму + 10 мг по сульфаметоксазолу на килограмм массы внутрь 1 раз в сутки в течение 4 недель.
Один из перечисленных препаратов может назначаться в течение 10 дней каждый месяц сроком на 3—4 месяца в возрастных дозировках:
- налидиксовой кислоты (неграм, невиграмон);
- пипемидиновой кислоты (пимидель, палин, пипегал и др.);
- 8-оксихинолина (нитроксолин, 5-НОК).
На фоне максимальной активности пиелонефрита, сопровождающейся синдромом эндогенной интоксикации, показана инфузионно-корригирующая терапия. Состав и объем инфузионной терапии зависят от состояния больного, показателей гомеостаза, диуреза и других функций почек.
Как правило, в остром периоде пиелонефрита, с учетом высокой активности антиоксидантной системы организма, терапия антиоксидантами не проводится. По мере стихания микробно-воспалительного процесса в почечной ткани, через 3—5 дней от начала антибактериальной терапии назначаются антиоксиданты сроком 3—4 недели (витамин Е, С, веторон, препараты, содержащие селен, — триовит, селцинк и др.). С учетом того что при микробно-воспалительном процессе в почечной ткани наблюдается вторичная дисфункция митохондрий, медикаментозная ее коррекция предусматривает применение препаратов коэнзима Q10 (кудесан, синергин), переносчиков полиненасыщенных жирных кислот (L-карнитин), кофакторов ферментных реакций энергетического обмена (рибофлавин, никотинамид, липоевая кислота), димефосфона.
С целью улучшения почечного кровотока у больных пиелонефритом применяются эуфиллин, курсы магнитотерапии.
У большинства детей пиелонефрит обычно сопровождается выраженными сдвигами в иммунной системе организма, влияющими на течение и прогрессирование заболевания.
Иммунокорригирующая терапия при пиелонефрите назначается:
- детям раннего возраста, имеющим возрастную дисфункцию иммунитета;
- при тяжелых и рецидивирующих вариантах течения пиелонефрита, протекающих на фоне полиорганной недостаточности и пороков развития;
- при затяжном течении пиелонефрита в послеоперационном периоде;
- при пиелонефрите у часто болеющих детей;
- при пиелонефрите, вызванном «госпитальными», полирезистентными штаммами (Pseudomonas, Proteus, Enterobacter, Citrobacter, Serratia, Hafnia и др.) и микст-инфекцией.
Иммуномодулирующая терапия в фазе максимальной активности, как правило, не назначается; она показана при стихании микробно-воспалительного процесса. Применение иммуномодулирующей терапии при пиелонефрите у детей способствует:
- сокращению продолжительности активного периода заболевания и сроков пребывания больного в стационаре;
- снижению риска рецидивирования пиелонефрита, повторных респираторных инфекций.
Применяются препараты рекомбинантного интерферона (виферон, реаферон). Виферон назначается ректально в зависимости от возраста: детям моложе 7 лет вводится виферон-1 (150 МЕ) по 1 свече дважды в день в течение 7—10 дней, затем прерывистыми курсами 2—3 раза в неделю в течение 4—6 недель. Детям старше 7 лет назначается виферон-2 (500 МЕ). Аналогичное курсовое лечение проводится у детей раннего возраста.
Реаферон применяется внутримышечно 2 раза в сутки не более 2 млн. МЕ. Препарат вводится ежедневно в течение 5—7 дней. С целью иммунокоррекции можно использовать лизоцим (перорально из расчета 5 мг/кг массы тела в сутки (не более 100—200 мг в сутки) в течение 10—20 дней или внутримышечно из расчета 2—5 мг/кг массы). Оправданно применение ликопида, препарат назначается детям начиная с периода новорожденности по 1 таблетке (1мг) 1 раз в день в течение 10 дней. У детей старше 14 лет можно использовать взрослые дозировки (таблетки по 10 мг) — по 1 таблетке (10 мг) 1 раз в день 10 дней. На фоне приема ликопида может отмечаться кратковременное повышение температуры в пределах 37,1—37,5°С . В ряде случаев с целью иммунокоррекции применяется иммунал, который назначается внутрь 3 раза в день в течение 4 недель (детям от 1 до 6 лет по 15—30 капель, старше 7 лет — по 30—45 капель на прием).
Бактериофаги назначаются внутрь при упорном высеве однотипного возбудителя из мочи и кала; при стойкой изолированной бактериурии. Фитотерапия показана в период ремиссии. Рекомендуются травы, обладающие противовоспалительным, антисептическим, регенерирующим действием.
При обструктивном пиелонефрите лечение проводится совместно с детским урологом или детским хирургом. Решается вопрос о показаниях к оперативному лечению, катетеризации мочевого пузыря и др. При выборе антибактериальных препаратов у детей с обструктивным пиелонефритом необходимо учитывать состояние функции почек и нефротоксичность антибиотиков. Использование аминогликозидов при выраженной обструкции не показано. У больных с незначительным снижением клубочковой фильтрации дозы «защищенных» пенициллинов, цефалоспоринов могут не подвергаться корректировке. При снижении клубочковой фильтрации более 50% по пробе Реберга дозы этих препаратов должны быть уменьшены на 25—75%. При выраженной активности обструктивного пиелонефрита с проявлениями синдрома эндогенной интоксикации наряду с этиотропным лечением проводится инфузионно-корирригирующая терапия. При выявлении артериальной гипертензии решается вопрос о назначении гипотензивных препаратов.
Успех терапии пиелонефрита, развивающегося на фоне метаболических нарушений, зависит от своевременной коррекции питания, назначения соответствующего питьевого режима, применения средств, нормализующих обменные процессы. При оксалурии назначаются витамины В6, Е, А. Длительность курса лечения составляет 15—30 дней, повторные курсы проводятся ежеквартально. Можно применять 2%-ный раствор ксидифона из расчета 3 мг/кг массы в день (чайная, десертная, столовая ложка в зависимости от возраста), курс лечения до 3—4 недель. Ксидифон противопоказан при гиперкальциемии, принимается вместе с витамином Е. При гипероксалурии показана окись магния, которая назначается в дозе 50—100—200 мг/сутки в зависимости от возраста 1 раз в день на 2—3 недели курсами 3—4 раза в год. Показан отвар овса, настой семени льна, проводятся курсы длительностью 1 месяц по 4 курса в год.
При вторичном пиелонефрите на фоне гиперуратурии показан прием витамина В6 (в первой половине дня, от 10 до 60 мг в сутки в зависимости от выраженности уратурии, в течение 3—4 недель). Назначается оротат калия, обладающий урикозурическим действием (0,3—0,5 г 2—3 раза в день, курс лечения 2—4 недели), антиоксиданты (витамины А, Е, С), уролесан, солуран, блемарен, магурлит, уралит.
Лечение пиелонефрита единственной почки проводится по общепринятой методике с учетом нефротоксичности антибактериальных препаратов (необходимо избегать применения аминогликозидов, цефалоспоринов I генерации, карбапенемов, монобактамов). При назначении антибактериальных препаратов следует учитывать состояние почек и при снижении функции последних использовать средние дозы препаратов. В случае развития артериальной гипертензии назначаются гипотензивные препараты. При развитии почечной недостаточности лечение проводится в условиях диализного центра.
Вакцинация детей с пиелонефритом осуществляется после достижения ремиссии, с обязательным предварительным лабораторным контролем анализов крови, мочи с целью уточнения активности процесса и функционального состояния почек. Вакцинация проводится по индивидуальному графику.
Показаниями к санаторно-курортному лечению у больных пиелонефритом являются:
- период стихания острого пиелонефрита (через 3 месяца от начала активности заболевания);
- первичный пиелонефрит в период ремиссии без нарушения функции почек и артериальной гипертензии;
- вторичный пиелонефрит в период ремиссии без нарушения функции почек и артериальной гипертензии;
Таким образом, сложность и многогранность патогенетических механизмов, лежащих в основе пиелонефрита у детей, высокий риск хронизации заболевания, связанный с особенностями макро- и микроорганизмов, требуют не только своевременного выявления микробно-воспалительного процесса в почечной ткани и мочевых путях с последующим применением достаточно интенсивной антибактериальной терапии, но и целого комплекса лечебных мероприятий, направленных на нормализацию метаболических нарушений, функционального состояния почек, восстановление гемо- и уродинамики, стимуляцию регенераторных процессов и уменьшение склеротических изменений в интерстиции почек.
Н. А. Коровина, доктор медицинских наук, профессор И. Н. Захарова, доктор медицинских наук, профессор Э. Б. Мумладзе Али Ахмед аль-Макрамани РМАПО, Москва
К 100-летию со дня рождения профессора П. Л. Сухинина
27 ноября 2002 года исполняется 100 лет со дня рождения профессора Сухинина Павла Леонидовича.
Павел Леонидович родился в Туле, в семье потомственного врача-педиатра Л. Г. Сухинина, который долгие годы был домашним доктором младших детей Л. Н. Толстого. Вся обстановка в семье способствовала тому, чтобы старшие дети Л. Г. Сухинина пошли по стопам отца и стали врачами.
В 1920 году П. Л. Сухинин поступил на медицинский факультет Московского университета. В 1923 году ему пришлось прервать учебу: будущий врач был арестован по делу «Московской теософской группы». К счастью, арест продолжался относительно недолго, 5 месяцев.
Прерванную учебу Павел Леонидович закончил в 1926 году и был оставлен в ординатуре профессора Д. Д. Плетнева, с которым проработал до 1938 года, времени трагической гибели профессора Плетнева.
В 1932 году Сухинин был приглашен на должность консультанта-терапевта в Московский областной институт акушерства и гинекологии. Проблемам сердечно-сосудистых заболеваний у беременных женщин и гинекологических больных посвящено более 60 научных публикаций Сухинина, монография «Эндокардиты пуэрперального периода», а также его докторская диссертация «Септические эндокардиты после аборта и родов».
Однако основная деятельность Павла Леонидовича по-прежнему была связана с клиникой факультетской терапии 1-го МОЛГМИ, а в годы Великой Отечественной войны — с Центральным военным госпиталем им. Н. Н. Бурденко. В 1952 году в связи с арестом руководителя клиники академика В. Н. Виноградова Сухинин подает заявление об увольнении и переходит на работу в Курский медицинский институт, где создает кафедру госпитальной терапии. Однако после возвращения в 1953 году В. Н. Виноградова к руководству клиникой и кафедрой Павел Леонидович возвращается в 1-й МОЛГМИ, не оставляя, однако, работу в Курске до 1955 года.
В 1955 году Сухинин становится руководителем терапевтической клиники Института скорой помощи им. Склифософского. В этот период в рамках клиники были подготовлены более 18 кандидатов и докторов медицинских наук. В 1964 году Сухинин добивается открытия первого в СССР Центра токсикологической неотложной помощи и становится его научным руководителем. В 1968 году на базе клиники создается кафедра госпитальной терапии третьего лечебного факультета МОЛГМИ, руководителем которой Сухинин остается вплоть до 1975 года. Умер он в 1983 году.
Жить Павлу Леонидовичу Сухинину пришлось в непростое время, однако он неизменно сохранял сострадание к пациентам, чувство долга, независимость суждений, доброту и внимание к ученикам и сотрудникам.