Первое описание гипоспадии датируется вторым столетием нашей эры в работе Galen, который впервые использовал данный термин. В течение первого тысячелетия единственным способом лечения данной патологии была ампутация полового члена дистальнее наружного отверстия. С тех пор произошли большие изменения в хирургическом лечении этого порока в лучшую сторону. В медицинской литературе описано более 300 различных методик коррекции данной патологии. Несмотря на то, что большинство методик, применяемых на сегодняшний день, были описаны за последние 60 лет, основные базовые принципы предложены более века назад.
Современные способы анестезии, микрохирургический инструментарий, шовный, перевязочный материал и антибактериальная терапия улучшают результаты лечения гипоспадии и, в большинстве случаев, позволяют выполнить реконструкцию за один этап в течение первого года жизни ребенка.
История оперативного лечения гипоспадии
Наиболее раннее описание данной патологии и лечения относится к работам Celsius (25 год н.э.) и Galen (второе столетие н.э.).
В 1874 году Duplay опубликовал свои работы, с которых начался современный этап развития методик реконструкции уретры. В настоящий момент описано более 300 способов операций. Большинство методик являются многоэтапными, при которых на первом этапе устраняется стеноз меата (наружного отверстия мочеиспускательного канала), если это необходимо, а на втором этапе проводится иссечение фиброзной хорды и коррекция искривления. Третьим этапом выполняется собственно пластика уретры по различным методикам.
Множество косметических и функциональных проблем связано с многоэтапными методами лечения: требуют множественных операций, наружное отверстие мочеиспускательного канала не выводится на верхушку головки полового члена, либо отмечается его ретракция (смещение вниз) за счет множественных манипуляций с тканями и образующихся рубцов.
Для уменьшения частоты осложнений Hinderer в 1960 году предложил одноэтапную методику лечения. Многочисленные модификации и новые методики были предложены различными хирургами в последующие десятилетия. В этих работах подтверждалось преимущество использования тканей без рубцов для реконструкции уретры при снижении количества оперативных пособий.
Этапы формирования уретры. Классификация
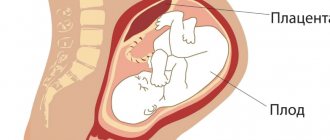
Гипоспадия – врожденный дефект, который возникает из-за нарушения развития уретры между 8 и 20 неделями беременности. Наружные половые органы идентичны у плодов мужского и женского пола до 8 недели гестации. В основном под влиянием тестостерона и его активного метаболита — дигидротестостерона — половые органы развиваются по мужскому типу. По мере роста фаллоса уретральная дорожка развивается от основания до головки полового члена.
По классической теории считается, что уретральные валики сливаются в области передней уретры, формируя трубчатую пенильную уретру и срединный шов. Формирование же головчатого отдела уретры происходит навстречу к уже сформированной стволовой части. Этим объясняется высокая частота венечных гипоспадий.
Крайняя плоть в норме образуется как разрастание кожи вокруг венечной борозды, которая растет циркулярно и сливается вокруг и над головкой. Нарушение слияния уретральных валиков препятствует процессу замыкания крайней плоти, в результате препуций при гипоспадии расположен по дорзальной поверхности в виде капюшона. В редких случаях может иметь место сохранная крайняя плоть с расщепленным меатусом – мегаломеатус.
Хорда (вентральное искривление ствола полового члена) часто сочетается с дистальной гипоспадией (до 90% случаев) и практически у всех пациентов с проксимальными формами. Возникает это из-за диспропорции роста кавернозных тел и изменённой уретры.
Гипоспадия классифицируется в зависимости от расположения наружного отверстия мочеиспускательного канала. Несмотря на то, что было предложено несколько классификаций, большинство хирургов применяют ту, что была описана Barcat и модифицирована Duckett, который оценивал формы гипоспадии после выпрямления кавернозных тел.
Гипоспадия подразделяется на:
- Переднюю (головчатая и венечная);
- Среднюю (дистально-стволовая, средне-стволовая и проксимально-стволовая);
- Заднюю (члено-мошоночная, мошоночная и промежностная).
Головчатая гипоспадия характеризуется расположением наружного отверстия уретры на головке полового члена, крайняя плоть дисплазирована, половой член чаще не искривлен. Выполняется одноэтапная коррекция.
При венечной форме гипоспадии наружное отверстие уретры располагается под головкой полового члена. Это наиболее часто встречаемая форма. Крайняя плоть расщеплена, искривление встречается чаще, чем при головчатой. Выполняется одноэтапная коррекция.
Стволовая гипоспадия – отверстие расположено где-либо на стволе полового члена, фиброзная хорда более выраженная, искривление имеет больший градус. Чаще выполняется одноэтапная коррекция.
Мошоночная гипоспадия – меат расположен в области мошонки, она расщеплена, может быть транспозиция полового члена в верхнюю или среднюю треть, кавернозные тела искривлены, губчатое тело уретры дисплазировано, требуется его удаление и реконструкция, мочеиспускание по женскому типу. При данной форме гипоспадии необходима корпоропластика. Предпочтительнее двухэтапные методики.
Промежностная гипоспадия относится к еще более проксимальной. Отмечается выраженная фиброзная ткань по вентральной поверхности полового челна с его искривлением. Большой дефект недостающей уретры, требующей реконструкции. Реконструкция кавернозных тел необходима. Предпочтительнее двухэтапные методики.
Передняя гипоспадия встречается в 50 % случаев, средняя — в 20%, задняя — в 30%.
Патогенез
В основе развития патологии лежит нарушение эмбриогенеза на 10–14 неделе гестации, что и приводит к нарушению нормального процесса дифференцировки зачаткового эпителия. При этом отмечается недоразвитие периферической части уретры и замыкается желоб уретры. Деформация пениса развивается вследствие неспособности уретральной борозды трансформироваться в трубчатый орган. Соответственно, на этом участке образуется короткий/плотный неэластичный соединительнотканный тяж (хорда), который укорачивает вентральную поверхность полового органа, что и приводит к его загибанию вниз.
Сочетанная патология
Гипоспадия часто сочетается с сужением наружного отверстия мочеиспускательного канала. Неопущенные яички и паховые грыжи являются аномалиями, чаще всего связанными с гипоспадией. В 1981 году в обзоре Khuri более 1000 пациентов с гипоспадиями сообщалось, что частота крипторхизма и паховой грыжи составила около 9%. При более тяжелых формах гипоспадии частота неопущения яичек превышала 30%, а сочетание с паховыми грыжами достигало 20%. Также отмечено сочетание с такими патологиями, как: крипторхизм — 9%, паховая грыжа — 9%, гидроцеле, свищ уретры, гипоплазия яичек, аномалии верхних мочевых путей и пузырно-мочеточниковый рефлюкс. Крайне редко встречаются сердечно-сосудистые и черепно-лицевые мальформации.
Сочетание гипоспадии с неопущением одного или двух яичек может быть связано с нарушением формирования пола и требует более полного эндокринологического, генетического обследования до операции. В 1999 году в исследовании, проведенном Kaefer et al., нарушение формирования пола было выявлено примерно у 30% пациентов с гипоспадией и крипторхизмом. При этом, чем более проксимально расположено наружное отверстие мочеиспускательного канала, тем более высока вероятность нарушения формирования пола (DSD). Если одна гонада не пальпируется, то возможность DSD возрастает до 50%, если оба яичка пальпируются, то 15%.
Частота встречаемости
Частота встречаемости данной аномалии составляет 1 на 250 родившихся мальчиков в среднем в мире и является наиболее распространенным заболеванием мочевого тракта. В некоторых странах отмечается тенденция к увеличению рождения детей с этой проблемой. В целом частота рождения достаточно постоянна — 0.26 на 1000 детей в Мексике и Скандинавии, 2.11 на 1000 новорожденных в Венгрии.
Частота гипоспадий выше у белокожих, чем у чернокожих, чаще встречается у евреев и итальянцев. Семейное наследование гипоспадии составляет около 7%.
Симптомы
Клиническая симптоматика гипоспадии определяется локализацией меатуса и степенью его сужения. Чем меатус расположен проксимальнее и чем его диаметр меньше, тем более выражена специфическая симптоматика. Так при легкой форме (головчатой) гипоспадии резкое расстройство мочеиспускания отсутствует, и такие пациенты в большинстве случаев в реконструктивной операции не нуждаются. При небольшом диаметре меатуса пациент жалуется на медленное/затрудненное мочеиспускание тонкой струей.
В случаях венечной гипоспадии отмечается частичное искривление полового органа, на фоне которого наблюдается затрудненное мочеиспускание. При этом, пациент вынужден принимать удобное положение для пениса, чтобы струя не была направлена в сторону ног.
При стволовой гипоспадии отмечается резкая деформация полового члена. При этом, пациент испытывает трудности при необходимости сходить в туалет: требуется сильно приподнимать пенис или мочиться в положении сидя. Сужение уретры препятствует свободному мочевыделению.
При промежностной/мошоночной гипоспадии внешние половые органы пациента видоизмененные: раздвоенная мошонка и деформированный критично маленький половой член. Процесс мочеиспускания при этой патологии может осуществляться исключительно в положении сидя. Выделение мочи значительно затруднено. Гипоспадия у мальчиков часто сочетается с различными аномалиями развития мочеполовой системы с характерными симптомами.
Причины
К возникновению гипоспадии приводят следующие факторы: генетические, эндокринные и экологические.
Генетические факторы. Среди монозиготных близнецов частота гипоспадии в 8 раз выше, чем в обычной популяции. Это ситуация может возникать из-за недостаточной выработки плацентой хорионического гонадотропина в критические периоды развития уретры.
Семейное наследование гипоспадии также имеет место. Вероятность рождения ребенка с данной патологией от отца с гипоспадией составляет около 8%. Наследование, вероятнее всего, является полигенным.
Эндокринные факторы. Снижение концентрации андрогенов во время беременности или блокирование их воздействия на ткани может привести к гипоспадии. В 1997 году по сообщениям Aaronson et al. было обнаружено, что 66% мальчиков с дистальной гипоспадией и 40% с проксимальными формами имели дефект в биосинтезе тестостерона.
Мутации в гене, ответственном за выработку фермента 5-альфа редуктазы, который превращает тестостерон в его активный метаболит дигидротестостерон, были связаны с возникновением данной патологии. В докладе, опубликованном в 1999 году Silver et al., было представлено, что почти у 10% мальчиков с изолированной гипоспадией был по крайней мере один затронутый аллель, отвечающий за выработку фермента 5-альфа редуктазы. Несмотря на то, что недостаток андрогенов приводит к возникновению гипоспадии, существуют другие причины, приводящие к нарушению формирования полового члена и уретры.
Некоторыми авторами было отмечено, что в странах с холодным климатом частота рождения детей с гипоспадией выше. Теоретически, это может быть связано с эффектом дневного света и солнца на функцию гипофиза, что в свою очередь влияет на гормональную среду матери и эмбриона. Однако другие авторы не заметили эту связь.
При экстракорпоральном оплодотворении (ЭКО) отмечается пятикратно повышенный риск рождения ребенка с аномалией половых органов по сравнению с контрольной группой. Это связано с воздействие прогестерона, который используется в протоколах ЭКО. Прогестерон является субстратом для 5-альфа редуктазы и действует как конкурентный ингибитор превращения тестостерона в дигидротестостерон. Другим эндокринопатиям или эндокринным аномалиям плода также отводится определенная роль.
Факторы окружающей среды. Во многих исследованиях на животных эстрогены были причиной возникновения данного порока. Химические вещества, обладающие значительной эстрогенной активностью, наблюдаются повсеместно в промышленно развитом обществе. Встречаются в пестицидах, которыми обрабатываются фрукты и овощи, эндогенные растительные эстрогены, попадающие через молоко животных, пластиковые накладки на металлических банках и фармацевтические препараты.
В исследовании Hadziselimovic сообщалось об увеличении концентрации эстрадиола в плацентарных базальных синцитиотрофобластах у мальчиков с неопущенными яичками по сравнению со здоровой популяцией. Неопущение яичек и гипоспадия скорее всего связаны, но не было доказано, что повышение концентрации эстрадиола приводит к гипоспадии.
Комбинированная теория. Растущее количество данных свидетельствует о том, что гипоспадия является полиэтиологичным заболеванием, включающим генетическую предрасположенность и воздействие факторов окружающей среды.
Дефицит андрогенов
Кластер причины развития болезни – гормональные нарушения: недостаточная выработка плацентой и яичниками мужских гормонов-андрогенов. Абсолютный (пониженная концентрация) или относительный (снижение чувствительности ткани) дефицит является основной причиной аномалий развития.
Известны многие ферментные дефекты, такие как дефицит 5α-редуктазы и рецептора андрогенов. В 10-70% случаев тяжелой проксимальной гипоспадии обнаруживается ферментный дефект синтеза андрогенов или гормональное заболевание, влияющее на гормональный баланс.
Прогноз
Использование современного анестезиологического пособия, шовного материала, микрохирургических инструментов, увеличительной техники, антибактериальной терапии позволяет выполнить оперативное лечение гипоспадии чаше всего за один этап с минимальным риском осложнений и получить превосходный косметический результат. Соблюдение оптимальных сроков оперативного лечения позволяет устранить психоэмоциональную составляющую у ребенка. Стремление выполнить оперативное лечение до 2 лет связано также и с тем, что ребенок не будет помнить сам факт лечения и пребывания в больнице.
Исследования, проведенные у пациентов, которым проводилось оперативное лечение гипоспадии, показали, что они более удовлетворены своей сексуальной жизнью, чем неоперированные.
Стоит обратить внимание, что методы лечения гипоспадии продолжают развиваться. Разрабатываются новые методы адгезии тканей: тканевые клеи и использование лазера для адгезии, что приводит к улучшению заживления ран и снижению риска образования свищей.
Клеточные технологии также активно развиваются и в скором времени позволят создать артифициальную уретру, особенно у пациентов с тяжелыми формами гипоспадии. Продолжается выявление факторов и понимание причин, приводящих к гипоспадии, что позволяет вырабатывать подход к профилактике данного состояния, проводить коррекцию внутриутробно.
Послеоперационный период
Пациенты выписываются после одного дня пребывания в больнице, но им требуется длительная послеоперационная помощь. Меры поддержки включают:
- Применение катетера. Используется для опорожнения мочи, содержащейся в мочевом пузыре, в течение первых 10 дней после процедуры. Без него мочеиспускание было бы невозможно.
- Повязка на рану. Гарантирует, что пенис будет обездвижен в течение нескольких дней, чтобы предотвратить инфекцию и позволить тканям зажить.
После операции нормально испытывать небольшую потерю крови и мочи. Необходимо принять меры для профилактики инфицирования. При появлении гноя, лихорадки и сыпи необходимо обратиться к врачу.
В течение 2-3 месяцев желательно исключить механическое травмирование пораженного участка. После операции необходимо регулярно посещать врача: через неделю, 3 и 6 месяцев, а также через год после коррекции. При этом специалист еще раз осмотрит внешний вид полового члена. К сожалению, ни одна операция по гипоспадии не обходится без шрамов. Однако хирург пытается ограничить разрезы средней линией нижней части полового члена. Эти порезы заживают с наилучшими возможными косметическими результатами.
Внешние проявления
Несмотря на то, что диагноз гипоспадии может быть установлен как при фетальной ультрасонографии, так и при проведении магнитно-резонансной томографии (МРТ), диагноз фиксируется обычно при осмотре новорожденного или при проведении диспансерного осмотра.
Крайняя плоть располагается по дорзальной поверхности в виде капюшона, на вентральной поверхности отсутствует. Передняя стенка уретры отсутствует, а наружное отверстие мочеиспускательного канала смещено проксимально. Редко бывает, что крайняя плоть сохранена и имеет нормальный вид. В этом случае гипоспадия обнаруживается во время проведения ритуального обрезания или по поводу фимоза или в более старшем возрасте, когда головка полового члена начинает выводиться за крайнюю плоть.
Наружное отверстие мочеиспускательного канала (меат) может располагаться на головке (60%), стволе полового члена (35%), в области мошонки или промежности (5%). У 75% пациентов отмечается сужение меата. Искривление полового члена в разной степени наблюдается у более 60%.
При выявлении гипоспадии во время обрезания манипуляция должна быть прекращена и пациент отправлен к квалифицированному урологу для консультации.
Фиброзная хорда, проводящая к искривлению, может быть видна невооруженным глазом, а может выявляться только во время эрекции. Проксимальные формы гипоспадии обычно сочетаются с расщеплением мошонки и пеноскротальной транспозицией.
Показания к операции
Меатотомия показана в любом возрасте, если сужение размеров наружного отверстия уретры вызывает нарушение процесса мочеиспускания (дизурия).
Коррекция гипоспадии в младшем возрасте показана по следующим причинам:
- — обеспечение нормального опорожнения мочевого пузыря (по мужскому типу) без разбрызгивания струи мочи и ее отклонения;
- — обеспечение нормальной эрекции и полового акта в будущем;
- — предупреждение инфекции мочевых путей;
- — корригирование возможного возникновения импотенции и бесплодия;
- — достижение нормального строения наружных половых органов;
- — обеспечение психосоциальной адаптации в обществе.
Сроки проведения операции
До 1980 года коррекция патологии проводилась у детей старше 3-х лет из-за большего размера органа. Однако генитальная хирургия в этом возрасте (осведомленность детей о половых органах и самоидентификация себя как личности в определенном поле происходит примерно в возрасте 18 месяцев) может привести к значительной психологической травме, включая ненормальное поведение и расстройство гендерной идентичности. Позднее оперативное лечение в период пубертата и старше приводит к более частым осложнениям, прежде всего, чаще происходит возникновение свищей, с вероятностью более 50%. В некоторых работах зарубежных авторов указывается на более высокое число осложнений у 5-летних пациентов, чем у годовалых.
В настоящее время большинство урологов стараются оперировать гипоспадию в возрасте 4-18 месяцев, с тенденцией к более ранним срокам. Это связано с улучшением эмоционального и психологического результата. В более раннем возрасте также происходит более быстрое заживление тканей.
Список источников
- Марченко А.С., Смирнов И.Е., Зоркин С.Н., Апакина А.В., Суходольский А.А., Шахновский Д.С. Лечение детей с гипоспадией. Детская хирургия. 2013. № 5. С. 40-44.
- Акранов Н. Р., Шарабидзе Г. Г. Парахирургические аспекты лечения мальчиков с гипоспадией (обзор литературы) // Репродуктивное здоровье детей и подростков. 2010, № 5, с. 39–48.
- Файзулин А. К., Прокопьев В. М., Демин Н. В. Современные методы лечения гипоспадии // Андрология и генитальная хирургия. 2009. № 2. 158 c.
- Володько Е.А. Основные характеристики нарушений формирования пола при гипоспадии у детей // Материалы VI Российского форума «Мать и Дитя», М., 2004. — С.554-555.
- Акранов Н. Р., Шарабидзе Г. Г. Парахирургические аспекты лечения мальчиков с гипоспадией (обзор литературы) // Репродуктивное здоровье детей и подростков. 2010, № 5, с. 39–48.
Лечение гипоспадии
Консервативного лечения гипоспадии не существует.
Хирургическое лечение гипоспадии преследует следующие цели:
- увеличение диаметра наружного отверстия мочеиспускательного канала;
- коррекция искривления кавернозных тел;
- реконструкция недостающего отдела уретры;
- восстановление нормального внешнего вида наружных половых органов.
Методики операций
Общие принципы основных этапов общие для всех методик. Вначале производится обнажение кавернозных тел от кожи полового члена. Фиброзные тяжи и «хорда», имеющиеся по вентральной поверхности, максимально иссекаются. Выполняется тест «искусственной эрекции» путем введения в кавернозные тела физиологического раствора, чтобы выявить любую девиацию полового члена. При невыраженном искривлении менее 45⁰ производится дорзальная пликационная корпоропластика под сосудисто-нервным пучком. При искривлении более 45⁰ целесообразно применять лоскутную корпоропластику или путем нанесения множественных насечек на вентральной поверхности белочной оболочки кавернозных тел. Также возможна коррекция искривления кавернозных тел путем пересечения белочной оболочки в точке максимального искривления и фиксации свободного трансплантата (слизистая щеки, кожа препуция или другие графты) на образовавшийся дефект. Данная методика приводит к устранению искривления и удлинению полового члена в отличие от пликационного способа коррекции.
При выраженной фиброзной «хорде», дисплазии губчатого тела уретры может потребоваться пересечение ее или иссечение. Различные способы пластики уретры могут быть использованы: тубуляризация самой уретральной площадки, использование местных кровоснабжаемых лоскутов, тканевых графтов или методика продвижения уретры (GAP procedures).
Наиболее часто применяемая методика при коррекции дистальных и среднестволовых гипоспадий – TIP (tubularized incised plate, Snodgrass). Этот способ позволяет создать уретру из местных тканей по принципу Duplay, но отличительной особенностью является рассечение задней стенки уретры, что создает возможность для формирования артифициальной уретры большего диаметра. Текущие исследования показывают, что данная технология используется большинством урологов во всем мире для лечения дистальных форм гипоспадии.
Далее мобилизуются крылья головки, чтобы накрыть ими сформированную уретру и придать головке более коническую форму. Избыточная кожа по дорзальной поверхности мобилизуется для закрытия дефекта на вентральной части.
Различный шовный материал применяется для пластики уретры, наиболее соответствующие требованиям современной пластической генитальной хирургии, является PDS 6-7/0 и Монокрил 6/0, как достаточно крепкие и быстро рассасывающиеся.
Множество исследований показало, что использование дополнительных слоев тканей (мясистая оболочка крайней плоти, вагинальная оболочка и др.) между уретрой и кожей снижает риск развития свищей. Спорным остается вопрос применения коротких уретральных стентов в комбинации с цистостомой и длительной катетеризации мочевого пузыря. В ретроспективном исследовании в 2015 году было показано, что более длительная катетеризация сроком до 3 недель приводит к меньшему количеству осложнений, чем при установке катетера менее 1 недели.
Повторные пластические операции при гипоспадии, проводимые в условиях недостатка пластического материала, составляют отдельную проблемную группу пациентов, имеющих больший процент осложнений. С целью коррекции гипоспадии у этих больных используются различные свободные трансплантаты: слизистая оболочка щеки, губы, нижней поверхности языка, кожа заушной области и др.
Коррекция члено-мошоночной транспозиции обычно выполняется как отдельный этап, так как дополнительные разрезы могут вызвать ишемию кожного лоскута, из которого сформирована уретра. Выполняется обычно через полгода после основного этапа операции, когда восстанавливается периферическое кровоснабжение.
Большинство форм гипоспадии корригируется за одну операцию, но при выраженном искривлении и удалении дисплазированного губчатого тела уретры целесообразно использовать поэтапный подход. При этом на первом этапе производится распрямление полового члена, создание уретральной площадки необходимого диаметра, а уретра формируется на втором этапе через 6 месяцев. На схеме представлен алгоритм при лечении проксимальной гипоспадии:
Гормональная терапия перед операцией
Многими специалистами используется гормональная терапия для увеличения размеров головки полового члена. Применяются предоперационные инъекции тестостерона или мази (кремы) на основе тестостерона или дегидротестостерона, а также уколы хорионического гонадотропина человека. В исследовании 182 детей с дистальной гипоспадией (средний возраст составил 30 месяцев) Asgari et al. было показано, что применение парентерального тестостерона может быть эффективно для снижения частоты осложнений с 12 до 5%.
Мы в своей практике применяем мазь Andractim Gel или Андрогель для предоперационной подготовки у пациентов с маленьким размерами головки полового члена.
Осложнения
Ранние осложнения включают кровотечение, воспаление, расхождение послеоперационных швов, некроз кожных лоскутов и отек. Поздние осложнения – свищи уретры, сужение уретры, вторичное искривление полового члена. Количество осложнений при лечении проксимальных форм гипоспадии выше, чем при дистальных. Послеоперационное кровотечение редко происходит и обычно контролируется компрессионной повязкой на половом члене.
Свищи уретры являются отдаленными осложнениями и выявляются чаще всего после удаления катетера, дренирующего мочевые пути. Вероятность образования свищей для большинства одноэтапных операций составляет около 10% по данным мировой литературы. При реконструкции проксимальных форм гипоспадии вероятность формирования свищей приближается к 40%. Свищи редко закрываются спонтанно и чаще всего необходима повторная операция через 6 месяцев. Вероятность рецидива свищей составляет около 10%.
Еще одним осложнением является меатальный стеноз или сужение мочеиспускательного канала. Стриктуры уретры могут возникнуть в отдаленном периоде и требуют бужирования, при неэффективности — оперативного лечения. Дивертикулы уретры могут появляться после реконструкции уретры с использованием препуциальной кожи. Созданная уретра не имеет каркасной основы, поэтому при появлении сопротивления току мочи в дистальных отделах возникает дивертикулоподобное расширение уретры. Данное осложнение обычно требует удаления излишка кожной ткани и сшивания уретральной трубки на катетере возрастного диаметра. Оптимальным является создание одного диаметра на всем протяжении.
Одним из осложнений является рост волос в уретре при использовании кожи, несущей волосяные фолликулы. В результате возникали конкременты в уретре, что требовало множественных повторных операций. Несмотря на то, что кожные лоскуты с волосяными фолликулами перестали использовать, такие пациенты до сих встречаются в практике уролога.
Консультация эндокринолога
При подозрении на нарушение формирования пола у пациента с гипоспадией, при сочетании гипоспадии с крипторхизмом или микропении, показана консультация эндокринолога.
Профилактика
Специфических профилактических мероприятий в отношении пациентов с гипоспадией не разработано. С учетом факторов риска развития данной патологии нужно стараться их избегать.
- Поздние роды.
- Исключить нервно-психическое перенапряжение во время беременности.
- Избегать инфекций, включая грипп, и внутриутробного инфицирования плода в первом триместре.
- Обследовать отца на предмет нарушения сперматогенеза.
- Исключить бесконтрольный прием прогестерона до беременности и пероральных контрацептивов во время беременности.
- Исключить алкоголь, курение и действие токсических веществ, в том числе пестицидов/гербицидов при беременности.
- Отказаться во время беременности от использования лака для волос (он содержит вредный для организма флатат).
Родителям
Оптимальный возраст для коррекции гипоспадии — 10 месяцев.
Коррекция гипоспадии чаще всего проводится за одну операцию.
Перед операцией может потребоваться использование гормональной мази. Мазь применяется за 3 недели до операции утром и вечером. Наносить мазь нужно на половой член, размер капли с ногтевую пластину большого пальца руки родителя.
Перед операцией нужно собрать необходимые анализы.
В послеоперационном периоде используется 2 памперса, катетер выводится во второй (внешний) памперс. Данная методика позволяет ребенку быть активным весь период нахождения в стационаре.
Антибактериальная терапия назначается на весь послеоперационный период.
После операции на половой член накладывается специальная компрессионная повязка, уретральный катер устанавливается сроком на 10-12 дней. По истечении этого срока повязка снимается, катетер удаляется.
Для оценки результата операции необходимо заснять на видео процесс мочеиспускания.
Использование анестезии или наркоза
При операции наиболее современным способом считается комбинированное обезболивание, когда применяется местная проводниковая анестезия.Препараты «маркаин» и «наропин» дают возможность обезболить ребенка от 4 до 9 часов после операции.
Если возникает такая необходимость, в дальнейшем можно применять традиционные анальгетики. Использование местного обезболивания позволяет уменьшить нагрузку на нервную систему, так как количество вводимых препаратов общего действия снижается.