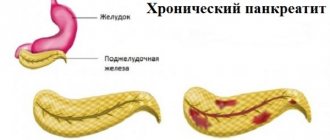
Фармакодинамика и фармакокинетика
Фармакодинамика
Метаболический препарат, оказывающий антигипоксическое и трофическое действие. Это высокомолекулярное соединение получают экстракцией из ткани миокарда свиней или крупного рогатого скота. По структуре близок к гемоглобину и играет основную роль в окислительно-восстановительных процессах в организме. Механизм действия связан с присутствием в молекуле железа, при переходе которого их одного состояния в другое, ускоряются реакции и обменные процессы, снижается гипоксия тканей.
Обладает высокой активностью в отношении супероксида, являющегося сильным окислителем — цитохром нейтрализует кислородные радикалы и действуют как «ловушка». Ингибирование кислородных радикалов в хрусталике глаза имеет значение в предотвращении развития катаракты.
Фармакокинетика
Полностью всасывается и проникает в клетки всех тканей.
Роль системы цитохрома Р450 в организме человека
Метаболизм лекарств в печени происходит в две стадии. Первая стадия биотрансформации происходит под действием цитохрома Р450, монооксигеназы и цитохром С-редуктазы. В результате окислительных реакций образуются полярные группы и метаболиты. Цитохром Р450 играет важную роль в окислительных процессах, поскольку система цитохрома выполняет большую часть этой работы. Эта система представлена протеинами, которые начинают метаболизм в тонкой кишке, но большая часть происходит в печени.
Изоферменты цитохрома представлены более, чем 55 формами и каждый способен метаболизировать несколько лекарств, подходящих ему по структуре. Это создает основу для взаимодействия лекарственных средств, одновременно поступающих в организм и зная это, можно предупредить тяжелые побочные реакции медикаментов. Вот некоторые примеры взаимодействия ЛС. Препараты, которые повышают активность ферментов, называются стимуляторами. Например, рифампицин, карбамазепин, фенитоин — сильные стимуляторы системы цитохрома, и препарат, принятый одновременно и метаболизирующийся этой системой, будет быстро выводиться из организма, не оказывая своего действия. Следовательно, эти препараты нельзя принимать вместе.
Есть и другой вид взаимодействия, когда вместе с одним лекарством человек употребляет другой — ингибитор цитохрома (например, антидепрессанты, кетоконазол, фторхинолоны, омепразол, циметидин, метронидазол, хлорамфеникол и многие другие). При этом замедляется его метаболизм, увеличивается период полураспада, возрастает риск передозировки и развития побочных реакций.
Роль семейства цитохромов P450 в патогенезе и лечении НАЖБП
Оксана Михайловна Драпкина, профессор, доктор медицинских наук:
– Мы продолжаем нашу программу. У нас лекции и дискуссии по гинекологии заканчиваются, мы полностью вошли в регламент, поэтому постараемся из него не выходить. Профессор Полунина Татьяна Евгеньевна открывает секцию гастроэнтерологии. Лекции «Роль семейства цитохромов P450 в патогенезе и лечении неалкогольной жировой болезни печени».
Татьяна Евгеньевна Полунина, профессор, доктор медицинских наук:
– Цитохромы P450 (CYP 450) – так называется большое семейство универсальных ферментов организма человека. Цитохромы P450 играют важную роль в окислении многочисленных соединений, таких как эндогенные соединения (стероиды, желчные кислоты, жирные кислоты, простагландины, лейкотриены, биогенные амины), а также экзогенные соединения (лекарственные препараты, продукты промышленного загрязнения, пестициды, канцерогены и мутагены), последние называются ксенобиотиками.
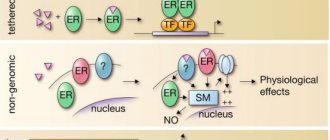
В данном слайде вы видите, где располагаются цитохромы P450. Они располагаются в гепатоците, в цитозоле. Эндоплазматический ретикулум является основой для расположения. И, в частности, липидная мембрана, которая содержит двухслойный слой фосфолипидов, имеет на себе несколько соединенных структур. Это цитохром, который включает в себя железопротеин, никотинамидадениндинуклеотид и оксидоредуктаза, которая включатся в комплекс метаболизма лекарственных препаратов и выше представленных ксенобиотиков.
Наиболее распространенными представителями этой группы, к которым обращаются клиницисты, являются цитохромы P452 АС, P450 2D, P450 2E1, P450 3A4. Эти ферменты катализируют широкий спектр метаболических реакций и один цитохром, может метаболизировать несколько лекарственных препаратов, которые имеют различную химическую структуру. Один и тот же лекарственный препарат подвергается различному воздействию в цитохроме P450 и в различных органах. И вот, в частности, важнейший цитохром, на который мы обращаем внимание, это цитохром P450 2E – важнейший изофермент цитохрома P450, он расщепляет липопротеины низкой плотности.
В настоящее время разработаны методы не только фенотипирования, которые основаны на субстратной специфичности определенных изоферментов цитохрома P450, но и активность того или иного фермента и метаболизма определяется по фармакокинетике маркерного субстрата и изменением концентраций неизмененного вещества и его метаболита. А вот определение изоферментов цитохрома P450 путем идентификации генов соответствующих изоферментов осуществляется с помощью полимеразной цепной реакции. Это называется генотипированием изофермента цитохрома P450.
На данном слайде мы видим, что в гепатоците то место, где расположены эндоплазматический ретикулум, цитохромы P450, которых насчитывается более 50, и лекарства, которые расщепляются в определенном цитохроме, оно в ряде случаев соединяется с цитохромом и образует везикулу, которая повреждает гепатоцит, вызывая при этом стресс и цитокины; приводит к активизации туморнекротического фактора и, в частности, является триггерным фактором для запуска каспаз, что проявляется с каталитическими процессами.
Неалкогольная жировая болезнь печени, которую впоследствии выделили в нозологическую единицу, стали называть как неалкогольная жировая болезнь печени (НАЖБП) с 1980 года, обнаружив в печени не злоупотребляющих алкоголем пациентов изменения, которые сходны с такими же, как при алкогольном поражении.
Естественное течение неалкогольной жировой болезни печени включает в себя стеатоз как начальную стадию, которая, не прогрессируя, может протекать бессимптомно, и стеатогепатит, который сопровождается ужасными вегетативными проявлениями, синдромом цитолиза и диспепсическими проявлениями. При развитии фиброза возникает достаточно серьезная проблема – цирроз печени, и развивается в дальнейшем портальная гипертензия и карцинома.
Хотелось бы обратить ваше внимание, что еще в 1894 году Кирнан предложил определенную архитектонику печени, которая состоит из балочного строения. На периферии балок, которые состоят из гепатоцитов полигональной формы, расположена триада: желчный ход, портальная вена и артерия. Данный слайд представляет нормальную здоровую печень и жировую инфильтрацию гепатоцитов. Стеатоз печени, который является одной из первых фаз развития неалкогольной жировой болезни печени, представлен в морфологическом виде на данной схеме.
Следующим вариантом развития воспалительного процесса, который приводит к фиброзной ткани, распространению ее по печени, мы видим стеатогепатит и в дальнейшем цирроз печени с развитием портальной гипертензии. Чаще всего это микронодулярный цирроз печени, который уже совершенно четко утвержден в стадиях развития неалкогольной жировой болезни печени, он сопровождается портальной гипертензией, варикозным расширением вен пищевода, желудка, осложнениями, которые типичны для цирроза печени, и летальным исходом.
При неалкогольном стеатогепатите наиболее часто развиваются моменты, которые связаны чаще всего как сопутствующие заболевания: сахарный диабет, ожирение. У пациентов неалкогольный стеатогепатит развивается до 75%, а если сочетается сахарный диабет и ожирение, то это уже 90% пациентов имеет неалкогольную жировую болезнь печени.
Печень, несомненно, главный орган-мишень, поражаемый при метаболическом синдроме. Инсулинорезистентность – ключевой признак, который является основой для накопления липидов внутри гепатоцитов, жировой дистрофии печени, неалкогольного стеатогепатита и цирроза печени.
Хотелось бы обратить внимание, что метаболический синдром включает в себя не только нарушения толерантности к глюкозе, но и дислипидемию, абдоминально-висцеральное ожирение, инсулинорезистентность и гиперинсулинемию, артериальную гипертензию, ранний атеросклероз, нарушение гемостаза, гиперурикемию, гиперандрогению. Хотелось бы сказать, что неалкогольная жировая болезнь печени, стеатоз, входит в состав метаболического синдрома и является в настоящее время квинтетом, который раньше назывался «смертельным квартетом».
Факторы риска, представленные на данном слайде, иногда меняются в разных странах, в частности американские позиции и европейские позиции незначительно разнятся. Но, тем не менее, окружность талии, уровень триглицеридов, липопротеидов, артериальное давление, в частности 130/85, уровень глюкозы – это те показатели, которые необходимо обязательно отслеживать у пациента с метаболическим синдромом.
Заболевания, ассоциированные с липидным обменом, это: неалкогольная жировая болезнь печени, сахарный диабет второго типа, ишемическая болезнь печени, гипертоническая болезнь.
В схеме патогенеза особое значение имеет инсулинорезистентность жировой ткани. Повышение липогенеза, то есть увеличения уровня жирных кислот, увеличение синтеза триглицеридов и липотоксичность приводят к тому, что развивается инсулинорезистентность, а это приводит к метаболическим дисфункциям, стрессу эндоплазматического ретикулума, в котором также происходит метаболизм жирных кислот и в частности липопротеидов, и к активации воспаления. Это клетки Купфера и звездчатые клетки, которые в дальнейшем приводят не только к тому, что повышается уровень липидов очень низкой плотности, несомненно, это приводит к тому, что развивается стеатогепатит с фиброзом, и мы получаем активность процесса, который движется в сторону цирроза печени.
На уровне гепатоцита жирные кислоты, которые подвергаются эстерификации в триглицериды и экспортируются в виде липопротеидов низкой плотности, это в нормальном гепатоците ситуация, которая связана с окислением в митохондриях, пероксисомах и микросомах.
Несомненно, в механизме инсулинорезистентности, который здесь представлен, ключевая роль принадлежит туморнекротическому фактору, свободным радикалам, лептину, жирным кислотам и увеличению липолиза, который приводит к поглощению жирных кислот, к нарушению β-окисления жирных кислот в митохондриях и также к накоплению жирных кислот в гепатоците.
Индукция цитохромов P450 4A11 и P450 2E1 приводит к перекисному окислению липидов, которое приводит, несомненно, к активизации моментов, связанных с накопление триглицеридов. Гиперинсулинемия – ключевой момент, который ведет к инсулинорезистентности. Он приводит также к увеличению гликолиза, синтезу жирных кислот и накоплению триглицеридов в гепатоцитах.
В следующем слайде виден механизм взаимодействия между микросомальным окислением и митохондриальным β-окислением. Обратите внимание, что митохондриальная Ω-оксидация и митохондриальная β-оксидация приводят к запуску так называемых рецепторов пероксисомального β-окисления и в частности рецепторов, активируемых в пролиферации пероксисом. Это приводит к экспрессии накопления определенного белка и, соответственно, ацетил-коэнзим А, который накапливается и запускает механизм, приводит к перегрузке дикарбоновыми жирными кислотами.
В следующем слайде вы видите, что стеатогепатит и фиброз формируются на фоне митохондриальных активных форм кислорода. Ключевым моментом для запуска фиброза является, несомненно, накопление малондиальдегида, который приводит к формированию воспалительных инфильтратов, фиброзу и активации звездчатых клеток. Звездчатые клетки запускают индукцию цитокинов, таких как туморнекротический фактор, трансформирующие факторы роста. Истощение антиоксидантной системы приводит к запуску Fas-леганд, митохондриальной активной формы кислорода, возникает некроз гепатоцита, и в дальнейшем развивается фиброзная ткань, которая является основой для развития цирроза.
На данном слайде представлена схема, вы видите избыток липидов, которые накапливаются в гепатоците. Митохондриальная дисфункция и дисфункция цитохрома P450 приводит к активизации перекисного окисления липида, запуску клетки Купфера, воспалительных цитокинов, активации звездчатых клеток и апоптозу, который в дальнейшем приводит к развитию некроза гепатоцита.
Метаболический синдром очень важен, потому что неалкогольная жировая болезнь печени, это часть метаболического синдрома. И не только на гепатоцит, в котором происходит повышение уровня липопротеидов низкой плотности и очень низкой плотности, триглицеридов (это очень важно), но также оказывается влияние на эндотелиальную клетку. Происходит эндотелиальная дисфункция и запускается также момент, который связан с перекисным окислением липидов, накоплением веществ, которые влияют на атеросклероз, внезапную смерть, сердечные приступы.
Несомненно, повышение уровня свободных жирных кислот связано с адипоцитами. И снижение в частности эстерифицированного холестерина также приводит к различным стрессам ядерного рецептора. А особенно важен в настоящее время так называемый активированный рецептор пролиферации пероксисом, именно к нему направлены все взоры ученых, которые работают с ожирением, с диабетом, с неалкогольной жировой болезнью печени.
Моноцит (макрофаг) в ряде случаев повышением уровня воспалительных ответчиков (туморнекротического фактора, интерлейкинов-6, мембранные толл-подобные рецепторы, свободные жирные кислоты) также запускает моменты, которые связаны именно с патологическими эффектами жирных кислот.
Критерии оценки инсулинорезистентности всем известны еще с 1985 года. Ее определяют индекс HOMA – Homeostasis Model Assessment, и уже более современный индекс QUICKI – Quantitave Insulin Sensitivity. Здесь представлены концентрация инсулина, глюкоза сыворотки крови, а также нормы.
Хотелось бы обратить внимание, что не всем пациентам с неалкогольной жировой болезнью печени необходимо проводить биопсию печени. У нас в настоящее время есть моменты, которые дают возможность нам определить уровень жировой инфильтрации печени. И в частности это фибротест.
В алгоритме диагностики неалкогольной жировой болезни печени мы уделяем внимание не только специфическим признакам, но также активности ферментов аланиновой и аспарагиновой трансаминазы, гамма-глутамилтранспептидазы, щелочной фосфатазы, обращаем внимание на прием алкоголя, который обсуждался у предыдущих коллег. И я хотела бы обратить внимание, конечно, на факторы риска: метаболический синдром, инсулинорезистентность, сахарный диабет. Назначается терапия по коррекции данной ситуации, при необходимости биопсия печени. Несомненно, требуются абсолютные показания для проведения биопсии. И если индекс массы тела превышает 35 и 40, тогда уже проводятся мероприятия, которые связаны с хирургическим лечением.
Хотела бы обратить ваше внимание на ряд лекарственных препаратов (нестероидные – противовоспалительный глюкокортикоз, и стероидные препараты, антибиотики тетрациклинового ряда), ряд нутрициологических факторов (голодание, быстрое снижение веса, хирургические вмешательства, метаболические генетические факторы, в частности, наследственный гемохроматоз, различные яды) и другие сопутствующие заболевания. Это очень важно для дифференциальной диагностики.
В стадии стеатоза важно лечение ожирения, инсулинорезистентности, дислипидемии. В стадии стеатогепатита важнейшим моментом является устранение окислительного стресса, воспаления и фиброза.
Избыточная индукция цитохрома P450 2E оказывает вредное воздействие на гепатоциты вследствие высвобождения свободных радикалов. Эссенциальные фосфолипиды действуют не только как антиоксиданты, но также служат очень важным моментом для снижения активности цитохрома 2E1, что показано в работах М.Алейник. Результаты некоторых исследований свидетельствуют о том, что введение эссенциальных фосфолипидов может уменьшить индукцию цитохрома P450 2E (работы Владимира Трофимовича Ивашкина, которые были представлены с Мариной Викторовной Маевской в российских источниках в 2004 году).
В формировании конечной стадии неалкогольной жировой болезни печени принимают участие стеллатные клетки. И в лабораторных экспериментах было продемонстрировано, что полное предотвращение активации стеллатных клеток с применением ингибиторов CYP2E1 предотвращают развитие цирроза.
Хотела бы обратить ваше внимание, что не только российский автор М.Алейник, а также японский автор Акияма в журнале «Гепатология» в 2009 году на основании модели алкогольного поражения печени также уделяет внимание цитохрому P450 2E, ацетил-КоА оксидазе и никотинамидадениндинуклеотид-оксидаз, что эссенциальные фосфолипиды проявляют противовоспалительную антиапоптотическую и противофиброзную активность при данной патологии.
Это теоретический вариант предположения применения ингибиторов цитохромов P450, а в частности препарата «Эссенциале», который является эталонным, и является важнейшим моментом для ингибирования цитохромов P450 2E и, соответственно, P450 4A11. Это предотвращает окисление липидов, гликолиз и снижает синтез жирных кислот.
В лечении неалкогольной жировой болезни печени представлены препараты: инсулиновые сенситайзеры, антиоксиданты, гепатопротекторы, антимикробные препараты.
Но я хотела бы обратить внимание на фосфолипиды мембран. Они являются главными липидными компонентами клеточных мембран. Повреждение фосфолипидных мембран ведет к синдрому цитолиза, а избыток реактивных составляющих кислорода приводит к повреждению фосфолипидных мембран на основании микросомального γ-окисления и пероксимального β-окисления. Соответственно, повреждения фосфолипидных мембран – это гибель клетки, что приводит к запуску фиброза и активации звездчатых клеток.
Повреждения структуры печени – это повреждение мембран. В варианте эссенциальных фосфолипидов представляет собой материал, который восстанавливает клеточные мембраны взамен липидов. Восстановление структуры печени дает возможность восстановлению функции печени.
Наши пациенты страдают не только алкогольной жировой болезнью печени, алкогольными гепатитами, а имеются и другие заболевания печени, это факт неоспоримый. Хотела бы обратить ваше внимание, что по данным Е. Кунца (монография 2008 года) эссенциальные фосфолипиды обладают антифибротическим эффектом, действием, стабилизирующим желчь и мембрану гепатоцита.
Это издание, которое было выпущено в 2008 году на основании фармакологических и клинических данных. Терапия эссенциальными фосфолипидами представляется предпочтительным выбором для значимого уменьшения проявления и устранений жировой болезни печени различной этиологии, развившейся вследствие употребления алкоголя, ожирения и если даже причину не удается усмотреть.
Я хотела бы обратить внимание, что существует несколько исследований по «Эссенциале». Эти исследования достаточно всем известны. Но хотела бы сказать, что и с сахарным диабетом «Эссенциале» дает возможность у пациентов с неалкогольной болезнью печени нормализовать уровень глюкозы, гликированного гемоглобина, сывороточного холестерина.
И в заключение я хотела бы сказать, что поражение печени, характеризующееся накоплением жира при отсутствии злоупотребления алкоголем известно как неалкогольная жировая болезнь печени. Факторами риска является ожирение, сахарный диабет второго типа. В патогенезе неалкогольной жировой болезни печени особое значение отводится избыточной активности цитохромов P450 2E1. Клинические варианты течения болезни: боль в правом подреберье, астеновегетативные и диспепсические расстройства, гепатомегалия. И наш алгоритм диагностики основан на последовательном исключении алкогольных и ятрогенных, а также вирусных поражений печени.
При анализе лабораторно-инструментальных исследований синдромы цитолиза и холестаза очень важны. Жировая дистрофия печени по результатам морфологического исследования является экспертной оценкой. В лечении необходимо снижать вес, длительно использовать инсулиновые сенситайзеры, антиоксиданты и гепатопротекторы «Эссенциале Н» в дозе 5-10 мл внутривенно капельно, с переходом на таблетированную форму по две капсулы три раза в день. Несомненно, вес снижать сложно, но необходимо корректировать функцию печени и других органов.
Спасибо за внимание.
Показания к применению
Раствор для инъекций:
- асфиксии новорожденных;
- отравления снотворными препаратами, алкоголем и наркотическими средствами;
- вирусный гепатит с печеночной комой;
- ишемические и дистрофические поражения миокарда;
- бронхиальная астма с дыхательной недостаточностью;
- пневмония;
- хроническая недостаточность кровообращения;
- тяжелые травмы;
- нарушения мозгового кровообращения;
- дыхательная недостаточность;
- операции на грудной клетке.
Глазные капли:
- дистрофия роговицы;
- кератит;
- помутнение роговицы.
Цитохром С, инструкция по применению (Способ и дозировка)
Препарат Цитохром С вводится внутривенно или внутримышечно. Перед применением препарата необходимо проверить чувствительность к нему. Для этого внутрикожно вводят 0,1 мл и выжидают 30 минут. При отсутствии реакции (крапивница, покраснение лица, зуд) можно приступать к инъекциям. Доза составляет 10-20 мг 1-2 раза в день. Лечение проводят 14 дней.
При сердечной недостаточности — внутривенно капельно 20 мг в течение 6-8 часов, разведя в 200 мл физиологического раствора. Суточная доза колеблется от 30 мг до 80 мг.
В период после операции на сердце — внутривенно по 10 мг 2 раза в день.
При печеночной коме, шоке, отравлениях — 50-100 мг внутривенно капельно.
При асфиксии новорожденным сразу после рождения вводят в пупочную вену 10 мг.
При бронхиальной астме — внутримышечно по 5-10 мг 2 раза в день.
Перед проведением повторного курса делают биологическую пробу.
Цитохром C лиофилизат д/р-ра д/ин 10мг фл №5
Состав
1 флакон содержит:
Действующее вещество: цитохром С.
Фармакокинетика
Цитохром-С — натуральный ферментный препарат из группы антигипоксических и метаболических средств. Цитохром С оказывает антигипоксическое, трофическое действие, стимулирует процессы регенерации. Цитохром С является ферментом, принимающим участие в процессах тканевого дыхания (является катализатором клеточного дыхания).
Цитохром С применяется в кардиологической практике в случае инфаркта миокарда, приводит к быстрому восстановлению больных. Цитохром С хорошо зарекомендовал себя как профилактическое средство при заболеваниях печени, сердечно-сосудистой системы.
Показания к применению
Цитохром-С применяют в комплексной терапии в качестве средства, улучшающего тканевое дыхание, при состояниях, сопровождающихся нарушением окислительно-восстановительных процессов в организме:
- асфиксии новорожденных,
- тяжелых травмах,
- до и после оперативного вмешательства (с целью предупреждения шока), в период ремиссии бронхиальной астмы с наличием дыхательной недостаточности, у больных с хронической обструктивной болезнью легких и сердечной недостаточностью,
- при вирусном гепатите, осложненном печеночной комой,
- при отравлении снотворными препаратами и окисью углерода
Противопоказания
Повышенная чувствительность к препарату, беременность, период лактации.
Способ применения и дозы
Препарат применяют внутривенно и внутримышечно. Перед применением Цитохрома-С следует содержимое флакона растворить в 4 мл воды для инъекций и определить индивидуальную чувствительность к нему. С этой целью внутрикожно вводят 0,1 мл препарата (0,25 мг). Если при этом в течении 30 минут не наступает реакция (покраснение лица, кожный зуд, крапивница), то можно приступать к лечению препаратом. Перед назначением повторного курса обязательно повторяют биологическую пробу.
Препарат вводят внутривенно медленно или внутримышечно в количестве 10-20 мг 1-2 раза в день. Курс лечения составляет 10-14 дней.
При сердечной недостаточности препарат разводят в 200 мл изотонического раствора хлорида натрия или 5 % раствора глюкозы и вводят внутривенно капельно (30-40 капель в минуту) в течение 6-8 часов. Суточная доза составляет 30-80 мг.
В послеоперационном периоде (операции по поводу врожденных и приобретенных пороков сердца) препарат вводят внутривенно 2 раза в день по 10 мг на инъекцию. Б случае тяжелого состояния (травма, шок, печеночная кома, отравление снотворными препаратами и окисью углерода), препарат назначают в количестве 50-100 мг. При асфиксии новорожденных препарат вводят в пупочную вену на протяжении первых двух минут после рождения в дозе 10 мг. При бронхиальной астме препарат назначают внутримышечно 2 раза в день в дозе 5-10 мг на инъекцию. Курс лечения продолжается от 14 до 25 дней в зависимости от тяжести гипоксии.
Условия хранения
В сухом, защищенном от света месте, при температуре не выше 8 C.
Срок годности
2 года.
Описание
Лиофилизированный порошок или пористая масса, уплотненная в таблетку, розовато-коричневого цвета.
Условия отпуска из аптек
По рецепту
Лекарственная форма
Лиофилизат для приготовления раствора для внутривенного и внутримышечного введения
Производитель и организация, принимающие претензии потребителей
САМСОН-МЕД, ООО
Фармакодинамика
Метаболическое средство, оказывает антигипокситическое, трофическое действие, стимулирует процессы регенерации. Является катализатором клеточного дыхания. Механизм действия препарата связан с наличием в простетической группе железа, способного переходить из окисленного состояния в восстановленное. В результате ускоряются эндогенные окислительно-восстановительные реакции и обменные процессы в тканях, улучшается утилизация кислорода и снижается гипоксия тканей при различных патологических состояниях.
Побочные действия
Озноб, гипертермия (при быстром введении в вену).
Взаимодействие
Не описано.
Отзывы о Цитохроме С
Отзывов об этом препарате нет, поскольку он используется в комплексном лечении гипоксических состояний или для предупреждения их. Поэтому сделать вывод об эффективности этого препарата не представляется возможным. Можно только доверять экспериментально-клиническим исследованиям. Так, например, это ЛС включалось в интенсивную терапию послеоперационного периода пациентам, перенесшим протезирования клапанов сердца. Инфузию препарат в дозе 0,5 г/кг проводили перед операцией и повторно сразу после операции. Был сделан вывод о его антигипоксической и противоишемшеской эффективности. Он повышает возможности сердечной мышцы в условиях ишемии, улучшает коронарный кровоток и сократительную функцию. Он оказался эффективным кардиопротектором в хирургии «открытого сердца».
Неоднократно изучался опыт применения этого препарата в остром периоде инфаркта миокарда. Хорошие результаты имеются при внутривенном введении этого препарата (даже разовом) в дозе 50-100 мг при отравлении окисью углерода.
Антиоксидантные свойства препарата используются при комплексном лечении диабетической нейропатии, для нормализации газообмена в системе «мать-плод» при фетоплацентарной недостаточности.
Цитохром Р450 (изоферменты CYP2C19 и CYP3A4)
Цитохром Р450
(CYP450) — большая группа ферментов, отвечающая за метаболизм чужеродных органических соединений и лекарственных препаратов. Ферменты семейства цитохрома Р450 осуществляют окислительную биотрансформацию лекарственных препаратов и ряда других эндогенных биоорганических веществ и, таким образом, выполняющих дезинтоксикационную функцию. С участием цитохромов происходит метаболизм многих классов лекарственных средств, таких как ингибиторы протонной помпы, антигистаминные препараты, ингибиторы ретровирусной протеазы, бензодиазепины, блокаторы кальциевых каналов и другие. Цитохром Р450 представляет комплекс белка с ковалентно связанным гемом (металлопротеином), обеспечивающим присоединение кислорода. Гем, в свою очередь, является комплексом протопорфирина IX и двувалентного атома железа. Число 450 обозначает, что восстановленный гем, связанный с СО, отличается максимумом поглощения света при длине волны 450 нм.
Цитохромы Р-450 участвуют не только в метаболизме лекарств, но и в превращении гемоглобина в билирубин, синтезе стероидов и др. Все изоформы цитохрома Р-450 объединены в семейства CYP1, CYP2, CYP3. Внутри семейств выделены подсемейства A, B, C, D, E. В пределах подсемейств изоформы обозначены порядковым номером. Например, CYP2C19 — наименование 19-го по порядку цитохрома подсемейства «С», семейства «2». Всего существует около 250 различных видов цитохрома Р-450, из них примерно 50 — в организме человека и только шесть из них (CYP1A2, CYP2C9, CYP2C19, CYP2D6, CYP2E1, CYP3A4) имеют отношение к метаболизму лекарств.
На активность цитохромов Р-450 оказывает влияние множество факторов — курение, алкоголь, возраст, генетика, питание, болезни. Эти факторы отвечают за формирование индивидуальных особенностей работы ферментов Р-450 и определяют эффекты лекарственного взаимодействия у конкретного пациента.
Важность цитохромов Р450 для гастроэнтерологии
Значительно возросший в последнее время интерес гастроэнтерологов к изоформам цитохрома Р450 CYP2C19 и CYP3A4 обусловлен в их ролью в метаболизме производных бензимидазола, к которым относятся все лекарственные препараты из группы по АТХ A02BC «Ингибиторы протонового насоса» (омепразол, панторазол, лансопразол, рабепразол и эзомепразол). Клинически существенно, что ген CYP2C19 отличается полиморфностью и от состояния этого гена у пациента в значительной степени зависит величина терапевтического эффекта различных ИПП.
Среди ИПП наибольшее ингибирующее действие в отношении CYP2C19 проявляет лансопразол, в меньшей степени омепразол и эзомепразол. Еще ниже эффект рабепразола, однако значительное ингибирующее воздействие на активность CYP2C19 оказывает его тиоэфир, образующийся в ходе неферментного метаболизма. Наименьшее влияние на CYP2C19 оказывает пантопразол. Наибольшее ингибирующее воздействие на CYP3A4 in vitro у пантопразола, далее (по мере уменьшения эффекта) омепразол, эзомепразол и рабепразол и лансопразол. Для пациентов, получающих несколько лекарственных препаратов, из ИПП предпочтительнее пантопразол (Бордин Д.С.).
Метаболизм пяти ингибиторов протонного насоса. Более темные стрелки обозначают более значимые пути метаболизма. Рисунок взят из статьи Marelli S., Pace F.
При активном участии CYP3A4 происходит метаболизм домперидона, цизаприда и большого числа других лекарств.
Целый ряд гастроэнтерологических препаратов ингибируют цитохром CYP3A4, оказывая тем самым влияние на фармакокинетику принимаемых совместно лекарств.
Проблема взаимодействия лекарств
В современной клинической практике широко распространено комбинированное применение лекарств, что связано с наличием у пациента нескольких заболеваний или недостаточной эффективностью монотерапии. При комбинированной терапии возможно взаимодействие лекарств. Более одного лекарства принимает примерно 56 % пациентов в возрасте до 65 лет и 73 % пациентов старше 65 лет. Прием двух лекарств приводит к их взаимодействию у 6 % пациентов. Назначение 5 (или 10) лекарств повышает частоту взаимодействий до 50 (или 100) %.
Потенциально опасные комбинации лекарств являются серьезной клинической проблемой. Имеются данные, что от 17 до 23 % назначаемых врачами комбинаций лекарств являются потенциально опасными. Только в США из-за непредусмотренного взаимодействия лекарств умирает 48 тысяч больных в год. FDA сняло с регистрации несколько лекарств (в том числе прокинетик цизаприд) по причине их потенциально опасных взаимодействий с другими лекарствами, приводивших, в том числе и к летальным исходам.
Основные механизмы взаимодействий лекарств связаны с изменением их фармакокинетики или фармакодинамики. Наиболее существенными, согласно современным представлениям, являются изменения фармакокинетики при метаболизме лекарств с участием цитохромов Р-450.
Примером опасного взаимодействия является недавно обнаруженное взаимодействие ИПП и клопидогрела, широко применяемого при лечении больных ишемической болезнью сердца. Для уменьшения риска гастроинтестинальных осложнений больным, получающим ацетилсалициловую кислоту в комбинации с клопидогрелом, назначают ИПП. Поскольку биоактивация клопидогрела происходит с участием CYP2C19, прием ИПП, метаболизируемых этим цитохромом, может снизить активацию и антиагрегантный эффект клопидогрела. В мае 2009 года на конференции Общества сердечно-сосудистой ангиографии и вмешательств (SCAI) были представлены данные, свидетельствующие, что одновременное использование клопидогрела и ИПП значительно повышает риск возникновения инфаркта миокарда, инсульта, нестабильной стенокардии, необходимости повторных коронарных вмешательств и коронарной смерти (Бордин Д.С.).
Цитохром CYP2C19
Изоформа цитохрома Р450 CYP2C19 (S-мефенитоин гидроксилаза) катализирует реакции 5-гидроксилирования пиридинового кольца и 5′-деметилирования в бензимидазольном кольце. В человеческом организме CYP2C19 располагается в гепатоцитах.
Все типы мутаций гена CYP2C19 могут быть были разделены на три группы:
- Без мутаций (гомозиготы), они же быстрые метаболайзеры ИПП.
- Имеющие мутацию в одной аллели (гетерозиготы), промежуточный тип метаболизма.
- Имеющие мутации в обеих аллелях, они же медленные метаболайзеры ИПП.
Распространенность генотипов CYP2C19, тип метаболизма и эффект ИПП при лечении кислотозависимых заболеваний даны в таблице:
| Генотип CYP2C19 | Распростра-ненность (Ткач С.М. и др., 2006) | Российская популяция (Никонов Е.Л.) | Тип метаболизма | Период полувыведения ИПП , T½, час (Лапина Т.Л.) | Кислото-ингиби-рующий эффект ИПП | |
| европеоидная раса | монголоидная раса | |||||
| Без мутаций (гомозиготы) | 90 % европеоидной популяции | 50,6 % | 34,0 % | Быстрый | 1 | Низкий |
| Мутация в 1-й аллеи (гетерозиготы) | 10 % европеоидной популяции | 40,5 % | 47,6 % | Промежуточный | — | Средний |
| Мутация в обеих аллеях | 20-30 % азиатской популяции | 3,3 % | 18,4 % | Медленный | 2–10 | Высокий |
Медленные метаболизаторы от быстрых и промежуточных отличаются двукратно более высокими концентрацией ИПП в плазме крови и периодом полувыведения. Полиморфизм гена, кодирующего изоформу 2С19, определяет различную скорость метаболизма ИПП у пациентов. В связи с вышесказанным подбор ИПП рекомендуется проводить под контролем суточной рН-метрии
(Хавкин А.И., Жихарева Н.С., Дроздовская Н.В.).
- CYP2C19 активно метаболизирует следующие лекарства: трициклические антидепрессанты (амитриптилин, кломипрамин, имипрамин), антидепрессант — селективный ингибитор обратного захвата серотонина циталопрам, антидепрессант — ингибитор МАО моклобемид, антиконвульсионные и антиэпелиптические средства (диазепам, примидон, фенитоин, фенобарбитал, нордазепам), ингибиторы протонной помпы (омепразол, панторазол, лансопразол, рабепразол и эзомепразол), противомалярийное средство прогуанил, НПВП диклофенак и индометацин, а также: варфарин, гликлазид, клопидогрел, пропранолол, циклофосфамид, нелфинавир, прогестерон, тенипозид, тетрагидроканнабинол, каризопродол, вориконазол и другие
- сильные ингибиторы CYP2C19: моклобемид, флувоксамин, хлорамфеникол (левомицетин)
- неспецифические ингибиторы CYP2C19: ИПП омепразол и лансопразол, Н2-блокатор циметидин, НПВП индометацин, а также флуоксетин, фелбамат, кетоконазол, модафинил, окскарбазепин, пробенецид, тиклопидин, топирамат
- индукторы CYP2C19: рифампицин, артемизинин, карбамазепин, норэтистерон, преднизон, зверобой.
Влияние различных генотипов CYP2C19 на эффективность эрадикации Helicobacter pylori
У пациентов с генотипом «быстрых» метаболизаторов отмечается быстрый метаболизм ингибиторов протонной помпы, следовательно, антисекреторный эффект от приема последних имеет у них меньшую выраженность, чем у лиц с фенотипами «промежуточных» и «медленных» метаболизаторов. Разница в антисекреторном эффекте может определить более низкий уровень эрадикации Helicobacter pylori
у «быстрых» метаболизаторов. Таким образом, имеет место более высокая эффективность эрадикационной терапии у пациентов с генотипами «медленных» (88,9%) и «промежуточных» (82,7%) метаболизаторов выше по сравнению с «быстрыми» (см. рисунок).
Влияние различных генотипов CYP2C19 на эффективность эрадикации Helicobacter pylori. БМ – «быстрые» метаболизаторы, ПМ – «промежуточные» метаболизаторы, ММ – «медленные» метаболизаторы (Маев И.В. и др.)
В силу того, что молекулярно-генетические исследования малодоступны практикующему врачу, заподозрить «быстрых» метаболизаторов можно ориентируясь на сохранение болевого абдоминального синдрома на 3–4-е сутки от начала приёма ИПП, а также принимая во внимание медленную эндоскопическую динамику при эпителизации эрозий и рубцевании язвенных дефектов у пациента. В свою очередь, недостаточность антисекреторного эффекта от терапии с применением ИПП можно верифицировать методом суточной внутрижелудочной рН-метрии (Маев И.В. и др.).
Цитохром CYP3A4
Фермент CYP3A4 катализирует реакцию сульфоксидирования, приводящую к образованию сульфогруппы. CYP3A4 является одним из самых важных для фармацевтики цитохромов, так как им биотрансформируется, по крайней мере, частично, около 60 % окисляемых препаратов. Хотя активность CYP3А4 широко варьирует, он не подвержен генетическому полиморфизму. Расположение CYP3А4 на апикальных мембранах энтероцитов тонкой кишки и гепатоцитах облегчает исполнение им метаболизм лекарств, предшествующий попаданию вещества в системный кровоток, что известно, как «эффект первого прохождения».
Генетический дефект CYP3A4 может быть причиной развития вторичного синдрома удлиненного интервала Q-T при приёме цизаприда и, как следствие, развития сердечной артимии (Хавкин А.И. и др.).
- CYP3A4 является основным ферментом при метаболизме следующих лекарств: имуннодепрессанты (циклоспорин, сиролимус, такролимус), средства, применяемые при химиотерапии (анастрозол, циклофосфамид, доцетаксел, эрлотиниб, тирфостин, этопозид, ифосфамид, паклитаксел, тамоксифен, тенипозид, винбластин, виндезин, гефитиниб), противогрибковые средства (клотримазол, кетоконазол, итраконазол), макролиды (кларитромицин, эритромицин), трициклические антидепрессанты (амитриптилин, кломипрамин, имипрамин), антидепрессанты — селективные ингибиторы обратного захвата серотонина (циталопрам, эсциталопрам, флуоксетин, сертралин), антипсихотики (арипипразол, галоперидол, зипрасидон, рисперидон), опиоидные анальгетики (альфентанил, кодеин, метадон, фентанил), бензодиазепины (алпразолам, клоназепам, мидазолам, флунитразепам), гиполипидемические статины (аторвастатин, ловастатин, симвастатин), блокаторы кальциевых каналов (амлодипин, верапамил, дилтиазем, нифедипин, фелодипин), половые гормоны (левоноргестрел, мифепристон, тестостерон, эстрадиол, этинилэстрадиол, финастерид), а также амиодарон, буспирон, венлафаксин, силденафил и другие
- CYP3A4 также принимает участие (но не является основным ферментом) в метаболизме ИПП (омепразол и эзомепразол), цизаприда и многих других лекарств
- сильные ингибиторы CYP3A4: ингибиторы ВИЧ-протеаз (индинавир, нелфинавир, ритонавир), антибиотики-макролиды (кларитромицин, телитромицин, эритромицин), компоненты сока грейпфрута (бергамоттин), противогрибковые средства (итраконазол, кетоконазол, флуконазол, а также апрепитант, кверцетин, нефазодон и другие
- ингибиторы CYP3A4: Н2-блокатор циметидин, обезболивающее бупренорфин, компонент кофе кофестол и многие другие
- индукторы CYP3A4: антиконвульсанты и нормотимики (карбамазепин, окскарбазепин, фенитоин), компонент зверобоя гиперфорин, а также кипротерон, модафинил, невирапин, рифампицин, фенобарбитал, этравирин, эфавиренз и многие другие.
Материалы для профессионалов здравоохранения, рассматривающие роль CYP2C19 и CYP3A4 и их генотипов при терапии органов ЖКТ
Видео
Кадр из видео: Эмбутниекс Ю.В. Принципы ведения пациентов с рефрактерной формой ГЭРБ
Кадр из видео: Карева Е.Н. Могут ли генетические особенности пациента быть причиной рефрактерной ГЭРБ? Фармакогенетическое управление эффективностью ИПП
На сайте GastroScan.ru в разделе «Видео» имеются подраздел для пациентов «Популярная гастроэнтерология» и подраздел «Для врачей», содержащий видеозаписи докладов, лекций, вебинаров по различным направлениям гастроэнтерологии для профессионалов здравоохранения.
Статьи и авторефераты
- Никонов Е.Л. Клинико-патогенетические особенности различных видов антисекреторной терапии у больных кислото-зависимыми заболеваниями. Автореферат диссертации на соискание ученой степени д.м.н. Москва, 2004.
- Морозов С.В., Цодикова О.М., Исаков В.А., Гущин А.Е., Шипулин Г.А. Сравнительная эффективность антисекреторного действия рабепразола и эзомепразола у лиц, быстро метаболизирующих ингибиторы протонного насоса. // Экспериментальная и клиническая гастроэнтерология. — 2003. — №6.
- Исаков В.А. Безопасность ингибиторов протонного насоса при длительном применении // Клиническая фармакология и терапия. – 2004. – №13(1).
- Пасечников В.Д. Ключи к выбору оптимального ингибитора протонной помпы для терапии кислотозависимых заболеваний // РЖГГК. – №3. – 2004.
- Бордин Д.С. Безопасность лечения как критерий выбора ингибитора протонной помпы больному гастроэзофагеальной рефлюксной болезнью // Consilium Medicum. – 2010. – Том 12. – № 8.
- Лебедева Е.Г., Маев И.В., Белый П.А. Влияние полиморфизма гена CYP2C19 на эффективность использования ингибиторов протонной помпы в лечении гастроэзофагеальной рефлюксной болезни // Лечащий Врач. № 7. 2011.
- Юренев Г.Л., Казюлин А.Н., Юренева-Тхоржевская Т.В. Влияние кислотосупрессивной терапии на клиническое течение ишемической болезни сердца с рефрактерным болевым синдромом в грудной клетке // Терапия. 2015. №2(2).
- Карева Е.Н. Рабепразол через призму «метаболизм — эффективность» // РМЖ. 2016. октябрь.
- Леонова М.В. Генетический полиморфизм CYP2C19 – предиктор клинической эффективности ингибиторов протонной помпы // Лечебное дело. – 2015. №4. С. 30-39.
- Белый П.А. Влияние полиморфизма гена CYP2C19 на эффективность использования ингибиторов протонной помпы в лечении гастроэзофагеальной рефлюксной болезни. Автореф. дисс. к.м.н., 14.01.04 — внутренние болезни. Москва, 2011.
На сайте GastroScan.ru в разделе «Литература» имеется подраздел «Ингибиторы протонной помпы», содержащий публикации для профессионалов здравоохранения, обсуждающие, в том числе, метаболизм ИПП с участием цитохромов Р450 CYP2C19 и CYP3A4. Назад в раздел
Цена Цитохрома С, где купить
Купить можно практически во всех аптеках городов России. Стоимость 5 ампул лиофилизата в аптеках Москвы составляет 1171-1135 руб., раствора — 1130-1135 руб.
- Интернет-аптеки РоссииРоссия
ЗдравСити
- Цитохром С лиоф. пригот. р-ра в/в и в/м введ. фл. 10мг 5штООО Самсон-Мед
1713 руб.заказать