Определение эндометриоза как процесса, при котором за пределами полости матки происходит доброкачественное разрастание ткани, по морфологическим и функциональным свойствам подобной эндометрию, сохраняется неизменным на протяжении последнего столетия. Вопросы лечения эндометриоза остаются нерешенной научной проблемой и являются предметом клинических исследований во многих странах мира [1, 2].
Наиболее важными клиническими симптомами эндометриоза, определяющими показания к лечению, являются тазовые боли, нарушение нормальных менструальных кровопотерь, бесплодие, расстройства функции тазовых органов. Степень выраженности и набор проявлений болезни индивидуально варьируют. Характерные для аденомиоза (эндометриоза тела матки) симптомы — менометроррагия и перименструальные кровянистые выделения обусловлены как циклическими превращениями эктопического эндометрия, так и нарушением сократительной функции матки. Тазовые боли, как правило, усиливающиеся накануне и во время менструации, типичны как для наружного эндометриоза, так и для аденомиоза. Другим симптомом, cвойственным эндометриозу (при отсутствии иных видимых причин), является бесплодие, сопутствующее этой патологии в 46—50% случаев [3, 4]. Сравнение эффективности методов диагностики позволило определить, что ультразвуковое исследование (УЗИ) является оптимальным и общедоступным диагностическим методом в алгоритме обследования больных с различными формами эндометриоза [5, 6].
Бесспорно в настоящее время положение — невозможность ликвидации анатомического субстрата эндометриоза ни одним из воздействий, кроме хирургического, после чего целесообразно проведение адъювантной гормональной терапии с целью предупреждения рецидива заболевания [3, 7, 8]. Однако, несмотря на бурное развитие и широкое внедрение в практику современных гормональных препаратов, добиться полного излечения этого заболевания не удается, но уменьшить выраженность таких тягостных симптомов, как кровотечение, боль, диспареуния, возможно, что, несомненно, повышает качество жизни и снижает риск гистерэктомии в репродуктивном возрасте [7, 8].
Обычно эндометриоз развивается на фоне относительной и абсолютной гиперэстрогении при дефиците прогестерона. Именно поэтому патогенетической основой гормональной терапии является временное угнетение функции яичников, т. е. уменьшение секреции эстрадиола — создание псевдоменопаузы за счет блокады гипофизарно-яичниковой системы с инициацией гипоэстрогении, приводящей к регрессу очагов эндометриоза [6, 9, 10]. Для гормональной терапии эндометриоза чаще всего применяют комбинированные синтетические эстроген-гестагенные препараты, прогестины, антигестагены, антигонадотропины, антиэстрогены, андрогены. Агонисты гонадотропин-рилизинг-гормона (аГнРг) в настоящее время являются наиболее эффективными препаратами для лечения больных с эндометриозом позднего репродуктивного возраста в послеоперационном периоде [7—11].
Цельнастоящего исследования — изучение эффективности и безопасности препарата «Бусерелин-лонг ФС» в дозе 3,75 мг, лиофилизата для приготовления суспензии для внутримышечного введения пролонгированного действия, производства ЗАО «Ф-Синтез», Россия, у пациенток позднего репродуктивного возраста с эндометриозом матки. Этот препарат является синтетическим аналогом эндогенного ГнРГ, он конкурентно связывается с рецепторами клеток передней доли гипофиза, вызывая кратковременное повышение уровня половых гормонов в плазме крови, в дальнейшем приводит к полной обратимой блокаде гонадотропной функции гипофиза, ингибируя, таким образом, выделение ЛГ и ФСГ. В результате наблюдается подавление синтеза половых гормонов в гонадах, что проявляется снижением концентрации эстрадиола в плазме крови до постклимактерических значений. После первого введения бусерелина к 21-му дню у женщин концентрация эстрадиола снижается до уровня, соответствующего овариэктомии или постменопаузе. Концентрация тестостерона и эстрадиола сохраняется сниженной в течение всего периода лечения, проводимого каждые 28 дней, что приводит к торможению роста и обратному развитию очагов эндометриоза. После прекращения лечения восстанавливается физиологическая секреция гормонов.
Перед исследователями были поставлены следующие задачи:
— оценить уровень гормонов ЛГ, ФСГ, эстрадиола до лечения препаратом «Бусерелин-лонг ФС» и на фоне лечения;
— оценить эхографические данные при трансвагинальном ультразвуковом исследовании матки и придатков до лечения препаратом «Бусерелин-лонг ФС» и на фоне лечения;
— оценить состояние и патологические изменения эндометрия до и после лечения препаратом «Бусерелин-лонг ФС» с помощью аспирационной биопсии эндометрия;
— оценить безопасность применения препарата «Бусерелин-лонг ФС» в дозе 3,75 мг, лиофилизата пролонгированного действия производства , Россия.
Материал и методы
Клиническое исследование проводилось в 2012 г. на базе нескольких лечебных учреждений России, в том числе и в условиях гинекологического отделения Государственного бюджетного учреждения здравоохранения Московской области «Московский областной научно-исследовательский институт акушерства и гинекологии».
Протокол клинического исследования включал 50 пациенток в возрасте от 35 до 45 лет (средний возраст составлял 39,28±3,37 года) с уровнем фолликулостимулирующего гормона ≤15 мМЕ/мл в сыворотке крови в ранней фолликулярной фазе с диагнозом: эндометриоз матки I, II, III стадии, подтвержденный эхографически и гистероскопически, с миомой матки или без нее (включая 4 пациенток с субмукозной миомой матки размером более 3 см в периоде подготовки к резекции миоматозного узла), соответствовавших всем критериям включения и не имевших критериев исключения, высказавших согласие на включение в исследование и подписавших «Информированное согласие пациента». Обязательным условием было использование барьерных методов контрацепции в течение всего исследования.
Клиническое исследование включало период скрининга (отбора пациенток) и период исследования.
• Период скрининга (от начального визита до первого введения пациентке исследуемого препарата) включал 1—30 дней.
• Период исследования (с 1-го дня введения препарата, который соответствовал 2—5-му дню менструального цикла, следующего за периодом скрининга, до финального визита) включал 112—116 дней.
Пациентки, прошедшие скрининг и удовлетворявшие критериям включения и исключения, были включены в исследование. Лечение препаратом «Бусерелин-лонг ФС» начинали на 2—5-й день менструального цикла, следующего за периодом скрининга, и продолжали на протяжении 112—116 дней (всего 4 внутримышечных инъекции препарата с интервалом 28 дней).
Период скрининга (визит 0)
Информированное согласие на участие в клиническом исследовании у всех пациенток было получено до начала процедур скрининга. Каждая пациентка, согласившаяся принять участие в исследовании, лично подписывала и датировала в двух экземплярах «Информационный листок пациента» с формой информированного согласия. После подписания один экземпляр «Информационного листка пациента» с формой информированного согласия оставался в исследовательском центре, а один экземпляр выдавался на руки пациентке.
Оценка соответствия представляла собой совокупность оценок, выполняемых в течение 1—30 дней перед первым введением препарата, для определения возможности включения конкретной пациентки в исследование.
Исследователь проводил с пациенткой беседу, в ходе которой собирался медицинский анамнез и проводилась оценка соответствия критериям включения в исследование.
Осмотр перед последующим наблюдением эффективности и безопасности препарата (визит 5)
Осмотр перед последующим наблюдением эффективности и безопасности препарата выполнялся через 28—32 дня после последнего его введения (визит 4).
Цель этого осмотра — обеспечение благоприятного эффекта лечения пациенток и подтверждение того, что все параметры, определенные при оценке соответствия, сохранились в клинически допустимых пределах. При значениях, выходящих за пределы данного диапазона и имеющих клиническую значимость, наблюдение должно было осуществляться до достижения их нормализации или адекватного объяснения их изменений.
В периоде скрининга было установлено, что жизненно важные показатели, включая электрокардиограмму (ЭКГ), у всех участниц находились в пределах нормы. Рост колебался от 152 до 178 см и в среднем составлял 164,82±5,94 см, а масса тела — от 48 до 109 кг и в среднем составляла 66,93±13,16 кг. Также оценивались гемодинамические показатели. Средний показатель систолического артериального давления (САД) соответствовал 113,3±8,06 мм рт.ст., а сам показатель колебался от 90 до 125 мм рт.ст. Показатель диастолического артериального давления (ДАД) колебался от 60 до 85 мм рт.ст. (в среднем 70,34±7,56 мм рт.ст.). Частота сердечных сокращений (ЧСС) варьировала от 54 до 82 уд/мин (в среднем 70,38±6,17 уд/мин). Температура тела колебалась от 36 до 36,8 °С (в среднем 36,51±0,18 °С).
Также в период скрининга протоколом исследования было предусмотрено проведение гистероскопии с биопсией. Для некоторых пациенток по решению исследователя и согласованию со спонсором, гистероскопия с биопсией не проводились, так как диагноз «эндометриоз матки» был однозначно поставлен по результатам УЗИ и клинической картине и не вызывал сомнений, что позволило пациенткам избежать болезненной инвазивной процедуры.
Все пациентки, включенные в исследование, имели верифицированный диагноз: эндометриоз матки I, II, III стадии.
Среднее значение ФСГ варьировало от 6,28±3,39 мМЕ/мл, а сам показатель колебался от 1,9 до 15,44 мМЕ/мл. Одна пациентка, по согласованию со спонсором, была принята в исследование, несмотря на значение ФСГ 15,44 мМЕ/мл, так как незначительное отклонение исходного уровня ФСГ (менее 0,5 мМе/л) не повлияло на результаты исследования. Таким образом, 49 из 50 скринированных пациенток удовлетворяли критерию включения «Уровень ФСГ≤15 мМЕ/мл в сыворотке крови в ранней фолликулярной фазе».
Среднее значение ЛГ составляло 6,18±6,55 мМЕ/мл, а сам показатель колебался от 0,5 до 40 мМЕ/мл, эстрадиола — 461,6±352,9 пмоль/л, а сам показатель колебался от 69,75 до 1755 пмоль/л.
При УЗИ оценивалось значение срединного маточного эха (М-эхо), которое в среднем составляло 6,0±3,22 мм, сам показатель варьировал от 1,1 до 13 мм. У 100% пациенток бактериоскопические показатели влагалищного мазка находились в пределах нормы.
В большинстве случаев эндометриоз сочетался с другой гинекологической патологией, что было отмечено у 41 (82%) участницы, среди них: с миомой матки — 39 (78%); с доброкачественными заболеваниями яичников — 2 (4%). Среди всех обследованных бесплодием страдали 5 (10%), первичным — 3 (60%), вторичным — 2 (40%). У 7 (14%) из 50 пациенток в анамнезе отмечались самопроизвольные выкидыши и неразвивающиеся беременности, причем у 2 (4%) имело место привычное невынашивание.
Перед началом клинических исследований 35 пациенткам была произведена миомэктомия. Показаниями к выполнению оперативного лечения явились: быстрый рост опухоли — у 32 (64%) пациенток; атипичное расположение миоматозных узлов — у 25 (50%); большие и гигантские размеры узлов в сочетании с симптомом сдавления смежных органов и нарушением их функции — у 6 (12%) и болевым симптомом — у 29 (58%); с симптомом кровотечения, приводящим к анемизации, — у 34 (68%) больных.
Досрочно прекратила участие в исследовании 1 пациентка, которая отозвала согласиепо личным причинам, не связанным с применением препарата. В ходе проведения клинического исследования не было зарегистрировано ни одного серьезного нежелательного явления, связанного с применением препарата.
Результаты и обсуждение
Перечень параметров эффективности
Протоколом были предусмотрены следующие критерии эффективности:
1. Исследования уровня гормонов в крови:
— снижение уровня ЛГ до 7,4±7,3 мМЕ/мл;
— снижение уровня ФСГ до 7,0±5,6 мМЕ/мл;
— снижение уровня эстрадиола <110 пмоль/л.
2. Инструментальные исследования:
— трансвагинальное ультразвуковое исследование матки и придатков — уменьшение толщины срединного маточного эха до 4—6 мм. Изменения патологических структур миометрия при различных степенях аденомиоза на фоне лечения;
— аспирационная биопсия эндометрия — изменение патологических структур в эндометрии или атрофия эндометрия.
3. Оценка состояния здоровья при помощи «Вопросника пациента» — оценка жалоб, общего состояния, эмоционального состояния, физического состояния, симптомов менопаузы.
Динамика уровня ЛГ
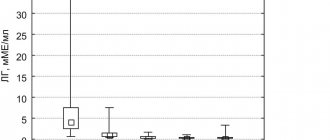
. При визите в период скрининга, а также при визитах 2—5 проводился анализ крови пациенток для определения уровня ЛГ (рис. 1).
Рис. 1.Динамика уровня ЛГ на фоне применения препарата «Бусерелин-лонг ФС».
Достижение целевого уровня ЛГ<7,4±7,3 мМЕ/мл было у 100% пациенток уже к визиту 2 после начала терапии препаратом «Бусерелин-лонг ФС».
К визиту 5 наблюдалось снижение уровня ЛГ у всех пациенток в среднем более чем в 6 раз по отношению к визиту в период скрининга.
Таким образом, 50 (100%) из 50 пациенток удовлетворяли критерию эффективности «Снижение уровня ЛГ до 7,4±7,3 мМЕ/мл».
Динамика уровня ФСГ
. При визите в период скрининга, а также при визитах 2—5 проводился анализ крови пациенток для определения уровня ФСГ.
При анализе уровня ФСГ на фоне терапии препаратом «Бусерелин-лонг ФС» (рис. 2) выявлено статистически значимое снижение уровня данного гормона к визитам 2, 3, 4 и 5.
Рис. 2.Динамика уровня ФСГ на фоне применения препарата «Бусерелин-лонг ФС».
Таким образом, популяция пациенток (n
=50) в целом удовлетворяла критерию «Снижение уровня ФСГ до 7,0±5,6 мМЕ/мл»: среднее значение уровня ФСГ у пациенток к визиту 5 составляло 4,54±2,5 мМЕ/мл. Понижение уровня ФСГ к визиту 5 наблюдалось у 33 (66%) из 50 пациенток. Поскольку, исходя из литературных данных, терапия аналогами ГнРГ не всегда приводит к понижению уровня ФСГ у пациенток с эндометриозом, при представлении заключения об эффективности препарата следует учитывать и другие параметры эффективности.
Динамика уровня эстрадиола
. При визите в период скрининга, а также при визитах 2—5 проводился анализ крови пациенток для определения уровня эстрадиола.
Уже к визиту 2 было зарегистрировано статистически значимое снижение уровня эстрадиола, стойко сохранявшееся в течение всего курса терапии (рис. 3).
Рис. 3.Динамика уровня эстрадиола на фоне применения препарата «Бусерелин-лонг ФС».
Из 50 пациенток 32 (64%) достигли целевого уровня эстрадиола ≤110 пмоль/л. В исследовании U. Cirkel и соавт. [12] уровень эстрадиола у пациенток с эндометриозом, получавших терапию бусерелином, уменьшался в среднем до 164±32 пмоль/л после 3 мес лечения, а в исследовании W. Dmowski и соавт. [13] — до 132±18 пмоль/л, что несколько выше показателя в 110 пмоль/л, выбранного в качестве конечной точки в настоящем исследовании.
У 4 пациенток выявлено значимое увеличение уровня эстрадиола к визиту 5, при значимом уменьшении его уровней к визитам 3—4. У 1 пациентки не выявлено значимого повышения/понижения уровня эстрадиола к визиту 5, при значимом уменьшении его уровня к визитам 3—4. Причиной могло быть отклонение в дате проведения визита 5 или так называемый «ребаунд-эффект», когда вскоре после отмены применения аГнРГ наблюдается кратковременное значительное повышение концентрации половых гормонов.
Таким образом, 32 (64%) из 50 пациенток удовлетворяли критерию эффективности «Снижение уровня эстрадиола ≤110 пмоль/л». В целом для 45 (90%) пациенток из 50 лечение препаратом «Бусерелин-лонг ФС» явилось эффективным по показателю снижения уровня эстрадиола, исходя из значимого снижения уровня эстрадиола по отношению к исходному уровню.
Параметры М-эха
. При визите в период скрининга, а также при визитах 2—5 проводилось трансвагинальное ультразвуковое исследование матки и придатков для выявления изменений патологических структур миометрия при различных степенях эндометриоза на фоне лечения.
На фоне лечения препаратом «Бусерелин-лонг ФС» уже к визиту 2 наблюдалось статистически значимое уменьшение толщины эндометрия (рис. 4).
Рис. 4.Изменение толщины эндометрия на фоне терапии препаратом «Бусерелин-лонг ФС».
Таким образом, 49 (98%) из 50 пациенток удовлетворяли критерию эффективности «Уменьшение толщины срединного маточного эха до 4—6 мм».
Результаты проведения аспирационной биопсии эндометрия
. Для выявления изменений в эндометрии или атрофии эндометрия на фоне лечения препаратом «Бусерелин-лонг ФС» при визите в период скрининга и при визите 5 у пациенток проводилась биопсия эндометрия. По результатам проведенной аспирационной биопсии, у 33 пациенток из 50 при визите 5 можно заключить, что у большинства пациенток — 29 (88%) из 33 — наблюдалась атрофия эндометрия либо снижение степени гиперплазии эндометрия при визите 5 по отношению к визиту в период скрининга.
Данные опроса пациенток.
При каждом визите, в том числе визите в период скрининга, пациентки заполняли вопросник. Вопросник состоял из нескольких вопросов, часть которых позволяла оценить изменения в субъективном восприятии болевых симптомов, в физическом и эмоциональном состоянии собственного здоровья пациентками («1. Как бы Вы оценили состояние Вашего здоровья?», «2. Как бы Вы оценили состояние своего здоровья сейчас по сравнению с тем, что было 4 нед назад?», «3.1. В какой степени состояние Вашего здоровья ограничивает Вас в выполнении тяжелых физических нагрузок (поднятие и перенос тяжестей, бег, подъем по лестнице на несколько пролетов, ходьба на несколько километров)?», «3.2. В какой степени состояние Вашего здоровья ограничивает Вас в выполнении умеренных физических нагрузок (подъем по лестнице на один пролет, ходьба на несколько сотен метров, самостоятельно пропылесосить или вымыть пол)?», «3.3. В какой степени состояние Вашего здоровья ограничивает Вас в выполнении легких физических нагрузок (пройти 100 м, вытереть пыль, одеться)?», «4. Как бы Вы оценили свое физическое состояние сейчас по сравнению с тем, что было 4 нед назад?», «5. Как бы Вы оценили свое эмоциональное состояние по сравнению с тем, что было 4 нед назад?», «6. Насколько сильную физическую боль Вы испытывали в течение последних 4 нед?»). Пациентки могли выбрать только один вариант ответа на каждый вопрос.
Бусерелин Депо или Лонг – что лучше?
Производитель – основной пункт, в чем различаются между собой Бусерелин Лонг и Депо. Производитель Бусерелин-депо закупает действующее вещество в Китае, а на территории РФ просто расфасовывает его. Для Бусерелин-лонг все создается в собственной лаборатории, нигде не закупается. С клинической точки зрения, разницы практически нет – оба препарата будут работать и окажут свой эффект. Какому препарату отдать предпочтение зависит сугубо от лечащего врача и пациента: кому-то хочется сэкономить, кто-то не доверяет китайским производителям или желает поддерживать отечественные компании. Во всем остальном оба препарата полностью аналогичны.