Фармакологические свойства препарата Инсулин детемир
Современные рекомбинантные ДНК-технологии позволили улучшить профиль действия простого (регулярного) инсулина. Инсулин детемир производится методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae, является растворимым базальным аналогом человеческого инсулина пролонгированного действия с беспиковым профилем действия. Профиль действия значительно менее вариабелен по сравнению с изофан-инсулином и инсулином гларгин. Пролонгированное действие обусловлено выраженной самоассоциацией молекул инсулина детемир в месте инъекции и связыванием молекул с альбумином посредством соединения с боковой жирно-кислотной цепью. Инсулин детемир по сравнению с изофан-инсулином в периферических тканях-мишенях распределяется медленнее. Эти комбинированные механизмы замедленного распределения обеспечивают более воспроизводимый профиль абсорбции и действия инсулина детемир. Инсулин детемир характеризуется значительно большей интраиндивидуальной предсказуемостью действия у пациентов по сравнению с инсулином НПХ или инсулином гларгин. Указанная предсказуемость действия обусловлена двумя факторами: инсулин детемир остается в растворенном состоянии на всех этапах от его лекарственной формы и до связывания с инсулиновым рецептором и буферным эффектом связывания с альбумином сыворотки крови. Путем взаимодействия со специфическим рецептором внешней цитоплазматической мембраны клеток, образует инсулин-рецепторный комплекс, стимулирующий внутриклеточные процессы, в том числе синтез ряда ключевых ферментов (гексокиназа, пируваткиназа, гликогенсинтетаза и др.). Снижение содержания глюкозы в крови обусловлено повышением ее внутриклеточного транспорта, усилением усвоения тканями, стимуляцией липогенеза, гликогеногенеза, снижением скорости продукции глюкозы печенью и др. Для доз 0,2–0,4 ЕД/кг 50% максимальный эффект наступает в интервале от 3–4 ч до 14 ч после введения. После подкожного введения наблюдался фармакодинамический ответ, пропорциональный введенной дозе (максимальный эффект, продолжительность действия, общий эффект). После п/к инъекции детемир связывается с альбумином через свою жирнокислотную цепь. Тем самым в состоянии устойчивого действия концентрация свободного несвязанного инсулина значительно уменьшается, что приводит с стабильному уровню гликемии. Продолжительность действия детемира в дозе 0,4 ЕД/кг — около 20 ч, поэтому препарат назначается дважды в сутки для большинства пациентов. В долгосрочных исследованиях (6 мес) показатель уровня глюкозы в плазме крови натощак у пациентов с сахарным диабетом I типа был лучше по сравнению с изофан-инсулином, назначаемым в базис/болюсной терапии. Гликемический контроль (гликозилированный гемоглобин — HbA1c) на фоне терапии инсулин детемиром был сравним с таковым при лечении изофан-инсулином, с более низким риском развития ночной гипогликемии и отсутствием увеличения массы тела на фоне его применения. Профиль ночного контроля глюкозы является более плоским и ровным у инсулина детемир по сравнению с изофан-инсулином, что отражается в более низком риске развития ночной гипогликемии. Максимальная концентрация инсулина детемир в сыворотке крови достигается через 6–8 ч после введения. При двукратном ежедневном режиме введения устойчивые концентрации препарата в сыворотке крови достигаются после 2–3 введений. Инактивация сходна с таковой у препаратов человеческого инсулина; все образующиеся метаболиты являются неактивными. Результаты исследований связывания белков in vitro и in vivo показывают отсутствие клинически значимых взаимодействий между инсулином детемир и жирными кислотами или другими препаратами, связывающимися с белками крови. Период полувыведения после п/к инъекции определяется степенью всасывания из подкожной ткани и составляет 5–7 ч в зависимости от дозы. При п/к введении концентрации в сыворотке крови были пропорциональны введенной дозе (максимальная концентрация, степень всасывания). Особые группы пациентов Фармакокинетические свойства были исследованы у детей (6–12 лет) и подростков (13–17 лет) и сравнены со взрослыми с сахарным диабетом типа I. различий в фармакокинетических свойствах не выявлено. Клинически значимых различий в фармакокинетике инсулина детемир между пожилыми и молодыми пациентами, или между пациентами с нарушением функции почек и печени и здоровыми пациентами не выявлено.
Введение
В настоящее время для достижения компенсации пациентов с сахарным диабетом (СД) имеется полный арсенал лекарственных средств. Однако, несмотря на большое число групп препаратов для лечения диабета, самым эффективным («золотым») остается инсулин. Его открытие – одно из наиболее значимых событий в медицине и фармакологии, что подтверждается тремя нобелевскими премиями, присужденными за работу с молекулой инсулина. Совсем скоро медицинская общественность отметит 100-летний юбилей со дня создания этого уникального препарата.
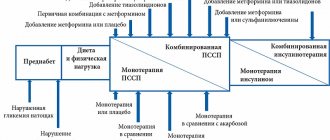
История инсулина – это история достижений медицины. Открытие инсулина определило кардинально новый подход к лечению СД. От момента открытия препарата до начала его промышленного производства и клинического использования прошло всего 2 года. Первая инъекция инсулина человеку была сделана 11 января 1922 г., им стал 14-летний подросток с СД 1 типа (СД1). С того момента началась грандиозная эра инсулиновой терапии. Можно выделить следующие значимые вехи в развитии инсулинотерапии: выделение инсулина в 1921 г., использование животного (бычьего) инсулина в 1922 г. (рис. 1), создание протамина-цинк-инсулина в 1936 г., нейтрального протамина Хагедорна в 1946 г. и инсулина Ленте в 1952 г., использование рекомбинантных технологий для синтеза генно-инженерных человеческих инсулинов в 1977 г. [1–3]. Появление технологии рекомбинантной ДНК в 1980-х гг. позволило изменить молекулярную структуру инсулина и модифицировать те области взаимодействия лиганд-рецептор, которые оставались неизменными при использовании «человеческих инсулинов» [4]. Первое поколение базальных инсулинов было достаточно далеко от физиологического профиля инсулина. Фармакокинетический профиль инсулина НПХ (нейтральный протамин Хагедорна) достигал максимума через 6–10 часов после инъекции с последующим устойчивым его снижением [5]. Скорость абсорбции инсулина НПХ постоянно изменяется во времени и создает малопредсказуемые фармакокинетические профили, повышая риск развития гипогликемических эпизодов, прежде всего ночных гипогликемий [6]. Новой эрой в инсулинотерапии стала разработка в 1990-е гг. аналогов инсулина быстрого действия и базальных аналогов в начале 2000-х (рис. 2). Первым базальным аналогом стал инсулин гларгин, созданный в 2000 г., вслед за которым в 2005 г. был разработан инсулин детемир. Несмотря на значительный прогресс, достигнутый в понимании фармакокинетики, фармакодинамики и механизмов действия инсулина, до настоящего времени актуальными остаются вопросы, связанные с отсутствием полной имитации профиля эндогенного инсулина. Инсулины длительного действия – наиболее используемые препараты инсулина в клинической практике, что связано с массой пациентов с СД 2 типа (СД2) в популяции и необходимости назначения им инсулинотерапии через несколько лет от момента установления диагноза. Именно базальные инсулины становятся стартовыми при назначении инсулина пациентам с СД2 [7].
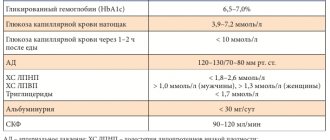
К основным целям терапии СД относятся достижение и поддержание целевых значений гликемии, необходимые для профилактики поздних осложнений диабета и низкого риска гипогликемий [8]. Результаты популяционных исследований свидетельствуют о том, что гипогликемии служат наиболее значимым фактором, препятствующим достижению адекватного гликемического контроля, и значительно ухудшают качество жизни пациентов [9]. Традиционные препараты человеческого инсулина имеют вариабельность абсорбции, значительные различия фармакодинамического эффекта, определяющие отсутствие достижения стабильного и продолжительного уровня инсулина плазмы. Вариабельность действия инсулинов вызывает значительные колебания гликемии и вероятность развития гипогликемических состояний.
С целью решения указанных проблем создан аналог инсулина длительного действия, обладающий рядом отличительных свойств и имеющий пролонгированный эффект, – инсулин детемир. Инсулин детемир (Левемир®) – нейтральный, растворимый базальный аналог человеческого инсулина пролонгированного действия с плоским профилем действия, который производится методом биотехнологии рекомбинантной ДНК с использованием штамма Saccharomyces cerevisiae. Инсулин детемир обеспечивает воспроизведение, близкое к базальному физиологическому инсулиновому профилю, что дает преимущества в виде более предсказуемого профиля действия по сравнению с инсулином НПХ [10]. Молекулярная структура инсулина детемир отличается от структуры человеческого инсулина отсутствием треонина в положении B30 и присоединением к лизину в положении B29 миристиновой кислоты (жирнокислотного остатка из 14 атомов углерода – С14; рис. 3). Такое строение молекулы позволило получить инсулиновый аналог, который остается в растворенном состоянии после произведенной инъекции. Молекулы инсулина детемир в готовом растворе соединены в гексамеры. При попадании инсулина детемир в интерстициальную жидкость подкожно-жировой клетчатки происходит самоассоциация гексамеров с формированием дигексамеров за счет контакта между цепями жирных кислот молекул инсулина [10], а также связывание гексамеров с альбумином. При дальнейшем разведении происходит распад гексамеров на димеры и мономеры, способные медленно проходить через стенку капилляра. Большинство мономеров (около 98%) быстро связываются с молекулами альбумина сыворотки крови. Свободные мономеры инсулина детемир выходят из циркуляции и достигают тканей-мишеней, в которых инсулин детемир связывается рецептором инсулина на мембране клеток-мишеней, что запускает сигнальный процесс как основной биологический эффект – передачу сигнала в клетки органов-мишеней [11, 12].
Инсулин детемир имеет широкое применение при СД1 и СД2 в комбинации с инсулинами короткого/ультракороткого действия, а также с представителями практически всех других групп неинсулиновых противодиабетических средств: детемир+метформин, детемир+препараты сульфанилмочевины/глиниды, детемир+иДПП-4, детемир+ингибиторы α-глюкозидазы, детемир+аГПП-1, детемир+иНГЛТ-2.
За период более 15 лет от начала использования инсулина Детемир накоплены масса наблюдений и значимый клинический опыт использования данного базального аналога инсулина.
Клиническая эффективность и безопасность инсулина детемир
Представленные данные мета-анализов и рандомизированных клинических исследований показали, что инсулин детемир имеет высокую клиническую эффективность во всех возрастных группах. Значимо я снижение у пациентов риска всех гипогликемических состояний, в т.ч. ночных, вне зависимости от типа СД и его длительности. Результаты всех проведенных клинических исследований подтверждают большую предсказуемость действия инсулина детемир по сравнению с инсулином НПХ. В международном наблюдательном исследовании PREDICTIVE™ 303 (n=5603) проведена оценка эффективности терапии инсулином детемир пациентов с СД2 с использованием упрощенного алгоритма самостоятельной титрации доз (A1) по сравнению со стандартным врачебным алгоритмом титрации (А2) в амбулаторных центрах первичной помощи в течение 6 месяцев [14]. Исследование показало, что у пациентов, переведенных с инсулина гларгин, уровень гликозилированного гемоглобина (HbA1c) снизился через 26 недель с 8,4 до 8,0% в группе титрации А1 и с 8,4 до 8,2% в группе А2 (р=0,052).
У пациентов, переведенных с терапии инсулином НПХ на таковой инсулином детемир, уровень HbA1c снизился с 8,2 до 8,0% в группе А1, с 8,3 до 8,2% в группе А2 (р=0,38). Средние суточные дозы инсулина детемир через 26 недель терапии составили 0,69 и 0,57 ЕД/кг в группах титрации А1 и А2 соответственно у пациентов, переведенных с терапии инсулином гларгин 100. В группе пациентов, получавших исходно инсулин НПХ, дозы составили 0,74 и 0,53 ЕД/кг в группах А1 и А2 соответственно. Оценка частоты гипогликемий (эпизод/пациент/месяц) показала снижение через 26 недель с 0,72 исходно до 0,56 в группе титрации А1, с 0,74 до 0,39 в группе А2 у пациентов, переведенных на терапию инсулином детемир с инсулина гларгин. В группе предшествовавшей терапии инсулином НПХ показано аналогичное снижение частоты гипогликемий. По результатам исследования у пациентов, переведенных с терапии базальным инсулином гларгин±ПССП (пероральные сахароснижающие препараты) или НПХ инсулин на терапию инсулином детемир в амбулаторных центрах первичной помощи, показано значительное улучшение гликемического контроля на фоне умеренного снижения массы тела и достоверного снижения риска гипогликемий [14].
Оценка эффективности и безопасности терапии инсулином детемир в условиях повседневной клинической практики (исследование PREDICTIVE™) 2377 пациентов Европейской когорты с СД2, ранее не получавших инсулин, с плохим гликемическим контролем на пероральной сахароснижающей терапии показала, что через 3 месяца после старта терапии инсулином детемир выявлено достоверное снижение уровня HbA1c и низкая частота развития гипогликемий без тяжелых эпизодов. Было отмечено более выраженное снижение массы тела пациентов, которым отменили предшествовавшую терапию препаратами сульфонилмочевины или тиазолидиндионами по сравнению с теми, кто продолжал пероральную терапию без изменений [15]. У пациентов с СД2 терапия инсулином детемир в сочетании с предшествовавшей терапией ПССП либо в результате замены предшествовавшего базального инсулина обеспечивала быстрое и значимое улучшение гликемического контроля, снижение риска гипогликемий и снижение массы тела [16].
Аналогичные результаты получены в исследовании PREDICTIVE™ у 682 пациентов с СД1 Европейской когорты (38% мужчин, средний возраст – 40,3 года, длительность диабета составила 19,7 года, индекс массы тела [ИМТ] – 25,3±4,1 кг/м2), получавших терапию инсулином детемир в качестве базального компонента базис-болюсного (ББ) режима терапии в течение 6 месяцев. Предшествовавшая терапия представлена инсулином гларгин в ББ-режиме терапии. За 29 недель наблюдения общая частота эпизодов гипогликемии снизилась с 67,3 пациенто-лет до 47,3 (p<0,0001). Было показано снижение частоты тяжелых и ночных эпизодов гипогликемии (до 2,0 и 9,0 пациенто-лет; p<0,0001 для обоих сравнений). Средний уровень HbA1c и интраиндивидуальная вариабельность гликемии натощак также достоверно снизились. У пациентов отмечено достоверное снижение средней массы тела, наиболее выраженное у пациентов с высоким ИМТ (29–31 кг/м2 [-1,7 кг], >31 кг/м2 [-2,0 кг]). Перевод на терапию инсулином детемир в ББ-режимах терапии пациентов, получавших терапию инсулином гларгин в ББ-режиме, обеспечивает улучшение гликемического контроля и снижение частоты гипогликемий с умеренным снижением массы тела [17]. Полученные данные исследования PREDICTIVE™ свидетельствуют: можно получить дополнительные преимущества в плане эффективности и безопасности терапии при замене базального инсулина гларгин на инсулин детемир в ББ-режимах терапии пациентов с СД1.
Однонаправленные изменения углеводного обмена были также получены в нескольких исследованиях пациентов с СД1. В открытом исследовании с параллельными группами (16 недель) 408 пациентов с СД1 были рандомизированы в группы терапии инсулином детемир либо инсулином НПХ [18]. В качестве болюсного инсулина пациенты получали ультракороткий аналог инсулина аспарт. HbA1c и уровень глюкозы плазмы натощак (ГПН) в динамике в группе терапии инсулином детемир были достоверно ниже по сравнению с инсулином НПХ (p=0,027). Вариабельность значений глюкозы плазмы перед завтраком, по данным самостоятельного мониторинга гликемии, была ниже на терапии инсулином детемир, так же как и легких эпизодов гипогликемий (25%; p=0,046; 32%; p=0,002 соответственно), по сравнению с группой пациентов, находящихся на терапии инсулином НПХ. Таким образом, общий гликемический контроль на фоне терапии инсулином детемир был достоверно лучше по сравнению с терапией инсулином НПХ [18].
В 6-месячном сравнительном многонациональном исследовании с параллельными группами 448 пациентов с СД1 были рандомизированы на терапию инсулином детемир или НПХ в сочетании с быстродействующим инсулином аспарт [19]. В то время как показатели контроля гликемии были аналогичными между группами, интраиндивидуальная вариабельность была значительно ниже при терапии инсулином детемир по сравнению с терапией инсулином НПХ (p<0,001). Кроме того, терапия инсулином детемир сопровождалась значительным снижением риска всех гипогликемий, в т.ч. ночных (на 22 и 34% соответственно). К концу исследования масса тела была достоверно ниже у пациентов в группе терапии инсулином детемир.
Таким образом, результаты ряда исследований терапии пациентов с СД1 и СД2 позволяют говорить о том, что можно получить дополнительные преимущества в плане эффективности и безопасности терапии при замене базальных инсулинов НПХ и гларгин на инсулин детемир. Инсулин детемир показал свою наибольшую эффективность и безопасность при введении 2 раза в сутки в дозе 0,4 ЕД/кг массы тела [20, 21].
Длительность действия инсулина детемир и его вариабельность
Важным минусом традиционных препаратов человеческого инсулина является их непредсказуемая активность, что связано с непостоянной всасываемостью препаратов. Период всасывания 50% инсулина детемир из подкожно-жирового депо составляет 10,2±1,2 часа по сравнению с 2,0± 0,1 для мономерного ацилированного инсулина [22]. Пролонгированное действие препарата Левемир® обусловлено выраженной самоассоциацией молекул инсулина в месте инъекции и связыванием молекул препарата с альбумином через соединение с боковой жирнокислотной цепью; 98–99% циркулирующего инсулина детемир связано с альбумином, что позволяет создавать более медленный по сравнению с человеческим инсулином трансэпителиальный транспорт из крови в интерстициальную ткань, т.е. дальнейшее продление действия детемира связано с циркуляцией в кровотоке, где его концентрация поддерживается за счет прочной связи с альбумином сыворотки крови. Указанные механизмы замедленного распределения обеспечивают более прогнозируемый и воспроизводимый профиль абсорбции и действия препарата Левемир® по сравнению с инсулином-изофан [10, 23].
Для оценки сахароснижающих эффектов инсулина детемир обследованы группы здоровых добровольцев, пациенты с СД1 и СД2 методом эугликемического клемпа [24, 25]. Средняя продолжительность действия инсулина детемир составила около 24 часов для пациентов с СД1 и более 24 – для пациентов с СД2 [22], однако имела различия у отдельных больных. Инсулин детемир характеризуется дозозависимой длительностью своего действия, что было продемонстрировано в рандомизированном двойном слепoм перекрестнoм исследовании пациентов с СД1 [26, 27]. С использованием 24-часового эугликемического клэмпа параметры пациентов мониторировали в течение суток в ответ на введение инсулина НПХ (0,3 ЕД/кг) и инсулина детемир (0,1 ЕД/кг; 0,2; 0,4; 0,8; 1,6 ЕД/кг). Исследование показало, что при введении инсулина детемир формируется плоский пролонгированный фармакодинамический профиль с высокой предсказуемостью действия по сравнению с НПХ инсулином.
В настоящем исследовании определена линейная взаимосвязь дозы инсулина детемир и ответной реакции в виде длительности действия: длительность действия инсулина детемир при его дозе 0,4 ЕД/кг составила 20 часов, при увеличении дозы более 0,4 ЕД/кг длительность его действия увеличивалась и достигала 22–24 часов.
В настоящее время оценка эффективности лечения СД не ограничивается уровнем HbA1c, а определяется размахом и частотой колебаний суточной гликемии. В связи с этим другой значимой проблемой инсулинотерапии является значительная вариабельность инсулинов, приводящая к колебаниям уровня глюкозы в крови и повышением частоты гипогликемий, что в свою очередь снижает вероятность достижения целевых показателей гликемии [27]. В конце XX в. предложено около 30 различных критериев, характеризующих вариабельность гликемии, для получения которых используются результаты самоконтроля гликемии и непрерывного суточного мониторинга.
Меньшая вариабельность действия инсулина детемир по сравнению с другими базальными инсулинами (НПХ и гларгин 100) связана с рядом его свойств. Абсорбция инсулина детемир не зависит от ресуспендирования или растворения микропреципитатов. Детемир – растворимый инсулин, ввиду чего не требуется ресуспензирования препарата, а в месте инъекции не образуются преципитаты [4, 5, 10]. Обратимое связывание с альбумином плазмы определяет буферный эффект детемира, при котором не происходит немедленного изменения фармакодинамического ответа. В связи с этим детемир имеет более плоский, более длинный и более предсказуемый профиль действия, чем НПХ инсулин, что способствует снижению риска осложнений диабета [25]. Профиль действия инсулина детемир значительно менее вариабелен по сравнению с инсулином-изофан и инсулином гларгин (AUCGIR, 0–24 ч для инсулина детемир составляет 0,074, 0,466 – для инсулина-изофан и 0,231 – для инсулина гларгин; GIRmax для инсулина детемир составляет 0,053, 0,209 – для инсулина-изофан и 0,130 – для инсулина гларгин) [10].
В рандомизированном двойном слепом исследовании 54 пациентам с СД1 в условиях эугликемического клемпа (целевая концентрация глюкозы в крови 5,5 ммоль/л) вводили однократно дозы 0,4 ЕД/кг инсулина детемир, гларгина 100 или инсулина НПХ [28]. Результаты исследования показали, что инсулин детемир ассоциирован с меньшей интраиндивидуальной изменчивостью в утилизации глюкозы, чем НПХ-инсулин и инсулин гларгин (рис. 4).
В одноцентровом исследовании параллельных групп (MTB Medizintechnik, Ulm, Germany) ставили цель оценить изменчивость фармакодинамики и фармакокинетики для инсулинов детемир, НПХ и гларгин у 54 пациентов с СД1 (возраст – 38±10 лет, длительность диабета – 18±9 лет). Показано, что при сравнении вариабельности свойств инсулина детемир с двумя базальными инсулинами (НПХ инсулином и инсулином гларгин) детемир имел более предсказуемый глюкозоснижающий профиль со значительно меньшей изменчивостью по сравнению с другими инсулинами [27, 29]. Более низкую вариабельность инсулина детемир демонстрирует 95%-ный интервал прогнозируемой частоты гипер- и гипогликемий при терапии инсулином детемир по сравнению с инсулинами НПХ и гларгин. Риск развития выраженной гипогликемии (на 50% ниже по сравнению с обычным средним уровнем гликемии): примерно 2 раза в год с инсулином детемир, 57 раз в год с инсулином НПХ и 27 в год с инсулином гларгин [29]. Эти результаты показали, что более низкая изменчивость инсулина детемир служит значимым фактором для пациентов на инсулинотерапии, определяя улучшение метаболического контроля с меньшим числом колебаний уровня глюкозы в крови при терапии изо дня в день.
Гипогликемии
Одна из самых важных последствий изменчивости инсулина – увеличение риска гипогликемий, что служит основным барьером к эффективному и безопасному управление диабетом. Для оценки преимуществ инсулина детемир ввиду снижения риска гипогликемий при достижении компенсации СД был проведен мета-анализ четырех открытых рандомизированных многоцентровых клинических исследований 1180 пациентов с СД1. Была дана оценка частоты тяжелых и легких гипогликемий на фоне терапии инсулином Детемир, вводимого 1 или 2 раза в сутки (число эпизодов на 1 пациента в месяц), и на фоне терапии НПХ инсулином (n=810). Оценка показала, что риск гипогликемий был на 22% ниже в группе терапии инсулином детемир по сравнению с группой инсулина НПХ (р<0,001). Более того, при улучшении показателей HbA1c риск развития гипогликемий имел дальнейшую тенденцию к снижению [30]. По данным Кокрейновского обзора (2009), риск симптоматических, а также ночных и тяжелых эпизодов гипогликемии был в среднем на 16 и 18%, 34 и 37%, 30 и 50% ниже при использовании инсулинов гларгина и детемира, чем инсулина НПХ соответственно [8].
В 26-недельном многоцентровом рандомизированном исследовании с участием 322 пациентов с СД1 применение инсулина детемир продемонстрировало снижение риска ночных гипогликемий и тяжелых гипогликемий на 32 и на 72% соответственно по сравнению с инсулином гларгин [31], что доказало меньшую вариабельность действия инсулина детемир по сравнению с другими базальными инсулинами [32].
Эффективность и безопасность инсулина детемир в различных группах пациентов
Доказанные преимущества применения инсулина детемир при лечении СД у беременных пациенток
Сахарный диабет во время беременности приводит к возникновению массы фетальных и материнских осложнений. Инсулин является наиболее эффективным армакологическим средством для контроля гипергликемии во время беременности и может ограничивать неблагоприятные исходы. Инсулин детемир с 2012 г. разрешен к использованию для лечения беременных женщин с диабетом.
Проведена оценка эффективности и безопасности действия инсулина детемир у беременных женщин с СД1 по сравнению с НПХ-инсулином [33]. Доля пациенток, достигших целевого уровня HbA1c (6,0%) на 24-й и 36-й неделях беременности, существенно не различалась от терапии инсулинами детемир и НПХ. В то время как ГПН были значительно ниже в группе беременных, получавших терапию инсулином детемир по сравнению с НПХ- инсулином (см. таблицу). Набор массы тела пациенток, получавших инсулины детемир и НПХ, был идентичен и составил 11,5 и 11,0 кг соответственно.
В исследовании не было получено разницы между исходами беременности у пациенток на терапии инсулинами детемир и НПХ: рождение ребенка с массой тела меньше 10-го процентиля или выше 90-го процентиля для гестационного возраста и пола, преждевременные роды (<37 гестационных недель), ранняя смерть плода (<22 гестационной недели), перинатальная смертность, наличие врожденных пороков развития [34]. Масса тела новорожденных была 3504 и 3571 г соответственно в группах детемира и НПХ-инсулина. В группе женщин, получавших терапию инсулином детемир, 46% детей были крупными для гестационного возраста, 19% имели макросомию, в группе НПХ-инсулина 54% новорожденных были большими для гестационного возраста и 26% – с макросомией.
Перинатальные исходы служат ярким отражением течения беременности. Рандомизированное контролируемое исследование направлено на сравнение эффективности и безопасности инсулина детемир и НПХ- инсулина у беременных женщины с СД1. Две группы пациенток были рандомизированы на инсулины детемир (n=152) и НПХ-инсулин (n=158) либо в период 12 месяцев до наступления беременности, либо на 8–12-й неделях беременности. Результаты исследования: 128 и 136 новорожденных детей в группах с терапией детемир и НПХ- инсулин, 11 и 9 – ранние потери плода, 2 и 1 – перинатальная смерть соответственно [35]. В исходе беременности 16 детей имели пороки развития; детемир – 8 (5,6%), НПХ – 8 (5,5%). Частота побочных эффектов была одинаковой в группах. Терапия инсулином детемир не вызывала проблем с безопасностью со стороны матери и плода, препарат переносился так же хорошо, как и НПХ-инсулин [36, 37].
Инсулин детемир и СД1 у детей и подростков: вопросы эффективности и безопасности
Особую группу пациентов представляют дети и подростки с СД.
В рандомизированном контролируемом 6-недельном исследовании параллельных групп дана сравнительная оценка эффективности и безопасности инсулинов детемир и НПХ в комбинации с инсулином аспарт при СД1 у детей и подростков. 347 детей 6–17 лет были включены в исследование [38]. В обеих группах был достигнут сходный уровень HbA1c при более предсказуемом гликемическом профиле инсулина детемир и меньшей интраиндивидуальной вариабельности гликемии. Отмечен значительно более низкий риск (26%) ночных гипогликемических эпизодов на терапии инсулином детемир по сравнению с инсулином НПХ, значительно более низкий ИМТ у детей и подростков, получавших терапию инсулином детемир. Исследование показало, что сочетание двух аналогов инсулина в условиях ББ-терапии (детемир+аспарт) позволяет реализовать преимущества каждого из указанных препаратов и получить более выраженный клинический эффект: эффективное снижение уровня HbA1c, меньшая вариабельность гликемии, достоверное снижение гипогликемических состояний, прежде всего ночных, и меньшие значения ИМТ [39].
Эффективность и безопасность ББ-терапии инсулинов детемир и НПХ в комбинации с инсулином аспарт у детей 2–16 лет с СД1 [40]
Инсулин детемир показал сходный уровень HbA1c с НПХ-инсулином в контрольных точках 12-й, 26, 38 и 52-й недели в общей когорте пациентов, доказав свою эффективность. При этом определена достоверно меньшая вариабельность во всех точках наблюдения по сравнению с НПХ-инсулином в общей когорте детей и подростков (SD 3,01 против 3,68 ммоль/л; p<0,001). При оценке динамики массы тела (SDS, Z-score) у детей получены достоверные различия: SD-score массы тела составила на терапии инсулином детемир 0,18, в то время как на терапии НПХ-инсулином 0,33 (средняя разница – -0,15, 95% ДИ – -0,23–-0,07; р<0,001).
Наиболее значимым показателем в исследовании была оценка гипогликемических эпизодов на протяжении 52 недель терапии. Было зарегистрировано 3 эпизода гипогликемии в отсутствие ночных гипогликемий в группе инсулина детемир по сравнению с 15 эпизодами в группе НПХ-инсулина, в т.ч. 6 ночных гипогликемий.
В других исследованиях в группах детей в возрасте 6–17 лет с СД1 показатель HbA1c на 26-й неделе наблюдения существенно не различался между реципиентами инсулина детемир и инсулина НПХ [41], при значительной разнице ГПН при проведении собственных измерений пациентами на инсулине детемир по сравнению с НПХ-инсулином (p<0,001). Уровни ГПН были значительно ниже в группе детей в возрасте 6–17 лет, получавших терапию инсулином детемир, по сравнению с инсулином НПХ. Средний ИМТ при Z-оценке был также значительно ниже в группе инсулина детемир, чем у пациентов на НПХ-инсулине (0,08 и 0,26 соответственно; p<0,001) [42].
В другом исследовании изменение среднего стандартного отклонения (SD) массы тела пациентов в возрасте 2–16 лет составило -0,12 против 0,04 (р<0,001) в группах терапии инсулинами детимир и НПХ соответственно [43]. Среднее значение базальной дозы инсулина в группе терапии инсулином детемир составило 32,2 и 31,0 ЕД/сут в группе НПХ-инсулина у детей в возрасте 6–17 лет [44]. По результатам другого исследования, у реципиентов инсулина детемир и НПХ-инулина базальная доза была 0,60 и 0,58 ЕД/кг массы тела/сут в возрастной группе 2–16 лет [45].
Таким образом, инсулин детемир продемонстрировал свою эффективность и безопасность в детской возрастной группе и показан к лечению СД у подростков и детей в возрасте от 1 года и старше.
Роль и место инсулина детемир в терапии пациентов старших возрастных групп
Одним из важнейших принципов терапии СД является баланс гликемического контроля с риском побочных эффектов. Особое внимание представляют пожилые пациенты с учетом целого ряда клинических, лабораторных и психосоциальных особенностей. Это прежде всего наличие сочетанной полиорганной патологии, в т.ч. патологии печени и почек, сердечно-сосудистые риски, неспецифические жалобы и бессимптомное течение, микро- и макроангиопатии уже при выявлении СД, нарушение когнитивных функций. В связи с этим оценка эффективности и безопасности препарата имеет большое значение для лиц пожилого возраста.
В международном открытом неинтервенционном исследовании A1chieve проведена оценка клинической безопасности и эффективности применения инсулина детемир в возрастной группе 65 лет и старше с СД2 при переходе на инсулин детемир с ПССП или НПХ-инсулина. В субанализ 24-недельного исследования был включен 15 241 пациент. Терапия инсулином детемир в течение указанного периода привела к значительному улучшению гликемического контроля и качества жизни в результате снижения частоты тяжелых и ночных гипогликемий по сравнению с исходной частотой (р<0,05) [46]. Интересными были полученные данные по динамике массы тела: 24-недельная терапия привела к значительной потере массы тела у пациентов, переведенных на инсулин детемир с другого инсулина, в то время как те пациенты, которые впервые получали терапию инсулином, имели незначительный прирост массы тела [46].
Пожилые пациенты особенно уязвимы к возникновению гипогликемий. Целью наблюдательного исследования, проведенного в течение 24 недель в реальной клинической практике, была оценка терапии инсулином детемир с участием 3219 исследователей и 2817 проектных площадок из десяти стран [47, 48]. Инсулин детемир вводили однократно пациентам с СД2 в группах старше и младше 75 лет, получавших лечение одним или несколькими пероральными противодиабетическими препаратами. Общая когорта составила 17 374 участника, из которых 2398 (14%) были старше 75 лет. Исходный уровень HbA1c был сходен в группах пациентов старше и младше 75 лет (HbA1c – 8,8±1,5 и 8,9±1,6% соответственно). Оценка эффективности терапии инсулином детемир показала, что после 24 недель лечения также наблюдалось аналогичное снижение уровня HbA1c в двух группах: 7,6±1,1 и 7,5±1,2%. Частота развития тяжелой гипогликемии (пациенто-год) снизилась в исследовании в обеих возрастных группах: от 0,057 до 0,007 у пациентов в возрасте старше 75 лет и от 0,042 до 0,005 у пациентов младше 75 лет. Оценка массы тела показала сходное снижение средних значений в обеих группах: -0,5 кг у пациентов старше 75 лет и -0,6 кг – младше 75 лет. Результатом исследования в реальной клинической практике стало доказательство эффективности и безопасности терапии инсулином детемир в старшей возрастной группе без связи с повышенным риском развития тяжелой гипогликемии или набора массы тела [49].
Заключение
Опыт реальной клинической практики свидетельствует: пациенты с СД часто не достигают компенсации заболевания. Во многом это связано со значительными перепадами гликемии в течение суток, высоким уровнем вариабельности гликемии. Аналог инсулина длительного действия инсулин детемир – эффективная и хорошо переносимая базальная инсулинотерапия пациентов с СД1 и СД2. Применение инсулина детемир в составе ББ-терапии или в виде базальной терапии вместе с ПССП способствует улучшению гликемического контроля, более низкой изменчивости гликемии, снижению риска возникновения гипогликемических состояний, в т.ч. ночных гипогликемий, меньшему увеличению массы тела по сравнению с НПХ-инсулином. Таким образом, современные режимы инсулинотерапии с применением инсулиновых аналогов, в т.ч. инсулина детемир, позволяют достигать компенсации углеводного обмена, предупреждать формирование и прогрессирование осложнений, способствуя улучшению качество жизни пациентов с СД.
Применение препарата Инсулин детемир
Предназначен для подкожного введения. Доза определяется индивидуально в каждом конкретном случае. Инсулин детемир следует назначать 1 или 2 раза в сутки исходя из потребности пациента. Пациенты, которым требуется применение дважды в день для оптимального контроля за уровнем глюкозы крови, могут вводить вечернюю дозу либо во время ужина, либо перед сном, либо через 12 ч после утренней дозы. Инсулин детемир вводится п/к в область бедра, передней брюшной стенки или плечо. места инъекций следует менять даже при введении в одну и ту же область. Как и при использовании других инсулинов, у пожилых пациентов и пациентов с почечной или печеночной недостаточностью следует более тщательно контролировать уровень глюкозы крови и корригировать дозу инсулина детемир индивидуально. Коррекция дозы может быть также необходима и при усилении физической активности пациента, изменении его обычной диеты или при сопутствующем заболевании.
Результаты
В результате непрямого сравнения клинической эффективности инсулина гларгин 300 ЕД/мл и инсулина детемир, проведённого через общего компаратора — инсулин гларгин 100 ЕД/мл — и основанного на вычислении ОШ исходя из соотношения числа пациентов, достигших/не достигших целевого уровня HbA1c (см. табл. 1), были получены следующие результаты (табл. 6).
Таблица 6
Результаты непрямого сравнения клинической эффективности и переносимости инсулина гларгин 300 ЕД/мл с инсулином детемир
| Направление сравнения | Достижение целевого уровня HbA1c | Тяжёлые гипогликемии | |||
| ОШ | 95 % ДИ | ОШ | 95 % ДИ | ||
| Инсулин гларгин 300 ЕД/мл → инсулин гларгин 100 ЕД/мл | 1,20 | (1,02; 1,42) | 0,58 | (0,40 | 0,82) |
| Инсулин гларгин 100 ЕД/мл → инсулин детемир | 1,06 | (0,92; 1,22) | 1,01 | (0,86 | 1,12) |
| Непрямое сравнение инсулин гларгин 300 ЕД/мл → инсулин детемир | 1,27 | (1,02; 1,58) | 0,72 | (0,56 | 0,88) |
Вероятность достижения целевого уровня HbA1с<7 % при применении инсулина гларгин 300 ЕД/мл достоверно выше (на 20 %), чем при использовании инсулина гларгин 100 ЕД/мл. ОШ для сравнения инсулин гларгин 100 ЕД/мл → инсулин детемир составило 1,06, причём доверительный интервал пересекает значение 1,0, что свидетельствует о сопоставимой эффективности этих аналогов инсулина и совпадает с данными прямых сравнительных исследований (в частности, при анализе практики инсулинотерапии у 16 341 больного СД 2 [32]). Непрямое сравнение рассчитанных значений ОШ для инсулина гларгин 300 ЕД/мл и инсулина детемир показало, что вероятность достижения у больных уровня HbA1с<7 % при применении гларгина достоверно выше (на 27 %). Высчитанная частота достижения компенсации СД 2 в течение 6-месячного периода составила 25,3 % для инсулина гларгин 300 ЕД/мл и, с учётом вышеприведённого ОШ, 19,9 % для инсулина детемир. Прямые затраты на препараты представлены в табл. 1, они высчитаны на основе дозировок, определённых в входе непрямого сравнения препаратов из расчёта массы тела больного в 70 кг. Видно, что суточные дозировки инсулина детемир по результатам непрямого сравнения ожидаются выше на 13,8 % в сравнении с инсулином гларгин 300 ЕД/мл. В то же время с учётом разницы в стоимости этих препаратов годовой курс инсулина гларгин 300 ЕД/мл по стоимости не различается с таковым у инсулина детемир. Эти затраты, как мы покажем далее, не всегда являются экономическим основанием для принятия решения о назначении того или иного инсулина, поскольку они не отражают общие расходы (прямые и непрямые) на лечение.
Параметр ОШ в отношении вероятности развития тяжёлого гипогликемического события статистически достоверно ниже у инсулина гларгин 300 ЕД/мл (см. табл. 6). Если считать, что в группе инсулина гларгин 300 ЕД/мл в течение года происходит одна тяжёлая гипогликемия, то тогда в группе инсулина детемир ожидается 1,38 таких событий. При этом расчёт показывает разницу в более чем 5 000 руб. на лечение тяжёлой гипогликемии в группах (табл. 8).
В табл. 7 представлены прямые медицинские и немедицинские (оплата листков нетрудоспособности), а также непрямые (потери ВВП) затраты (расходы). Расчёты свидетельствуют о том, что в целом затраты на лечение инсулином гларгин 300 ЕД/мл не превышают таковые на лечение инсулином детемир. При этом с медицинской точки зрения инсулин гларгин имеет некоторые преимущества по сравнению с инсулином детемир:
- все 100 % больных могут применять инсулин гларгин 300 ЕД/мл 1 раз в сутки, в то время как процент получающих детемир однократно в день при СД 2 — не более половины [33], что не вполне удобно для длительного лечения и, возможно, лежит в основе того, что в 52,7 % случаев через 24 мес. происходит отказ больных от введения препарата [32], а это крайне негативно может сказаться на прогнозе заболевания;
- количество гипогликемий симптомных, тяжёлых меньше;
- возможно «гибкое» дозирование инсулина гларгин 300 ЕД/мл (3 ч до/после привычного времени введения) без ущерба клиническому эффекту [34].
Таблица 7
Затраты в зависимости от достижения / не достижения компенсации СД 2 (1 случай, руб.)
| Сердечно-сосудистое событие | Прямые медицинские средневзвешенные затраты при недостижении HbA1с<7 % (руб.) | Прямые медицинские средневзвешенные затраты при достижении HbA1с<7 % (руб.) | Прямые немедицинские затраты (руб.) | Средневзвешенные прямые немедицинские затраты при недостижении HbA1с<7 % (руб.) | Средневзвешенные прямые немедицинские затраты при достижении HbA1с<7 % (руб.) | Непрямые затраты (руб.) | Средневзвешенные непрямые затраты при недостижении HbA1с<7 % (руб.) | Средневзвешенные непрямые затраты при достижении HbA1с<7 % (руб.) |
| Артериальная гипертензия | 17 780,87 | 12 624,42 | 6 327,22 | 3 028,87 | 2 150,50 | 15 463,43 | 7 402,43 | 5 255,72 |
| Нарушения сердечного ритма | 11 065,04 | 7 856,18 | 6 327,22 | 1 288,70 | 914,97 | 15 463,43 | 3 149,51 | 2 236,15 |
| Стенокардия | 11 013,27 | 7 819,42 | 11 863,54 | 2 243,71 | 1 593,04 | 28 993,92 | 5 483,53 | 3 893,30 |
| Хроническая сердечная недостаточность | 4 733,32 | 3 360,66 | 11 863,54 | 1 339,65 | 951,15 | 28 993,92 | 3 274,05 | 2 324,57 |
| Инфаркт миокарда | 12 242,48 | 8 692,16 | 96 490,09 | 6 818,25 | 4 840,96 | 235 817,24 | 16 663,49 | 11 831,08 |
| Инсульт | 11 234,34 | 7 639,35 | 120 217,16 | 5 829,82 | 3 964,27 | 293 805,09 | 14 247,80 | 9 688,50 |
| Суммарно | 68 069,32 | 47 992,19 | 20 549,01 | 14 414,89 | 50 220,81 | 35 229,32 |
Таблица 8
Затраты на лечение СД 2 инсулином гларгин 300 ЕД/мл и инсулином детемир (на 1 пациента/год, руб.)
| Тип затрат | Инсулин-гларгин 300 ЕД/мл | Инсулин-детемир | Разница инсулин гларгин 300 ЕД/мл-инсулин детемир |
| Прямые затраты | |||
| Затраты на инсулинотерапию | 15 856,33 | 15 682,59 | 173,74 |
| Затраты на лечение ССС-осложнений* | 63 882,66 | 64 064,08 | -181,42 |
| Затраты на лечение тяжёлой гипогликемии** | 15 180,00 | 20 948,84 | -5 768,84 |
| Оплата временной нетрудоспособности | 19 894,88 | 19 325,28 | -569,60 |
| Суммарно прямые затраты | 114 813,87 | 120 020,79 | -6 346,12 (-4,3 %) |
| Непрямые затраты | |||
| Недополученный ВВП*** | 46 226,00 | 47 230,12 | -1 004,12 (-2,1 %) |
| Итого общие затраты | 161 039,87 | 167 250,91 | -7 350,24 (-3,7 %) |
Примечания: * — с учётом всех событий для пациентов, как достигших, так и не достигших целевого уровня HbA1c; ** — научно обоснованное допущение о количестве тяжёлых состояний (см. в тексте); *** — в результате временной нетрудоспособности.
Уместно отметить, что тем, кому показан инсулин детемир, его следует назначать, несмотря на вышеприведённые аргументы в пользу инсулина гларгин 300 ЕД/мл.
Двусторонний анализ чувствительности при изменении цен на сравниваемые препараты (табл. 9) подтверждает выводы основного сценария об экономической целесообразности применения инсулина гларгин 300 ЕД/мл с точки зрения общих расходов на лечение СД 2 в течение года (табл. 8). Можно, конечно, считать, что потенциальное снижение расходов на 4—5 % не так существенно, но если вспомнить о числе больных, нуждающихся в эффективной и безопасной инсулинотерапии, то экономические выгоды применения более дешёвых программ терапии становятся очевидными.
Таблица 9
Анализ чувствительности в отношении изменения цен на сравниваемые препараты
| Изменение цены на инсулин детемир (за ЕД) | Изменение цены на инсулин гларгин 300 ЕД/мл (за ЕД) | ||||||||||
| -50 % | -40 % | -30 % | -20 % | -10 % | 0 % | 10 % | 20 % | 30 % | 40 % | 50 % | |
| 30 % | -18,5 % | -7,5 % | -16,5 % | -15,4 % | -14,4 % | -13,3 % | -2,3 % | -1,3 % | -0,2 % | 0,8 % | 1,9 % |
| 20 % | -17,7 % | -16,6 % | -15,6 % | -14,5 % | -13,5 % | -12,4 % | -3,4 % | -0,3 % | 0,7 % | 1,8 % | 2,8 % |
| 10 % | -16,8 % | -15,7 % | -14,7 % | -13,6 % | -12,5 % | -10,5 % | -4,4 % | 0,6 % | 1,7 % | 2,7 % | 3,8 % |
| 0 % | -15,9 % | -14,8 % | -11,5 % | -7,9 % | -5,7 % | -3,7 % | -1,6 % | 1,8 % | 2,7 % | 4,2 % | 4,8 % |
| -10 % | -5,0 % | -3,9 % | -2,8 % | -1,7 % | -0,6 % | 0,4 % | 1,5 % | 2,6 % | 3,7 % | 4,8 % | 5,8 % |
| -20 % | -4,0 % | -2,9 % | -1,8 % | -0,7 % | 0,3 % | 1,4 % | 2,5 % | 3,6 % | 4,7 % | 5,8 % | 6,9 % |
| -30 % | -3,1 % | -2,0 % | -0,9 % | 0,2 % | 1,3 % | 2,4 % | 3,5 % | 4,6 % | 5,7 % | 6,8 % | 7,9 % |
Побочные эффекты препарата Инсулин детемир
Побочные реакции, наблюдаемые у пациентов, применяющих инсулин детемир являются в основном дозозависимыми и развиваются вследствие фармакологического эффекта инсулина. Гипогликемия, как правило, является наиболее частым побочным эффектом. Гипогликемия развивается в случае, если введена слишком высокая доза препарата относительно потребности организма в инсулине. Реакции в местах введения могут наблюдаться при лечении приблизительно у 2% пациентов. Доля пациентов, получающих лечение и у которых ожидается развитие побочных эффектов, оценивается как 12%. Частота развития побочных эффектов во время клинических исследований, представлена ниже. Нарушения метаболизма и расстройства питания: частые (1/100, ≤1/10). Гипогликемия: симптомы гипогликемии как правило развиваются внезапно. Они включают «холодный пот», бледность кожных покровов, повышенную утомляемость, нервозность или тремор, чувство тревоги, необычную усталость или слабость, нарушение ориентации, снижение концентрации внимания, сонливость, выраженное чувство голода, нарушение зрения, головную боль, тошноту, сердцебиение. Тяжелая гипогликемия может приводить к потере сознания и/или судорогам, временному или необратимому нарушению функции головного мозга вплоть до летального исхода. Общие расстройства и реакции в местах введения препарата: частые (1/100, ≤1/10). Реакции в местах введения: реакции местной гиперчувствительности (покраснение, припухлость и зуд в месте инъекции) могут развиваться во время лечения инсулином. Эти реакции обычно носят кратковременный характер и исчезают при продолжении лечения. Редкие (1/1000, ≤1/100). Липодистрофия: может развиваться в месте инъекции в результате несоблюдения правила смены места инъекции в пределах одной области. Отеки: могут возникать на начальной стадии инсулинотерапии. Эти симптомы обычно носят временный характер. Нарушения иммунной системы: редкие (1/1000, ≤1/100). Аллергические реакции: крапивница, кожная сыпь могут развиваться вследствие гиперчувствительности. Признаками гиперчувствительности могут быть зуд, потливость, желудочно-кишечные расстройства, ангионевротический отек, затруднения дыхания, сердцебиение, снижение АД. Развитие реакций гиперчувствительности может быть потенциально опасным для жизни. Нарушения зрительной функции: редкие (1/1000, ≤1/100). Нарушения рефракции: аномалии рефракции могут возникать на начальной стадии инсулинотерапии. Эти симптомы обычно являются временными. Диабетическая ретинопатия. Длительное улучшение контроля гликемии снижает риск прогрессирования диабетической ретинопатии Однако, интенсификация инсулинотерапии с резким улучшением контроля углеводного обмена может привести к временному усилению признаков диабетической ретинопатии. Расстройства со стороны нервной системы: очень редкие (1/10000, ≤1/1000). Периферическая нейропатия: быстрое улучшение контроля гликемии может приводить к состоянию острой болевой нейропатии, которая обычно является обратимой.
Материалы и методы
Прямое сравнение (англ. head-to-head) применения инсулина гларгин 300 ЕД/мл с инсулином де-темир в условиях реальной клинической практики не проводилось. В связи с этим было осуществлено непрямое сравнение их клинических эффектов через общий препарат сравнения — инсулин гларгин 100 ЕД/мл, с которым проводились сравнительные исследования как у инсулина гларгин 300 ЕД/мл, так и у инсулина детемир. Поскольку регистрационные клинические исследования имеют ряд ограничений, обусловленных особенностями их дизайна, для проведения сравнения были выбраны исследования применения сравниваемых препаратов в условиях реальной клинической практики. Исследования, отобранные для анализа, приведены в табл. 1.
Таблица 1
Исследования реальной клинической практики, использованные при проведении непрямого сравнения
| № | Описание | Общее число больных | Больные, достигшие целевого уровня HbA1c /тяжёлые гипогликемии, n | Больные, не достигшие целевого уровня HbA1c, n |
| 1 | Ретроспективное когортное исследование исходов применения инсулина гларгин 300 ЕД/мл в сравнении с инсулином гларгин 100 ЕД/мл у взрослых пациентов с сахарным диабетом 1 и 2 типа на основе Канадского регистра больных сахарным диабетом [12] | Инсулин гларгин 100 ЕД/мл 188 | 53/6 | 135 |
| Инсулин гларгин 300 ЕД/мл 188 | 51/4 | 137 | ||
| 2 | Исследование DELIVER Naive по оценке достижения целевого снижения HbA1c и случаев гипогликемии у инсу-лин-наивных пациентов, получавших инсулин гларгин 300 ЕД/мл в сравнении с инсулином гларгин 100 ЕД/мл в условиях реальной клинической практики [13] | Инсулин гларгин 100 ЕД/мл 2008 | 432/127 | 1576 |
| Инсулин гларгин 300 ЕД/мл 1004 | 251/39 | 753 | ||
| Суммарно 1-2 | Инсулин гларгин 100 ЕД/мл 2196 | 485/133 | 1711 | |
| Инсулин гларгин 300 ЕД/мл 1192 | 302/43 | 890 | ||
| 3 | Ретроспективный анализ данных более 40 программ здравоохранения США, собранных в национальной базе медицинских данных Innovus IMPACT с 2006 по 2010 гг. Оценивались исходы использования инсулина гларгин (100 ЕД/мл) и инсулина детемир [14] | Инсулин гларгин 640 | 153/50 | 487 |
| Инсулин детемир 640 | 149/38 | 491 | ||
| 4 | Ретроспективный анализ данных реальной клинической практики лечения пациентов с сахарным диабетом 2 типа, начавших терапию инсулином гларгин (100 ЕД/мл) или инсулином детемир на основе базы данных General Electric (GE) Centricity EMR США [15] | Инсулин гларгин 3467 | 745/198 | 2722 |
| Инсулин детемир 915 | 176/47 | 739 | ||
| Суммарно 3-4 | Инсулин гларгин 4107 | 898/248 | 3209 | |
| Инсулин детемир 1555 | 325/85 | 1230 |
Непрямое сравнение проводили с использованием программы Канадского агентства по лекарственным средствам и технологиям здравоохранения [16] в соответствии с требованиями Методических рекомендаций по проведению непрямых сравнений лекарственных препаратов, разработанных ФГБУ «Центр экспертизы и контроля качества медицинской помощи» Министерства здравоохранения Российской Федерации («ЦЭККМП» Минздрава РФ) [17]. В качестве критерия эффективности, в отношении которого проводилось непрямое сравнение, был выбран «суррогатный» исход — достижение целевых значений HbA1c<7 %. Сделано допущение, что ночные и тяжёлые гипогликемии классифицируются как тяжёлые (уровень глюкозы плазмы крови менее 3,0 ммоль/л).
Рассчитывали отношение шансов (ОШ, англ. odds ratio, OR) [18] по следующим схемам:
- определяли ОШ для сравнения инсулин глар-гин 300 ЕД/мл — инсулин гларгин 100 ЕД/мл;
- определяли ОШ для сравнения инсулин гларгин 100 ЕД/мл — инсулин детемир;
- через общий препарат сравнения — инсулин гларгин 100 ЕД/мл — определяли ОШ для сравнения инсулин гларгин 300 ЕД/мл → инсулин детемир.
ОШ рассчитывали по формуле [19]:
ОШ = (A х D)/(B х С), где
ОШ — отношение шансов;
А — частота достижения уровня HbA1с<7,0 % в первой группе;
С — частота достижения уровня HbA1с<7,0 % во второй группе;
В — частота недостижения уровня HbA1с<7,0 % в первой группе;
D — частота недостижения уровня HbA1с<7,0 % во второй группе.
При этом использовалась стандартная четырёхполосная таблица (табл. 2).
Таблица 2
Матрица четырёхполосной таблицы для расчётов ОШ
| Препараты | Достижение HbA1c<7,0 % (я, %) | Недостижение HbA1c<7,0 % (я, %) | Всего |
| Препарат 1 | A | B | A+B |
| Препарат 2 | C | D | C+D |
| Всего | A+C | B+D |
95 % доверительный интервал (ДИ) для рассчитанного ОШ определяли по формулам:
для верхней границы
для нижней границы
Если в качестве исходных данных в анализе использовали несколько источников, число пациентов, достигших или не достигших целевого уровня HbA1c <7 %, суммировали и рассчитывали ОШ на основе суммарных значений.
Частота тяжёлых гипогликемий (глюкоза плазмы крови менее 3,0 ммоль/л) определена в соответствии с данными ретроспективного анализа реальной клинической практики у 831 456 больного СД 2 [20]. Для инсулина гларгин 300 ЕД/мл вероятность тяжёлой гипогликемии, требующей госпитализации, составила 0,07 (частота / «наивный» больной), в то время как для инсулина детемир она была статистически достоверно выше — 0,15. Нами произведены расчёты соотношения гипогликемий на основе непрямого сравнения рассматриваемых программ инсулинотерапии. Существуют разные подходы к оценке стоимости этой ятрогении; мы использовали данные, согласно которым она оценивается в 15 180 руб. расходов отечественного здравоохранения [21].
Сделано научное допущение, что средние суточные дозы инсулинов в реальной клинической практике соответствуют таковым, которые получены в ретроспективном исследовании [22]. Так, расчётная средняя суточная доза инсулина гларгин 300 ЕД/мл составила 0,29 ЕД/кг, а инсулина детемир— 0,33 ЕД/кг. Несмотря на различия в дозировках инсулина гларгин 100 ЕД/мл и 300 ЕД/мл по данным рандомизированных исследований, нами было принято допущение, что их дозы в сутки в реальной клинической практике не различаются [15][23].
Цены на сравниваемые препараты инсулинов определены как по государственному реестру предельных отпускных цен [24], так и на основании данных производителя и представлены в табл. 3.
Таблица 3
Стоимости инсулинов, использованных в анализе
| МНН | Торговое наименование | Объём в упаковке (ЕД) | Производитель | Стоимость упаковки, руб. | Цена с 10 % НДС и 11,98 % ТН* | Стоимость 1 ЕД, (руб.) | Суточная доза (ЕД/кг) | Суточная доза (ЕД) | Стоимость года терапии (руб.) |
| Инсулин гларгин 300 ЕД/ мл | Туджео СолоСтар | 1350 | ЗАО «Санофи-Авентис Восток», Россия | 2 343,29** | 2 886,42 | 2,14 | 0,29 | 20,3 | 15 856,33 |
| 2250 | 3 905,23** | 4 810,38 | 2,14 | ||||||
| Инсулин детемир | Левемир ФлексПен | 1500 | Ново Нордиск А/C, Дания | 2 263,68 | 2 788,36 | 1,86 | 0,33 | 23,1 | 15 682,59 |
Примечания: * НДС — налог на добавленную стоимость; ТН — регулируемая оптовая надбавка [25]; ** — стоимость, которую производитель планирует перерегистрировать в соответствии с Правилами [26].
При оценке нагрузки на бюджет системы здравоохранения и бремени заболевания учитывали данные по частоте сердечно-сосудистых осложнений (сердечно-сосудистых событий — ССС) у пациентов с СД 2 согласно данным отечественно фармакоэпидемиологического исследования ФОР-САЙТ-СД2 [27] (табл. 4).
Таблица 4
Частота сердечно-сосудистых заболеваний при сахарном диабете 2 типа [27]
| Сердечно-сосудистое заболевание | Частота встречаемости, % |
| Артериальная гипертензия | 69,10 |
| Нарушения сердечного ритма | 29,40 |
| Стенокардия | 27,30 |
| Хроническая сердечная недостаточность | 16,30 |
| Инфаркт миокарда | 10,20 |
| Инсульт | 7,00 |
Стоимость лечения обострений рассчитывали с учётом тарифов КСГ (табл. 5). Частота чрескожного коронарного вмешательства (ЧКВ) при инфаркте миокарда составляет 75 %, в связи с чем средневзвешенные затраты на лечение инфаркта миокарда составят 109 087,80 руб. Размер базовой ставки на один законченный случай лечения в круглосуточном стационаре, согласно ПГГ на 2022 г., составляет 34 713,70 руб. [28].
Таблица 5
Стоимость лечения обострений CCЗ согласно тарифам КСГ [29]
| Заболевание | КСГ | Коэффициент затрат | Стоимость законченного случая, руб. | Среднее значение стоимости, руб. | |
| Инфаркт миокарда | st13.001 | Нестабильная стенокардия, инфаркт миокарда, лёгочная эмболия (уровень 1) | 1,42 | 49 293,454 | 75 675,87 |
| st13.002 | Нестабильная стенокардия, инфаркт миокарда, лёгочная эмболия (уровень 2) | 2,81 | 97 545,497 | ||
| st13.003 | Инфаркт миокарда, лёгочная эмболия, лечение с применением тромболитической терапии | 3,48 | 120 803,676 | ||
| st25.004 | Диагностическое обследование сердечно-сосудистой системы | 1,01 | 35 060,837 | ||
| st25.005 | Операции на сердце и коронарных сосудах (уровень 1) | 2,11 | 73 245,907 | 120 225,11 | |
| st25.006 | Операции на сердце и коронарных сосудах (уровень 2) | 3,97 | 137 813,389 | ||
| st25.007 | Операции на сердце и коронарных сосудах (уровень 3) | 4,31 | 149 616,047 | ||
| Нарушения сердечного ритма | st13.004 | Нарушения ритма и проводимости (уровень 1) | 1,12 | 38 879,344 | 54 326,94 |
| st13.005 | Нарушения ритма и проводимости (уровень 2) | 2,01 | 69 774,537 | ||
| Инсульт | st15.013 | Кровоизлияние в мозг | 2,82 | 97 892,634 | 112 559,17 |
| st15.014 | Инфаркт мозга (уровень 1) | 2,52 | 87 478,524 | ||
| st15.015 | Инфаркт мозга (уровень 2) | 3,12 | 108 306,744 | ||
| st15.016 | Инфаркт мозга (уровень 3) | 4,51 | 156 558,787 | ||
| Стенокардия | st27.006 | Стенокардия (кроме нестабильной), хроническая ишемическая болезнь сердца (уровень 1) | 0,78 | 27 076,686 | 58 232,23 |
| st27.007 | Стенокардия (кроме нестабильной), хроническая ишемическая болезнь сердца (уровень 2) | 1,7 | 59 013,29 | ||
| st13.001 | Нестабильная стенокардия, инфаркт миокарда, лёгочная эмболия (уровень 1) | 1,42 | 49 293,454 | ||
| st13.002 | Нестабильная стенокардия, инфаркт миокарда, лёгочная эмболия (уровень 2) | 2,81 | 97 545,497 | ||
| Артериальная гипертензия | st27.005 | Гипертоническая болезнь в стадии обострения | 0,7 | 24 299,59 | 37 143,66 |
| st25.004 | Диагностическое обследование сердечно-сосудистой системы | 1,01 | 35 060,837 | ||
| st38.001 | Соматические заболевания, осложнённые старческой астенией | 1,5 | 52 070,55 | ||
| ХСН | st25.004 | Диагностическое обследование сердечно-сосудистой системы | 1,01 | 35 060,837 | 41 916,79 |
| st27.008 | Другие болезни сердца (уровень 1) | 0,78 | 27 076,686 | ||
| st27.009 | Другие болезни сердца (уровень 2) | 1,54 | 53 459,098 | ||
| st38.001 | Соматические заболевания, осложнённые старческой астенией | 1,5 | 52 070,55 | ||
| Реабилитация после ИМ | Оказание медицинской помощи по тарифу КСГ 350 «Медицинская кардиореабилитация (5 баллов по ШРМ)» | 64 164,40 | |||
| Реабилитация после инсульта | Оказание медицинской помощи по тарифам КСГ 341-344 «Медицинская реабилитация пациентов с заболеваниями центральной нервной системы (3-6 баллов по ШРМ)» — среднее значение КЗ | 119 105,17 | |||
При оценке затрат на лечение ССС учитывали, что достижение HbA<7 % позволяет снизить частоту сердечно-сосудистых событий [30]. Так, ожидается снижение частоты всех ССС на 29 % (95 % ДИ 0,51—0,98), инсульта — на 32 % (95 % ДИ 0,46—0,99).
Помимо прямых затрат на лекарственную терапию и лечение обострений учитывали также косвенные затраты, ассоциированные с оплатой временной нетрудоспособности и недополученным объёмом ВВП в результате временной нетрудоспособности. Частота летальных исходов при СД 2, по данным фармако-эпидемиологического исследования ФОРСАЙТ-СД2, составляет 40,6 на 100 000 больных или 0,0406 %. При оценке затрат на оплату временной нетрудоспособности учитывали медиану среднемесячной заработной платы за 2022 г. в 42 364,00 руб. [31]. В этом случае среднедневная заработная плата составит 1 412,13 руб. Сделано допущение, что оплата временной нетрудоспособности осуществлялась в 100 % размере.
При оценке объёма недополученного ВВП учитывали, что в 2022 г. он был 103 626,60 млрд руб. Трудоспособное население России в 2018 г. составило 82 264,00 тыс. человек (56,01 %) при общей численности населения 146 880,00 тыс. человек. Исходя из этого ВВП на душу трудоспособного населения в 2022 г. составил 1 259 683,46 руб. за год или 3 451,19 руб. за календарный день. При этом учитывали среднюю длительность нетрудоспособности при различных сердечно-сосудистых событиях: инфаркт миокарда — 122 дня, стенокардия и хроническая сердечная недостаточность — по 15 дней, артериальная гипертензия и нарушения сердечного ритма — по 8 дней.
Финальное значение суммарных затрат рассчитывали, учитывая:
- прямые затраты на сравниваемые инсулины и лечение сердечно-сосудистых событий (прямые медицинские затраты), а также расчётные данные по стоимости тяжёлой гипогликемии;
- косвенные затраты на оплату временной нетрудоспособности (прямые немедицинские затраты), и затраты, ассоциированные с недополученным ВВП за период временной нетрудоспособности (непрямые затраты).
Особые указания по применению препарата Инсулин детемир
Инсулин детемир обеспечивает лучший гликемический контроль (на основании измерения глюкозы плазмы крови натощак) по сравнению с применением изофан-инсулина. Недостаточная доза инсулина или прекращение лечения, особенно при сахарном диабете I типа, может приводить к развитию гипергликемии или диабетического кетоацидоза. Как правило, первые симптомы гипергликемии появляются постепенно, в течение нескольких часов или дней. К этим симптомам относятся жажда, учащенное мочеотделение, тошнота, рвота, сонливость, покраснение и сухость кожи, сухость во рту, потеря аппетита, запах ацетона в выдыхаемом воздухе. При сахарном диабете I типа без соответствующего лечения гипергликемия приводит к развитию диабетического кетоацидоза и может привести к смерти. Гипогликемия может развиться, если доза инсулина слишком высока по отношению к потребности в инсулине у конкретного пациента. Пропуск приема пищи или интенсивная физическая нагрузка могут приводить к гипогликемии. После компенсации углеводного обмена, например при интенсифицированной инсулинотерапии, у пациентов могут измениться типичные для них симптомы-предвестники гипогликемии, о чем больные должны быть проинформированы. Обычные симптомы-предвестники могут исчезать при длительном течении сахарного диабета. Сопутствующие заболевания, особенно инфекционные и сопровождающиеся лихорадкой, обычно повышают потребность организма в инсулине. Перевод с других видов инсулина Перевод больного на новый тип инсулина или инсулин другого производителя должен происходить под строгим врачебным контролем. При изменении концентрации, производителя, типа, вида (животный, человеческий, аналоги человеческого инсулина) и/или метода его производства (генно-инженерный или инсулин животного происхождения) может потребоваться коррекция дозы. Пациенты, переходящие на лечение инсулином детемир, могут нуждаться в изменении дозы по сравнению с дозами ранее применявшегося инсулина. Необходимость в коррекции дозировки может возникнуть уже после введения первой дозы или в течение первых нескольких недель или месяцев. Инсулин детемир не следует вводить в/в, так как это может привести к состоянию тяжелой гипогликемии. Всасывание при в/м введении происходит быстрее и в большей степени по сравнению с подкожным введением. Если инсулин детемир смешивается с другими видами инсулина, профиль действия одного или обоих компонентов изменится. Смешивание инсулина детемир с быстродействующим аналогом инсулина, таким как инсулин аспарт, приводит к профилю действия со сниженным и отсроченным максимальным эффектом по сравнению с их раздельным введением. Перевод с инсулинов средней продолжительности действия и пролонгированных инсулинов на инсулин левемир может потребовать коррекции дозы и времени введения. Как и при использовании других инсулинов, рекомендуется тщательный контроль уровня глюкозы крови во время перевода и в первые недели назначения нового инсулина. Возможно, потребуется коррекция сопутствующей гипогликемической терапии (дозы и времени введения короткодействующих типов инсулина или дозы пероральных гипогликемизирующих средств). Инсулин детемир не предназначен для использования в инсулиновых насосах. Применение в период беременности и кормления грудью. В настоящее время отсутствуют данные клинического применения инсулина детемир в период беременности и кормления грудью. Исследование репродуктивной функции у животных не выявили различий между инсулином детемир и человеческим инсулином по показателям эмбриотоксичности и тератогенности. В целом, необходимо тщательное наблюдение беременных женщин, страдающих сахарным диабетом в течение всего срока беременности, а также при планировании беременности. Потребность в инсулине в I триместр беременности обычно уменьшается, затем во II и III триместрах возрастает. Вскоре после родов потребность в инсулине быстро возвращается к уровню, который был до беременности. У женщин кормящих грудью может потребоваться коррекция дозы инулина и диеты. Влияние на способность управления автомобилем и работу с механизмами. Способность пациентов к концентрации внимания и скорость реакции могут нарушаться во время гипогликемии или гипергликемии, что может представлять опасность в тех ситуациях, когда эти способности особенно необходимы (например, при управлении автомобилем или работе с машинами и механизмами). Пациентам необходимо рекомендовать предпринимать меры для предупреждения развития гипогликемии и гипергликемии при вождении автомобиля и работе с механизмами. Это особенно важно для пациентов с отсутствием или снижением выраженности симптомов-предвестников развивающейся гипогликемии или частыми эпизодами гипогликемии. В этих случаях следует рассмотреть целесообразность управления автомобилем или выполнения подобных работ.
Введение
События последних месяцев, потрясшие цивилизацию, снова и снова заставляют всерьёз задуматься о повышении эффективности лечения хронических заболеваний, поскольку именно такие группы больных наиболее уязвимы, в том числе и в период вирусных эпидемий [1]. Не является исключением и сахарный диабет 2 типа (СД 2) — больные, у которых не достигнут эффективный контроль заболевания, оцененный по достижению целевого уровня гликированного гемоглобина (HbA1c), переносят инфекционные и иные стрессовые ситуации в целом тяжелее, вероятность ухудшения прогноза заболевания повышается, требуются дополнительные меры лечебного воздействия, что отражается и на расходах общественного здравоохранения [2]. Эффективная и безопасная инсу-линотерапия всегда считалась основой контроля СД, несмотря на разработку и внедрение в клиническую практику в последние 20 лет новых классов противо-диабетических средств. Наша страна обладает большим опытом применения как отечественных аналогов инсулина (инсулин гларгин 100 ЕД/мл и 300 ЕД/ мл), отвечающих требованиям строгого, но в тоже время индивидуализированного, контроля СД, так и зарубежных (инсулин детемир, инсулин деглудек).
Инсулин гларгин и инсулин детемир повсеместно применяются в отечественной клинической практике более десятилетия. Парадигма эффективного контроля СД 2 с помощью этих препаратов предусматривает своевременную инсулинизацию с целью предупреждения микро- и макрососудистых осложнений заболевания и снижения тем самым расходов на лечение [3]. При этом имеют право на существование как различные подходы к сопоставлению дозировок этих аналогов инсулина, так и к кратности их назначения [4][5]. Инсулин гларгин 100 ЕД/мл и инсулин детемир не решают ключевой проблемы инсулинотерапии — гипогликемии. Кроме того, длительность гипогликемизирующего эффекта этих препаратов уже не удовлетворяет всё возрастающим критериям удобства применения пациентами, желающими иметь средства с максимально возможной длительностью действия, минимальным объёмом вводимого вещества без возникающих липодистро-фий кожи, средствами, не влияющими на массу тела и т. п., что важно для оптимизации образа жизни.
Вопросы продолжительности действия, улучшенного профиля безопасности, в том числе и при титра-ции, гибкость назначения (3 ч до/после привычного времени введения) в случае необходимости во многом решаются с приходом в практику новых аналогов: инсулина гларгин 300 ЕД/мл (Туджео СолоСтар, производство ЗАО «Санофи-Авентис Восток», Россия) и инсулина деглудек (Тресиба, производство А/О «Ново Нордиск», Дания), которые в силу отличительных особенностей фармакодинамики и фармакокинетики относят к препаратам второго поколения [6][7]. Тем самым подчеркивается их высокий фармакологический потенциал по контролю СД обоих типов при минимуме нежелательных эффектов, прежде всего, гипогликемических событий и нейтрального влияния на массу тела. Теперь хорошо известно, что гипогликемия — это не только фактор увеличения риска внезапной смерти в 2 раза, госпитализации, сердечно-сосудистых катастроф на 30-40 %, но и ятрогения, существенно увеличивающая расходы системы здравоохранения на компенсацию СД [8][9].
Увеличение расходов в случае учащения гипогли-кемических событий при СД 2 продемонстрировано и для отечественных условий реальной практики. В большей степени это относится к инсулину НПХ, частота симптоматических и тяжёлых гипогликемий при применении которого с целью эффективного (до цели) контроля заболевания выше в сравнении с инсулином гларгин 100 ЕД/мл в несколько раз [10]. Расходы в группах больных, у которых применяются инсулин гларгин 100 ЕД/мл и инсулин НПХ, различаются: несмотря на более высокую стоимость аналога инсулина (при сравнении стоимости ЕД активности), затраты на контроль СД 2 оказываются в целом ниже, в том числе и за счёт меньшего числа гипогликемий [11]. На этих примерах отчётливо прослеживается доказательство того, что низкая стоимость единицы активного вещества не должна быть определяющей в выборе препарата для лечения, поскольку более важно, сколько стоит добиться клинической эффективности (контроль СД 2), на какой срок и с какими нежелательными эффектами.
В настоящее время, когда основными аналогами инсулина в нашей стране при СД 2 являются инсулин гларгин и инсулин детемир, с новой силой поднимается вопрос о сравнительных стоимостных аспектах лечения СД 2 этими препаратами. Учитывая внедрение инсулина гларгин 300 ЕД/мл, сузим вопрос до сопоставления экономических различий между ним и инсулином детемир, поскольку он до настоящего времени не изучен.
Таким образом, целью данного анализа является изучение сравнительной экономической эффективности инсулина гларгин 300 ЕД/мл и инсулина дете-мир при СД 2.
Взаимодействия препарата Инсулин детемир
Имеется ряд лекарственных средств, которые влияют на потребность в инсулине. Гипогликемическое действие инсулина усиливают: пероральные гипогликемические препараты, ингибиторы МАО, ингибиторы АПФ, ингибиторы карбоангидразы, неселективные β-адреноблокаторы, бромокриптин, сульфонамиды, анаболические стероиды, тетрациклины, клофибрат, кетоконазол, мебендазол, пиридоксин, теофиллин, циклофосфамид, фенфлурамин, препараты лития, препараты, содержащие этанол. Гипогликемическое действие инсулина ослабляют: пероральные контрацептивы, ГКС, тиреоидные гормоны, тиазидные диуретики, гепарин, трициклические антидепрессанты, симпатомиметики, даназол, клонидин, блокаторы медленных кальциевых каналов, диазоксид, морфин, фенитоин, никотин. Под влиянием резерпина и салицилатов возможно как ослабление, так и усиление действия препарата Октреотид/ланреотид может как повышать, так и снижать потребность организма в инсулине. Блокаторы β-адренорецепторов могут маскировать симптомы гипогликемии и задерживать восстановление после гипогликемии. Алкоголь может усиливать и пролонгировать гипогликемический эффект инсулина. Несовместимость Некоторые лекарственные средства, например, содержащие тиол или сульфит, при добавлении к раствору инсулина детемир, могут вызывать его разрушение. Поэтому не следует добавлять инсулин детемир в инфузионные р-ры.
Передозировка препарата Инсулин детемир, симптомы и лечение
Определенной дозы, позволяющей говорить о передозировке инсулина не установлено, однако гипогликемия может развиваться постепенно, если была введена слишком высокая доза для конкретного пациента. Симптомы гипогликемии. Лечение: легкую гипогликемию пациент может устранить сам, приняв внутрь глюкозу, сахар или богатые углеводами продукты питания. Поэтому, больным сахарным диабетом рекомендуется постоянно носить с собой сахар, сладости, печенье или сладкий фруктовый сок. В случае тяжелой гипогликемии, когда пациент находится без сознания, следует ввести 0,5–1 мг глюкагона в/м или п/к, (может вводить обученный человек), либо в/в р-р декстрозы (глюкозы); INSERT INTO `info` (`ID`, `Name`, `NameBase`, `TEXT`, `IsUsed`, `Description`, `KeyWords`) VALUES (может вводить только медицинский работник). Также необходимо в/венное введение декстрозы в случае, если через 10–15 мин после введения глюкагона пациент не приходит в сознание. После восстановления сознания пациенту рекомендуется принять пищу, богатую углеводами с целью профилактики рецидива гипогликемии.
Список аптек, где можно купить Инсулин детемир:
- Москва
- Санкт-Петербург